燃油氧化脱硫催化剂的研究进展
吕树祥,刘 昊,王 超
(天津科技大学化工与材料学院,天津 300457)
近年来,随着车辆保有量的增加,人们对燃油的需求量也在逐渐增加,而面对日趋严格的燃油含硫量的限制,各国逐步开展燃油脱硫技术的研究[1].目前主要的燃油脱硫技术包括加氢脱硫(HDS)和非加氢脱硫(NHDS)两类[2].HDS是较为成熟的脱硫技术,但其操作条件苛刻、设备投资大,同时由于含硫物质的空间位阻效应,噻吩类化合物不能有效脱除[3].相比之下,吸附脱硫(ADS)、生物脱硫(BDS)、萃取脱硫(EDS)、氧化脱硫(ODS)等[4]非加氢脱硫技术能耗更低、操作更便捷.其中,氧化脱硫技术因为具有脱硫率高、反应条件温和等特点,被称为面向21世纪的绿色脱硫工艺[5],工业化应用潜力巨大.
1 氧化脱硫机理
氧化脱硫技术是指燃油中的含硫化合物,如硫醇、硫醚以及噻吩类化合物[6]等,在一定条件下被氧化剂氧化为极性较强的含氧硫化物.由于含硫化合物中的碳硫键极性与碳氢键极性相近,且硫原子与碳原子杂化后会产生一个空的d轨道,这就使得含硫化合物在氧化脱硫过程中易被氧化为相应的砜类物质和磺酸类化合物,如图1[7]所示.小分子含硫化合物易被氧化为磺酸类化合物,而噻吩类杂环含硫化合物则被氧化剂氧化为相应的亚砜和砜类化合物.不同于小分子的硫醇和硫醚,噻吩类化合物较难使用加氢脱硫技术去除,但随着噻吩类化合物苯环上电子云密度的增大,其氧化反应相对速率同步增大(见表1[6]),因此氧化脱硫技术主要用于去除燃油中的噻吩类化合物.而含硫化合物中的硫原子经过氧原子的亲电加成后,含硫化合物的极性相对增强,随后可利用合适的方式将其从燃油中分离,进而达到脱硫的目的[8-10].

图1 有机含硫化合物的氧化机理 Fig.1 Oxidative mechanism of organic sulfur compounds

表1 有机含硫化合物电子云密度及其氧化反应活性 Tab.1 Electron cloud density and oxidation reaction activity of organic sulfur compounds
2 氧化脱硫中的催化剂
2.1 有机酸催化剂
有机酸催化氧化法以过氧化物(大多为过氧化氢) 作为氧化剂,有机酸(如甲酸[11]、乙酸[12]等)作为催化剂,以此构建过氧化物-有机酸催化体系[13-15],利用体系内产生的过氧酸将含硫化合物氧化为相应的亚砜类或砜类化合物,从而增大含硫化合物的极性并利用极性溶剂萃取脱除.
林朋等[16]利用H2O2–甲酸催化体系对催化裂化(FCC)汽油进行深度氧化脱硫,在反应温度为60℃的条件下,加入1mL异丁醛、0.05g硫酸亚铁、5mL甲酸和5mL H2O2对50mL FCC汽油进行30min的氧化脱硫反应,最终脱硫率可达92.4%;张腾云等[17]利用H2O2–乙酸催化体系,加入理论量两倍的过氧乙酸(PAA),在反应温度为50℃的条件下,进行30min的氧化脱硫反应,加氢柴油的硫含量从295.8mg/kg下降到13.4mg/kg,脱硫率可达95.5%;王雪琴[18]利用过氧乙酸体系考察其对汽油的氧化脱硫效果,在反应温度为40℃、反应时间为20min的条件下,过氧乙酸体系对汽油的脱硫率可达93.5%,汽油中硫含量从407.1mg/L降低到26.6mg/L.
在有机酸催化体系中,提高氧化效率和选择性是最核心的问题[19],实验证明反应体系中溶剂的芳香性强弱会对硫化物氧化的速度产生影响.为了提高催化氧化脱硫的反应效率,提高氧化剂在体系内的传质效率,可以通过加入助剂形成乳液氧化体系的方式对H2O2体系加以改进,如李瑞丽等[20]向脱硫体系中加入分散剂Span-80,在相同的条件下,H2O2–甲酸体系脱硫率可达85.58%,而H2O2–甲酸–Span-80体系对重油FCC柴油的脱硫率可达98.27%,硫含量从12500mg/L下降到216mg/L,证明分散剂Span-80的加入可以显著提升H2O2–甲酸催化体系的氧化效率;刘倩倩[21]采用磷钨酸和季铵盐自制双亲性相转移剂对FCC柴油进行氧化脱硫,发现使用甲酸和双亲性相转移剂会显著提升H2O2催化体系的脱硫效果,在氧硫比(物质的量比)为3.5、反应温度为50℃时,脱硫率达到95%.
有机酸催化氧化法的相关理论研究起步较早,催化反应活性较高,体系也较为成熟,在一些研究中还会向H2O2–有机酸催化体系中添加部分助剂来保持氧化剂的稳定并降低体系内传质阻力或利用超声波为反应体系提供能量,利用超声场介入改变原有液–液相界面平衡关系[22-23],加强在液–液相界面处的湍动效应和微扰效应,提高液–液传质效率和乳化效果,降低发生氧化脱硫反应的门槛,加速氧化反应的进行[24-27].一般来说,H2O2作为氧化剂与多种类型的催化剂组合均具有较好的氧化脱硫性能[28],但是通常需要加入过量的H2O2,在反应中产生的水也易与油品混溶,可能会导致油品乳化.为了避免H2O2作为氧化剂造成的油水两相之间传质阻力过大的麻烦,大量研究人员将目光转到油溶性的有机过氧化物上[29].虽然使用油溶性的有机过氧化物作为氧化剂避免了H2O2造成的油水两相传质的问题,但是油溶性的有机过氧化物成本较高,并且副产物叔丁醇难以分离,导致燃油的辛烷值会降低,进而影响燃油质量.同时,H2O2–有机酸催化体系中使用的有机酸催化剂在经过长时间使用后会造成设备的腐蚀,反应结束后有机酸催化剂的分离与再生问题也未能找到合适的处理方式,同时较高的氧化剂成本也逐渐成为制约有机酸催化氧化法发展的瓶颈.相比之下,使用离子液体催化剂、过渡金属氧化物催化剂和有机–无机杂化材料催化体系等固体催化剂,不仅便于催化剂的分离和再生,而且避免了用于催化的有机酸溶于燃油中使油品质量降低的弊端.
2.2 离子液体催化剂
离子液体是一类由离子组成的液态熔盐[30-31],具有熔点低、热稳定性好、功能可调等优点,其作为一种新型的绿色介质已被广泛应用于石油化工等领域.在离子液体催化氧化体系中,由于含硫化合物在离子液体中的溶解度大于其在燃油中的溶解度,因而含硫化合物会不断地从燃油中萃取至离子液体中,并与氧化剂反应生成砜类物质,进而达到燃油深度氧化脱硫的目的.
2.2.1 中性离子液体和酸性离子液体
Lo等[32]将离子液体和油品氧化脱硫相结合,利用中性离子液体[C4mim]PF6作为催化剂和萃取剂、H2O2作为氧化剂时,在70℃的条件下经过6h的反应,DBT模拟油的硫含量从758mg/kg下降至7.8mg/kg,脱硫率约为 99%.Zhang等[33]利用[HDBN]Cl/nZnCl2(n=1,2,3)催化剂探索了Lewis酸性离子液体对模拟油的脱硫性能,催化剂在使用6个周期后仍能保持超过95%的氧化脱硫活性,在随后对柴油的氧化脱硫性能测试中,硫含量从559.7mg/kg下降至6.5mg/kg,脱硫率达到98.8%;但ZnCl2含量的增加会导致阴离子与阳离子之间的相互作用增强,显著增大了离子液体的黏度,降低了体系内的传质效率,导致催化性能降低.Xu等[34]制备了[C4mimCl]CoCl2离子液体,使用Co2+与过氧单磺酸钾(KHSO5)反应后生成的强氧化性的硫酸根自由基作为氧化剂对模拟油体系进行氧化脱硫,结果表明在适宜的条件下,模拟油中含硫化合物(DBT)的脱除率达到了97%,使用6个周期后仍能保持96%以上的脱硫率;但随着离子液体使用量的增加,过量的Co2+会成为自由基清除剂消耗硫酸根自由基,阻碍氧化反应的进行.
2.2.2 杂多酸离子液体
杂多酸离子液体具有良好的可设计性,在萃取氧化脱硫中有着广泛应用.杂多酸离子液体催化剂同时拥有杂多酸阴离子优异的催化性能和离子液体的疏水性,有利于萃取氧化脱硫反应的进行.Wang 等[35]使用杂多酸离子液体催化氧化体系进行氧化脱硫研究,利用[C3SO3Hnhm]3PW12O40作为催化剂,在氧硫比(物质的量比)为15、反应温度为50℃的条件下,对硫含量为800mg/kg的DBT模拟油进行105min的氧化脱硫反应,最终脱硫率可达99.4%.Lü等[36]合成了非均相催化剂[C4mim]5PMo10V2O40,以氧气为氧化剂对模拟油体系进行氧化脱硫研究,在初始氧分压0.2MPa、反应温度125℃、催化剂用量0.5%的条件下反应4h,可将93.4%的DBT从模拟油中脱除;在反应了5个周期后,仍可保持90%左右的脱硫率.随后,Liao等[37]在此基础上对原有催化剂进行改进,制备了(NH4)xH4-xPMo11VO40(x=1,2,3,4)催化剂,在120℃的反应温度下反应2h,可将全部含硫化合物从模拟油体系中氧化脱除;在对不同含硫化合物进行氧化脱硫实验后发现,硫化物的脱除选择性为DBT>4,6-DMDBT>BT,这表明含硫杂环化合物的氧化效率不仅与硫原子上电子云密度有关,更与含硫化合物的空间位阻效应有关[38-39].Zhuang等[40]合成了3种不同的杂多酸[Cnmim]PMoV(n=2,4,6),以H2O2为氧化剂对模拟油体系进行探究,结果表明在50℃的条件下反应2h,[C2mim]PMoV可将94.1%的DBT从模拟油中脱除;随着烷基链的增长,催化剂疏水性增大,在萃取相中的溶解度也相应地增大,进而提高了氧化脱硫的效率[41].
2.2.3 负载型离子液体
离子液体虽然催化活性高、复用性强,但制备工艺较为复杂且不易回收再利用,因此将离子液体负载到适合的载体上,在保障其催化性能的同时提高其可回收性是目前研究的一个重要方向.目前常用的载体包括Al2O3[42]、SiO2[43]、TiO2[44]、碳材料[45]、金属有机骨架化合物(MOFs)[46]、分子筛[47]等.
由于SiO2具有较高的比表面积和较大的孔径结构,使其成为负载离子液体的最佳载体之一.在利用过渡金属对SiO2表面进行改性之后,离子液体可通过配位键锚定在SiO2载体上,降低了离子液体在回收再生时的损耗[48].李佳蓉[49]利用微孔SiO2为载体,负载杂多酸离子液体,对2000mg/kg的DBT模拟油进行氧化脱硫测试,结果表明在以空气为氧化剂(流量为750mL/min)、反应温度为60℃的条件下,经过90min的反应,mi-SiO2@聚(1–乙烯基咪唑)–PMoW(mi-SPIP)和mi-SiO2@聚(4–乙烯基吡啶)–PMoW(mi-SPVP)均表现出了较高的脱硫率(脱硫率分别为99.37%和98.61%).
TiO2可以以各种不同形态存在,且其表面的缺电子结构与硫原子上的孤对电子有较强的吸附作用,有利于脱硫反应的顺利进行,这些因素都使得TiO2成为一种非常合适的载体[50].Xun等[51]制备了一系列[Cnmim]4SiW12O40-TiO2(n=4,8,16)催化剂,并发现当钨与钛物质的量比为0.1、碳链中碳原子数为16、H2O2与DBT物质的量比为2时,脱硫率可达到95.3%,循环8个周期仍能维持较高活性.
MOFs类载体由于具有高比表面积、超高可调孔隙率以及较好的稳定性,因而在催化剂领域有着广泛的应用[52].Ribeiro等[53]利用MIL-101负载了Keggin型离子液体TBA3PW12O40,在50℃条件下反应1h可将DBT完全氧化.具有多孔结构的分子筛因可作为催化剂活性组分的优良载体而被应用于多种催化有机反应,如SBA-15、MCM-41等分子筛近年来已被广泛应用于催化氧化脱硫反应[54-55].Mirante等[56]在用三甲胺进行功能化的SBA-15分子筛上负载了(PW11Ti)2OH,制备了一种(PW11Ti)2OH@TM-SBA-15催化剂,在氧硫比(物质的量比)为9、反应温度为70℃的条件下催化氧化1h后,模拟油体系内的硫含量从2350mg/kg下降到425mg/kg,取得了比较好的脱硫效果.
离子液体是一类常见的氧分子活化催化剂[57],在氧气氧化脱硫反应中展现出了较高的催化活性,同时使用离子液体进行催化反应的条件相对较为温和,离子液体催化剂参与催化氧化脱硫反应的过程如图2[58]所示,包括萃取过程、氧化过程和再生过程,图2中从左到右的3个过程分别为离子液体在H2O2/O2体系、H2O2/NaClO体系和O2体系下参与反应的过程.使用离子液体作为催化剂对燃油氧化脱硫有着较好的选择性[48,59],但复杂的制备工艺在一定程度上影响了其工业化的进程.
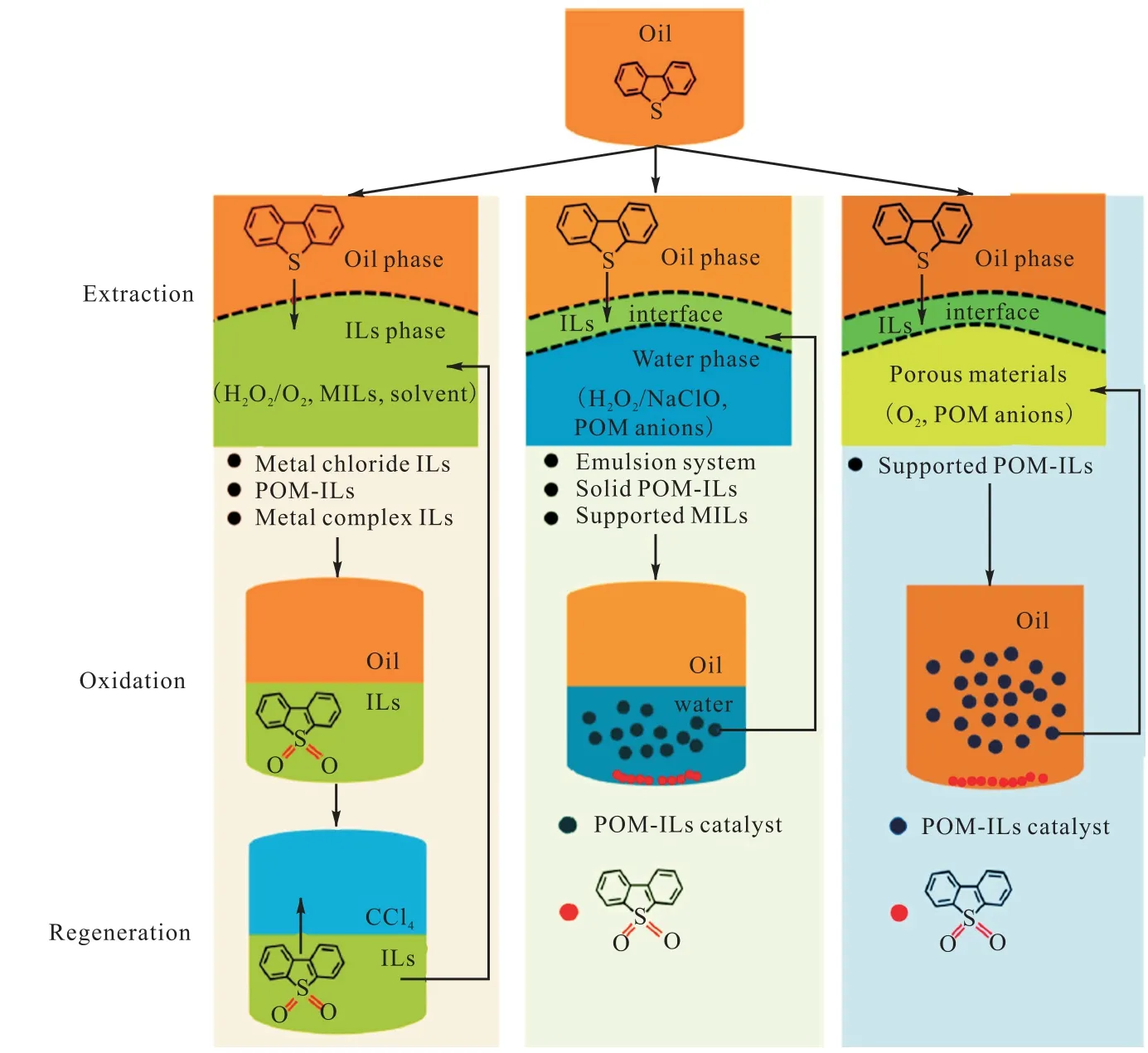
图2 离子液体催化氧化机理 Fig.2 Oxidative mechanism of ILs catalyst
除了离子液体的制备工艺复杂,其高成本、高黏度以及氧化产物的分离等都是亟待解决的问题.目前负载型离子液体因其载体具有较大的比表面积,增大了离子液体与燃油的接触面积,有效降低了催化氧化过程中离子液体的使用量,降低了使用成本.同时,由于负载型离子液体不易腐蚀设备,负载型离子液体相较其他类型的离子液体展现出了极为广阔的应用前景,在未来研发出更多成本更低、性能更优异的载体材料,简化制备路线并探索出一套完备的再生方法后,离子液体会在工业化生产中大量应用.
2.3 过渡金属氧化物催化剂
在过渡金属催化氧化体系中,由于过渡金属对含硫化合物中的C—S键的裂解和转化有着较高的活性[60],C—S键往往会和过渡金属形成一种高活性的硫化物或硫化物络合物.因此,使用过渡金属会大大降低C—S键的键能,使含硫化合物更易于发生转化.将过渡金属负载在合适载体上往往会带来更多的Lewis酸性位点,这些酸性位点往往可以作为电子受体吸附含硫化合物中具有富电子特性的硫原子.过渡金属氧化物ODS机理如图3[61]所示,过渡金属氧化物在催化反应过程中会与氧化剂形成一种过氧金属物质,便于电子从硫原子上攻击过氧金属的O—O键,从而进行氧化反应生成相应的砜类物质[62-63].
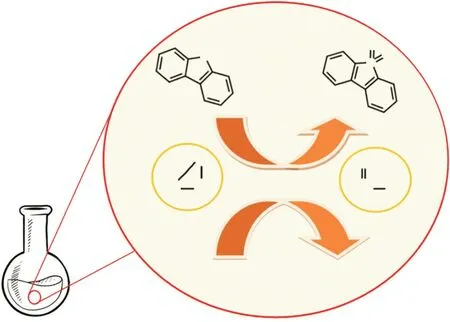
图3 过渡金属氧化物ODS机理 Fig.3 ODS mechanism of transition metal oxide catalyst
2.3.1 Mo基催化剂
Akbari等[64]使用过渡金属氧化物催化氧化体系,利用负载型催化剂MoO3/Al2O3在314K的条件下对模拟油中的BT、DBT、4,6-DMDBT的脱硫率可达100%.Zou等[65]利用原位合成法制备了一种3D有序介孔催化剂Mo/KIT-6-Ti,在60min内可将模拟油中的含硫物质(DBT)氧化99%以上,其表观速率常数为浸渍法所制备催化剂的16.3倍.Tian等[66]和Lu等[67]利用γ-Al2O3为载体制备了负载型Mo/γ-Al2O3催化剂,在氧硫比(物质的量比)为2.3、反应温度为60℃的条件下反应40min,可从体系中脱除超过99%的BT、DBT和4,6-DMDBT,并根据实验结果构建了负载型Mo/γ-Al2O3催化剂的萃取–氧化脱硫的动力学模型.Mo及其金属氧化物还被广泛地负载在其他的载体上,Wang等[68]使用半导体材料g-C3N4作为载体,将MoO3负载在3种不同形貌的g-C3N4载体上,制备了3种MoO3/g-C3N4催化剂,并在对模拟油的氧化脱硫实验中发现利用管状g-C3N4作为载体制备的MoO3/g-C3N4催化剂有着最高的催化活性.Wang等[69]将MoO3负载于超小介孔SiO2纳米粒子(UMSN)上,制备了一种亚纳米MoO3/UMSN催化剂,对模拟油进行氧化脱硫测试;在70℃、15min的反应条件下,模拟油中的DBT转化率可达100%,转化频率(TOF)为53.3h-1,并将MoO3/UMSN催化剂的高活性归因于UMSN的亚纳米尺寸和其介孔材料的特性.Wang等[70]使用TBHP作为氧化剂,利用DBT的十氢化萘溶液(5000mg/kg)探究Mo/M41C-6%催化剂失活的原因,经过8h的持续测试,作者认为催化剂ODS活性下降的主要原因是Mo活性位点和SiM41C框架结构吸附了氧化反应所产生的砜类物质,阻碍了含硫化合物在Mo活性位点上的进一步转化.Hu等[71]利用硅烷化试剂在SiO2载体表面锚定了Mo物种,制备了一种锚定型Mo-NH2-SiO2催化剂,由于其高疏水性和Mo物种在催化剂表面的高分散度,在对柴油(硫含量为21500mg/kg)的实际测试中取得了80.4%的脱硫率,同时体现了较好的稳定性,为制备高活性、高稳定性的燃油氧化脱硫催化剂提供了新的途径.
2.3.2 Ti基催化剂
Li等[72]使用溶胶–凝胶法制备了纳米TiO2催化剂,在343K、氧硫比(物质的量比)为10的条件下,经过50s的反应即可完全脱除100mg/kg DBT模拟油中的全部含硫物质,并证明锐钛矿型纳米TiO2比金红石纳米TiO2和无定形纳米TiO2脱硫效果更好.Li等[73]利用水热法制备了TiO2-SiO2催化剂,在紫外光照射下经过1h的反应即可完全氧化DBT模拟油中的全部含硫物质.Zuo等[74]利用溶胶–凝胶法制备了TiO2-TBOT催化剂,在333K、60min、DBT模拟油用量为15mL、氧硫比(物质的量比)为4的条件下,可完全脱除320mg/kg DBT模拟油中的含硫物质,作者还提出了二氧化钛催化剂的热催化氧化脱硫机理.Vu等[75]制备了一种MWNTs/TiO2催化剂,并对714mg/kg的商用柴油进行氧化脱硫实验,在120min反应后可将反应体系内所有的含硫化合物脱除,并认为多壁碳纳米管(MWNTs)和二氧化钛的协同作用是提升光催化氧化柴油反应效率的原因.
2.3.3 V基催化剂
Zou等[76]利用球磨法制备了V2O5纳米颗粒,在优化反应条件后,对500mg/kg的DBT模拟油中DBT的脱除率可达99.7%,氧化后油品中硫含量<2mg/kg;并且在实验过程中还发现,与块状V2O5催化剂相比,利用球磨法制备的V2O5催化剂具有较多的氧空位,在催化氧化的过程中也更容易将O2活化为超氧化物自由基(2O·-),从而达到深度脱硫的目的.Wang等[77]利用NH4VO3和EDTA-2Na原位制备了碳材料负载的V2O5催化剂,利用异丙苯过氧化氢作为氧化剂,可将DBT模拟油中99.8%的含硫物质氧化脱除;并认为在异丙苯过氧化氢的作用下,催化剂中的V(Ⅴ)=O基团转化为一种亲电子的过氧化物(V(Ⅳ)—O—O·)参与到氧化脱硫反应中,将含硫化合物氧化为对应的砜类物质.Rivoira等[78]制备了一系列VOx-SBA-15催化剂,并用铝和镓对SBA-15骨架进行改性,以提高催化剂的活性,在使用H2O2作为氧化剂的条件下可在较短时间内完成对模拟油体系内DBT的氧化脱除.González等[79]在Ti-MCM-41表面负载了钒氧化物,并认为增大V5+的占比可提升VOx/Ti-MCM-41催化剂催化氧化脱硫的活性.
2.3.4 其他过渡金属催化剂
Subhan等[80]制备了一系列复合金属氧化物催化剂,并在室温下对DBT模拟油进行实际氧化脱硫实验,发现脱硫活性Mn-Co-Mo/Al2O3>Mn-Ni-Mo/Al2O3>Co-Mo/Al2O3>Ni-Mo/Al2O3.田亚杰 等[81]利用γ-Al2O3为载体制备了XO-Fe2O3/γ-Al2O3催化剂(X=La,Ce,Co,Cu),在适宜条件下CuOFe2O3/γ-Al2O3可在120min内将噻吩脱除95%以上.Ramos等[82]利用SBA-15分子筛和Zr改性的SBA-15分子筛作为载体负载活性组分FeOx制备了FeOx/SBA-15和FeOx/Zr-SBA-15催化剂,在适宜条件下可以在30min内完成对模拟油体系内DBT的氧化脱除;实验结果表明,两种催化剂表面都有Lewis酸,酸量与铁含量和锆的改性有关,随着锆的加入,锆与SBA-15载体相互作用,通过增加表面酸性抑制无定型氧化铁的形成,提高了催化剂表面Lewis酸量,进而提高了氧化脱硫的效率.Mousavi-Kamazani等[83]利用一步法合成了Cu2O-CeO2催化剂,并利用光催化氧化脱硫法对噻吩模拟油进行脱硫活性测试,在180min内光催化氧化效率可达84%,作者认为表面空穴(h+)和2O·-是催化氧化过程中的主要活性物质.虽然在利用氧气作为氧化剂的条件下使用过渡金属氧化物[84]也可取得一定的脱硫效果,但反应时需要较高温度,同时仍需要使用较多有机溶剂作为萃取剂,且不易达到深度脱硫的要求[85],造成这一现象的原因可能是过渡金属的氧转移能力较弱,不利于催化氧化反应的进行.
从目前的研究成果来看,使用过渡金属及其氧化物作为负载型催化剂的活性中心进行催化氧化脱硫反应依旧是当下负载型催化剂的主要趋势,使用Mo、Ti和V等过渡金属的催化剂表现出了较高的催化活性.若在氧化过程中使用超声波或光照等辅助措施,并对催化剂的载体进行改性处理,使用Cu、Cr、Co等其他过渡金属催化剂的氧化脱硫催化活性可进一步提高.因此,对催化剂载体进行改性或使用超声波等辅助措施不失为一种提高过渡金属催化剂氧化脱硫活性的有效方法.
2.4 Ti纳米管
不同于过渡金属氧化物催化剂,Ti纳米管(TiNT)因其具有较好的催化效果以及可调控的结构形貌而备受关注[86].Lü等[87]和莫冬梅等[88]利用水热法和溶胶–凝胶法制备了一系列的Ti纳米管,对不同含硫化合物进行脱硫活性测试,发现氧化脱硫活性从高到低依次为DBT>BT>Th>4,6-DMDBT,验证了Ti与过氧化物形成的η1和η2构型在氧化脱硫反应中的氧化机理,并提出了钛纳米管催化剂相应的热催化氧化脱硫机理.随后,Yao等[89]利用HCl对水热法合成的长钛纳米管进行改性,制备了一种非典型的短钛纳米管催化剂,在适宜条件下反应30min可将反应体系内所有的含硫化合物(DBT)脱除,并对比了不同长度钛纳米管氧化含硫化合物的机理(如图4[89]所示),认为形成了η1构型的Ti-H2O2络合物是钛纳米管具有较高催化效果的关键.

图4 Ti纳米管氧化脱硫的机理 Fig.4 ODS mechanism of TiNT
结合目前的研究结果来看,TiNT作为一种纳米材料具有其独特的催化氧化特点,其与H2O2相结合所生成的Ti-η1-OOH活性中间体可以较为有效地氧化脱除油品中的DBT和BT等含硫物质,但是对含硫化合物中S原子上电子云密度过低或空间位阻较大的含硫化合物(如噻吩和4,6–二甲基二苯并噻吩)脱除效果不佳.针对这种现象,可以改变TiNT的制备条件,增大TiNT的孔径和层间距,同时负载一些对噻吩等含硫物质有选择吸附作用的金属离子,提高含硫物质接触催化剂活性位点的概率.
2.5 MOFs材料
在有机-无机杂化材料催化体系中,MOFs材料在催化反应中是一种高效的催化剂,但由于大多数MOFs的孔道特性不能使芳香族含硫化合物直接抵达无机金属中心,因此在较早的研究中MOFs材料通常作为载体出现在催化氧化脱硫反应体系中.随着对MOFs材料的研究愈发深入[90],在对MOFs材料进行不断优化之后,越来越多的MOFs材料可直接作为催化剂被应用于催化氧化脱硫反应中.Liao等[91-92]制备了用不同官能团改性的UIO-66催化剂和一系列MIL-125催化剂,发现UiO-66(Zr)-NO2和MIL-125(300)具有最好的脱硫性能,并可以在长时间的反应后保持较高的反应活性.Vallés-García等[93]制备了利用硝基改性的MIL-101(Cr),并与均相乙酸铬和非均相Cr2O3的催化活性进行比较,发现MIL-101(Cr)-NO2催化剂比乙酸铬活性高5倍,比Cr2O3活性高6倍,凸显了MOFs材料对比传统非均相催化剂时催化活性高的优势.表2列举了其他MOFs材料,在适宜条件下,使用MOFs作为催化剂均可获得较好的氧化脱硫效果.
随着MOFs材料种类的不断丰富,越来越多的大孔径、高热稳定性的MOFs材料作为催化剂被应用到氧化脱硫反应中.但目前这类研究大多停留在脱除模型化合物的阶段,将其应用于真实燃油的研究鲜有报道,相信在对现有成熟的MOFs材料开展相应官能团化、表面修饰等复合研究,并针对现有MOFs材料的缺陷结构进行可控构筑,探究真实油品中相关组分对MOFs催化氧化的影响,完善MOFs催化氧化脱硫体系理论后,使用MOFs材料会为真实燃油的氧化脱硫提供一条崭新的道路.
3 结 语
燃油中的含硫化合物为环境保护带来了诸多问题,氧化脱硫技术在20世纪70年代出现,其以反应条件温和以及不需要氢能等特点而备受关注.但目前对于氧化脱硫的研究大多停留在理论研究的阶段,所研究的大多是硫含量较低的模拟油,对于硫含量较高的真实油品的研究鲜有报道.如何才能将所制备的高活性、高稳定性的催化剂逐步应用于工业化生产是下一阶段氧化脱硫研究人员需要解决的一个问题.目前使用固体催化剂催化氧化脱硫仍是主要研究方向,虽然使用固体催化剂可以有效解决有机酸氧化脱硫体系中催化剂的分离再生问题,但也并非没有缺点,如:使用固体催化剂进行氧化脱硫反应的体系主要为固–液体系或固–液–气三相反应体系;在反应过程中通常会使用一些辅助手段使催化剂、氧化剂、油溶性硫化物接触充分,相应地会导致燃油易乳化、生产过程不易连续化;分离氧化后产生的砜类物质会导致油品收率下降、与小分子含硫化合物反应相对速率没有加氢脱硫高、未反应的氧化剂从反应体系内分离困难等问题.这些都是氧化脱硫技术日后需要解决的问题.随着脱砜方法的改进,脱砜的方法逐渐由物理吸附脱砜转向碱催化脱砜,氧化脱硫所得砜类物质可以在碱性催化剂催化下分解产生无硫有机化合物和硫氧化物气体(SO2、SO3等),后者可以容易地从反应体系内分离,前者则可以留存在燃油中,缓解了辛烷值、十六烷值下降的问题.针对氧化脱硫工艺对小分子含硫化合物相对反应速率较低、不易脱除的问题,则可以利用含硫化合物的加氢脱硫活性与氧化脱硫活性顺序相反的特点,首先使用传统加氢脱硫工艺先脱除小分子含硫化合物,再利用氧化脱硫工艺脱除余下的杂环类化合物,以此方法实现深度脱硫的目标.相信在未来,氧化脱硫技术会日益成熟、完善,也会有更多低成本、高活性、长寿命的催化剂出现在燃油氧化脱硫工艺中.

