魔芋葡甘聚糖基热可逆凝胶研究进展
石文娟,苗丽坤,孙炜炜,乔冬玲,姜发堂,陈 胜*
(1 湖北工业大学生物工程与食品学院 武汉 430068 2 武汉黄鹤楼新材料科技开发有限公司 武汉 430000)
魔芋葡甘聚糖(Konjac glucomannan,KGM)是从魔芋块茎中分离得到的可溶性非离子多糖,是一种高分子、水溶性非离子型天然多糖。其中D-葡萄糖和D-甘露糖残基以1∶1.5 或1∶1.6 的分子比通过β-1,4-糖苷键连接形成分子主链[1-2],在主链甘露糖的C3 位置,通过β-1,3-糖苷键链接其支链,据研究表明[3]每32 个糖残基上结合3 条支链,每条支链含有几个至几十个糖残基,且平均每19 个糖残基上以酯的方式结合1 个乙酰基[4]。
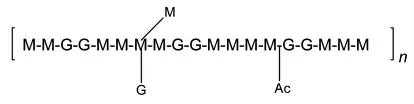
图1 KGM 的分子结构式[5]Fig.1 Molecular structure formula of KGM[5]
KGM 分子链是半柔性链,它自发卷曲形成螺旋结构。KGM 分子链上乙酰基团的空间位阻使其螺旋结构中存在大量的空隙,可以容纳大量的水[6]。KGM 特殊的分子结构赋予其凝胶性,主要表现在3 个方面:1)在碱性条件下脱乙酰基,通过分子内和分子间的氢键作用形成三维网络结构,形成热不可逆凝胶;2)与其它组分复配后产生协同作用,形成热可逆凝胶;3)通过添加硼砂等交联剂,与其自身分子链发生配位作用,通过复合物螺旋链的并排聚集沉淀,形成热稳定凝胶[7]。KGM 基凝胶具有生物降解性高、生物相容性好、环境响应性敏锐、固液共存等众多优势,因而成为众多科学工作者研究的焦点,被广泛应用于食品、医药、化工和功能材料等领域[8]。
KGM 基热可逆凝胶是将KGM 与其它多糖共混后,组分之间通过非共价相互作用力(如静电相互作用、氢键、疏水相互作用、范德华力)发生协同增效作用,形成稳定性高、弹性好的一类凝胶[2]。该类型的凝胶可克服纯KGM 凝胶内聚性低、机械性能不足、结构完整性弱、加工和贮藏过程中稳定性不足、保质期短以及保水性低等弱点[9-10]。近年来,随着国内外学者对KGM 基热可逆凝胶研究的深入,其应用领域拓展至药物缓释载体、伤口敷料、生物组织支架和吸附剂材料等方面[4]。
目前关于KGM 基热可逆凝胶的研究大多通过表征复合溶胶的流体力学特性、借助电子显微镜等手段表征其复合结构形态,以及通过凝胶强度测试其力学性能进行分析[11],如利用流变仪分析KGM 与可得然胶复配体系的频率扫描、黏度测试、温度扫描,利用原子力电子显微镜和透射显微镜观察复合体系的结构形态[12-13]。从分子组装角度来讲,KGM 基热可逆凝胶依靠组分间非共价相互作用进行组装,其构筑单元的本质不变。研究KGM 与其它组分之间如何通过协同效应组装形成稳定有序的高级结构,明确分子结构与体系及凝胶化过程之间的关系,有利于进一步了解和提升KGM 基热可逆凝胶的性能。本文从分子组装角度综述KGM 基热可逆凝胶的形成机理,归纳总结KGM 基热可逆凝胶体系的流变学、凝胶特性和力学性能,为改善KGM 基热可逆凝胶强度和体系稳定性提供参考。
1 KGM 基热可逆凝胶
天然多糖根据其本身能否形成凝胶可分为凝胶多糖和非凝胶多糖。天然凝胶多糖溶于水中便可得到凝胶,基于得到凝胶的热可逆性及其模量的温度依赖性,可将其细分为以下4 种类型[14-16]:
1)冷致凝胶,多糖溶液仅能在低温下获得凝胶,如卡拉胶、结冷胶、琼脂等;
2)热致凝胶,多糖溶液仅能在高温下获得凝胶,如纤维素衍生物、可得然胶等;
3)多糖溶液不仅能在较低温度下获得凝胶,还可在较高温度下获得凝胶,而在中间的温度内呈现出溶液状态,如甲基纤维素和明胶的混合溶液等;
4)溶液仅在中间某段温度时可获得凝胶,如去半乳糖残基的木葡聚糖等[9]。
KGM 与凝胶多糖或非凝胶多糖均可通过协同作用形成热可逆凝胶。胶体间的协同增效性在实际应用中非常广泛,它不仅能够节省价格较高多糖的用量,还可获得比单一凝胶更好的应用效果。如KGM 可与卡拉胶和结冷胶螺旋表面上形成弱连接,抑制卡拉胶和结冷胶分子本身有序结构的形成,继而两者共同形成三维网络,增强其凝胶强度。KGM 与琼脂共混可改善单一琼脂凝胶的脆性,得到硬度和稳定性更佳的凝胶。KGM 与纤维素衍生物共混可形成物理交联的互穿网络,改善凝胶的强度,还可增强复合膜的透光率、力学性能和吸湿性等。
1.1 KGM/卡拉胶复合热可逆凝胶
卡拉胶(Carrageenan)是以1,3-α-D-吡喃半乳糖和1,4-β-D-吡喃半乳糖作为基本骨架,由线性多糖类硫酸酯盐和3,6-脱水半乳糖直链聚合物而成的天然高分子聚合物,具有良好的增稠性和胶凝性。根据半酯式硫酸基团的组成和结构,可将卡拉胶分为7 种,其中以κ 型(Kappa)卡拉胶凝胶性能最好,应用也最广泛。κ-卡拉胶(KC)主要从红藻等海藻中提取,其凝胶性能主要与其化学组成和分子结构有关:在热溶液中,卡拉胶分子以无规卷曲状存在;当溶液温度降低时,卡拉胶分子逐渐向螺旋状转变,形成单螺旋体;当溶液温度继续降低时,卡拉胶分子间形成双螺旋体,双螺旋体聚集组成立体网状结构形成凝胶。
单一的KC 凝胶存在脆性过大、弹性较小、析水严重等问题[17-18]。研究发现,葡甘聚糖胶可增加KC 凝胶的强度和弹性,并能够缓解凝胶脱水收缩的问题[19]。Sewall 等[20]的研究表明KC 和KGM 两者的协同作用与KC 中半乳聚糖的硫酸酯含量密切相关。KGM 属于葡甘露聚糖,其酯基在葡甘聚糖主链上非随机分布,且酯基之间的距离与KC螺旋聚集体的长度非常吻合[19],因此两者可通过强氢键结合产生协同作用,形成具有良好力学性能的互穿网络结构(IPN)[21],并且凝胶强度在一定程度上随着硫酸酯含量增加而增强。在食品工业中,常将KGM 加至KC 凝胶中以降低凝胶的脱水收缩程度和脆性,增加凝胶弹性模量的线性范围[22-23]。

图2 卡拉胶分子结构式[24]Fig.2 Molecular structure formula of carrageenan[24]
1.2 KGM/琼脂复合热可逆凝胶
琼脂(Agar)是一种从红藻中提取的亲水性多糖,主要由1,3 糖苷键连接的β-D-吡喃半乳糖和1,4 糖苷键连接的3,6-脱水-α-L-吡喃半乳糖或琼脂二糖组成[26]。琼脂的凝胶化过程是热可逆的,这与体系内氢键的形成有关:琼脂加热后在水溶液中以无规卷曲的形式存在,水溶液冷却的过程中,琼脂分子链发生聚集重排,形成螺旋结构,随后螺旋结构进一步聚集形成琼脂凝胶[16]。低浓度的琼脂溶液易形成凝胶,其凝胶热稳定性较好、凝胶力强、切割性好。此外,琼脂具有优异的生物相容性,近年来被用于可生物降解包装膜的设计和研发[27]。

表1 KGM/KC 复合体系的性能研究Table 1 Study on the properties of KGM/KC composite systems

图3 琼脂分子结构式[28]Fig.3 Molecular structure formula of agar[28]
纯琼脂凝胶坚硬易脆,将KGM 与琼脂复配可改善纯琼脂凝胶的脆性,增加其柔性。KGM 与琼脂分子之间的的协同作用,减少了琼脂螺旋结构的聚集,形成了紧凑的网络结构[6],提高了复合体系的稳定性。Qiao 等[29]将琼脂与KGM 进行复配制备复合膜,研究复合膜的多尺度结构、亲疏水性和机械性能,研究表明琼脂与KGM 具有良好的相容性,两者之间存在相互作用,复合膜不具有可见的微米级相分离特征。Yuan 等[6]研究发现添加KGM可以提高琼脂水凝胶的柔韧性,且随着KGM 浓度的增加,复配体系分子链缠结变得更复杂,所形成的网络结构更加紧凑,持水能力更强。同时,KGM具有出色的溶胀性能,在溶胀后吸收了大量体积的水。在冻结过程中,水分子的滞留会形成许多小的冰晶,从而导致水凝胶的小孔的形成,这可以为药物的储藏等提供相对较大的空间。
1.3 KGM/纤维素衍生物复合热可逆凝胶

表2 KGM/琼脂复合体系性能研究Table 2 Study on the properties of KGM/agar composite systems
纤维素是世界上最丰富的可再生天然高分子聚合物,由脱氧葡萄糖单元通过β-1,4 糖苷键连接而成[15],其分子组成为(C6H10O5)n,具有明显的不熔不溶性。分子链除两端各含一个端基外,每个葡萄糖单元中都有3 个极性羟基,在一定条件下可形成大量分子内和分子间氢键;且纤维素是多环结构,分子链为半刚性链,结晶度高,在结构上具有高度的规整性,具有聚合度高、分子取向性好、化学稳定强等特点[31-32]。由于纤维素链上含有大量的羟基,因此可通过酯化、氧化、醚化等多种方法对其进行化学改性,得到具有优良应用性能的纤维素衍生物,具有重要的工业潜力[33]。目前,纤维素衍生物的应用越来越广泛,在食品工业中常用的有甲基纤维素(Methyl cellulose,MC)、羟丙基纤维素(Hydroxy propyl cellulose,HPC)、羟丙基甲基纤维素 (Hydroxy propyl methyl cellulose,HPMC)、羧甲基纤维素 (Carboxy methyl cellulose,CMC)、乙基纤维素 (Ethyl cellulose,EC)等。这些纤维素衍生物均能通过物理交联制备水凝胶,将其与KGM 进行物理共混可改善KGM 的应用性能[31,34-37]。

图4 纤维素分子结构式[38]Fig.4 Molecular structure formula of cellulose[38]
MC、HPC、HPMC 均为非离子型纤维素衍生物醚,由高度取代的区域(称为“疏水性区域”)和较少取代的区域(称为“亲水性区域”)组成[39]。CMC是一种线性水溶性阴离子纤维素衍生物醚,沿疏水主链具有多个亲水性羧基,也具有两亲性。而EC 为一种半结晶纤维素聚合物衍生物,是一种水不溶性高分子材料。在KGM 分子中,甘露糖单元由于其顺式构型而表现出憎水性,其含量越高,KGM 溶解性越差,同时在分子链中形成以甘露糖单元相互连接的不含侧链区域的机率越高。KGM的此种结构容易被螺旋分子链结构的纤维素混合醚所取代,从两者的分子结构上来看,二者的分子链都具有一定的柔性,两者共混后分子间可形成类似于螺旋状的结构,当很多链都缠结到一起时,可形成互穿网络的结构[34]。

图5 MC(a)[40]、HPC(b)[33]、HPMC(c)[34]、CMC(d)[41]、EC(e)[42]分子结构式Fig.5 Molecular structure formula of methyl cellulose(a)[40],hydroxy propyl cellulose (b)[33],hydroxy propyl methyl cellulose (c)[34],carboxyl methyl cellulose (d)[41]and ethyl cellulose (e)[42]
国内外对于MC 与KGM 物理共混后所得凝胶和复合膜的相容性、微观结构、力学性能、孔隙形态均作了很多研究[43-46]。研究表明,MC 与KGM复配能够有效地抑制KGM 凝胶的热可逆性和分子团聚现象,并且两者之间通过氢键作用形成了结构更致密、热稳定性更好的凝胶[43]。HPC 分子中存在大量的羟基,有很强烈的自聚集趋势,能够形成物理交联的凝胶网络结构[47-48]。研究表明,一定浓度的KGM 与HPC 复配制成的复合膜,质地均匀、网络结构清晰。与KGM 和HPC 各自的单一膜相比,KGM/HPC 复合膜的力学性能、吸湿性、透光性都得到了改善[49]。HPMC 与KGM 复配体系中,KGM 分子链上未被取代的甘露糖单元可与HPMC 分子链上憎水性基团-OCH3、-[OCH2CH(CH3)]n 通过疏水作用形成弱交联的疏水缔合区域,形成以HPMC 分子为骨架并与KGM 分子相连接的结构。该结构可以缓解KGM 分子在高温条件下的降解行为,还可以延缓和部分阻止HPMC热凝胶化作用[50]。在碱性条件下,CMC 分子上的羧基通常以羧甲基纤维素钠(Na-CMC)的形式存在,CMC 含有大量的羟基和羧基等亲水性基团,能够与KGM 分子形成氢键相互作用[51-54]。Li 等[37]、Wu等[41]和Xiao 等[55]将KGM 与EC 共混后制成乳液和复合膜,研究共混体系的相变行为、流变特性、微观结构以及机械性能等。结果表明,KGM/EC 乳液稳定且无相分离现象,两者通过氢键相互作用,在水油界面形成分子组装网络结构,同时复合体系的疏水性能和机械性能有所提高。
1.4 KGM/结冷胶复合热可逆凝胶
结冷胶(Gellan gum,GG)是一种线性阴离子多糖,具有平行双螺旋结构,主链由β-1,3-D-葡萄糖、β-1,4-D-葡萄糖醛酸、β-1,4-D-葡萄糖和α-1,4-D-L-鼠李糖组成。天然GG 的葡萄糖单元上含有的酰基影响GG 的凝胶特性:低酰基GG 可产生牢固的非弹性的和脆性凝胶[56]。它既可形成热可逆凝胶,类似于琼脂和明胶,也能形成盐诱导的凝胶,类似于海藻胶和卡拉胶,这些性质使GG的应用具有多样性[57]。Okamoto 等[58]通过动态或静态光散射技术研究发现GG 溶胶-凝胶的转变过程符合渗滤模型(Percolation model)。在凝胶化过程中,GG 显示出从无序状态(单链) 到有序状态(双链)的转变。处于有序状态的GG 分子刚性较强,其持久长度(Persistence length)为98 nm,回转半径约为100 nm,在较低质量浓度下(0.1 g/mL)也能够相互缠结形成凝胶结构。

图6 结冷胶分子结构式[59]Fig.6 Molecular structure formula of gellan gum[59]
随着对天然大分子高聚物研究的增多,结冷胶凝胶以及与KGM 复合凝胶的研究也逐步受到关注。Mei 等[60]的研究表明GG 与KGM 共混体系为假塑性流体,两种聚合物的分子链可通过缠结或范德华相互作用形成物理交联点,这些交联点处于动态偏离-重建平衡状态。双螺旋构象的GG 分子与KGM 之间发生协同相互作用,在较低温度(例如25 ℃)下,KGM 分子附着在GG 螺旋表面上形成弱连接,抑制结冷胶分子本身有序结构的形成,继而两者共同形成三维网络。Nishinari等[61]采用动态黏弹测试和差示扫描量热法对KGM和GG 共混体系内两者相互作用进行了研究。研究发现,GG/KGM 复合物的模量与温度、频率有关,对KGM 的分子质量有很强的依赖性。徐潇[57]和Xu 等[62]研究了KGM 和GG 复合膜的结构和流变特性,研究表明两者在一定化学剂量比的条件下存在物理相互作用,纯溶胶和共混体系均呈现出非牛顿流体特征。
1.5 KGM/黄原胶复合热可逆凝胶
黄原胶(Xanthan gum,XG) 是一种天然多糖,由β-1,4 键连接的D-葡萄糖基主链及2 个D-甘露糖和1 个D-葡萄糖醛酸组成的三糖侧链交替连接而成,侧链绕主链骨架反向缠绕,通过氢键维系形成棒状双螺旋结构。棒状双螺旋结构间靠微弱的非极性共价键结合形成螺旋复合体[63]。天然状态的黄原胶具有较为规整的双螺旋结构,经长时间加热,其螺旋链将伸展成无序的卷曲状,冷却后,其卷曲链和螺旋链共存于体系中[64]。

图7 黄原胶分子结构式[65]Fig.7 Molecular structure formula of xanthan gum[65]
KGM 与黄原胶在单独存在的情况下均不能形成凝胶,属非凝胶性多糖。KGM 与黄原胶在一定条件下复配能够形成凝胶,并显现出协同增效作用。倪俊杰等[65]、陈文平等[66]、曾瑞琪等[67]将KGM与黄原胶进行复配,发现KGM 与黄原胶质量比为3∶7 时,复配凝胶的黏度最高,且黏度随温度的升高而下降。倪俊杰等[65]采用数学拟合对黄原胶和KGM 不同配比凝胶的储能模量随总质量分数的变化进行分析,发现复合凝胶的储能模量随总质量分数的变化情况符合power-law 模型。当KGM含量适当增加时,黄原胶侧链与KGM 分子中的葡甘聚糖发生相互穿插,从而能形成较为致密的微观网络结构,因此使得复配体系的抗剪切性能有一定程度的提高。当KGM 与黄原胶复配比为3∶7时,两者的协同作用最大,凝胶强度最强。当KGM与黄原胶复配比在1∶9~4∶6 之间时,幂律系数n随KGM 含量的增加而减小,说明在此复配比范围内黄原胶对复配凝胶起主导作用;当两者复配比高于4∶6 时,n 值随KGM 含量的增加而增加,说明KGM 对复配凝胶起主导作用。
KGM/黄原胶复合凝胶体系中两者的协同作用受电解质的影响,Williams 等[68]将黄原胶分别与KGM 和刺槐豆胶复配形成热可逆凝胶,在没有电解质的情况下,KGM 与杂乱无序的黄原胶链发生相互作用,而当0.04 mol/dm3NaCl 存在时,KGM能够与有序的黄原胶链相互作用,刺槐豆胶在有无电解质存在的情况下均与有序的黄原链发生相互作用。Gaio 等[69]通过圆二色谱和差示扫描量热法研究了黄原胶和KGM 分别在溶液和凝胶相中的协同作用。通过圆二色性检测到的大分子复合物在溶液中有序区域的熔化温度与相应的凝胶相熔化温度一致,表明负责黄原胶/KGM 凝胶形成的连接区的前体是有序状态组织的部分侧链。Fitzpatrick 等[70]通过改变黄原胶的精细结构来控制黄原胶/KGM 混合凝胶的性质,研究表明黄原胶由于分子缔合而与KGM 形成热可逆凝胶,该凝胶在水中比在电解质存在下强度更强,并且凝胶强度按照去乙酰化的黄原胶/KGM>黄原胶/KGM 的顺序降低。
1.6 KGM 与刺槐豆胶复配
刺槐豆胶(Locust bean gum,LBG)又称槐豆胶、洋豆胶、角豆胶,是从刺槐树种子胚乳中提取的一种植物多糖胶[71]。LBG 以β-D-1,4 糖苷键连接的甘露糖为主链,在某些D-甘露糖基的1→6位上连接一个β-D-吡喃半乳糖,且半乳糖与甘露糖的比例为1∶4[72]。LBG 本身无法形成凝胶,由于在其分子构架上有相对较多的未被取代的甘露糖基能与其它天然胶(如卡拉胶、黄原胶、瓜尔豆胶等)形成复合体,得以形成或加强凝胶作用。槐豆胶与其它天然胶复配产生协同增效作用,可大大增加其黏度、凝胶能力及强度[71-76]。在工业生产中常常将LBG 与KGM 以及黄原胶、卡拉胶等多糖复配来增加其黏度、凝胶性、弹性等,从而扩大食品胶的使用范围并提高使用性能。
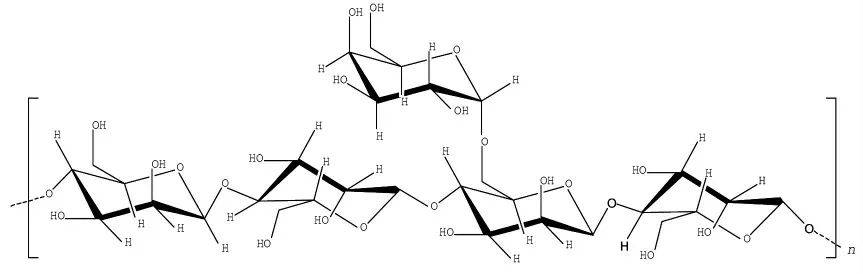
图8 LBG 分子结构式[71]Fig.8 Molecular structure formula of locust bean gum[71]
LBG 分子表现出具有D-甘露糖基残基的线性主链的嵌段结构,称为“平滑区域”,D-半乳糖基短残基与聚合物主链结合的区域称为“毛状区域”[77]。有研究对刺槐豆胶水溶胶的流变学性质进行表征,结果显示:刺槐豆胶水溶胶是一种非牛顿流体,属于假塑性流体中的触性流体。郭肖[72]对刺槐豆胶与黄原胶、卡拉胶、瓜尔豆胶、海藻酸钠、KGM 和罗望子胶等复配胶的流变学性质进行表征。结果表明,刺槐豆胶与黄原胶、卡拉胶、瓜尔豆胶复配产生“1+1>2”的协同作用;与海藻酸钠产生“1<1+1<2”的协同作用;与KGM 和罗望子胶产生“1+1<1”的拮抗作用。Sewall 等[20]、Tom 等[78]、Kun 等[79]研究了LBG-KC-KGM 三元复配体系的流变特性以及凝胶特性,研究发现LBG 与KC、KC与KGM 之间均具有协同作用,而三者的复配没有发生新的相互作用,仅是LBG 与KC 和KC 与KGM 两组分凝胶效果的综合。
2 结论
KGM 基凝胶具有生物降解性高、生物相容性好、环境响应性敏锐、固液共存等众多优势,因而成为众多科学工作者研究的焦点,被广泛应用于食品行业、医药领域、化工行业和功能材料等方面。KGM 基热可逆凝胶的应用性能很大程度上取决于复合体系中不同组分间的分子相互作用,因此本文从分子组装的角度出发,综述了KGM 分别与卡拉胶、琼脂、纤维素衍生物、结冷胶、黄原胶和刺槐豆胶形成热可逆凝胶的协同增效作用机理及相关性能研究,旨在为改善KGM 基热可逆凝胶强度和体系稳定性提供参考。

