抗肿瘤坏死因子-α诱导克罗恩病患者肠黏膜愈合情况的回顾性分析
卢立男,刘丹,刘冰熔
(郑州大学第一附属医院 消化内科,河南 郑州 450000)
克罗恩病(Crohn’s disease,CD)是受遗传、环境和肠道微生物群影响的具有多因素病因的异质性疾病,病因暂不明确,可累及胃肠道的任何部位,常导致狭窄、脓肿或瘘管等进行性并发症。大量研究证实与仅获得临床缓解相比,获得内镜下黏膜愈合可减少近期及远期并发症,改善CD病程和预后。2021年国际炎症性肠病研究组织发布的STRIDE-Ⅱ共识再次强调了内镜下黏膜愈合作为治疗炎症性肠病的关键长期目标[1]。经临床观察,内镜下回结肠各段对同一药物的反应不同步。最近发表的Versify试验是一项评估使用维得利珠单抗治疗CD的内镜缓解情况的开放性研究,显示内镜下CD病变的位置可能影响CD患者的内镜黏膜愈合率[2]。以英夫利昔单抗(infliximab,IFX)为代表的抗肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)药物被批准用于中、重度CD诱导及维持缓解多年,在降低手术率、减少CD复发方面显示出良好的疗效[3]。然而,关于其在回结肠不同节段(即末端回肠、升结肠、横结肠、降结肠和乙状结肠、直肠)诱导及维持黏膜愈合的疗效尚不清楚。明确CD患者回结肠不同肠段对IFX的不同反应有助于指导临床治疗,本研究回顾性分析了接受抗TNF-α治疗的CD患者,探讨接受治疗3个月及12个月后回结肠各节段黏膜愈合情况。
1 资料和对象
1.1 一般资料回顾性收集2018年10月至2021年6月在郑州大学第一附属医院接受抗TNF-α治疗的34例中、重度CD患者。资料收集过程如图1所示。所有患者在基线肠镜检查时均可见溃疡。(1)纳入标准:①由相关临床表现、影像学及病理等证据支持诊断为CD[4];②规范接受抗TNF-α药物(包括IFX或阿达木单抗)治疗1 a以上,用法遵循《抗肿瘤坏死因子α单克隆抗体治疗炎症性肠病专家共识(2017)》[5];③资料完整,接受抗TNF-α药物治疗前及治疗后第3个月和第12个月均进行了实验室指标检查、结肠镜检查。(2)排除标准:①肠道病变为狭窄或穿透性;②有回结肠切除或回肠吻合术病史;③抗TNF-α治疗期间罹患感染性疾病或出现肠道狭窄、穿孔、梗阻等并发症;④任一阶段内镜检查缺失;⑤接受抗TNF-α治疗期间对IFX或阿达木单抗诱导治疗无应答或维持治疗期间继发性失应答。
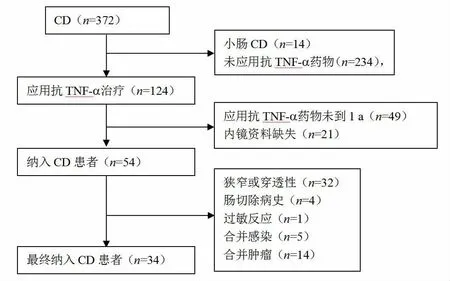
图1 CD患者筛选示意图
1.2 观察指标(1)基线资料:年龄、性别、体质量指数(body mass index,BMI)、病程、吸烟状况、病变部位、应用生物制剂种类。(2)比较治疗前、治疗3个月及12个月时炎症指标变化,包括C反应蛋白(Creactive protein,CRP)、红细胞沉降率。(3)内镜下表现:治疗前、治疗后第3、12个月各回结肠段(末端回肠、升结肠、横结肠、降结肠和乙状结肠、直肠)的内镜下黏膜愈合情况。黏膜愈合定义为先前被确定为结肠或回肠的至少1个区段有溃疡的患者,在后续内镜检查中所有区段均无黏膜溃疡(包括阿弗他溃疡)。
1.3 数据分析采用SPSS 25.0统计软件行数据处理。定量资料呈正态分布采用均数±标准差(±s)表示;偏态分布采用中位数和四分位数[M(P25,P75)]表示,组间比较采用Friedman检验,组间两两比较采用Bonferroni检验。定性资料用频数和百分数(%)表示;二分类重复测量资料用率及其95% CI表示,采用广义估计方程进行统计分析。P<0.05(双侧)为差异有统计学意义。
2 结果
2.1 基本资料应用抗TNF-α药物治疗的34例CD患者中男26例(76.5%),年龄(32.5±12.0)岁。应用抗TNF-α治疗前BMI为(21.1±2.9)kg·m-2,病程为24.0(12.8,36.0)个月,有吸烟史2例(5.9%)。根据蒙特利尔分类,疾病部位以回结肠病变型 为 主,共 26 例(76.5%),回 肠 型 有 8 例(23.5%),无单纯结肠病变型。接受生物制剂治疗类型以IFX单药治疗为主,有24例(70.6%);IFX合用硫唑嘌呤者其次,有6例(17.6%);IFX合用糖皮质激素者和单独应用阿达木单抗治疗者各有2例(5.9%)。
2.2 炎症指标评估采用Friedman检验,比较治疗前、治疗3个月和治疗12个月时34例CD患者接受抗TNF-α治疗的CRP水平显示总体差异有统计学意义(P<0.001)。采用Bonferroni法校正显著性水平后进行两两比较结果显示,34例CD患者接受抗TNF-α治疗3个月、12个月较治疗前CRP降低(P<0.05),治疗12个月与3个月相比差异无统计学意义(P>0.05)。34例抗TNF-α治疗患者治疗前、治疗3个月和12个月时红细胞沉降率总体差异有统计学意义(P<0.05),其中治疗3个月、12个月与治疗前相比红细胞沉降率下降(P<0.05),治疗12个月与3个月相比差异无统计学意义(P>0.05)。见表1。

表1 治疗前、治疗3个月、治疗12个月的炎症指标[M(P25,P75)]
2.3 内镜下黏膜愈合情况广义估计方程整体检验(表2)和参数估计结果(表3)显示,不同部位及不同时间点的CD病变黏膜愈合率差异有统计学意义(P<0.001)。除末端回肠外,结肠各部位不同时间点总体黏膜愈合率差异有统计学意义(P<0.05)。其余回结肠段黏膜愈合率较治疗前无明显变化(P>0.05)。横结肠及升结肠的黏膜愈合情况优于其他回结肠段。治疗3个月时,50.0%(13/26)的横结肠和35.7%(10/28)的升结肠节段实现黏膜愈合,差异有统计学意义(P<0.05)。治疗12个月时,84.6%(22/26)的横结肠和67.9%(19/28)的升结肠、32.0%(8/25)降结肠和乙状结肠、28.0%(7/25)直肠病变实现内镜下黏膜愈合,与治疗前及治疗3个月相比差异有统计学意义(P<0.05)。不同部位CD病变经抗TNF-α药物治疗前及诱导黏膜愈合后图像见图2。
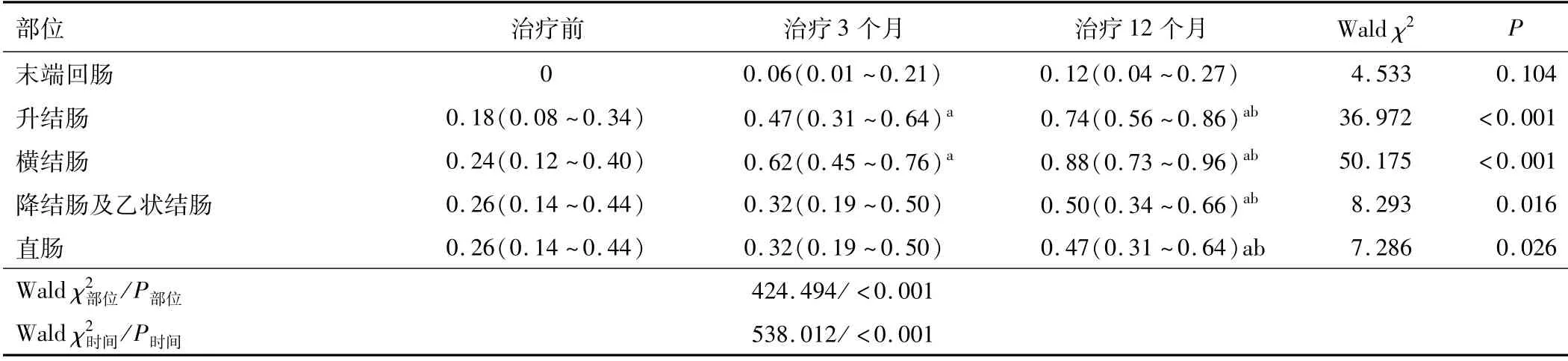
表2 治疗前、治疗3个月、治疗12个月不同部位黏膜病变愈合率及95% CI
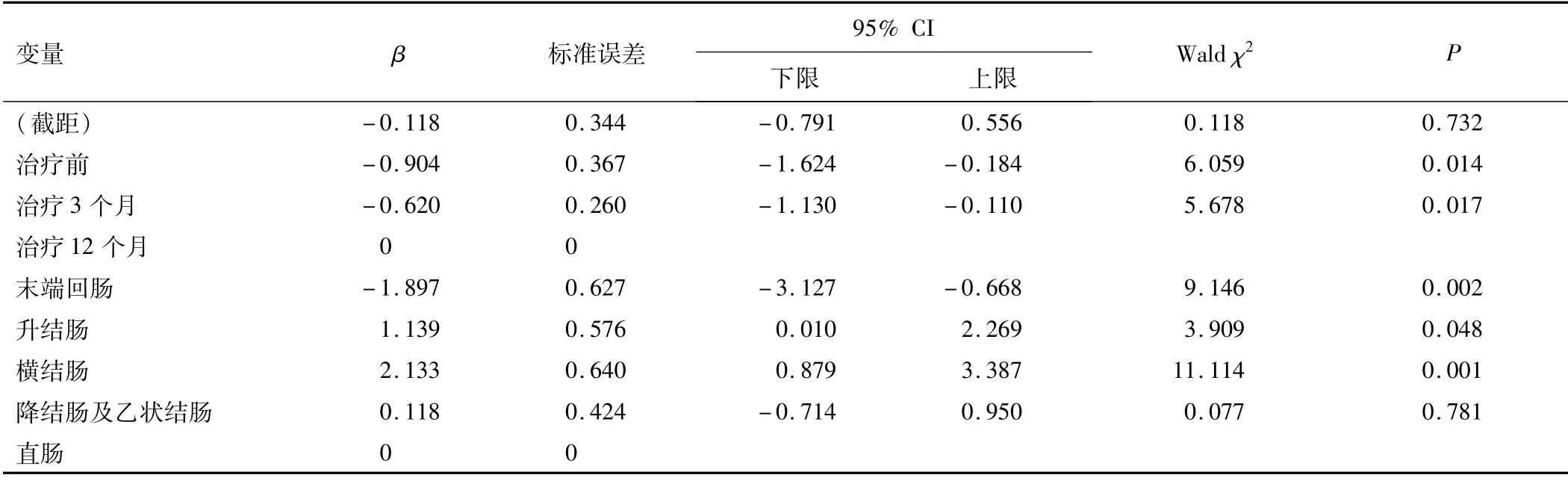
表3 广义估计方程参数估计结果

图2 抗肿瘤坏死因子(TNF)治疗前及诱导黏膜愈合后克罗恩病(CD)病变内镜图像
3 讨论
随着对CD病因和发病机制研究的深入,不同部位CD表现出越来越多的差异。CD遗传易感性分析显示,疾病位置是CD疾病的一个内在方面,部分由遗传决定,并且是疾病行为随时间变化的主要驱动因素,如NOD2对疾病行为的影响完全是由其与疾病部位的关联驱动的[6]。肠道微生态在CD发病中起关键作用,对肠道不同节段的微生物区系进行分析显示盲肠微生物群比空肠和回肠复杂,直肠及乙状结肠微生物群落种类更多,每个区域的微生物群组成存在差异[7]。同样,回肠和结肠CD溃疡边缘的蛋白质组学分析也显示出不同的病理生理过程[8]。CD可累及胃肠道的各个位置,不同位置疾病进展风险或并发症的表现不同[9]。现有的CD蒙特利尔表型分类法根据病变累及部位不同将CD大致分为累及回肠末段型、结肠型、回结肠型、上消化道型,这一分类显然不能满足目前CD危险分层的需求。已有证明经抗TNF-α治疗后,小肠CD溃疡比回结肠CD溃疡更难愈合,但是目前对于抗TNF-α治疗对回结肠不同节段的改善作用了解仍有限[10]。
本研究统计了抗TNF-α诱导和维持治疗后,34例CD患者各个回结肠段的黏膜病变和黏膜病变愈合情况,结果显示,不同回结肠段病变对抗TNF-α治疗的反应不同,总体结肠段改善优于回肠段。与治疗前相比,接受抗TNF-α诱导治疗3个月后有35.7%的升结肠段及50.0%的横结肠段CD病变黏膜愈合,维持治疗12个月后只有末端回肠与治疗前相比黏膜愈合无明显改善。这可能受到抗TNF-α药物诱导肠道炎症消退机制的影响。本研究结果与其他研究结论存在差异。在Versify试验中,接受维得利珠单抗治疗52周后,横结肠CD内镜缓解率最高,其次为降结肠、直肠、升结肠,末端回肠最低[2]。不同部位的CD病变对同一药物的反应存在差异,不同药物对CD各节段诱导及维持缓解的反应不同。TAILORIX研究对122例病程较短、生物幼稚的CD患者内镜缓解相关的危险因素进行无反应者归因分析,12周时内镜愈合与CD在基线内镜下的位置、性别、肠外CD表现以及基线时有无溃疡性狭窄相关,到第54周时内镜愈合仅与基线内镜下的CD位置相关[11]。这表明无论作用机制如何,疾病部位都会影响CD内镜检查结果[12-13]。这一发现提供了根据特定的受累部位调整治疗抗TNF-α策略以增强反应的可能性。远端和近端回结肠区域的愈合不一致也意味着所有节段的结肠镜检查对于全面评估疾病活动性是重要的,远端结肠黏膜愈合不能代表近端回结肠黏膜愈合情况。本研究排除了狭窄及穿透性CD,因狭窄性及穿透性病变是影响CD黏膜愈合的独立危险因素,常需要手术等单独的治疗策略,会对病变部位这一变量产生较大的干扰,影响探讨病变位置这一变量对抗TNF-α治疗CD结果的准确性。
生物制剂开创了CD靶向治疗的新时代,其良好的抗炎作用能够诱导患者获得临床症状、生物化学指标的好转及黏膜缓解愈合,改善CD自然病程及患者预后。随着生物制剂种类的增多,可用于CD治疗的选择增加,按照部位对CD进行分型可以对疾病进展风险较高、预后较差的患者进行分层,以此筛选出能够早期从生物制剂(或联合治疗)中受益的患者,也可以针对不同部位CD选择最佳药物治疗方案或药物排序,这也对CD的诊断和评估提出了更高的要求[14]。
综上所述,回结肠不同肠段CD病变对抗TNF-α治疗的反应不同,结肠段总体黏膜愈合情况优于末端回肠,横结肠和升结肠的黏膜愈合率最高。不同回结肠段黏膜愈合率的差异有助于对CD患者进行危险度分层,实现生物制剂的个体化治疗。病变部位对抗TNF-α药物治疗CD黏膜愈合的影响需要前瞻性研究进行验证。

