超高效液相色谱与单四极杆质谱法同时测定胃复春片中7个成分含量
崔雨晴,米卓尔,刘傲雪,周丹丹,沙禕炜
[鉴甄检测技术(上海)有限公司,上海 200131]
胃复春片是由红参、香茶菜、麸炒枳壳3味药制成的复方制剂,是国家中药保护品种,临床用于慢性萎缩性胃炎、胃癌前病变、慢性浅表性胃炎、胃及十二指肠溃疡等,具有疗效好、安全性高等特点。研究[1-4]表明,人参皂苷及其代谢产物具有显著的抗肿瘤作用,尤其是人参经蒸制成红参后,转化的新成分能够加强抗肿瘤效果;香茶菜中二萜类、酚酸类、黄酮类成分,具有抑菌消炎、抗肿瘤、免疫调节等作用;枳壳中黄酮类成分,具有抗肿瘤、抗微生物、抗炎等作用。上述化学成分构成胃复春片的复杂体系,共同发挥健脾益气、活血解毒之功效。2020年版《中华人民共和国药典》以红参对照药材、人参皂苷Rb1、Re、Rg1对照品作为参照,对制剂中红参进行薄层鉴别。含量测定项仅对麸炒枳壳中柚皮苷进行含量测定。现行标准对制剂中的香茶菜未作任何质量控制,故无法有效控制胃复春片的质量。本研究采用超高效液相色谱(ultra high performance liquid chromatography,UPLC)串联单四极杆质谱(quadrupole dalton,QDA)法测定胃复春片中橙皮苷,新橙皮苷,迷迭香酸,人参皂苷Re、Rg1、Rf、Rb1成分的含量,以期为胃复春片质量标准的提升提供参考。
1 仪器与试药
1.1 仪器 Waters Acquity H-Class-QDA超高效液相色谱-质谱联用仪:沃特世科技有限公司;XSE105DU电子天平:梅特勒-托利多仪器有限公司;MS204TS/02电子天平:梅特勒-托利多仪器有限公司;P120H超声仪:德国Elma Schmidbauer GmbH;Elix Advantage 15超纯水制备仪:默克密理博。
1.2 试药 新橙皮苷(纯度97.8%,批号 8177):购自上海诗丹德生物技术有限公司;橙皮苷(纯度95.3%,批号 110721-202019)、迷迭香酸(纯度90.5%,批号 111871-201706)、人参皂苷Re(纯度93.9%,批号 110754-202028)、人参皂苷Rg1(纯度93.4%,批号 110703-201933)、人参皂苷Rf(纯度99.3%,批号 111719-201806)、人参皂苷Rb1(纯度93.1%,批号 110704-202028):购自中国食品药品检定研究院。色谱纯乙腈:默克公司;色谱纯甲醇:默克公司;质谱纯甲酸:赛默飞世尔科技有限公司;分析纯甲醇:上海泰坦科技有限公司。14批胃复春片、缺红参阴性制剂、缺麸炒枳壳阴性制剂和缺香茶菜阴性制剂均由杭州胡庆余堂药业有限公司提供。
2 方法与结果
2.1 溶液的制备
2.1.1 对照品溶液制备 精密称取橙皮苷、新橙皮苷、迷迭香酸、人参皂苷Re、人参皂苷Rg1、人参皂苷Rf、人参皂苷Rb1对照品适量,加甲醇制成每毫升含橙皮苷6 μg、新橙皮苷80 μg、迷迭香酸8 μg、人参皂苷Re 8 μg、人参皂苷Rg16 μg、人参皂苷Rf 3 μg、人参皂苷Rb115 μg的混合对照品溶液。
2.1.2 供试品溶液制备 取本品研细,精密称定0.5 g,置具塞锥形瓶中,精密加入50%甲醇溶液50 mL,密塞,称定质量,超声处理(功率330 W,频率37 kHz)30 min,放冷,再称定质量,用50%甲醇溶液补足减失的质量,摇匀,滤过,取续滤液作为供试品溶液。同法制备阴性样品溶液。
2.2 色谱条件 色谱柱:Waters X-select HSS T3(3.0 mm×150 mm,2.5 μm);流速:0.5 mL/min;流动相:乙腈(A)-0.05%甲酸水溶液(B)。梯度洗脱程序如下:0~4 min,25%~26% A;4~5 min,26%~34% A;5~8 min,34%~35% A;8~10 min,35%~50% A;10~12 min,50%~95% A;12~13 min,95%~25% A;13~16 min,25% A。柱温:30 ℃;进样量:1 μL;采用电喷雾离子源(ESI源),负离子检测,选择性离子监测模式(SIR),毛细管电压为0.8 kV,离子源温度为600 ℃,以m/z609.13(橙皮苷、新橙皮苷,锥孔电压20 V)、m/z359.15(迷迭香酸,锥孔电压15 V)、m/z991.47(人参皂苷Re,锥孔电压15 V)、m/z845.49(人参皂苷Rg1、人参皂苷Rf,锥孔电压15V)、m/z1 107.60(人参皂苷Rb1,锥孔电压40 V)为测定离子。
2.3 方法学考察
2.3.1 专属性 分别精密吸取空白溶液、混合对照品溶液、供试品溶液和阴性样品溶液各1 μL,进样测定,记录色谱图。各通道内样品色谱图中出现与对照品色谱图中保留时间一致的色谱峰。色谱图见图1。
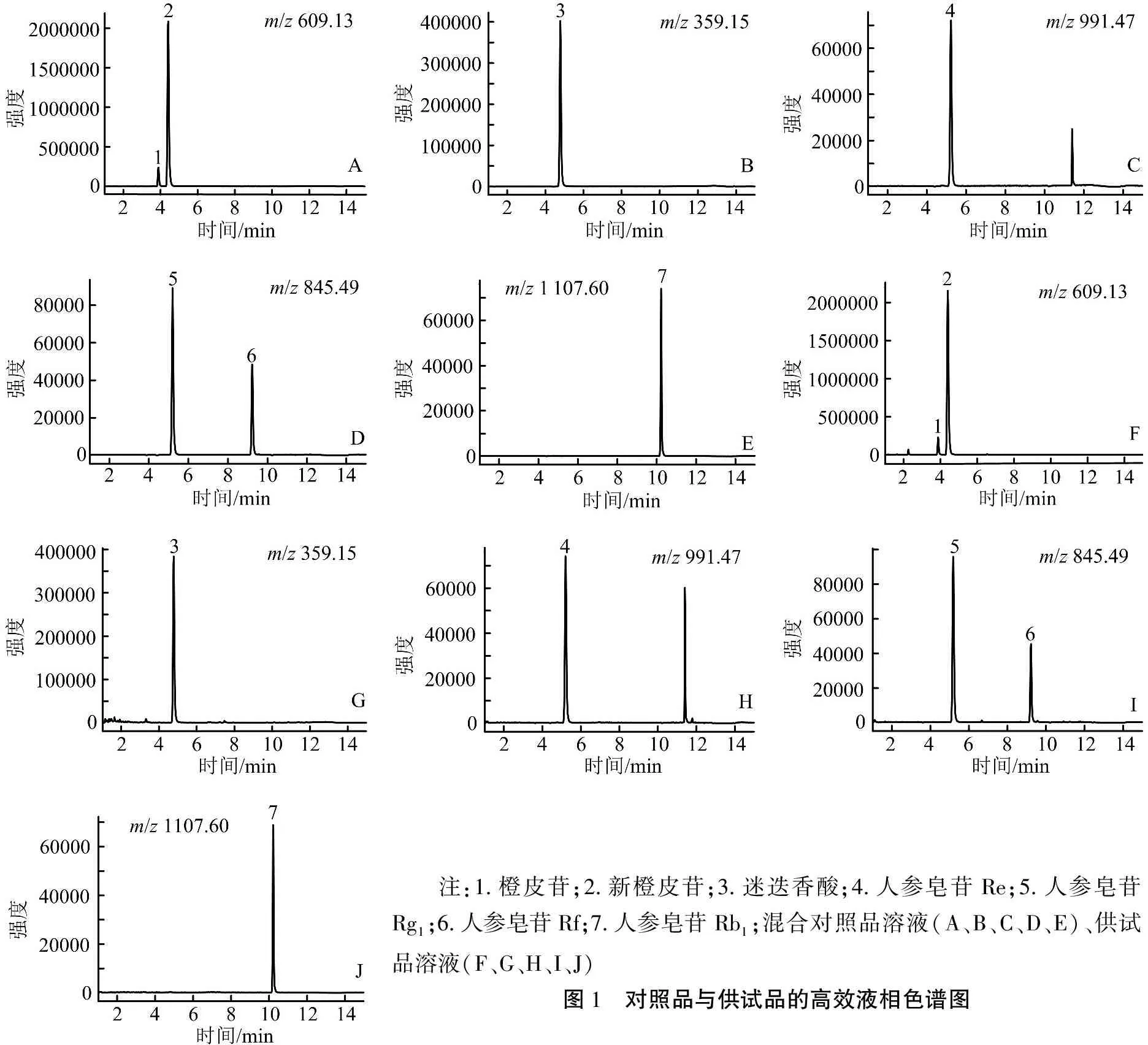
注:1.橙皮苷;2.新橙皮苷;3.迷迭香酸;4.人参皂苷Re;5.人参皂苷Rg1;6.人参皂苷Rf;7.人参皂苷Rb1;混合对照品溶液(A、B、C、D、E)、供试品溶液(F、G、H、I、J)图1 对照品与供试品的高效液相色谱图
2.3.2 线性方程、检测限和定量限 取橙皮苷、新橙皮苷、迷迭香酸、人参皂苷Re、Rg1、Rf、Rb1的混合对照品溶液,用甲醇稀释配制为7个不同浓度的混合对照品溶液,进样分析。以对照品的峰面积(y)对相应的浓度(x)进行线性回归,得回归方程、相关系数和线性范围;以各化合物的信噪比(S/N)等于3时相对应的浓度确定为最低检测限(limit of detection,LOD),以各化合物的信噪比(S/N)等于10时相对应的浓度确定为最低定量限(limit of quantity,LOQ)。见表1。

表1 胃复春片中7个成分的标准曲线和LOD、LQD
2.3.3 精密度 取混合对照品溶液,连续进样6次。橙皮苷、新橙皮苷、迷迭香酸、人参皂苷Re、人参皂苷Rg1、人参皂苷Rf、人参皂苷Rb1峰面积的RSD分别为1.0%、0.5%、2.2%、0.8%、0.8%、2.2%、2.1%,表明仪器精密度良好。
2.3.4 重复性 按“2.1.2”项下供试品溶液的制备方法,平行制备6份供试品溶液(样品批号:19066119),测定橙皮苷、新橙皮苷、迷迭香酸、人参皂苷Re、人参皂苷Rg1、人参皂苷Rf、人参皂苷Rb1的峰面积,计算含量。6份样品中橙皮苷、新橙皮苷、迷迭香酸、人参皂苷Re、Rg1、Rf、Rb1含量的RSD值分别为0.6%、0.5%、2.2%、1.1%、1.0%、1.2%、0.8%,表明样品重复性良好。
2.3.5 稳定性 同一供试品溶液在室温条件下放置0、2、4、8、12、24 h后,进样测定。样品中橙皮苷,新橙皮苷,迷迭香酸,人参皂苷Re、Rg1、Rf、Rb1含量RSD值分别为2.1%、1.5%、1.4%、2.1%、2.5%、2.0%、3.4%,表明供试品溶液在24 h内稳定。
2.3.6 加样回收率试验 精密称取6份已知含量的胃复春片0.25 g,精密加入一定量的混合对照品溶液,使其加入量与所取胃复春片中各指标成分量之比控制在1∶1左右。按“2.1.2”项下制备供试品溶液,进样测定,计算橙皮苷,新橙皮苷,迷迭香酸,人参皂苷Re、Rg1、Rf、Rb1平均回收率依次为89.3%、99.9%、101.2%、94.4%、91.8%、90.4%、94.2%,RSD分别为1.5%、1.3%、2.1%、3.1%、3.5%、3.1%、2.8%,表明方法准确度良好。
2.3.7 耐用性考察 采用不同流速(0.4、0.5、0.6 mL/min);不同柱温(28、30、32 ℃);不同色谱柱Waters X-select HSS T3(3.0 mm×150 mm,2.5 μm)、Agilent Infinity Lab Poroshell 120 EC-C18(3.0 mm×150 mm,2.7 μm)和Waters CORTECS®T3(4.6 mm×150 mm,2.7 μm)测定同一批次样品成分含量,各成分含量RSD值均小于5%,方法耐用性良好。
2.3.8 样品含量测定 取14批胃复春片样品,分别按“2.1.2”项下制备供试品溶液,进样测定,计算含量,结果14批胃复春片样品每片含橙皮苷(0.19±0.02)mg、新橙皮苷(2.78±0.16)mg、迷迭香酸(0.48±0.21)mg、人参皂苷Re (0.23±0.02)mg、人参皂苷Rg1(0.18±0.01)mg、人参皂苷Rf(0.08±0.01)mg、人参皂苷Rb1(0.47±0.06)mg。
3 讨论
3.1 指标性成分的选择 胃复春片物质基础研究[5]表明,枳壳中主要含柚皮苷、橙皮苷、新橙皮苷等黄酮类成分,其中柚皮苷含量最高,2020年版《中华人民共和国药典》标准中仅测定柚皮苷的含量,为了更全面反映制剂中枳壳质量,选取橙皮苷、新橙皮苷为测定指标。红参为生粉入药,人参皂苷类成分具有较弱的紫外吸收,且在制剂中的含量较低,传统的紫外检测器的灵敏度较差。2020年版《中华人民共和国药典》标准中仅以人参皂苷的定性鉴别难以真实反映其质量,故选取人参皂苷Re、Rg1、Rf、Rb1为定量测定指标。香茶菜并未被2020年版《中华人民共和国药典》收载,其在处方中用量最大。本研究选择酚酸类迷迭香酸作为指标性成分对其进行质量控制。
3.2 检测方法的选择 中药复方的化学成分较复杂,采用高效液相色谱分析时间较长。王桂峰等[6]建立高效液相色谱法同时测定胃复春片中的人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1、柚皮苷、新橙皮苷,检测时间为60 min。张红霞等[7]采用高效液相色谱串联质谱法同时测定胃复春片中的11种成分(柚皮苷、人参皂苷Re、人参皂苷Rg1、人参皂苷Rb1、人参皂苷Rf、人参皂苷Rb2、人参皂苷Rg2、人参皂苷Rd、人参皂苷20(R)-Rg3、冬凌草甲素、表诺多星醇)的含量。由于高效液相色谱串联质谱法仪器的价格高昂,维护成本高,普及程度低等特点,无法满足中药企业日常的样品检验需求,方法的实际应用性不高。QDA检测器是一种质谱检测器,能够与液相分离系统完美兼容,对紫外检测器或二极管阵列检测器进行有效的补充。QDA检测器可以获得相当于单四极杆质谱仪的质谱信息,其价格相对较低,操作简单,维护保养方便,在药品分析领域的应用越来越多[8-9]。
3.3 实验条件的优化 锥孔电压是影响QDA检测器相应信号强弱的关键参数,在参数可调的范围内,以样品中所含各成分色谱峰的峰面积为考核指标对其进行优化。通过加酸来调节流动相的pH,促进化合物的离子化,改善峰形。本实验考察了乙腈-0.02%甲酸、乙腈-0.05%甲酸、乙腈-0.1%甲酸、乙腈-0.05%甲酸(含2 mmol/L甲酸铵)等,结果发现,乙腈-0.05%甲酸的响应值比较稳定,且峰形对称。同时,分别考察了提取溶剂、提取时间、料液比对成分提取的影响,优选的供试品制备方法为50%甲醇为溶剂,料液比为1∶100,超声时间30 min。
3.4 样品的测定 采用UPLC-QDA法对14批胃复春片中的黄酮类、酚酸类、人参皂苷类成分进行测定。结果表明,不同批次间胃复春片的黄酮类和人参皂苷类成分含量相差不大,而香茶菜中迷迭香酸含量范围为每片0.27~1.05 mg(RSD=43.7%),表明投料用药材质量差异较大。本研究建立的UPLC-QDA法同时测定7个指标成分含量,可全面反映复方中麸炒枳壳、香茶菜、红参药材的质量,能够有效地监控产品的稳定性,为其质量提供保障。

