慢性阻塞性肺疾病患者INOS、HIF-1α及PPAR-γ的表达及与气流阻塞的相关性研究
王纪伟 孙晓丽 景小丽
郑州阳城医院呼吸内科,河南省登封市 452470
慢性阻塞性肺疾病(Chronic obstructive pulmonary disease,COPD)是由于气道炎症的存在,导致呼吸系统产生病理生理改变,能进一步发展为肺心病和呼吸衰竭的慢性疾病[1]。炎症细胞分泌高浓度蛋白酶和氧化产物引起的氧化应激是COPD的主要发病机制,由于气道分泌物增多,慢性咳嗽、咳痰、气短和呼吸困难成为本症典型症状[2]。
过氧化物酶增殖物激活受体(Peroxisome proliferactor-activited receptors,PPARs)是核激素受体家族中的配体激活受体,目前已发现包括PPAR-α、PPAR-β/δ、PPAR-γ在内的三个亚型[3]。PPAR-γ是重要的细胞分化转录因子,在人体的脂肪组织、血管平滑肌组织、心肌组织中均有表达[4]。其中气道上皮组织中的PPAR-γ可对细胞活素介导的诱生型一氧化氮合酶(Inducible nitric oxide synthase,INOS)的表达产生抑制作用,而INOS作为一种同工酶,当其表达受到抑制时,其在免疫系统对抗病原体的能力也得到削弱[5]。此外,低氧诱导因子(Hypoxia-inducible,HIF-1)是一种调节氧稳态的核心转录因子,由HIF-1α及HIF-1β两个亚基组成[6]。近年来有研究发现,在伴有不同程度缺氧的COPD患者中HIF-1出现异常表达,推测其与气道炎症、重塑及肺动脉高压等病理改变有密切关系[7]。目前关于INOS、HIF-1α及PPAR-γ在COPD患者中的表达及临床意义存在诸多争议,本研究通过研究COPD患者血清和肺组织中INOS、HIF-1α及PPAR-γ的表达和变化,并分析其与气流阻塞之间的关系,现报道如下。
1 资料与方法
1.1 一般资料 回顾性分析我院2018年9月—2019年9月因肺部占位性病变行支气管镜检查的217例患者临床资料,根据吸烟史、有无COPD史及肺功能检查将受试者分为三组:A组(72例COPD患者)、B组(70例吸烟肺功能正常者)及C组(75例不吸烟肺功能正常者),三组性别、年龄、体质指数比较无显著差异(P>0.05),A组、B组吸烟指数比较无显著差异(P>0.05),见表1。

表1 三组一般资料比较
A组纳入标准:满足COPD诊疗标准[8]者;临床资料完整者;无支气管哮喘病史。排除标准:合并严重重要器脏疾患者;合并除COPD以外的其他肺部疾病者;入组前3个月内有呼吸、消化系统感染者。B、C组近2个月均无呼吸系统疾病史,且体格检查、胸部X线摄片及肺通气功能测定均未见异常。
1.2 研究方法 收集所有研究对象临床资料,比较不同人群一般资料、肺功能指标、INOS、HIF-1α及PPAR-γ表达的水平,并分析其与气流阻塞程度的相关性。其中,通气指标[第1秒用力呼气容积(FEV1)、用力肺活量(FVC)及FEV1/FVC]以70%为界,分为≥70%和<70%, 而<70%部分又以依次递减10%再分级, 以此表达气流阻塞的严重程度。
1.3 检测方法
1.3.1 标本收集:所有研究对象术前于空腹状态下抽取静脉血5ml,离心(3 000r/min,15min)后取血清,并保存在-20℃冰柜中。术前雾化吸入2%利多卡因麻醉气道,取仰卧位,给予鼻塞吸氧和心电监护,支气管镜经鼻腔进入气道,活检部位选择肺占位病变的对侧叶支气管间脊,钳取组织置于多聚甲醛中固定、梯度酒精脱水、透明后石蜡包埋,做2μm厚切片以备免疫组织化学抗体染色用。
1.3.2 试剂:鼠抗人PPAP-γ一抗及兔抗人INOS、HIF-1α均购自Santa cruze公司,即用型SP试剂盒、DAB染色试剂及苏木素盒购自北京中杉金桥有限公司。
1.3.3 免疫组化肺组织INOS、HIF-1α及PPAR-γ的表达:制备聚赖氨酸防脱切片,常规脱蜡、抗原修复及山羊血清封闭。严格按照试剂盒检查步骤,并进行DAB染色、苏木素复染,然后脱水封片。在显微镜400倍下用全自动图像分析系统对阳性染色进行分析,测定三者的平均吸光度值,随机检测4个高倍视野后计算平均值,作为该切片的代表值。
1.3.4 肺功能测定:COPD患者于早起时吸入支气管扩张剂后用肺功能仪检测肺功能,反复检测3次,取最高值,记录FEV1、FVC及FEV1/FVC。

2 结果
2.1 三组肺功能比较 A组FEV1、FVC及FEV1/FVC较B组、C组低,差异有统计学意义(P<0.05),而B、C组FEV1、FVC及FEV1/FVC比较无显著差异(P>0.05),见表2。

表2 三组肺功能指标比较
2.2 INOS、HIF-1α及PPAR-γ免疫组织化学平均吸光度值比较 A组和B组间INOS、HIF-1α及PPAR-γ表达比较无显著差异(P>0.05);C组INOS、HIF-1α表达水平较A组、B组低,PPAR-γ表达水平较A组、B组高,差异有统计学意义(P<0.05),见表3。
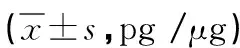
表3 三组INOS、HIF-1α及PPAR-γ免疫组织化学平均吸光度值比较
2.3 INOS、HIF-1α及PPAR-γ表达与肺功能相关性 PPAR-γ与FEV1、FVC及FEV1/FVC呈正相关(P<0.05),INOS、HIF-1α与FEV1、FVC及FEV1/FVC呈负相关(P<0.05),见表4。

表4 INOS、HIF-1α及PPAR-γ表达与肺功能相关性分析
3 讨论
COPD是一种常见的、治疗耗资较高的可预防性慢性呼吸系统疾病,可对人们日常生活能力造成严重影响。在COPD的影响下,呼吸道中多个器官组织的结构被破坏,可出现相应的病理生理学改变[9]。其中持续的气道阻塞是本病的主要特点,随着COPD的进展,长期慢性缺氧可导致肺血管功能异常,造成肺循环的结构重组[10]。因此对参与COPD气道阻塞发生和发展的相关指标水平进行研究,对评估患者疾病严重程度等方面有重要意义。
3.1 INOS与COPD 一氧化氮合酶为一种重要的同工酶,在内皮细胞、巨噬细胞、神经吞噬细胞及神经细胞等中都有着广泛的分布。INOS是一氧化氮合酶的亚型之一,其生物活性、调节方式等有一定的特性[11]。由于INOS为非钙离子依赖型,在静息细胞中无表达,而当细胞受到炎症因子或免疫微生物刺激时则会催化合成大量一氧化氮[12]。而一氧化氮可参与机体氧化还原过程,并产生一氧化氮分子使血管扩张,当机体内一氧化氮浓度高于生理浓度时,可造成严重的氧化损伤。此外,一氧化氮的代谢产物可活化基质金属蛋白酶,降解肺实质的组分细胞外基质,导致肺气肿等的发生,且此种作用机制在COPD的发展中发挥着关键作用[13]。杨加鹏等[14]研究发现,肺癌患者INOS表达升高,认为肺部无机物的赋存及INOS参与的相关信号通路的激活促进了肺部病变的发生。另外在鼠实验[15]中也发现,注入高剂量羟基红花黄色素A的大鼠INOS水平显著升高。本研究结果显示,A组和B组患者INOS的表达均较C组强,通过相关性分析亦发现INOS与FEV1、FVC及FEV1/FVC呈负相关(P<0.05)。由此可证实,COPD患者支气管黏膜中可分泌高浓度INOS,而INOS及其代谢物可使肺组织脂质过氧化,高浓度下可加重肺功能损伤,形成一个恶性循环。值得注意的是,吸烟能导致人体血浆中脂质过氧化物的增加,加速COPD的形成。
3.2 HIF-1α与COPD HIF-1α为具有转录活性的核蛋白,具有相当广泛的靶基因谱,包括炎症发展、缺氧适应及肿瘤生成等相关的靶基因[16]。当其与相关的靶基因结合后,通过转录和转录后调控可产生一系列相应的反应,通常会给机体带来病理性损害。近年来,关于COPD病理改变与HIF-1α的关系引起人们重视。由于HIF-1α可促进趋化因子释放介导气道炎症及起到重塑,改变气道内纤维功能,导致黏膜黏液的高分泌。鞠鑫鹏等[17]研究发现COPD合并肺部癌变组织HIF-1α呈强阳性表达,经相关性分析发现肺组织匀浆HIF-1α与肺功能指标负相关,并推测其与肺功能的异常改变有关。本研究结果显示,HIF-1α在A组和B组的支气管黏膜上皮细胞、肺泡巨噬细胞的胞浆中表达增强,免疫组织化学平均吸光度值也高于C组(P<0.05);进一步通过相关性分析,发现HIF-1α与FEV1、FVC及FEV1/FVC呈负相关(P<0.05),提示HIF-1α表达与COPD患者气道阻塞关系密切。
3.3 PPAR-γ与COPD PPARs是一类配体依赖的转录调节因子,具有N端区、居中高保守DNA结合区和C端的激素结合区。其配体通常为脂溶性分子,当其与各自的配体结合后可引起机体的变化,促进或抑制靶基因的表达。PPAR-γ作为其主要的亚型之一,与多种炎性细胞的活性和表达关系密切。其在原位支气管气道上皮细胞中有表达,可抑制此类细胞的活性,并激活内源性PPAR-γ,拮抗炎性反应。Raoufy等[18]认为PPAR-γ具有改变巨噬细胞的转运,增加巨噬细胞吞噬功能等作用,可促进实用性免疫反应的发生,减轻包括COPD在内的多种疾病状态。而李巧荣[19]发现吸烟可导致COPD患者及肺功能正常患者支气管黏膜组织PPAR-γ表达增强,认为其可能与烟草导致肺功能下降有关。而这基本与本研究关于PPAR-γ的结果一致,进一步提示其表达可反映COPD患者气道阻塞程度。
综上所述,COPD患者INOS、HIF-1α表达增强,而PPAR-γ表达减弱;INOS、HIF-1α及PPAR-γ与气道阻塞有显著的相关性,在诱导机体PPAR-γ的表达或提高其活性,对缓解COPD患者肺功能下降有一定作用,可作为临床治疗的新思路。

