心力衰竭患者25-羟基维生素D3缺乏与血管内皮功能异常及动脉粥样硬化程度的相关性分析
黄文霞,李海涛,黄玉冰,廖旺
(海南省人民医院·海南医学院附属海南医院心血管内科,海南 海口 570311)
心力衰竭是指由于心脏的收缩功能和(或)舒张功能发生障碍,导致静脉系统血液淤积,动脉系统血液灌注不足,从而引起的心脏循环障碍症候群,是心脏疾病的终末阶段[1]。动脉粥样硬化是由于脂肪、血栓、结缔组织和碳酸钙等在血管内沉积所造成的一种血管异常状态,可导致动脉壁增厚变硬、血管腔狭窄,是冠心病的重要病理基础[2]。而血管内皮功能异常也是动脉硬化发展为多种心血管事件的关键原因[3]。随着心力衰竭发病机制和临床诊治相关研究的不断深入,心力衰竭与血管内皮功能异常及动脉粥样硬化的密切相关性已得到证实。血清25-羟维生素D3[25-hydroxy vitamin D3,25(OH)D3]是维生素D在血液循环中存在的主要形式,参与多种心血管疾病的发生发展[4],其中以高血压[5]、慢性阻塞性肺疾病[6]和冠心病[7]等报道较多,但其与心力衰竭病理过程和预后转归的关系仍未明确。25(OH)D3还影响肾素血管紧张素醛固酮系统活性,可调节内皮功能[8]。本研究拟探讨25(OH)D3与血管内皮功能异常及动脉粥样硬化程度的相关性。
1 资料与方法
1.1 一般资料
选取2017年2月至2020年2月海南省人民医院收治的80例心力衰竭患者作为研究对象。所有患者中,男性46例,女性34例;年龄34~72岁,平均(56.46±8.76)岁;美国纽约心脏病协会(New York Heart Association,NYHY)心功能分级[9]:Ⅰ级23例,Ⅱ级19例,Ⅲ级24例,Ⅳ级14例。根据入院时25(OH)D3水平分为25(OH)D3缺乏组[25(OH)D3<15 ng/mL,n=48]和非25(OH)D3缺乏组[25(OH)D3≥15 ng/mL,n=32]。25(OH)D3缺乏组中,男性25例,女性23例;年龄35~70岁,平均(56.71±8.45)岁;NYHY心功能分级:Ⅰ级15例,Ⅱ级11例,Ⅲ例14例,Ⅳ8例。非25(OH)D3缺乏组中,男性15例,女性17例;年龄36~72岁,平均(56.84±8.43)岁;NYHY心功能分级:Ⅰ级8例,Ⅱ级8例,Ⅲ例10例,Ⅳ6例。两组一般资料比较,差异无统计学意义(P>0.05)。纳入标准:(1)符合心力衰竭的诊疗标准[10];(2)临床资料完整且自愿签署知情同意书;排除标准:(1)合并恶性肿瘤者;(2)合并精神疾病、痴呆和意识障碍等无法配合研究者;(3)合并代谢功能障碍,包括甲状腺功能异常、甲状旁腺疾病、通风等;(4)合并严重脑血管疾病者;(5)合并肝、肾功能异常者;(6)合并急性损伤、急慢性感染性疾病者。
1.2 检测方法
(1)25(OH)D3检测:入选对象于住院次日空腹抽取肘静脉血 5 mL,静置30 min后离心(3 000 rpm,15 min)取上清液。酶联免疫吸附测定(ELISA)法检测5(OH)D3水平,试剂盒购自南京森贝伽生物科技有限公司。检测步骤:样本混入标准液中,37 ℃温箱孵育2 h;反复3次洗涤液冲洗;加一抗工作液100 μL,37 ℃温箱孵育1 h;反复冲洗3次,拍干。加入辣根过氧化物酶标记链霉亲和素工作液100 μL;37 ℃温箱孵育0.5 h,洗涤液冲洗3次,拍干;每孔加底物工作液100 μL,避光37 ℃温箱孵育15 min;加终止液100 μL;测定光密度(optical density,OD)值,以OD值为纵坐标,标准品为横坐标绘制标准线,计算血清25(OH)D3水平。将25(OH)D3<15 ng/mL定义为缺乏[11]。(2)血管内皮功能检测:嘱患者检查前24 h停止使用血管活性药物、他汀类药物、阿司匹林等,静卧20 min后开始检查。检测仪器为以色列Itamar Medical公司生产的Endo-PAT2000内皮功能检测仪。患者取仰卧位,固定PAT探头后,嘱患者手指插入探头内,充气。随后将手指拿出,使探针悬空,在手指根部放置定位环。将袖带束于另一侧肘上2 cm处,PAT基线稳定5 min后开始充气。检测袖臂带充气前与放气后的PAT信号比率,即可得出反应性充血指数(reactive hyperemia index,RHI)。正常情况下RHI>1.67,内皮功能障碍时RHI≤1.67[12]。RHI值越高,血管内皮功能越好。
1.3 观察指标
(1)动脉粥样硬化程度:颈动脉超声检测采用美国Philips公司生产的HP5500型超声心动图仪,配备7~13 MHz的探头。患者取仰卧位,暴露检查部位。分别从双侧颈总动脉、颈动脉分叉处及颈内动脉起始部及颈内动脉的近侧壁和远侧壁进行纵向和横向扫描、图像采集及处理。检测内容包括颈动脉内膜中膜厚度(intima-media thickness,IMT)的测定及对粥样斑块的探测。动脉粥样硬化诊断标准[13]:IMT≥1 mm或存在动脉斑块(超声表现为局部隆起、增厚并向腔内突出,一般厚度在1.2 mm以上,回声均匀并显著增强,回声后方伴有声影;软斑表现为回声与内中膜相近,后方并无声影;混合性斑块表现为以上两种回声均存在)。颈动脉粥样硬化程度判别标准:取左右两侧颈总动脉内中膜厚度的平均值作为研究对象最终的IMT值,并将其作为评价动脉粥样硬化的指标,IMT≥1.2 mm为粥样硬化斑块。(2)危险因素的纳入:本研究纳入的危险因素包括年龄、性别、NYHY、身体质量指数(BMI)。同时记录患者实验室检查结果,包括总胆固醇(TC)、甘油三酯(TG)、高密度脂蛋白(HDL-C)、低密度脂蛋白(LDL-C)/载脂蛋白B(ApoB)、空腹血糖、24 h尿蛋白定量、血肌酐(SCr)等。
1.4 统计学分析
2 结果
2.1 两组RHI、IMT对比
25(OH)D3缺乏组RHI低于非25(OH)D3缺乏组,IMT则高于非25(OH)D3缺乏组,差异均有统计学意义(P<0.05)。见表1。
表1 两组RHI和IMT对比
2.2 25(OH)D3与RHI相关性分析
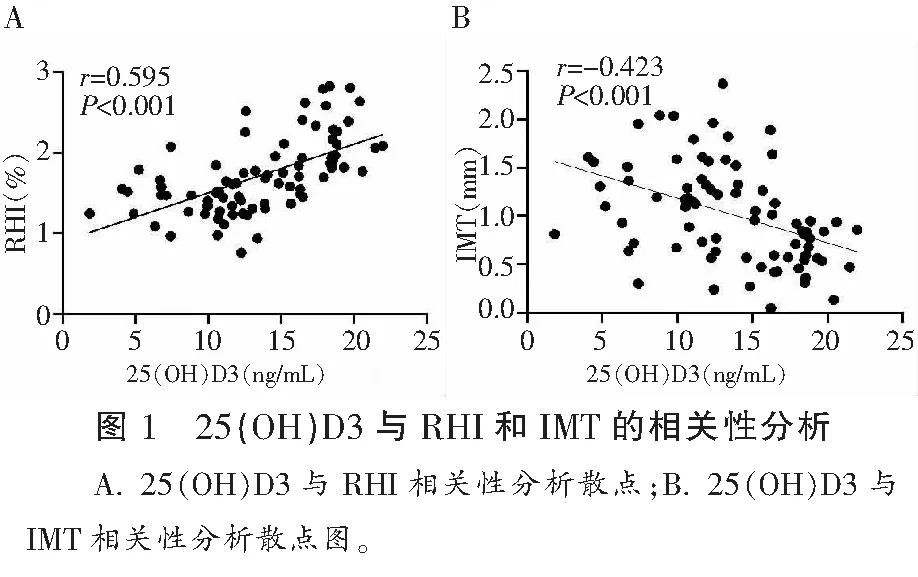
25(OH)D3与RHI呈正相关关系(r=0.595,P<0.001),与IMT呈负相关关系(r=-0.423,P<0.001)。见图1 。
2.3 单因素分析心力衰竭患者内皮功能障碍及动脉粥样硬化的影响因素
年龄、性别、TG、空腹血糖、24 h尿蛋白定量、SCr与心力衰竭患者内皮功能障碍无关(P>0.05),NYHY、TC、HDL-C、LDL-C/ApoB、25(OH)D3可能是影响心力衰竭患者内皮功能障碍的因素(P<0.05)。年龄、性别、NYHY、TG、LDL-C/ApoB、24h尿蛋白定量与心力衰竭患者动脉粥样硬化无关(P>0.05),TC、HDL-C、空腹血糖、SCr、25(OH)D3是影响心力衰竭患者动脉粥样硬化的单因素(P<0.05)。见表2及表3。
表3 影响心力衰竭患者动脉粥样硬化的单因素分析
2.4 多因素分析心力衰竭患者内皮功能的影响因素及心力衰竭患者内皮功能的影响因素
TC及25(OH)D3是心力衰竭患者RHI的影响因素(P<0.05)。HDL-C及25(OH)D3是心力衰竭患者IMT的影响因素(P<0.05)。见表4及表5。
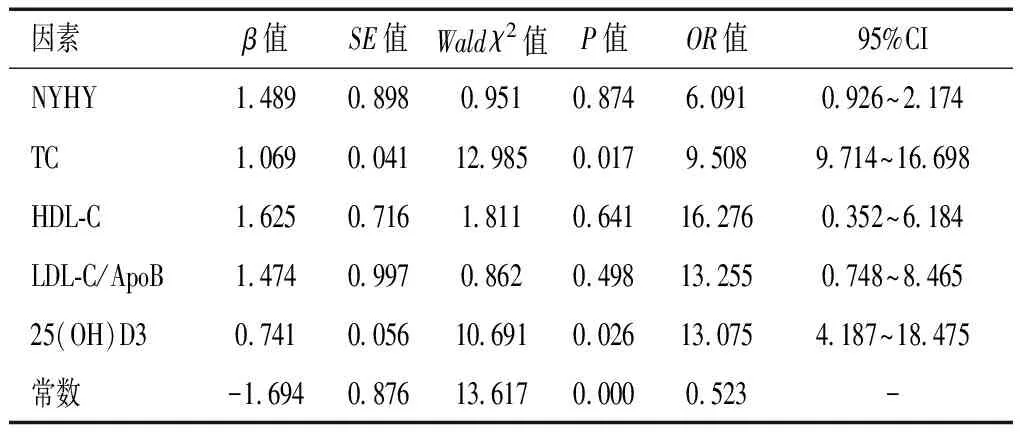
表4 心力衰竭患者RHI的影响因素多元线性逐步回归分析
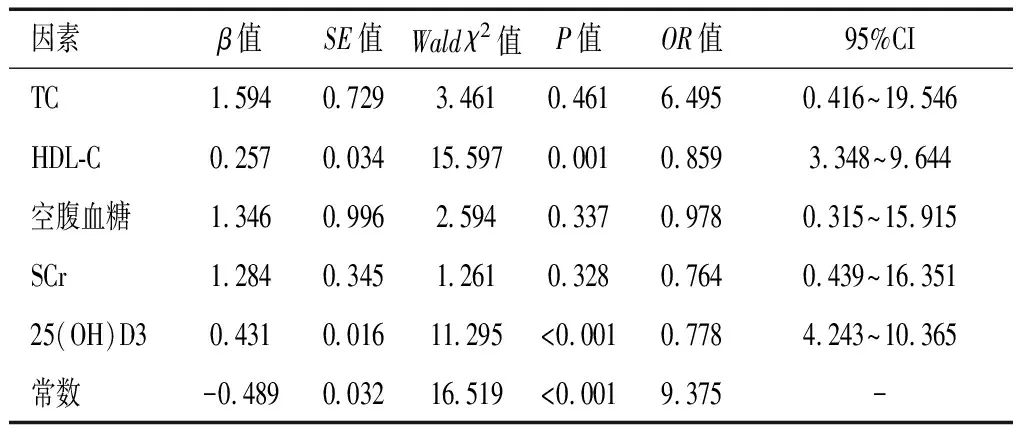
表5 心力衰竭患者IMT的影响因素多元线性逐步回归分析
3 讨论
维生素D类固醇衍生物属脂溶性维生素,为环戊烷多氢菲类化合物。动脉粥样硬化是心力衰竭发生的关键原因,而血管内皮功能损伤是动脉粥样硬化的首要临床表征。25(OH)D3是维生素D在人体内主要的表现形式,具有广泛的生理作用,25(OH)D3缺乏在心血管疾病患者中普遍存在[14]。因此,揭示25(OH)D3缺乏与血管内皮功能异常及动脉粥样硬化病变程度的相关性及潜在的机制可为心力衰竭的临床诊治提供新的靶点。
本研究通过Pearson分析显示,25(OH)D3水平与RHI呈正相关,与IMT呈负相关(P<0.05)。脂质浸润、内膜损伤、炎症反应、氧化应激、细胞外基质降解及血管壁重构等,均与内皮功能损伤密切相关。25(OH)D3可能通过以下几个方面影响内皮功能:(1)25(OH)D3在靶细胞与维生素受体结合后,可产生对靶基因的特定DNA序列发挥作用的特定复合物,进而调节结构基因的表达[15]。(2)25(OH)D3可抑制平滑肌增殖,进而影响内皮细胞和平滑肌细胞功能。25(OH)D3缺乏则可刺激血管平滑肌细胞增殖,并促进其向内膜迁移,降低血管张力的调节功能[16]。(3)血管病变患者体内往往存在炎症介质与细胞因子动态平衡的失调,而25(OH)D3可通过调节CD3+/CD4+T细胞、淋巴细胞和单核细胞/巨噬细胞分化,释放炎性细胞因子来介导血管炎症,进而改善内皮功能[17]。当25(OH)D3不足时,机体对炎症发应抑制效率降低,内皮功能损伤将更为显著。(4)维生素D可影响血管内皮功能及血管平滑肌细胞的迁移、增殖、钙化等,进而可调节血管弹性,影响血管内皮功能[18]。
而在本研究多因素分析中,25(OH)D3均是影响血管内皮功能异常及动脉粥样硬化程度的独立危险因素(P<0.05),提示25(OH)D3可通过调节内皮功能,影响动脉粥样硬化进展,参与心力衰竭病程。成乐等[19]认为,维生素D能通过维生素受体明显诱导内皮细胞一氧化氮(nitric oxide,NO)生成,25(OH)D3参与动脉粥样硬化进程主要依赖其对NO水平的关系。因此,25(OH)D3缺乏时可导致NO加速平滑肌增生和激活巨噬细胞与内皮细胞黏附,诱导泡沫组胞生成,促进血小板黏附与聚集,最终导致粥样硬化病变。吴丽美等[20]发现血维生素D水平与颈动脉粥样硬化有关。而李太勇等[21]通过logistics回归分析发现,在脑梗死患者中,低水平25-(OH)D水平是颈动脉粥样硬化斑块的独立危险因素。类似的,陈燕等[22]发现血清25-(OH)D3水平在老年慢性心力衰竭患者中显著降低,认为其水平与患者病情严重程度以及近期发生心血管事件的发生存在紧密联系。
综上所述,心力衰竭患者25(OH)D3水平与RHI呈正相关关系,与IMT呈负相关。25(OH)D3缺乏是影响血管内皮功能异常及动脉粥样硬化程度的独立危险因素,及时监测心力衰竭患者25(OH)D3水平有利于改善其临床预后转归。

