伊维菌素合成产物中杂质的分离与鉴定
高月麒,王克华,马志珺,林 旸,李晓露*,任风芝*
(1.华北制药集团新药研究开发有限责任公司 微生物药物国家工程研究中心 河北省工业微生物代谢工程技术研究中心,河北 石家庄 052165;2.华北制药集团爱诺有限公司,河北 石家庄 052165)
近年来,随着环境保护意识的增强及绿色生态农业的发展,生物农药在农药领域倍受青睐。阿维菌素类生物农药,因具有选择性高、低毒无公害、与环境相容性好等特点,受到研究者的重视。伊维菌素为十六元环结构的大环内酯类抗生素,通过阿维菌素B1a的C22、C23位上的双键加氢还原而成,比阿维菌素结构更稳定、安全性更高、持效期更长[1-2]。伊维菌素由于具有高效、用量少、副作用小等特点,广泛应用于牛、马、猪、羊的肺线虫及胃肠道线虫的治疗[3-6]。
随着公众对药品安全的日益关注,国内外对药物杂质的研究越来越重视,ICH及国家食品药品监督管理局都相继发布了杂质研究的指导原则,国外药典也对杂质进行了相应的规定。为满足伊维菌素注册需求、与国际接轨,作者以阿维菌素为起始原料,经催化加氢反应得到伊维菌素粗品,采用二维色谱纯化技术对伊维菌素粗品中的关键杂质进行分离提纯,并对杂质的结构进行鉴定,拟为伊维菌素的质量研究和高端认证提供技术支持。
1 实验
1.1 试剂与仪器
阿维菌素B1a(纯度≥98.5%),华北制药集团爱诺有限公司;乙腈,色谱纯,Merck公司;甲苯、甲醇,分析纯,天津科密欧化学试剂有限公司;纯化介质(UniSil C18),苏州纳微科技股份有限公司;纯化水,自制。
OptiMax 1001型反应釜,梅特勒-托利多公司;高效液相色谱仪(SPD-M20A 型紫外检测器),日本岛津公司;二维液相制备系统,北京创新通恒科技有限公司;T-1000型天平,常熟双杰测试仪器厂;AVANCE Ⅲ-500型核磁共振波谱仪,Bruker公司;LC-MS(ACQUITY UPLC系统,Xevo TQ MS型质谱检测器,2998型PDA检测器,Masslynx工作站),Waters公司。
1.2 伊维菌素粗品的合成
在反应釜中加入甲苯300 mL、阿维菌素B1a原粉100 g,在氮气搅拌下加入催化剂1.5 g,升温至70 ℃,通入氢气进行加氢反应,反应液过滤、干燥,即得伊维菌素粗品95 g。
1.3 伊维菌素杂质的分离纯化
将伊维菌素粗品用甲醇溶解,经中压柱(填料UniSil C18,30 μm,1 000 mL)进行初分离,洗脱剂为甲醇-水(85∶15,体积比,下同),根据洗脱峰分段收集洗脱液,洗脱液减压浓缩、干燥,即得高比例的杂质粗品。
将杂质粗品用甲醇溶解,经0.45 μm滤膜过滤,采用二维液相制备系统进行分离纯化,按照色谱图出峰分别进行目标馏分的收集,收集液减压浓缩、干燥,即得伊维菌素杂质纯品。
1.4 检测条件
制备色谱条件:UniSil C18色谱柱(30 mm×250 mm,10 μm),洗脱剂为乙腈-甲醇-水(54∶12∶34),流速为16 mL·min-1,检测波长为245 nm。
质谱条件:电喷雾离子源(ESI),正、负离子检测,离子源温度为150 ℃,电离电压为3.0 kV,电喷雾接口干燥气(N2)流速为600 L·h-1,锥孔电压为30 V,脱溶剂气温度为350 ℃。
核磁共振条件:样品用CDCl3溶解,用500 MHz型波谱仪检测。
2 结果与讨论
2.1 伊维菌素粗品的HPLC分析(图1)
由图1可知,在阿维菌素加氢反应过程中,除生成主产物伊维菌素外,也生成了副产物杂质1、杂质2、杂质3、杂质4。
2.2 伊维菌素杂质的分离纯化
采用二维色谱纯化技术对伊维菌素粗品中的主要杂质进行分离提纯,得到4个杂质纯品,杂质1、杂质2、杂质3、杂质4的质量分别为35 mg、20 mg、27 mg、45 mg,其色谱纯度均大于95%,分别为98.6%、95.7%、97.1%、99.1%。
2.3 伊维菌素杂质的结构表征
2.3.1 质谱分析(图2)
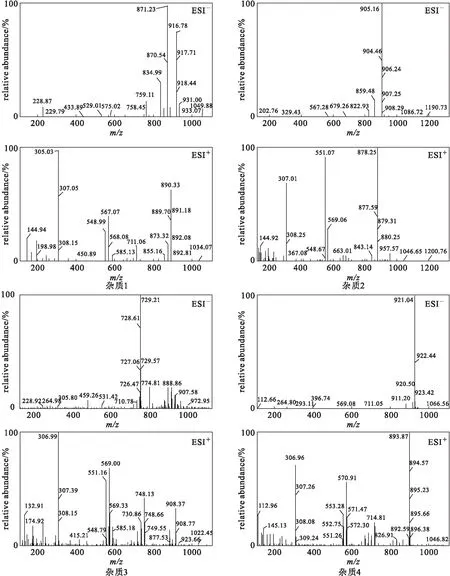
图2 伊维菌素杂质的质谱图
2.3.2 核磁共振波谱分析
13CNMR、1HNMR数据分别见表1、表2。
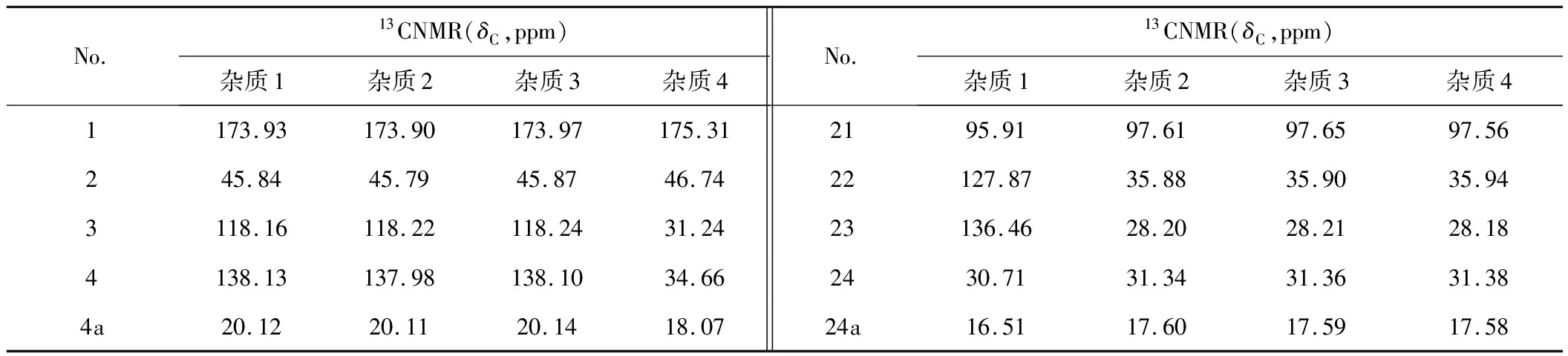
表1 伊维菌素杂质的13CNMR数据

表2 伊维菌素杂质的1HNMR数据
2.4 伊维菌素杂质的结构鉴定
杂质1:由ESI+准分子离子峰图谱得到m/z873[M+H]+,m/z890[M+NH4]+;由ESI-准分子离子峰图谱得到m/z871[M-H]-。推定杂质1的相对分子质量为872。由核磁共振波谱数据可知,杂质1的13C化学位移和1H化学位移与文献[7-8]中阿维菌素B1a的一致,确定杂质1为阿维菌素B1a。
杂质2:由ESI+准分子离子峰图谱得到m/z878[M+NH4]+;由ESI-准分子离子峰图谱得到m/z859[M-H]-,m/z905[M-H+HCOOH]-。推定杂质2的相对分子质量为860,较杂质1的相对分子质量少12。比对杂质2与杂质1的核磁共振波谱数据,发现差别在C3′a位碳信号消失,推测-OCH3变为了-OH;且C22、C23位双键消失,而增加了化学位移为δ35.88和δ28.20的两个碳信号,说明杂质2的C22、C23位为饱和键。综上,确定杂质2为3′-OH-H2B1a。
杂质3:由ESI+准分子离子峰图谱得到m/z748[M+NH4]+;由ESI-准分子离子峰图谱得到m/z729[M-H]-。推定杂质3的相对分子质量为730。比对杂质3与杂质1的核磁共振波谱数据,发现差别在C14a、C15~C20位碳信号消失;且C22、C23位双键消失,而增加了化学位移为δ35.90和δ28.21的两个碳信号,说明杂质3的C22、C23位为饱和键。综上,确定杂质3为EP9.0中有关物质H。
杂质4:由ESI+准分子离子峰图谱得到m/z894[M+NH4]+;由ESI-准分子离子峰图谱得到m/z921[M-H+HCOOH]-。推定杂质4的相对分子质量为876,较杂质1的相对分子质量多4。比对杂质4与杂质1的核磁共振波谱数据,发现差别在C3、C4位双键消失,而增加了化学位移为δ31.24和δ34.66的两个碳信号,说明杂质4的C3、C4位为饱和键;且C22、C23位双键消失,而增加了化学位移为δ35.94和δ28.18的两个碳信号,说明杂质4的C22、C23位为饱和键。综上,确定杂质4为EP9.0中有关物质K(H4B1a异构体)[9]。
杂质1、杂质2、杂质3、杂质4的结构式见图3。
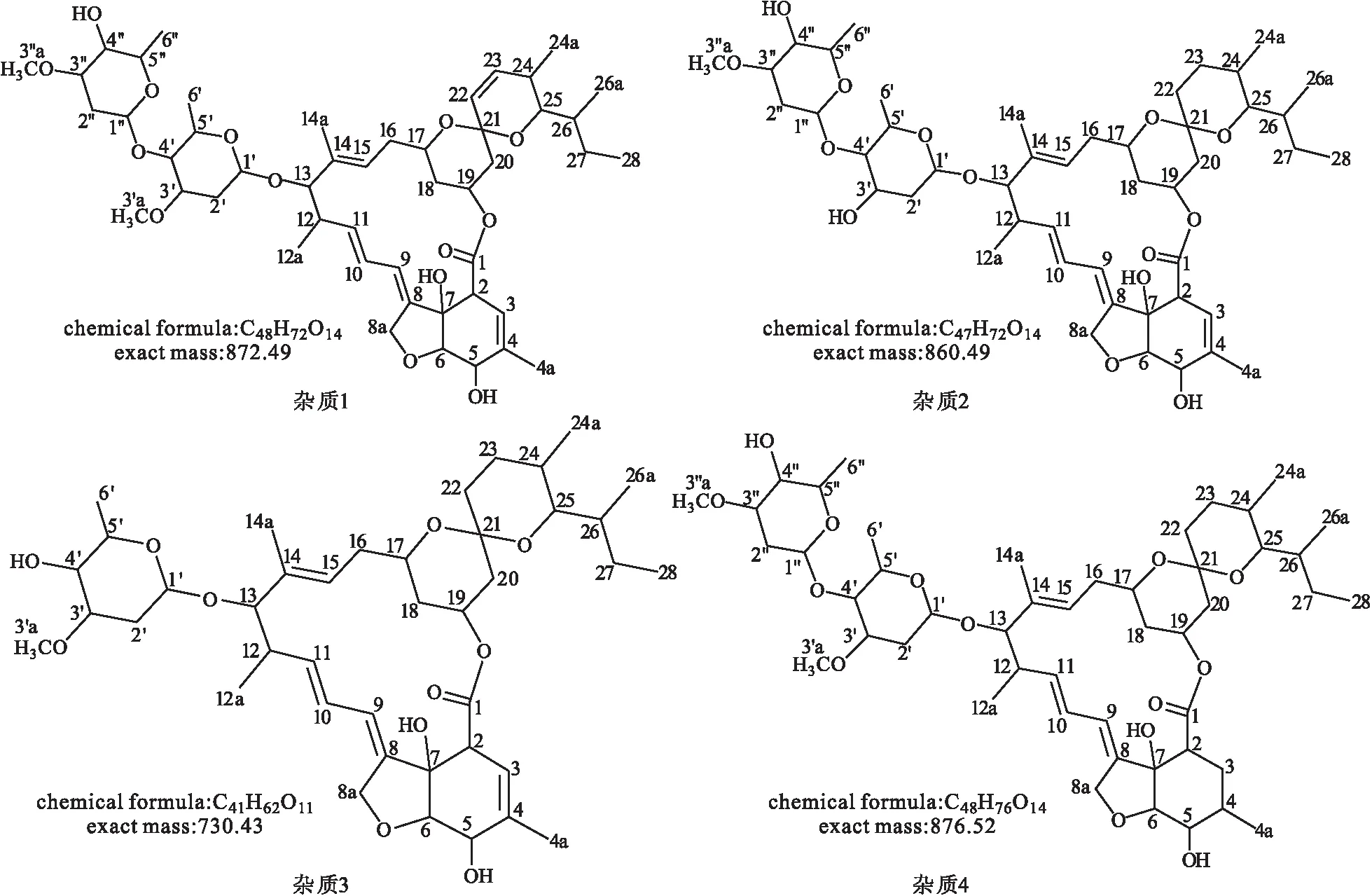
图3 杂质1、杂质2、杂质3、杂质4的结构式
3 结论
采用二维色谱纯化技术,从伊维菌素合成产物中分离得到4个杂质,并对杂质的结构进行了鉴定。结果发现,4个杂质的结构与伊维菌素骨架结构一致,均为同系列化合物,其中杂质1为阿维菌素B1a,杂质2为3′-OH-H2B1a,杂质3为EP9.0中有关物质H,杂质4为EP9.0中有关物质K(H4B1a异构体)。该研究通过对伊维菌素合成产物中杂质的归属研究,为产品的国内外注册及进入国际高端市场提供了有力支持,同时在更好地控制产品质量、保障用药安全方面具有十分重要的意义。

