胸腔镜下疝针治疗先天性膈疝效果观察
党坚 卢雄才 龙育 罗博文
先天性膈疝(congenital diaphragmatic hernia,CDH)是先天畸形疾病[1],发病率为1/2 500~1/5 000,熊晓峰等[2]在研究中指出,约有90%的CDH患儿病发部位为膈肌后外侧(单侧、双侧均有可能),也称先天性后外侧膈疝或胸膜裂孔疝,手术修补缺损一直是CDH最有效的治疗方法,其中胸腔镜修补手术由于操作方便,效果较为理想一直被作为首选术式。疝针术式是一种简化了手术操作的新型术式,不仅操作简单,修补病灶也更为严密和牢固,有较好的治疗反馈,李炳等[3]指出,在胸腔镜视野辅助下,应用疝针实施膈疝修补术、膈肌折叠术等具有较高的成功率,且安全性好,患儿的恢复效率较高,复发率较低,因此将两者联合作为CDH的主要治疗方法具有可行性,但目前以疝针治疗先天性膈疝的研究相对较少。本文开展对比研究,旨在通过对胸腔镜下联合疝针治疗先天性膈疝的疗效、安全性进行分析,为先天性膈疝患儿的治疗提供新的途径。
1 资料与方法
1.1 一般资料
研究对象为我院2018年1月—2020年10月诊断为小儿先天性膈疝,并行胸腔镜下治疗的患儿40例,采用随机数字表法分观察、对照组,每组各20例。患儿监护人均签署知情同意书,本研究经医院医学伦理委员会审批,审批编号:YX20200306-1。
纳入标准:(1)新生儿期以后临床检查确诊的CDH患儿;(2)术前经影像学(X线、MRI等)发现胃肠、肝肾等腹部器官组织疝入胸腔;(3)具有胸腔镜手术指征;(4)无代谢、免疫系统疾病。排除标准:(1)消化道畸形、心脏畸形者;(2)存在水电解质紊乱者;(3)合并染色体遗传病者;(4)低出生体质量足月儿;(5)创伤性、后天性膈疝者;(6)伴血性疾病者。观察组男13例,女7例,年龄10 d~1岁2个月,平均(7.31±1.82)个月;出生时胎龄33.23~41.34周,平均(37.34±2.64)周;手术时体质量2.80~4.91 kg,平均(3.79±0.26)kg;早产儿2例;膈疝:右侧4例,左侧16例;术前准备1~5 d,平均(3.07±1.13)d。对照组男14例,女6例,年龄10 d~1岁1个月,平均(7.52±1.63)个月;出生时胎龄33.54~41.05周,平均(37.44±2.64)周;手术时体质量2.82~4.86 kg,平均(3.81±0.24)kg;早产儿2例;膈疝:右侧5例,左侧15例;术前准备1~5 d,平均(3.15±1.24)d。两组一般资料比较,差异无统计学意义(P>0.05),具有可比性。
1.2 方法
两组患儿术前均给予常规术前辅助措施,如持续吸氧,调节手术室温度以保暖,控制饮食减轻肠胃压,纠正电解质及维持酸碱平衡,对于有微循环异常的患者,给予适当剂量的多巴胺等相关药物进行控制和改善,提前配合手术开展麻醉和通气措施,摆放体位(健侧卧位),并给予情绪安抚措施。
对照组:均在患侧肩胛下角线第5或6肋间做切口,置入5 mm Trocar,随后建立人工气胸,压力保持5~10 mmHg,等待疝入器官组织部分回缩腹腔后,再次于肩胛下角线第5~7肋间、腋前线第4~6肋间做切口,随后置入3 mm Trocar,利用器械将未完全回缩的疝入组织送回腹腔,检查送回组织情况,在确定回复原位后,将未完全发育的膈肌进行缝合,缝合采用带线雪橇针,使用操作钳、持针器将其从体外传入,间断缝合缺损膈肌,缝合从张力最小缺损内侧进针,采用滑结打结法,必要时可在疝囊(或较薄处膈肌),以褥式缝合结束[4-5]。缝合完毕后鼓肺检查有无缺漏,常规放置胸腔闭式引流瓶。
观察组:均在患侧肩胛下角第4或5肋间做切口,同样置入5mm Trocar和建立气腹(5~10 mmHg),在疝入组织部分回缩入腹腔后,在腋后线第7或8肋间置入3 mm Trocar作操作孔,并将疝入组织放置回腹腔,根据膈肌缺损情况,从张力最小处缝合,方向由两侧向中间,于胸壁疝环水平刺入带线疝针,置入4号丝线,以丝线缝合缺损膈肌边缘,将丝线一端留置,再抽出疝针,刺入弹簧钩针,穿过膈肌后,将留置丝线引导于胸壁外侧,并于肋骨打结和固定[2,6],间断缝合3~4针,将缺损的膈肌边缘固定于胸壁上。
术后予无创辅助呼吸,并做抗感染处理,监测患者体液情况,根据检测结果进行适当补液,术后还需定期检测生命体征,增加巡视次数,对于切口渗血、肛门排气排便等异常情况需及时上报。患儿术后均接受12个月随访,每月到院门诊复查胸部X线片、CT、呼吸频率、运动能力及肺功能等。
1.3 观察指标
(1)治愈(腹腔脏器容量、胸内压力恢复正常,脏器功能障碍消失,呼吸循环机能恢复正常)率;(2)手术、术后撤机、住院时间及术中出血量;(3)复发率及并发症(伤口感染、呼吸窘迫)的发生率。
1.5 统计学方法
应用SPSS 20.0统计学软件进行数据分析,计量资料以()表示,组间比较采用t检验,计数资料以率(%)表示,组间比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组疗效比较
两组患儿无手术失败,观察组治愈出院18例(90.0%)、死亡2例(10.0%),分别于术后3 d和15 d死亡,死亡原因为术后硬肿症和肺不张各1例。对照组治疗出院15例(75.0%)、死亡5例(25.0%),分别于术后3 d和11 d死亡,死亡原因为硬肿症1例、肺不张2例、重度肺动脉高压合并呼吸衰竭2例。观察组治愈率显著高于对照组,差异有统计学意义(χ2=4.716,P<0.05)。
2.2 两组手术相关指标比较
观察组手术、术后撤机、住院时间及术中出血量低于对照组,差异有统计学意义(P<0.05),见表1。
表1 两组手术相关指标比较 ()
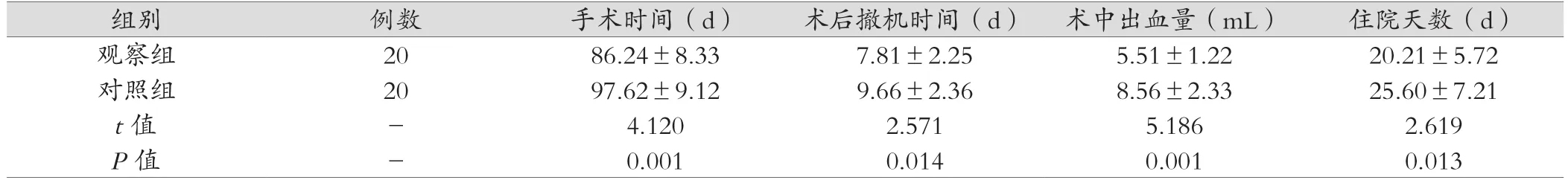
表1 两组手术相关指标比较 ()
组别 例数 手术时间(d) 术后撤机时间(d) 术中出血量(mL) 住院天数(d)观察组 20 86.24±8.33 7.81±2.25 5.51±1.22 20.21±5.72对照组 20 97.62±9.12 9.66±2.36 8.56±2.33 25.60±7.21 t值 - 4.120 2.571 5.186 2.619 P值 - 0.001 0.014 0.001 0.013
2.3 两组复发率及并发症发生率比较
术后观察组治愈出院的18例均未见复发,复发率为0(0/18)。发生粘连性肠梗阻1例,并发症发生率为5.56%(1/18);对照组治愈出院的15例中1例于术后6月复发,复发率为6.67%(1/15),出现粘连性肠梗阻5例,并发症发生率为33.33%(5/15)。两组复发率比较,差异无统计学意义(χ2=1.238,P=0.266);两组并发症发生率比较,差异有统计学意义(χ2=4.244,P=0.039)。
3 讨论
CDH与胚胎异常发育具有密切的相关性,该病症会导致患儿部分原属腹腔的器官、组织经缺损膈肌进入胸腔,形成疝囊,对患儿的近期生命安全和远期发育造成严重影响,特别是横膈先天性发育不良,会对肺组织和纵膈进行压迫,从而对患儿的肺发育情况造成抑制,张丽芬等[7-8]学者分别在研究中指出,CDH会导致患儿的心肺功能低下,出现反复呼吸困难、发绀、呕吐、咳嗽等症状,其症状的轻重取决于膈肌缺损的位置、大小及疝入物种类。CDH的诊断有赖于产期超声筛查。目前对于CDH更建议实施产前超声检测,通过检测结果,可提前为患儿制订治疗方法,从而尽量减少CDH对患儿健康的影响,孙滨等[9]指出,产前超声对于先天性膈疝检测效果良好,检出率最高可达60%。本组的40例患儿中,在我院确诊23例,其中产前确诊仅为12例(52.17%),余17例由外院出生确诊后转入我院治疗,确诊率略低于文献报道。
CDH可通过术前超声确诊,主要采用手术治疗,如经胸/腹膈肌修补术,此类手术通常会开放患儿的胸腹部,由于患儿初生发育较差,短时间内接受手术恢复较为困难,且易感染,因此目前更多的是采用较为新型的胸腔镜、腹腔镜膈肌修补术。陈义初等[10]对腔镜手术与传统开胸手术进行比较,虽然效果较为理想,但存在手术时间较长和对于主刀医师操作熟练度较高的要求,因此要求CDH手术团队掌握手术适应证以及并发症预防、处理措施,还要在术前对病灶进行充分的评估。随着近年来微创技术的成熟和临床医师操作技巧总结推广,腹腔镜或胸腔镜已有成为CDH主要手术的趋势。研究指出,在胸腔镜进行膈肌手术具有较高的视野清晰度,能缩短手术时间,且创伤小,患儿恢复时间短等优点,可作为新生儿CDH的首选治疗术式[11-13]。本研究中,观察组手术、术后撤机、住院时间及术中出血量优于对照组(P<0.05),分析认为,相较于三孔法,腔镜术式减少了创口数,简化了手术步骤(如可不切除疝囊壁,拖出后一并行折叠缝合),另外三孔法虽然可达到空间立体操作的效果,但胸腔镜视野更好,能使医师尽快找到病灶,有助于医师尽快完成手术,而手术时间的缩短可减少患儿CO2的暴露时间;在胸腔镜的监视下进行手术可避免缝合针距过大或松散,并能将膈肌固定于肋骨上,从而使修补更为严密和牢固,同时避免了缝针对脏器的损伤,有利于减少患儿术中出血量,提升患儿术后恢复效率,提高患儿生存率[14-15]。自我院开展该术式以来,门诊随访发现,与行传统三孔法患儿对比,疝针法复发率差异无统计学意义(P>0.05),而疝针法并发症发生率较三孔法明显降低(P<0.05),分析认为,这可能受先天性膈疝的解剖位置影响,由于膈疝多位于膈肌后且进入胸腔,导致手术缝合受胸骨的影响,这对于常规三孔法的缝合有较大限制,而胸腔镜视野较好,能更好的完成缝合,对于膈肌缺损边缘、后缘和疝囊壁的损伤较小,加之胸腔镜下疝针不易漏针,折叠缝合的效果更好,且结扎线对周围器官组织刺激较小,炎性反应较弱,从而显著降低了患者的并发症发生率[16-18]。熊晓峰等[19]在研究中指出,胸腔镜下疝针法治疗CDH优于传统三孔法修补,这与本文的研究结果具有一致性。
综上所述,胸腔镜下联合疝针治疗小儿先天性膈疝效果显著,且安全可靠,疗效优于传统三孔胸腔镜修补术,是治疗先天性膈疝较为理想的术式,值得临床推广应用。

