不同电荷阴离子多糖对负载单宁酸的玉米醇溶蛋白纳米颗粒的稳定作用
梁晓,胡勇,徐金瑞,胡坤*
(1.广东药科大学公共卫生学院,广东广州 510006)(2.广东药科大学食品科学院,广东中山 528458)
单宁酸是一类天然多酚类物质,普遍存在于中草药植物的树皮或者果实中[1]。单宁酸含有较多的酚羟基,具有一系列独特的化学特性和生理活性[2],如可以与蛋白质、多糖、生物碱等发生相互作用,具有抗氧化[3]、抗肿瘤[4]、抗菌[5]、抗诱变特性[6]等活性。然而,单宁酸的生物活性和副作用与摄入剂量有关。膳食中摄入低剂量单宁酸可以对C3H雄性小鼠自发性肝肿瘤的形成产生强烈的剂量依赖性化学预防活性(高达87%)[7],或抑制肿瘤细胞蛋白酶体活性[8];但高剂量单宁酸能抑制铁的吸收,也会抑制酶的活性[9]。兔的口服单宁酸实验表明,单宁酸主要在胃肠道吸收,并且在24 h内被代谢和排泄[10]。因此,将单宁酸包埋于输送载体中,在消化道中可控释放,是持续发挥单宁酸活性及避免高剂量副作用的有效方式。Neculai等[10]用壳聚糖微球、壳聚糖与海藻酸钠静电复合物、壳聚糖与羧甲基纤维素的静电复合物微球负载单宁酸,研究其在不同pH环境下的释放单宁酸的动力学,三种微球对单宁酸的负载效率分别为14%、28.9%、6.3%。这是由于单宁酸是水溶性小分子,当与水溶性高分子溶液混合后采用沉积的方法制备多糖颗粒时,大部分的单宁酸仍保留在水中,导致负载效率低下。
在以蛋白质为输送载体的体系中,单宁酸常被用于交联强化蛋白质之间的聚集[11-13],而鲜见以蛋白质为载体负载单宁酸的研究。利用水溶性蛋白质包埋单宁酸需要特殊处理(如热处理),也会存在包埋效率低下的问题。玉米醇溶蛋白(zein)是玉米的主要贮藏蛋白,其疏水氨基酸残基比例超过50%,因此不溶于水而溶于高浓度的醇-水溶液[14]。利用这一特性可将醇溶性活性成分与玉米醇溶蛋白溶解在高浓度乙醇-水溶液中利用反溶剂法分散到水中制备自组装纳米颗粒[15,16]。与水溶性蛋白质的包埋作用相比,以玉米醇溶蛋白纳米颗粒负载单宁酸无需热处理,可望提高单宁酸的负载效率。然而zein纳米颗粒载体的缺陷是其表面疏水性强,在中性pH时颗粒的稳定性较差,且冻干后颗粒很难重新分散[17],限制了在食品及制药领域的应用。Hu等[18]首先报道利用zein与海藻酸钠制备核/壳型纳米颗粒,在酸性至中性pH范围内都有较好的稳定性及重分散性。其他阴离子多糖如果胶[19]、海藻酸丙二醇酯[20]、阿拉伯胶[21]等也被用于稳定zein纳米颗粒。目前关于不同电荷的多糖对zein纳米颗粒的稳定作用缺乏系统的研究,zein/阴离子多糖纳米颗粒对水溶性物质的负载也少见报道。本文将比较不同电荷类型的多糖对负载单宁酸的zein纳米颗粒稳定性的影响,揭示不同电荷的阴离子多糖稳定zein纳米颗粒的机制,为开发负载水溶性生物活性物质的玉米醇溶蛋白/多糖纳米颗粒输送体系提供依据。
1 材料和方法
1.1 材料与试剂
玉米醇溶蛋白(>90%)、高脂果胶(酯化度67%~71%)、阿拉伯胶(总灰分<4%)购自Acros;单宁酸(99.9%)、低酯果胶(橘皮果胶,半乳糖醛酸>74%)购自Sigma-Alorich;海藻酸丙二醇酯(纯度98%)购自阿达玛斯(Adamas);其他试剂均为分析纯。
1.2 主要仪器
IKA磁力搅拌器,R05,德国;pH-3CpH计,上海雷磁;RE 2000A旋转蒸发仪,上海亚荣生化;Nano-ZS 90激光粒度仪,Malvern,英国;Beta 1-8 LSCbasic冷冻干燥机,德国Chris;1B48F原子力显微镜,美国Bruker;Nova NanoSEM 430场发射扫描电镜,荷兰FEI。
1.3 溶液的制备
1.3.1 单宁酸-玉米醇溶蛋白乙醇溶液的制备
将1.0 g玉米醇溶蛋白加入到50 mL 85%(V/V)的乙醇溶液中,在室温条件下以磁力搅拌器搅拌30 min(500 r/min),然后加入0.1 g单宁酸继续搅拌30 min,离心(3000 r/min,10 min)除去不溶性杂质,得到澄清的溶液。
1.3.2 不同电荷特性多糖溶液的制备
分别称取0、0.005、0.011、0.022、0.033、0.055、0.077、0.1、0.15和0.2 g海藻酸丙二醇酯(PGA)、阿拉伯胶(GA)、高酯果胶(HMP)和低酯果胶(LMP)加入100 mL超纯水中,70 ℃水浴加热搅拌30 min,快速冷却后搅拌1 h,以1.0 mol/L HCl将溶液pH调至4.0,并补充蒸发损失的水分,3000 r/min离心除去不溶性杂质。
1.4 负载单宁酸的zein/阴离子多糖纳米颗粒制备
在800 r/min的速度搅拌条件下,用注射器将4 mL玉米醇溶蛋白-单宁酸乙醇溶液快速注射到16 mL pH 4.0的超纯水中,继续搅拌3 min,以旋转蒸发器除去乙醇,并用相同体积的pH 4.0纯水补充至20 mL,制得负载单宁酸的zein纳米颗粒。然后按照1:2比例将制得的分散液分散(900 r/min)到不同电荷特性的多糖溶液中,继续搅拌10 min,离心后(3000 r/min,10 min)除去大颗粒。
1.5 纳米颗粒粒径与ζ-电位的测定
将新鲜制备的zein/阴离子多糖纳米颗粒分散液用pH 4.0的超纯水稀释至蛋白浓度为0.05 mg/mL后,利用激光粒度仪测定其平均粒径、电位及颗粒多分散性(PDI)。
1.6 微观形貌观察
1.6.1 原子力显微镜(AFM)
取适量新鲜制备的样品(多糖浓度0.1%)用pH 4.0的超纯水稀释至蛋白浓度为0.05 mg/mL,然后取30 μL稀释后的样品滴至新的云母磁盘上自然晾干,原子力显微镜采用轻敲模式,采用图像分析软件对样品的微观形态进行分析。
1.6.2 场发射扫描电镜(FE-SEM)
取适量冷冻干燥的zein/阴离子多糖纳米颗粒样品经喷金后,在10.0 kV的加速电压下观察冻干样品的形态。
1.7 环境条件对zein/阴离子多糖纳米颗粒稳定性的影响
不同pH的颗粒稳定性用1 mol/L NaOH或者HCl溶液对新鲜配制的纳米颗粒进行调整,使得颗粒悬浮液pH为2.0~8.0。
盐浓度的影响:向新制备的颗粒悬浮液中加氯化钠,最终盐浓度范围为0~100 mmol/L NaCl。
热处理的影响:新鲜制备的悬浮液在80 ℃下加热不同(0~120 min),处理后的样品测定其平均粒径和多分散指数,以数码相机记录颗粒分散液的状态,评价环境压力对颗粒稳定性的影响。
1.8 颗粒得率及单宁酸负载效率的测定 1.8.1 颗粒得率测定
负载单宁酸的zein/低酯果胶纳米颗粒分散液经冷冻干燥后回收称重,颗粒得率和单宁酸的负载效率由下式计算:
式中:
w1——冻干的纳米颗粒质量,mg;
w0——单宁酸、玉米醇溶蛋白和低酯果胶的总质量,mg。
1.8.2 单宁酸负载效率的测定
参考Arroyo-Maya等[22]的方法并做修改。将负载单宁酸的Zein/低酯果胶纳米颗粒分散液离心(4000 r/min,20 min),然后通过10 ku膜过滤器过滤,收集滤液(体积记为v),经适度稀释后在278 nm波长测定其吸光度,根据标准曲线确定滤液中未包埋的游离单宁酸的浓度c。单宁酸负载效率由下式计算:
式中:
m0——投入的单宁酸质量,μg;
c——滤液浓度;
f——稀释倍数;
v——滤液体积。
1.8.3 单宁酸标准曲线
称取20 mg单宁酸溶于20 mL超纯水中,制备成浓度为1 mg/mL的单宁酸溶液,然后用超纯水分别稀释成0~20 µg/mL标准液,在278 nm波长测定其吸光度,建立单宁酸含量标准曲线y=0.0442x+0.0073,R2=0.9997。
1.9 数据处理
所有实验数据至少重复3次,数据结果以平均值和标准差表示。采用SAS(9.4)统计软件对数据进行统计分析,p<0.05表示有统计学差异。
2 结果与分析
2.1 多糖浓度与负载单宁酸的zein纳米颗粒稳定性
文献报道玉米醇溶蛋白等电点pI值为pH 6.2[23]。在pH 4.0的水中,反溶剂法制备的纳米颗粒带净正电荷,测得其ζ-电位为30.48 mV,以zein:单宁酸质量比10:1负载单宁酸后,纳米颗粒的电位为26.45 mV。因单宁酸带负电荷,导致zein纳米颗粒表面电荷下降,但下降幅度较小,说明单宁酸大部分被包埋在zein纳米颗粒的内部,从而对颗粒表面电荷的影响较小。
将负载单宁酸的zein纳米颗粒分散液按1:2体积比分散至pH 4.0的多糖溶液中,结果如图1。低浓度的多糖引起纳米颗粒的沉淀,而随着多糖浓度的增加,颗粒又重新稳定。不同多糖稳定颗粒所需的最低浓度存在明显的差异:海藻酸丙二醇酯(Propylene glycol alginate,PGA)、阿拉伯胶(gum Arabic,GA)、高酯果胶(High methoxy pectin,HMP)稳定颗粒所需的最低多糖浓度为0.055%(m/V),而低酯果胶(lowmethoxy pectin,LMP)为0.022%(m/V)。在pH 4.0时,测得PGA、GA、HMP以及LMP的ζ-电位分别为-17.25、-22.25、-28.48、-33.72 mV,多糖与带净正电荷的zein纳米颗粒发生静电吸引作用,吸附到zein颗粒的表面,使颗粒的电荷值急剧下降(图2),多糖浓度较低时,吸附的多糖降低了颗粒的表面电位但不足以完全覆盖颗粒表面[18],导致颗粒之间聚集而沉淀;随着多糖浓度的增加,越来越多的多糖分子吸附到颗粒表面,颗粒重新变得稳定。当多糖浓度达到0.10%时,纳米颗粒的ζ-电位均达到相对恒定的水平且接近多糖的ζ-电位,说明纳米颗粒表面包覆的多糖达到饱和(如图2),形成TZP/多糖核-壳型纳米颗粒。比较不同多糖包覆的纳米颗粒粒径发现(图3),TZP/PGA颗粒粒径最大,当多糖浓度为0.10%时,其粒径为506.70 nm。这是因为海藻酸丙二醇酯的ζ-电位较低,与zein纳米颗粒之间的静电相互作用较弱,导致颗粒稳定性较差,粒径较大。Sun等[24]亦报道负载槲皮素的zein/PGA颗粒粒径达到759 nm,说明PGA不能稳定zein纳米颗粒。其次是TZP/HMP,粒径为296.25 nm;而TZP/GA和TZP/LMP纳米颗粒的粒径分别为131.63、160.18 nm。
采用原子力显微镜观察纳米颗粒的微观形貌,如图4所示,负载单宁的纳米颗粒近似球形且分布比较均一(图4a),粒径50 nm左右,与粒度仪测定的结果接近(图3)。
多糖包覆的纳米颗粒在制样干燥时发生不同程度的颗粒聚集,且海藻酸丙二醇酯(图4b)、阿拉伯胶(图4c)、高酯果胶(图4d)包覆的颗粒聚集程度较高,而低酯果胶包覆的纳米颗粒聚集程度较低,说明颗粒稳定性较高(图4e)。
2.2 不同pH条件下TZP/多糖纳米颗粒的稳定性
玉米醇溶蛋白为两亲性高分子,其纳米颗粒表面电荷受水相pH的影响,从而影响其与阴离子多糖的相互作用,进而影响纳米颗粒的稳定性。基于海藻酸丙二醇酯包覆的纳米颗粒粒径较大,稳定性较差,故后续研究主要针对TZP/GA、TZP/HMP、TZP/LMP纳米颗粒。不同pH条件下纳米颗粒分散液的稳定性如图5:TZP/GA在pH 2.0及zein等电点附近(pH 6.0~6.5)不稳定,颗粒沉淀析出,在pH 3.0时分散液变浑浊;Gali等[21]报道以zein/GA颗粒负载流苏芸香(Ruta chalepensis)的芦丁提取物在pH 2~3、pH 7~8时粒径较大;而负载松香的zein/GA颗粒在pH 3.0时聚集沉淀[25],说明负载的客体极性对zein/GA颗粒在不同pH时的稳定性影响较大,疏水性客体更有利于zein/GA在高酸性及zein等电点pH时颗粒的稳定。TZP/HMP在pH 2.0~3.0澄清度下降;而TZP/LMP仅在pH 6.0时澄清度稍有下降,说明LMP比HMP对TZP的稳定作用更强。
纳米颗粒粒径及颗粒多分散性指数(PDI)随pH的变化如表1所示,TZP/GA颗粒在pH 3.0~5.0、pH 7.0~8.0时,颗粒粒径在120~160 nm之间,PDI约为0.20,说明纳米颗粒均一性较好,颗粒较为稳定。TZP/HMP颗粒的粒径在酸性pH时较大,最大粒径达到321.65 nm,但在zein等电点pH附近(pH 6.0~6.5)时粒径反而较低,在pH 7.0~8.0时,粒径最小。这是因为在中性到碱性pH时zein带净负电荷,与同为负电荷的高酯果胶之间主要发生静电排斥,多糖与zein颗粒之间相互作用较弱,部分多糖脱离颗粒表面,从而降低颗粒的粒径。随着pH值的增加,颗粒的PDI逐渐增大,当pH>5.0时,PDI大于0.34,表明TZP/HMP纳米颗粒粒径分布不均一,颗粒粒径差异明显,也说明在此条件下,高酯果胶与zein颗粒之间相互作用较弱,使得颗粒粒径分布发生较大的变化。TZP/LMP的粒径在pH 2.0~8.0范围内随pH值的增加而减小(从197.80 nm减小至105.98 nm)。但在pH 6.0时(接近zein等电点pH值)粒径稍有增加(由pH 5.0时的164.90 nm增加到pH 6.0时的178.73 nm),表明在等电点pH附近,低酯果胶与zein的静电相互作用相对较弱,导致颗粒粒径增加,但所有pH范围内纳米颗粒的PDI值都低于0.27。一般认为PDI低于0.30,纳米颗粒比较稳定,粒径分布比较均一,因此低酯果胶在pH 2.0~8.0均能较好的稳定纳米颗粒。
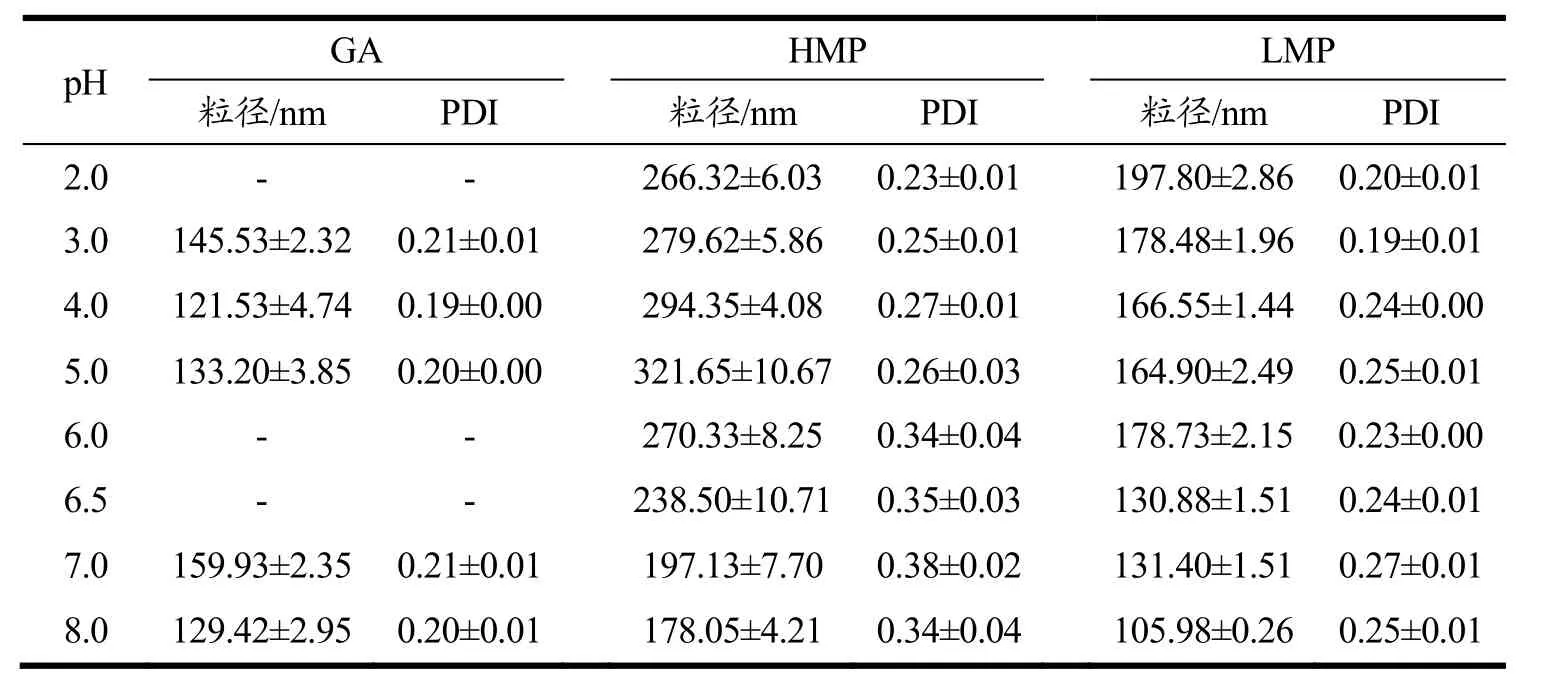
表1 不同pH条件下TZP/多糖纳米颗粒的粒径及PDITable 1 The particle size and PDI of TZP/polysaccharide nanoparticles at different pH
TZP/多糖纳米颗粒ζ-电位随pH的变化趋势见图6,纳米颗粒的ζ-电位随pH值的变化受到多糖分子的显著影响,表现出与多糖溶液相同的变化趋势,说明TZP纳米颗粒被多糖包覆。在pH 2.0时,TZP/GA的ζ-电位为0.02 mV(图6a),TZP/HMP的为-0.69 mV(图6b),而TZP/LMP则为-2.23 mV(图6c)。阿拉伯胶为含有蛋白质的羧基多糖,果胶为部分甲酯化的羧基多糖,羧基的pKa约为pH 3.5[26],在pH 2.0时,多糖分子中未与zein的-NH3+发生静电相互作用的游离-COO-质子化生成-COOH,导致纳米颗粒ζ-电位接近0,此时TZP/GA沉淀析出,TZP-HMP粒径稍微增加(266.32 nm);而TZP-LMP因存在一定的电荷排斥作用,颗粒得以稳定。在pH 6.0时,zein表面净电荷接近电中性,此时与阴离子多糖的静电相互作用最弱,电荷较弱的阿拉伯胶对TZP的稳定作用减弱,测得TZP/GA的ζ-电位(-18.48 mV)远低于TZP-HMP(-37.20 mV)及TZP-LMP(-39.31 mV),导致TZP/GA颗粒之间的静电排斥力较弱,从而失去稳定而沉淀。
2.3 离子强度对TZP/多糖纳米颗粒稳定性的影响
蛋白质与多糖之间的静电相互作用受离子强度的影响,从而影响纳米颗粒的稳定性。TZP/GA颗粒对离子强度最敏感(图7),10 mmol/L的NaCl即引起颗粒分散液混浊,当NaCl浓度增加到15 mmol/L时颗粒沉淀。当zein/GA颗粒负载姜黄素时,大于8 mmol/L的NaCl浓度即导致颗粒聚集[27]。以上结果说明阿拉伯胶与zein之间的静电相互作用较弱,较低浓度的中性盐即可达到电荷中和作用而使颗粒沉淀。与阿拉伯胶相比,TZP/HMP、TZP/LMP纳米颗粒对盐的耐受性较强,颗粒分散液在0~25 mmol/L NaCl浓度范围内仍然保持半透明状,但其粒径分别增加至370.70 nm(图8a)和279.88 nm(图8a),30 mmol/L的NaCl浓度时纳米颗粒发生聚集沉淀,而负载白藜芦醇的zein/LMP纳米颗粒则在70 mmol/L的盐浓度时发生沉淀[28]。此结果进一步表明,负载的客体的极性影响zein/阴离子多糖纳米颗粒的稳定性,疏水性客体有利于纳米颗粒与多糖的相互作用,使颗粒更为稳定。
2.4 颗粒的热稳定性
将颗粒分散液在80 ℃水浴加热处理120 min,TZP/GA、TZP/LMP分散液外观仍为澄清透明的状态,然而TZP/HMP分散液外观透明度下降。TZP/GA的粒径经热处理后明显下降,从未处理时的121.53 nm降至107.39 nm(图9a,p<0.05);而TZP/HMP的粒径从未处理时的294.35 nm增大至326.09 nm(图9b,p<0.05)。热处理对TZP/LMP的粒径无明显影响(图9c,p>0.05),表明TZP/LMP具有良好的热稳定性。
2.5 纳米颗粒得率及单宁酸负载效率
将TZP纳米颗粒分散液以1:2的体积比分散至浓度为0.11%低酯果胶溶液中,经冷冻干燥后收集干燥的TZP/LMP纳米颗粒,计算颗粒得率为95.10%,测得单宁酸的负载效率为88.97%,颗粒中单宁酸的含量为5.39%。亲水性小分子物质易溶于水,将其高效负载到蛋白质纳米颗粒中具有一定的挑战性[29]。Arroyo-Maya等[22]采用热处理和静电络合的方法,以乳清分离蛋白-甜菜果胶纳米颗粒负载花青素,负载效率为35%~55%。本文中的玉米醇溶蛋白/低酯果胶纳米颗粒对单宁酸的负载效率显著高于Arroyo-Maya等人[22]报道的花青素的负载效率,甚至接近疏水性的姜黄素[19]和白藜芦醇的负载效率[30]。利用SEM观察冷冻干燥的纳米颗粒为球形,直径范围为100~200 nm(图10a)。纳米颗粒的粒径分布为单峰(图10b),粒径和PDI分别为165.55 nm和0.23。
3 结论
玉米醇溶蛋白在pH 4.0时,以反溶剂法制备的纳米颗粒带净正电荷,可与阴离子多糖发生静电相互作用而形成核-壳型纳米颗粒。比较表面负电荷依次增加的海藻酸丙二醇酯、阿拉伯胶、高酯果胶、低酯果胶对负载单宁酸的zein纳米颗粒稳定性的影响,结果发现当多糖在颗粒表面达到饱和吸附时,可以稳定颗粒。这种稳定作用受阴离子多糖的ζ-电位影响,ζ-电位最弱的海藻酸丙二醇酯不能有效地稳定TZP,ζ-电位较弱的GA在强酸性pH值和zein等电点pH值附近无法稳定纳米颗粒,而ζ-电位最强的LMP在pH 2.0~8.0范围内均能稳定纳米颗粒。由于阴离子多糖与TZP以静电相互作用形成核-壳型纳米颗粒,其作用强度受离子强度的影响。表面电荷较低的阿拉伯胶,其与TZP形成的纳米颗粒对盐的稳定性最低,而表面电荷最强的LMP与TZP形成的纳米颗粒对盐的稳定性较高。以LMP作为稳定剂制备的TZP/LMP纳米颗粒对水溶性多酚单宁酸的负载率达到88.97%,单宁酸在颗粒中的含量为5.39%,明显优于水溶性蛋白(如乳清蛋白)纳米颗粒对亲水性活性成分的负载率。因此,本文报道的玉米醇溶蛋白/低酯果胶复合纳米颗粒可用于亲水性多酚的包埋与保护,可望用于亲水性活性成分的靶向输送和可控释放,今后的研究将集中于该体系在胃肠道环境中释放单宁酸的过程及生物利用度。

