高效液相色谱法测定黄体酮及有关物质
陈丽萍,周慧,张信,尤兴田
(扬州工业职业技术学院 化学工程学院,江苏 扬州 225127)
黄体酮是孕激素类药物,生理效应及临床治疗作用广泛,应用历史悠久。目前,黄体酮在《中国药典》2015年版二部中已有收载,高效液相色谱法测定其含量与有关物质的检测波长为241 nm[1-2]。鉴于黄体酮在生产中引入的中间体氢化物(5-孕甾烯-3β-醇-20-酮 3-醋酸酯)和水化物(5-孕甾烯-3β-醇-20-酮)在药典条件下不能检测,为保证各有关物质快速准确的测定,本文创建了高效液相色谱法波长200 nm 的检测方法,有利于更好地提高黄体酮质量和生产的稳定性,该方法未见药典收载,也未见文献报道。
1 实验部分
1.1 仪器与试药
Agilent 1260 高效液相色谱仪(二极管阵列检测器)。黄体酮对照品,批号100027-201209,纯度99.7%,中国药品生物制品鉴定所;黄体酮供试品,批号HT-p201806001,江苏联环药业有限公司;水解物工作对照品(精制品),批号HT-a20180201,AR,上海青析化工科技有限公司;氢化物工作对照品(中间体),批号20180201,国药集团化学试剂有限公司;甲醇、乙腈,色谱纯,天津康科德科技有限公司;水为超纯水。
1.2 实验方法
1.2.1 色谱条件色谱柱为Kromasill00-5 C18 (250 mm×4.6 mm,5 μm);流动相为甲醇-乙腈-水(25∶35∶40);柱温30 ℃;流速1.0 mL·min-1;检测波长200 nm;进样体积10 μL。
1.2.2 标准溶液的配制
取黄体酮对照品约40 mg,精密称定,置20 mL容量瓶中,加流动相溶解并稀释至刻度,摇匀,作为黄体酮对照品储备液。精密吸取黄体酮储备液1.0 mL,置 100 mL 容量瓶中,加流动相溶解并稀释至刻度,摇匀,作为黄体酮对照品溶液。
取水解物工作对照品(精制品)约10 mg,精密称定,置100 mL 容量瓶中,加稀释液溶解并稀释至刻度,摇匀,作为氢化物工作对照品储备溶液。精密吸取1.0 mL,置 10 mL 容量瓶中,加稀释液溶解并稀释至刻度,摇匀,作为水解物工作对照品溶液。
取氢化物工作对照品(中间体)约10 mg,精密称定,置100 mL 容量瓶中,加稀释液溶解并稀释至刻度,摇匀,作为氢化物工作对照品储备溶液。精密吸取1.0 mL,置10 mL 容量瓶中,加稀释液溶解并稀释至刻度,摇匀,作为氢化物工作对照品溶液。
1.2.3 黄体酮碱破坏溶液
取本品黄体酮对照品约25 mg,精密称定,置25 mL 容量瓶中,加0.1 mol·L-1氢氧化钠甲醇溶液10 mL 使溶解,置60 ℃水浴4 h,放冷;用1 mol·L-1盐酸溶液调节至中性,用稀释液稀释至刻度,摇匀。
1.2.4 黄体酮系统适用性溶液
精密吸取氢化物、水解物工作对照品储备溶液各1.0 mL,置10 mL 容量瓶中,加黄体酮碱破坏溶液稀释至刻度,摇匀,作为黄体酮(粗品)系统适用性溶液。
1.2.5 黄体酮试验溶液
取本品约10 mg,精密称定,置10 mL 容量瓶中,加少量稀释液溶解,精密吸取氢化物、水解物工作对照品储备溶液各1.0 mL,加稀释液至刻度,摇匀,作为黄体酮系统适用性溶液。
2 实验结果
2.1 方法学验证
2.1.1 专属性考察
在1.2.1 节色谱条件下进样,记录色谱图如图1所示,黄体酮主要杂质分离结果如表1所示。黄体酮在241 nm 有吸收,而已知杂质在241 nm 无吸收(图1A),在波长200 nm 下黄体酮和已知杂质水解物、氢化物以及碱破坏降解杂质有吸收(图1B)。由表1的结果可以看出,黄体酮和已知杂质水解物、氢化物以及碱破坏降解杂质的均可达到有效分离,表明该法的专属性好,可以有效检测黄体酮生产过程中在各苛刻条件下(碱水解)的降解产物及中间产物。
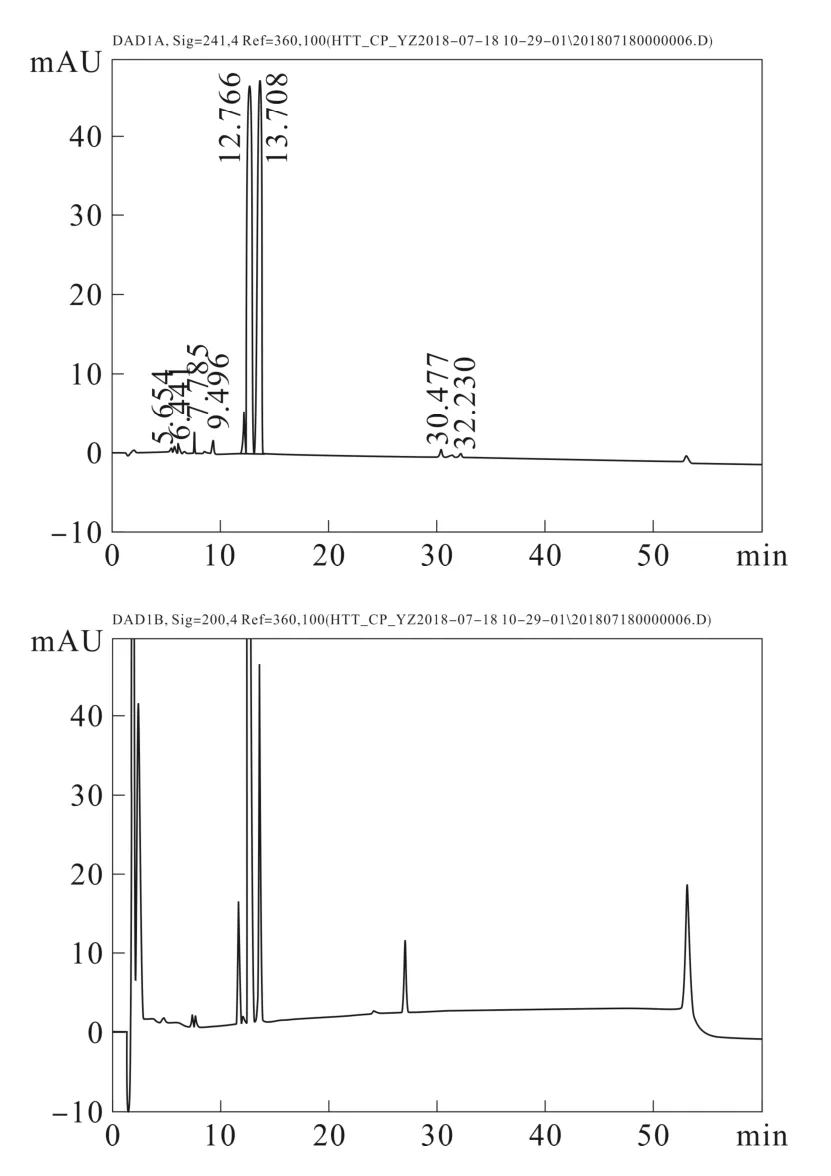
图1 专属性试验色谱图
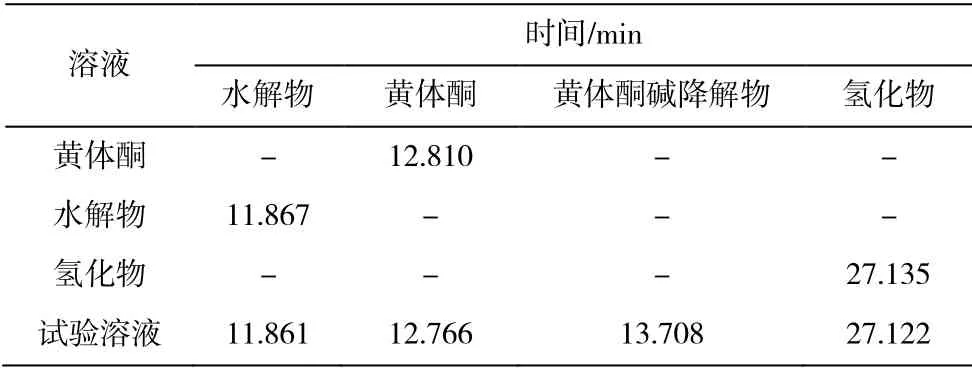
表1 黄体酮主要杂质分离结果
2.1.2 线性范围
2.1.2.1 黄体酮的线性范围
分别精密量取黄体酮储备液适量,加稀释溶剂稀释制成1 200、1 000、500、100、50、20、10、5、2、1、0.5、0.25 μg·mL-1的溶液,摇匀。按上述色谱系统(1.2.1),将上述标准溶液依次进样,记录峰面积。以峰面积(A)为纵坐标、浓度(C,μg·mL-1)为横坐标进行线性回归,得线性回归方程及关系,结果如表2所示。由表2可知,黄体酮(200 nm 波长)在0.25~1 200 μg·mL-1的质量浓度范围内呈良好的线性关系(R2为1.000 0 和0.999 93,n=7)。
2.1.2.2 有关物质的线性范围
分别精密量取适量水解物对照品储备溶液,加稀释溶剂稀释制成100、50、20、10、5、2、1、0.5、0.25 μg·mL-1的溶液,摇匀。
分别精密量取适量氢化物工作对照品储备溶液,加稀释溶剂稀释制成100、50、20、10、5、2、1、0.5、0.25 μg·mL-1的溶液,摇匀。
按上述色谱系统(1.2.1)将上述标准溶液依次进样,记录峰面积。以峰面积为纵坐标,质量浓度为横坐标进行线性回归,得线性回归方程及相关系数,结果如表2所示。水解物在0.26~104 μg·mL-1范围内呈良好的线性关系(R2=1.000 0,n=6),氢化物在 0.26~105 μg·mL-1的质量浓度范围内呈良好的线性关系(R2=1.000 0,n=6)。
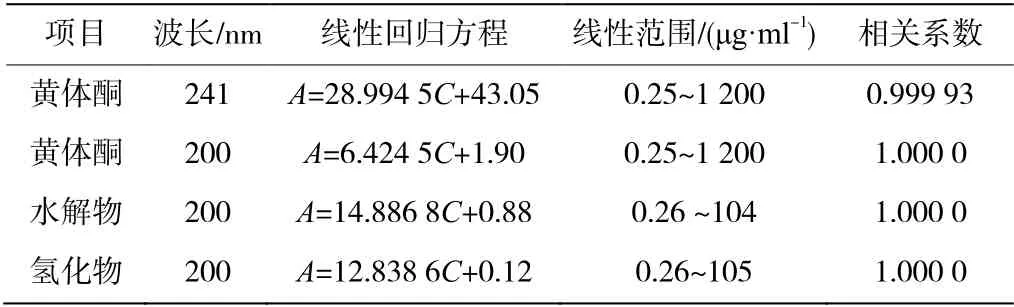
表2 线性关系测定结果
2.1.3 定量限与检测限
黄体酮、水解物、氢化物定量限溶液:精密吸取黄体酮对照品溶液0.4 mL、水解物工作对照品溶液5.0 mL、氢化物工作对照品溶液6.0 mL,置100 mL 容量瓶中,加稀释液稀释至刻度,摇匀,作为黄体酮、水解物、氢化物定量限溶液。
黄体酮、水解物、氢化物检测限溶液:精密吸取黄体酮、水解物、氢化物定量限溶液3.0 mL,置10 mL 容量瓶中,加稀释液6.0 mL,摇匀,作为黄体酮、水解物、氢化物检测限溶液
按本法测定,精密量取上述定量限溶液、检测限溶液分别进样10 μL,当信噪比S/N≥10 时,作为定量限溶液;当信噪比S/N≥3 时,作为检测限溶液。同时取各定量限溶液连续进样6 针,记录色谱图。结果表明,黄体酮、水解物和氢化物的定量限分别为0.040、0.517、0.640 μg·mL-1,均小于限度质量浓度(1.0 μg·mL-1);检测限质量浓度分别为0.013、0.172、0.213 μg·mL-1,均小于限度质量浓度(0.5 μg·mL-1)。
2.1.4 精密度试验
2.1.4.1 重复性
取6 份样品溶液检测,黄体酮、水解物、氢化物、未知杂质含量的相对标准偏差分别为0.02%、0、7.81%、0.37%,结果表明本方法重复性好。
2.1.4.2 中间精密度
2 位操作人员于2 天内分别按1.2.2 方法配制6份样品溶液进行分析,记录峰面积。2 位人员于2天内测得的黄体酮、水解物、氢化物、未知杂质含量的相对标准偏差分别为1.24%、0、0.39%、0.5%,结果表明方法的中间精密度符合可接受标准。
2.1.5 方法耐用性
固定其他色谱条件不变,将上述色谱条件分别改变流速(0.95、1.05 mL·min-1)、色谱柱温度(28、32 ℃)后进样,对水解物、黄体酮、碱降解物、氢化物分离度进行考察,实验结果表明,在上述色谱条件下,黄体酮与3 种杂质的分离度好,3 种杂质与黄体酮的相对保留时间(RRT)没有显著变化,各组分的含量基本恒定。因此,色谱条件的细微变化对测定结果没有影响。
2.2 样品测定
按 1.2.2 方法分别配制混合对照品溶液和样品溶液,按色谱系统1.2.1 色谱条件分别进样分析,按外标法计算黄体酮及各已知杂质的含量,其他未知杂质含量按不加校正因子的主成分自身对照法计算。样品测定结果见表3。
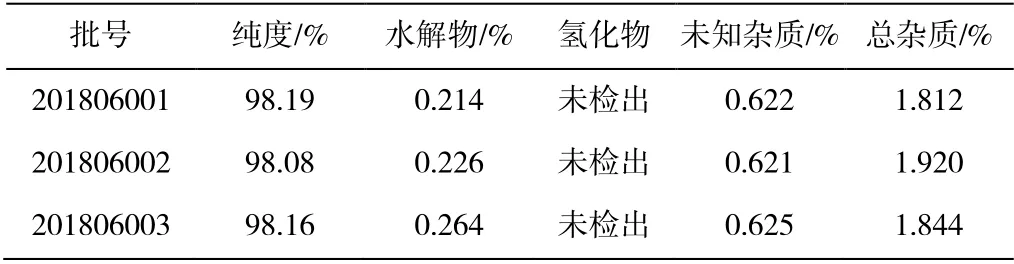
表3 黄体酮样品的测定结果
3 结 论
本文建立了高效液相色谱法200 nm 波长下测定黄体酮及有关物质的含量,本方法具有一定专属性、灵敏度、准确性、耐用性,可以作为黄体酮粗品、精制品质量的有效检验、监控。在黄体酮粗品波长200 nm 检测试验中,除了已知杂质水解物、氢化物等峰外,还检测出未知杂质峰。杂质分子结构、来源有待进一步分析研究,生产中暂归化法检测监控。

