响应面法优化辣椒籽油碱异构化制备共轭亚油酸工艺及其氧化稳定性
马 燕,许铭强,李喜弟,孟新涛,邹淑萍,张 婷,张 谦
(1.新疆农科院农产品贮藏加工研究所/新疆主要农副产品精深加工工程技术研究中心,乌鲁木齐 830091;2.新疆西尔单食品有限公司,乌鲁木齐 830091)
0 引 言
【研究意义】共轭亚油酸(conjugatedlinoleicacids, CLA)具有提高免疫力等一系列独特的生理功能[1,2],但天然CLA人体自身不能合成[3],多以高亚油酸植物油为原料形式转化生成。辣椒(CapsicumannumL.)是新疆“红色产业”的重要支柱作物之一[4],其在加工过程中会产生大量的副产物,辣椒籽作为辣椒主要加工副产物,籽油中富含不饱和脂肪酸,其中亚油酸含量72.2%~74.26%[5],可作为一种制备共轭亚油酸的经济、廉价原料新资源。若能利用高效、可行且易于生产的加工技术开发辣椒籽油CLA新资源功效食品,不仅可为规模化生产奠定基础,也可大幅度提高辣椒籽的全效利用率和附加值,对延长辣椒加工产业链,缓解资源,推进果蔬副产物综合利用和环境友好型的辣椒加工产业发展具有重要现实意义。【前人研究进展】目前,我国对CLA的研究起步较晚,现主要研究从山核桃油[6]、红花籽油[7]、茶油[8]、葵花籽油[9]等亚油酸含量较高的油脂中提取共轭亚油酸,但对辣椒籽油共轭亚油酸方面的研究尚未见相关报道。CLA的制备化方法主要有生物法[10]和化学法[11]。其中碱异构化化学法得到的产物无毒、易处理、更适合工业化生产[12]。【本研究切入点】采用碱异构化制备共轭亚油酸的主要影响因素(温度、压力、碱性催化剂和醇类溶剂种类)及加工工艺条件不同,会直接影响CLA的得率[13],需寻找能够大量廉价制取CLA的原料资源和可靠的制备方法[14]。需研究充分利用辣椒副产物—辣椒籽作为制备共轭亚油酸的新资源。【拟解决的关键问题】以冷榨后的辣椒籽油为试材,分析碱异构法制备辣椒籽油共轭亚油酸的各因素对转化效果的影响,研究碱异构法的主要影响因素;探讨各试验因素及交互作用对转化率的影响;通过总体优化,为获得辣椒籽油CLA最优工艺条件,为新资源产品研发及辣椒副产物综合利用提供理论和技术依据。
1 材料与方法
1.1 材 料
辣椒籽,新疆西尔单食品有限公司提供;辣椒籽油(亚油酸含量为72.82%),自制;CLA标准品,购于Sigma-Aldrich上海贸易有限公司。KOH、聚乙二醇、无水硫酸钠、碘化钾、浓盐酸、正己烷、三氯乙酸等试剂为分析纯,均购于北京化学试剂有限公司。
TP-A1000型电子天平,福州华志科学仪器有限公司; EMS-18A磁力搅拌器,天津市欧诺仪器仪表有限公司;共轭亚油酸制备装置(自制);UV-1800紫外可见分光光度计,日本岛津公司;101型电热鼓风干燥箱,北京市永光明医疗仪器厂;SENCO R-501旋转蒸发仪,上海申顺生物有限公司。
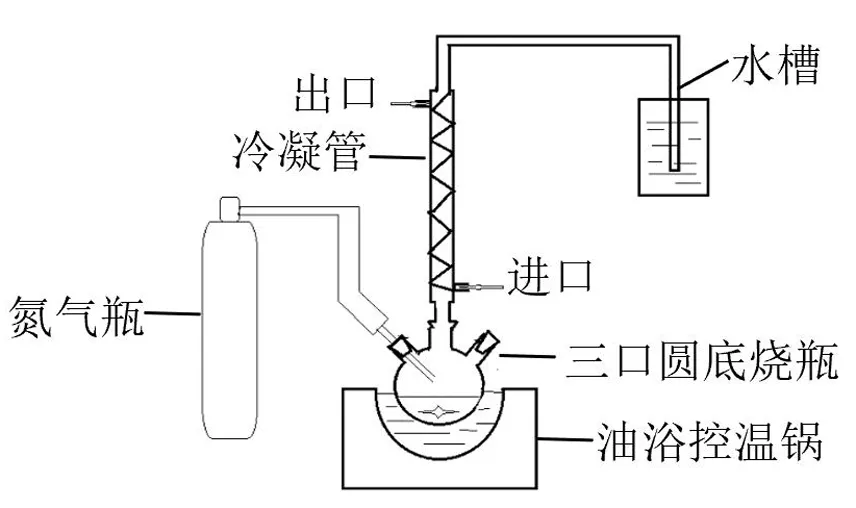
图1 自制共轭亚油酸反应装置Fig.1 Reaction diagram of conjugated linoleic acid by self-made device
1.2 方 法
1.2.1 CLA转化率的测定[8]
CLA标准曲线绘制: 将 CLA标准品100 mg用石油醚定容至 10 mL,配成标准溶液。从标准溶液中分别吸取20、40、60、80、100 μL CLA 定 容 至 100 mL,以正己烷为参比,采用紫外可见分光光度计测定其在 233 nm 处的吸光度。以 CLA 的质量浓度为横坐标, 吸光度为纵坐标,绘制 CLA 标准曲线,得到的回归 方程为y= 0.009 8x(R2= 0.999 6) 。
共轭亚油酸转化率的测定: 取一定量的 CLA样品,用正己烷稀释,振荡。以正己烷为参比,在 233 nm 处测其吸光度,利用标准曲线计算样品的质量浓度,并按下式计算 CLA 转化率:
1.2.2 碱异构化制备辣椒籽油 CLA实验设计
参考陈丽敏[15]和潘群文[16]等方法。称取一定质量的催化剂KOH与溶剂聚乙二醇加入辣椒籽油中,在氮气保护下油浴迅速加热至一定温度,充分反应一段时间后终止反应,冷却至 60℃,加入一定温水搅拌30 min,并用 0.5 mol/L的浓盐酸调节 pH至2; 待静置分层后,将上清液转移至分液漏斗中,用蒸馏水洗至中性,再用无水硫酸钠脱除多余水分,得辣椒籽油CLA样品,保存备用。
1.2.3 响应面法优化试验
在前期单因素试验得出较优的工艺条件(反应温度170℃、反应时间4 h、碱油比0.3、溶油比1.5)的基础上,以共轭亚油酸转化率为响应值,选择辣椒籽油反应温度(X1)、反应时间(X2)、碱油比(X3)和溶油比(X4)这4个因素作为对转化影响较大的试验因子。
1.2.4 辣椒籽油CLA氧化能力稳定性测定
将辣椒籽油和辣椒籽油CLA置于60℃烘箱中进行加速氧化,每隔2 d测定其过氧化值(POV)和TBA反应物。
1.2.4.1 过氧化值测定[17]
参照GB 5009.227-2016的测定方法进行测定。
1.2.4.2 TBA 反应物测定[18]
称取2 g 样品分别加入3 mL 蒸馏水、4 mL 20%三氯乙酸和2 mL 0.67%TBA混合均匀,沸水浴加热15 min后冷却,在5 000 r/ min条件下离心10 min,取下层清液于532 nm测定其吸光度。
1.3 数据处理
运用Design-Expert 11.00 进行响应面设计,采用Origin9.2软件进行图表绘制,利用Excel、SPSS 22.0进行数据分析和处理。
2 结果与分析
2.1 响应面优化
2.1.1 数学模型的建立
在前期单因素试验中,选择反应温度(150、160、170、180、190℃)、反应时间(2、3、4、5、6 h)、碱油比(0.9、0.7、0.5、0.3、0.1)和溶油比(0.5、1、1.5、2、2.5)进行4因素3水平试验,通过单因素试验确定辣椒籽共轭亚油酸制备较佳工艺参数为反应温度170℃、反应时间4 h、碱油比0.3、溶油比1.5,并在单因素的基础上以反应温度(X1)、反应时间(X2)、碱油溶比(X3)和溶油比(X4)为响应因子,进行辣椒籽油共轭油酸制备工艺优化研究,分析各因子对共轭转化率(Y1)的影响。表1,表2

表1 因素与水平Table 1 Factors and levels of response surface

表2 优化试验设计与结果Table 2 Optimize experimental designs and results

续表2 优化试验设计与结果Table 2 Optimize experimental designs and results
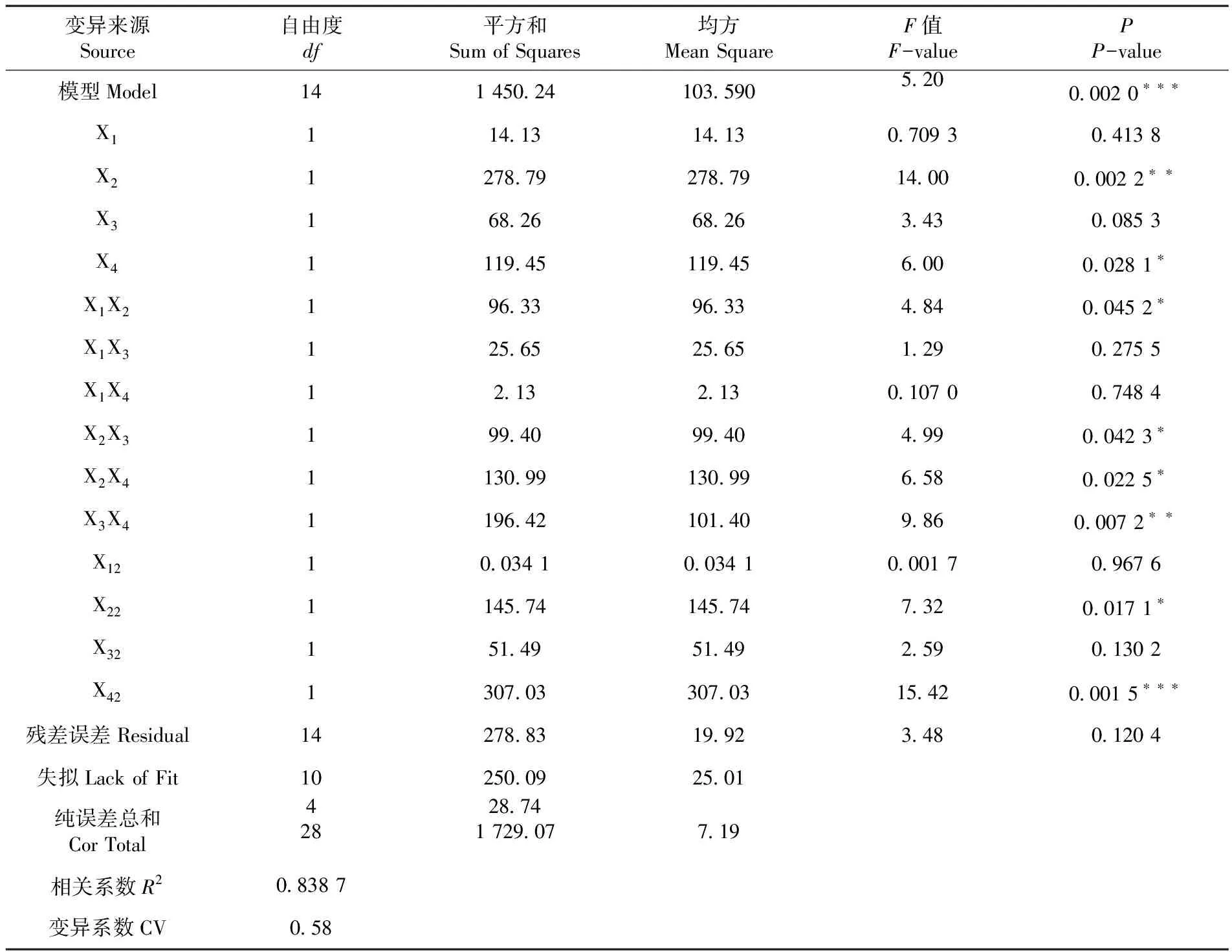
表3 回归模型系数及显著性检验结果Table 3 Regression coefficients and significant test for quadratic polynomial model equation
共轭转化率与反应温度、反应时间、碱油比和溶油比相互关系的二次多项数学回归方程:
Y=86.03+1.08X1+4.82X2+2.39X3+3.15X4-4.91X1X2-2.53X1X3+0.73X1X4-4.98X2X3-5.72X2X4-7.01X3X4-0.07X12-4.74X22-2.82X32-6.88X42
模型中P=0.002 0<0.01,回归模型极显著,P=0.120 4>0.1,失拟项不显著,该模型拟合程度良好,试验误差小;模型中的部分一次项、二次项和平方项影响显著。相关系数R2为0.838 7,模型方程拟合程度较好。设计实验中的CV为0.58%,实验精确度越高,回归方程符合模型建立。根据F值大小确定各因素对辣椒籽油CLA转化率的影响依次为:反应时间>溶油比>碱油比﹥反应温度。表3
2.1.2 响应面图分析与优化
研究表明,响应曲面图较为平缓,反应温度和碱油比、溶油比之间对共轭转化率交互作用不显著。响应曲面图较为陡峭,反应时间和碱油比、溶油比,碱油比和溶油比之间对共轭转化率交互作用显著。整个响应曲面呈山丘形,共轭转化率随着各因子量的上升而增大,达到最高值后逐渐缓慢,每个影响因子对共轭转化率都有一个最佳值。最优点:X1=-0.11,X2=-0.35,X3=-0.48,X4=0.31,并得到最佳工艺组合为:反应温度为169℃、反应萃取时间为4.4 h、碱油比为0.2、溶油比为1.7,模型预测共轭转化率为84.72%。图2

图2 因子交互与共轭转化率的响应面图Fig.2 Response surface diagram of factor interaction and conjugate conversion
2.1.3 验证实验
研究表明,共轭转化率分别为84.56%、84.13%、85.12%,平均值为84.60%(误差0.12%)。所得最大预测值接近验证值,建立的模型与实际情况比较吻合。
2.2 CLA的氧化稳定性
研究表明,相同天数的辣椒籽油CLA 过氧化值明显高于辣椒籽油过氧化值。辣椒籽油过氧化值(0.78~2.71 mmol/kg)和辣椒籽油CLA过氧化值(0.8~2.13 mmol/kg)在前6 d 的变化较为稳定,随后上升较快,到第14 d辣椒籽油的过氧化值达10.95 mmol/kg,约为辣椒籽油CLA 的1.75倍。吸光度值越高,TBA反应物的量越大。吸光度值随着天数的增加呈上升趋势,辣椒籽油吸光度值(0.125~0.3)和辣椒籽油CLA吸光度值(0.12~0.2)在前8 d 变化较为稳定,随后上升较快,到第14 d辣椒籽油的吸光度值达0.8,约为辣椒籽油CLA 的1.3倍。辣椒籽油CLA 具有较好的氧化稳定性。图3,图4
3 讨 论
在辣椒籽油CLA制备过程中,单一因素(反应时间、溶油比、碱溶比和反应温度)对CLA转化率虽有影响,但起主导作用的是不同因子间的交互效应,随着交互效应越显著,CLA转化率越高。碱油比与溶油比交互作用对CLA转化率影响极显著,反应时间与碱油比、反应时间和反应温度之间交互作用对CLA转化率显著,因子间的交互作用组合均存在单一最优水平,可用于碱异构化法制备辣椒籽油CLA工艺优化,同时可根据显著性分析结果,去除模型中不显著项[19],进一步得到以下简化模型:Y=86.03+4.82X2+3.15X4-4.91X1X2-4.98X2X3-5.72X2X4-7.01X3X4-4.74X22-6.88X42,获得转化率较高的辣椒籽油CLA。在操作过程中,虽然较高的反应温度有利于提高CLA转化率,但在反应过程中亚油酸易发生分解、热聚合及环化等副反应,不利于共轭化和活性成分[20],在操作过程中应严格控制反应温度。

图3 辣椒籽油和辣椒籽油CLA中过氧化值比较Fig.3 Comparison of peroxide value between pepper seed oil and pepper seed oil CLA

图4 辣椒籽油和辣椒籽油CLA中TBA反应物比较Fig.4 Comparison of TBA reactant between pepper seed oil and pepper seed oil CLA
过氧化值和TBA反应物分别反映了油脂氧化初产物和氧化产物生成量,是衡量油脂氧化稳定性的主要指标[21],测定过氧化值和TBA反应物能够更好地反映过氧化值稳定性。通过进一步对辣椒籽油CLA的氧化稳定性分析发现,辣椒籽油CLA较辣椒籽油具有较好的氧化稳定性,这可能与共轭不饱和脂肪酸和非共轭不饱和脂肪酸的氧化机理不同有关[22]。该结果与张红玉等[8,23]研究结果一致。辣椒籽油和辣椒籽油CLA的TBA反应物在前4 d 的吸光度值变化差异不大,这可能是由于CLA在氧化起始阶段的过氧化物积累较少, 并能较快地转变成氧化第二阶段产物导致[23]。后期可进一步探究其抗氧化机理,从而寻求提高其抗氧化水平的方法。
4 结 论
4.1采用响应面优化法建立了碱异构化制备辣椒籽油CLA的二次回归方程,并通过显著性分析得到影响辣椒籽共轭转化率的因素依次为:反应时间>溶油比>碱油比﹥反应温度;辣椒籽油CLA的最佳转化条件为:反应温度为169℃、反应萃取时间为4.4 h、碱油比为0.2、溶油比为1.7,此时共轭转化率为84.60%,辣椒籽油CLA较辣椒籽油具有更好的氧化稳定性。
4.2辣椒籽油CLA可作为一种良好的运动食品和营养辅助保健食品原料或功能性辅料。

