钠离子电池正、负极材料研究进展*
丁玉寅,祝鹏浩,陆继鑫,王存国
(青岛科技大学橡塑材料与工程教育部重点实验室 山东省橡塑材料与工程重点实验室,山东 青岛 266042)
钠离子电池(Sodium ion batteries,SIBs)的研究可追溯到20世纪80年代,与锂离子电池(Lithium ion batteries,LIBs)的发展几乎在同一时代[1-5]。早期研发的SIBs电极材料性能欠佳,导致SIBs发展处于停滞状态。但由于近年来全球含锂资源逐渐减少,锂盐价格逐渐升高,并且随着电动汽车的普及,动力电池需求不断增长,因此,新型二次电池如SIBs[6-8]、镁离子电池[9]、铝离子电池[10]及锂/硫电池[11-14]、锂/硅电池[15-18]等得到迅速发展。尤其是SIBs,相对于LIBs来说还具有以下优势[19]。(1)地壳中钠的储量规模极大,在金属储量中位列第四;(2)钠盐电导率明显高于锂盐,因此电解液具有较高的电导率;(3)SIBs在工作过程中可以放电到零伏而不会出现过放电;(4)SIBs的能量密度比较大。因此,上述SIBs的性能特点使SIBs成为未来替代LIBs的较佳选择。作者对SIBs工作原理、电极材料、电解质等方面的发展进行了详述。
1 SIBs工作原理
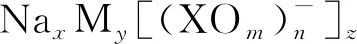
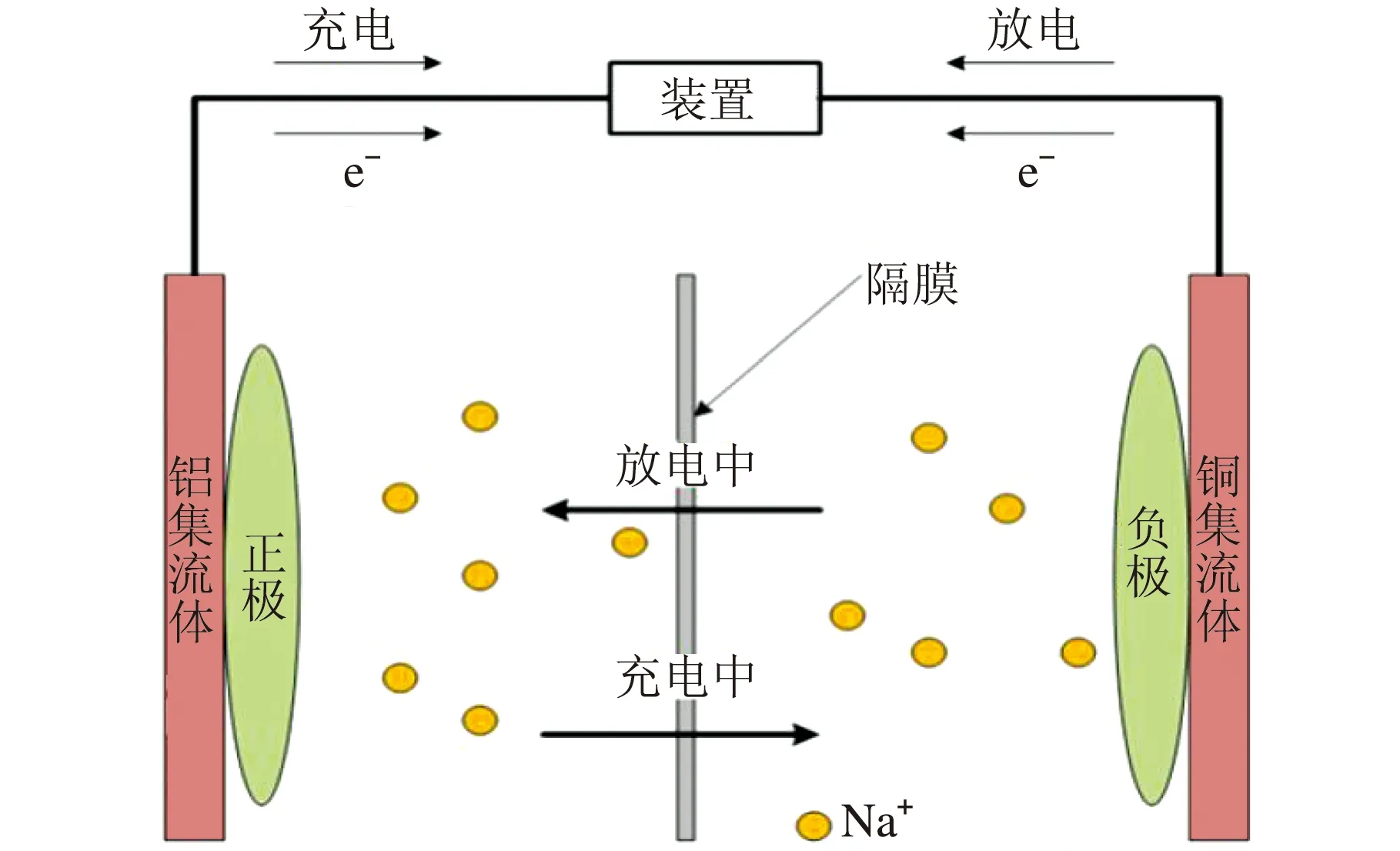
图1 Na+电池的工作原理示意图

(1)

(2)

(3)
2 SIBs分类
SIBs分为钠硫电池、钠盐电池、钠空气电池、有机系SIBs、水系SIBs等。
(1)钠硫电池。钠硫电池的负极为熔融液态金属钠,正极为单质硫,以固态β-Al2O3陶瓷作电解质兼隔膜,钠硫电池的比能量较高。
(2)钠盐电池。钠盐电池的负极为液态钠,正极为金属氯化材料,电解质为Na+导体β-Al2O3陶瓷。在放电过程中,负极发生氧化还原反应会产生Na+,穿过电解质以及次级电解液到达正极,充电过程则相反。钠盐电池使用的次级电解液通常为由氯化钠和三氯化铝组成的混合溶液。
(3)钠空气电池。钠空气电池正极通常采用多孔材料,由于材料中孔洞的存在不仅为气体的扩散提供通路,同时也为电极反应提供场所;另外,该电池的一个特点是在放电过程中生成物会逐渐填满孔隙,填满后意味着放电过程结束。
(4)有机系SIBs。有机系SIBs的负极由硬碳或可嵌钠材料组成,因为LIBs使用的石墨材料不适用于钠离子材料,而适用于SIBs的硬碳材料却由于价格高昂,已成为该类电池最大的缺陷之一。
(5)水系SIBs。水系SIBs与有机系电解质电池相比,电解质不同,因而水系比有机系电解质安全性能高。有机系SIBs由于自身存在的高成本、安全性能差等问题没有得到大规模应用,而水系SIBs的出现恰好弥补了有机系电解质电池的缺点,电池原料成本较低,且安全性能高,适合于大规模储能设备使用。
3 SIBs正极材料
正极材料决定电池能量密度、寿命及安全性。所以研究提供丰富的活性位点和畅通的Na+迁移通道成为现阶段SIBs的研究关键。由于Na+半径大,导致Na+嵌脱更困难,许多电极材料能在LIBs中广泛应用,但不能直接应用于SIBs中。当前研发的SIBs正极材料,主要包括过渡金属氧化物、聚阴离子化合物和普鲁士蓝类化合物等晶态材料。
3.1 过渡金属氧化物
过渡金属氧化物分为层状和隧道状,表达式为NaxMO2(M为Co、Fe等),见图2。

a 隧道结构
图2a为具有S型隧道结构和五边形隧道结构的过渡金属氧化物的晶体结构。Na+在S型隧道中可以可逆地脱嵌,而在五边形隧道中却不具备电化学活性。其中典型正极材料是含钠的锰氧化物如Na0.44MnO2,其Mn—O八面体结构起支撑作用,以保证在电化学循环过程中Na+的运动不会改变材料的结构,提高电池的循环寿命。另外,部分Ti取代Mn可以提高离子电导率,并改善隧道的尺寸和长度。
Zhou等[20]对含钠层状化合物进行如图2b和2c分类,主要分为O3型和P2型,其中P结构NaxMO2具有较高的层间距,有利于Na+的可逆脱嵌;而O结构具有更多的嵌钠位点,展现出高的比容量;因而通过P型和O型2种结构结合,可以获得兼具高倍率和高容量性能的NaxMO2正极材料。
上述材料结构简单,电极材料易于合成,而且原料丰富,被认为是最具有发展潜力的正极材料之一。层状过渡金属氧化物的充放电曲线通常呈现多个平台,对应于Na+脱嵌过程中的一系列相变和固溶体反应。因为Na+半径较大,材料结构会在电化学循环中产生不可逆的相变,使循环容量衰减,此外,部分层状过渡金属氧化物,其导电性和倍率性能较差。
3.2 聚阴离子化合物

聚阴离子型储钠材料,其稳定结构能够使Na+具有较高的扩散系数,较低的体积膨胀系数,且在循环过程中产生较少的相变,有利于循环稳定和安全性的提高。但链结构中所包含的较大的聚阴离子基团,降低了材料的离子导电性和循环过程中的容量保持率。
聚阴离子化合物的种类较多,如磷酸盐、焦磷酸盐等,最典型的聚阴离子正极材料是磷酸盐(其结构见图3),磷酸盐分为橄榄石型和NASICON(Na超离子导体)。但由于V2O5所含毒性较大,大规模使用会对环境及人体产生危害,因此开发无毒环保的NASICON型材料也是目前的主要研发方向之一。常见的聚阴离子化合物及其性能见表1[21]。
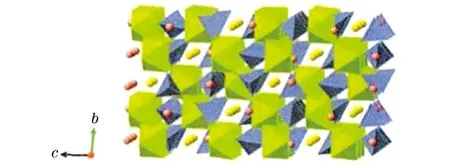
a NaFePO4沿a轴的结构图

表1 常见的聚阴离子化合物正极材料
3.3 非晶态材料
长程非晶态材料又称无定形材料,呈现长程或短程无序。因此,无规则结构可提供更多储钠位点,提高材料的理论比容量。当前适用于SIBs的非晶态材料较少,需要设计材料的构成和合成工艺,例如使用SiO2、B2O3等结构体代替P2O5形成玻璃骨架。
晶格限制较弱的非晶态材料具有极大的研究前景,但目前面临以下困难。(1)电导率低,不利于电池的高倍率性能。目前,可以通过热处理、离子掺杂、碳包覆等手段改善;(2)化学稳定性和耐酸碱性差,活性物质可能会溶解到电解质中,循环性能差。可以通过改善非晶态材料组成,调整材料物化性能,达到电化学性能与理化性能的平衡;(3)非晶态材料会产生结构变化。
总之,非晶材料由于晶格要求较少,Li+、Na+半径差异影响较小,因而锂化玻璃态材料可以通过离子替换变成钠化玻璃态材料,作为SIBs正极材料,而且极具研究前景。
4 负极材料的发展状况
由于Na+半径较大,传统的石墨材料无法满足高储钠能力,给负极材料的选择造成了极大困难,原本基于LIBs负极材料基础上进行的研究已经无法适用SIBs。
目前,碳基材料、金属材料与合金材料是研究较多的负极材料。根据充放电反应机理,也可分为嵌入型、合金型、转换型等电极材料。其中,碳基材料种类多、成本低、合成工艺简单,并且作为材料的负极拥有足够低的工作电位,但其较低的比容量一直是研发的重点;相比之下,金属材料具有更大的容量以及更高的安全性,但在Na+脱嵌过程中会存在较大相变,从而影响电池的循环性能,同时其电导率也很低。
4.1 嵌入型负极材料
嵌入型材料分为碳基材料和钛基氧化物。碳基材料又分石墨碳材料和非石墨碳材料,石墨碳材料已经在商用LIBs中得到普遍应用;与石墨储锂原理相似,Na+在充放电过程中嵌入石墨层间,形成石墨-钠插层化合物;同样,由于Na+半径过大,传统的石墨负极材料无法保证良好的储钠特性,在传统电解质中仅有小于20 mA·h/g的Na+存储容量。通常改性方法如下。(1)掺杂N、S元素或引入官能团、碳纳米管(CNT)等来增大层间距;(2)用醚基电解质抑制电解质的自发分解,在天然石墨表面形成薄层电解质薄膜界面,有利于Na+嵌入石墨层间。
对于碳基材料的早期研究,显示其比容量低、安全性差等特点。根据以前诸多研究,各种非晶碳的储钠性能非常优异,其中硬碳材料因较大的容量和较好的循环稳定性而获得更多的关注。硬碳材料是典型的嵌入型材料,因在高温下难以石墨化,又称之为不可石墨化碳。硬碳材料在微观上是不同取向的石墨微晶,Na+可以嵌入到取向不同的石墨层间空隙中,也可以部分地嵌入到石墨微晶片层上,其非平行取向的微观结构更有利于Na+的存储(硬碳材料的储Na+结构见图4)。
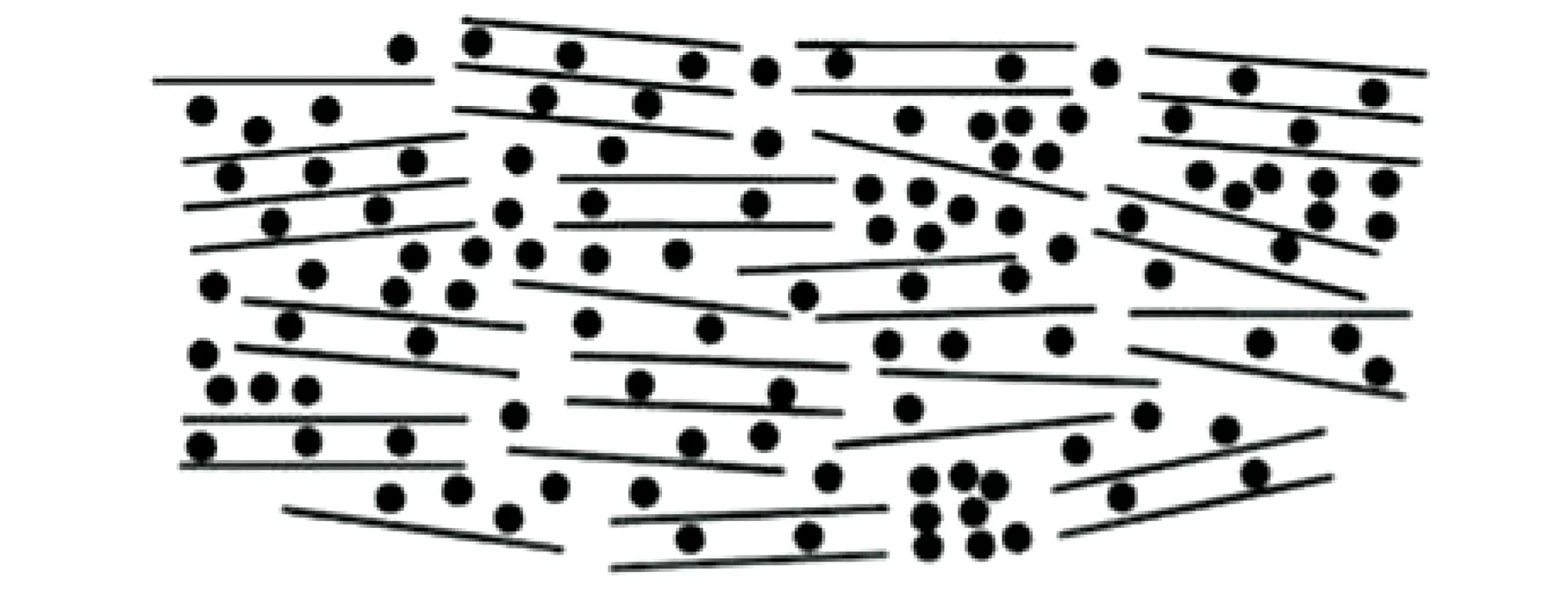
图4 Na+嵌入硬碳材料的结构模型
将沥青等一些含C的前驱体高温裂解可以制得硬碳。例如索莉瑶等[22]在1 000 ℃高温裂解中空碳球(直径约为50 nm),得到形貌均一的空心材料,循环100次后(100 mA·h/g),比容量达160 mA·h/g。这是因为中空结构有利于Na+的脱嵌,使离子迁移速度加快,有利于提高充放电速度。
嵌入型负极材料还有层状钛基氧化物,如不同晶型的氧化钛、钛酸锂和钛酸钠。钛基氧化物的储钠机理主要依靠氧化还原反应。为了促进Na+的传输与迁移,祁莹等以过渡金属二维层状材料(MXene)作前驱体,通过水热法自组装合成了绒球状的Na2Ti3O7@C,其在2 A/g下循环200圈仍保持119 mA·h/g的容量[23]。
4.2 合金型负极材料
相比于嵌入型负极材料(如硬碳材料的理论容量300 mA·h/g),合金型材料的理论容量更高,如Sn(847 mA·h/g)、Ge(369 mA·h/g)、P(2 596 mA·h/g)、Sb(660 mA·h/g)等[20]。合金材料的合成方法有水热法、溶胶-凝胶法、化学还原法等。另外,不存在类似嵌入型负极材料的较低电压平台,而导致Na沉积在电极表面,产生安全问题。但合金型负极材料与钠存在合金化反应,造成剧烈的体积膨胀[24-25],从而造成电极材料破裂,比容量下降。常见的解决方法有合金材料纳米化、与碳材料复合改性、结构设计等方法,从而可以有效地缓解这一现象。
近年来的研究表明,纳米结构的磷与碳基材料复合能够提高储钠性能[26]。Zhang等[27]用超声剥离得到少层黑磷,表面再修饰官能团,通过交联碳纤维,最终合成性能优异的少层黑鳞/聚(3,4-亚乙基二氧噻吩)复合物(E-BP/PEDOT)。由于少层黑磷的表面改性,碳纤维形成的导电网络有利于电荷传输,并且官能团的引入增强了电极和电解质之间的浸润过程。
设计合成二元金属键化合物可以同时具备高比容量和低体积膨胀率,因为二元金属中间态可以缓冲生成物的体积膨胀。Liu等[28]通过溶剂热法合成多孔的Ni3Sn2双金属微笼,空心核结构有利于抑制体积膨胀,同时产生的Ni均匀地包裹M-Sn,促进了离子迁移。Ni3Sn2金属微笼,在0.2C的电流密度下,经过400次循环后容量保持在700 mA·h/g。
4.3 转换型负极材料
转换型负极材料根据物质类型可以分为金属氧化物(MOx)、硫化物(MSx)和磷化物(MPx)。金属硫化物相较于金属磷化物与金属氧化物,其理论比容量较低,电压平台范围较宽,在电化学循环过程中,发生的体积膨胀率远小于后两者[29]。因此,关于体积膨胀的影响至今仍然是金属硫化物的主要研究方向,如Xu等[30]利用简单溶剂热法合成的氮掺杂石墨烯片负载MoS2纳米材料,通过负载增强MoS2的导电性,减小MoS2纳米材料的尺寸缩短Na+传输路径,扩大MoS2的层间距以提高Na+的传输速率,该实验明显改善了MoS2电化学性能。
转换型负极材料相比于合金型负极材料,拥有更高的比容量,在电循环过程中的体积膨胀率低于合金型材料。转换型负极材料在进行转换反应时往往会伴随着插层反应或合金化反应[31],因为金属的加入,导电性增加。依据金属的活泼性可分为两类。(1)加活泼金属Sn;(2)加不活泼金属Ge[32]。活泼金属会与碱金属Na发生转换反应和合金反应,生成物具有较高的比容量,同时降低复合物的体积膨胀。另外,为了抑制材料的体积膨胀而造成复合材料的脱落、剥离,通常会添加碳基材料进行复合改性,利用碳材料优异的导电网络,还可以提高Na+的传输速率。
5 结束语
综述了SIBs正负极材料的研究进展,并针对正、负极材料的某些缺陷,提供了相应的解决办法,最终通过对SIBs正负极材料内部结构的设计和优化提高SIBs的电化学性能,从而提高电池的可逆容量和循环寿命。目前,SIBs虽然已经开始商品化,但制备高性能SIBs电极材料将是未来重点研发方向之一,通过优化和改进电极材料,合成出匹配的电解质,改善电池的性能及安全性是未来SIBs要解决的两大重点课题。

