探寻命题思路 把握解题规律
——化学实验综合题的命题与解题剖析
吉林 赵鑫光 郝家琳
化学实验综合题通常以真实的化学化工实验为背景,通过系统的实验设计和完备的研究方法加以呈现。该试题因综合程度高、命题素材广、考查角度灵活等特点在高考中高频出现。该试题主要考查学生对基本仪器的识别与应用能力,物质的制备、除杂与分离操作能力,实验现象分析能力,实验步骤的改进和设计能力,语言描述、总结与评价能力以及数据处理能力等,具有较强的选拔功能。
近年来,化学实验综合题常通过新颖的实验情境,要求考生根据实验目的和原理,解决真实问题,将基础知识、必备技能和研究方法与情境结合,体现了高考命题对“证据推理与模型认知”及“科学探究与创新意识”化学学科核心素养的考查。本文尝试以“坎尼扎罗反应”为例,对化学实验综合题的命题与解题进行简单剖析,希望对广大一线教师有所帮助。
【反应原理】
意大利化学家坎尼扎罗在1895年,通过用草木灰处理苯甲醛获得了苯甲酸和苯甲醇,这个反应通常称为坎尼扎罗反应。它是一个含醛基化合物的歧化反应,其反应原理是
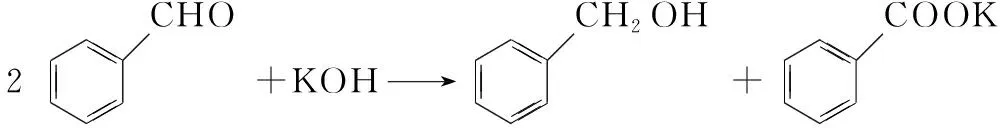
该反应过程中放出较大热量。
【实验装置】
本实验可能用到的实验装置如图所示:
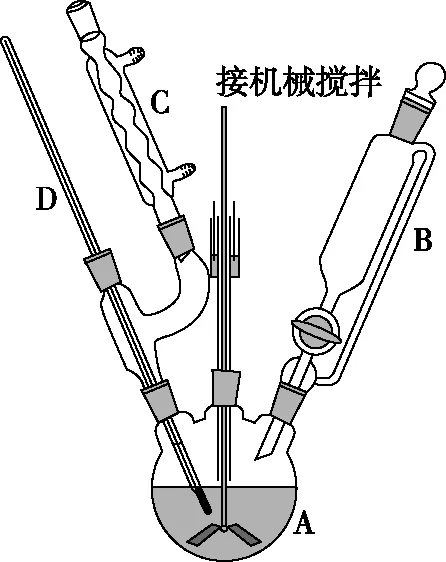
a
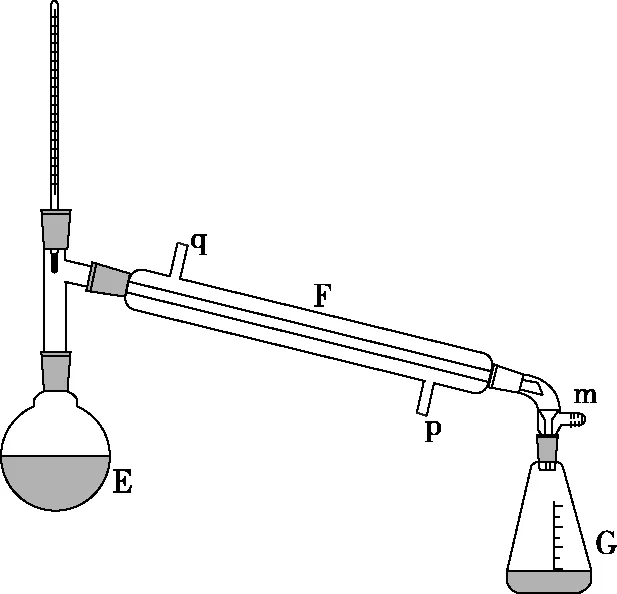
b

c

d
【实验步骤】
①向仪器A中加入0.1 mol新蒸馏的呋喃甲醛,用冰水浴冷却,向仪器B中加入8 mL 33%的NaOH溶液,在机械搅拌下,缓慢滴加氢氧化钠溶液,控制反应温度为8~12℃,滴加完成后保持温度在8~12℃,回流20 min,得到黏稠的黄色浆状物。
②将仪器A中的产物倒入盛有约20 mL水的烧杯中,粗产品完全溶解,溶液呈暗红色,将混合物倒入分液漏斗,用乙醚萃取4次,每次10 mL,合并醚层备用。
③向水层中分批加入25%盐酸,调节至pH=3,冷却结晶,过滤得到呋喃甲酸粗品(略带黄色)。
④在醚层中加入适量无水硫酸镁,振荡静置,过滤后转移至蒸馏装置,采用水浴蒸出乙醚,继续加热蒸馏得到产品呋喃甲醇3.5 mL。
⑤将呋喃甲酸粗品,用适量水加热溶解,停止加热稍冷后加入0.2~0.3 g活性炭,继续加热煮沸3~5 min,趁热减压过滤,将滤液冷却至室温后,再用冰水浴冷却,过滤,洗涤,80~85℃烘干,得到呋喃甲酸样品4.8 g。
⑥呋喃甲酸纯度的测定:取1.120 g呋喃甲酸样品,配成溶液,并在100 mL容量瓶中定容备用。配制氢氧化钾溶液,经邻苯二甲酸氢钾标定后,其浓度为0.080 0 mol·L-1。准确量取20.00 mL呋喃甲酸溶液于锥形瓶中,滴加合适的指示剂,用标定后的氢氧化钾溶液滴定,平行滴定三次的数据如表1所示。

表1
【相关信息】
实验中可能用到的相关物质的物理性质如表2所示。
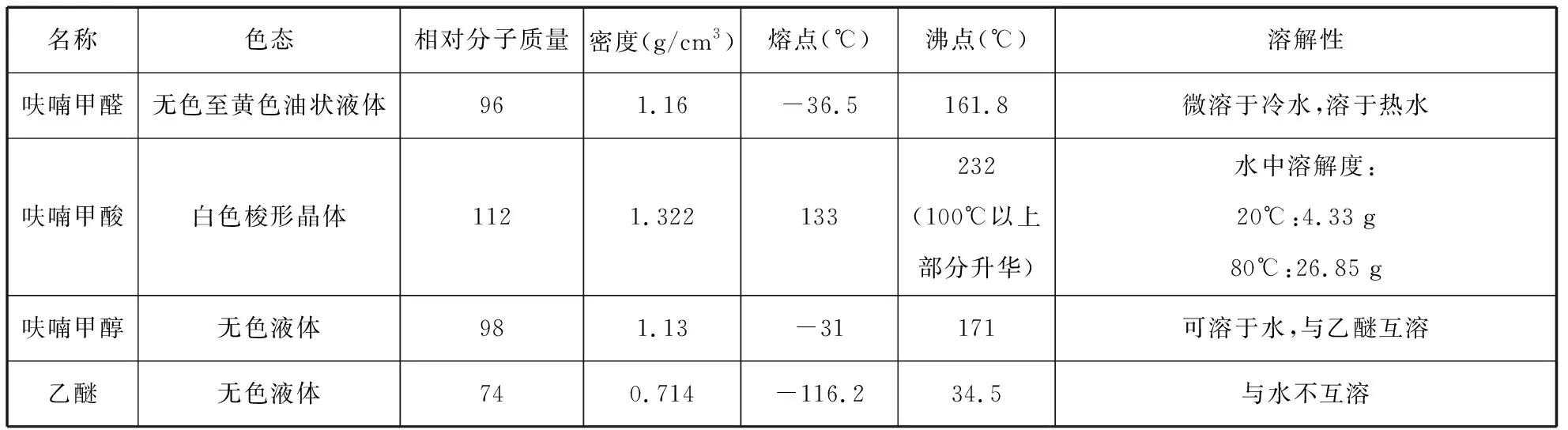
表2
【设问方向一:对实验原理的理解和分析】
(1)实验时要缓慢滴加氢氧化钠溶液,其原因是________________。
(2)反应过程中温度要控制在8~12℃,温度过高或过低对实验结果的影响是________。
(3)步骤③中化学反应的离子方程式为____________________________。
(4)配制的氢氧化钾溶液需要标定,其原因是________________。

【分析及参考答案】
(1) 由题干信息中“该反应过程中放出较大热量”可知该反应为放热反应,滴加氢氧化钠过快会使温度升高,发生副反应,影响产物的产率。
(2)温度过高,会导致发生副反应,使该反应产率降低;温度过低,反应速率过慢,使连续滴加的NaOH聚集,一旦开始反应温度将无法控制。
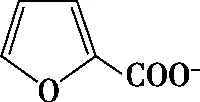
(4)因氢氧化钾固体会吸水,且配制溶液时氢氧化钾会与空气中的CO2反应,造成溶液浓度不准确,故滴定前应该用基准物进行标定,确定其准确浓度。
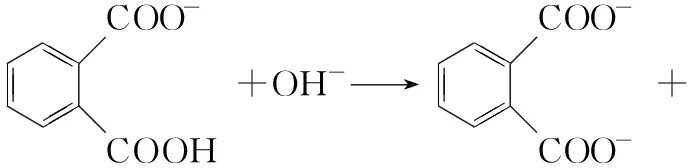
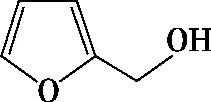
(6)由甲醛、苯甲醛、呋喃甲醛的结构简式可知,它们共同的特点是与醛基相连的碳原子上没有氢原子,而乙醛中与醛基相连的碳原子上有氢原子,故能发生坎尼扎罗反应的醛的结构特点为与醛基相连的碳原子上没有氢原子(或无α-H的醛)。
【设问方向二:对实验仪器的辨识和选择】
(7)装置图中,仪器A~G的名称分别是A_________,B_________,C_________,D_________,E_________,F_________,G_________。
(8)与普通分液漏斗相比,仪器B的优点是____________________________。
(9)在滴加氢氧化钠的过程中,机械搅拌的目的是________________。
(10)水浴蒸馏乙醚时应选用容积为________的圆底烧瓶。
A.25 mL B.50 mL C.100 mL D.250 mL
(11)步骤⑥中准确称量呋喃甲酸样品应使用的仪器是________。
【分析及参考答案】
(7)考查对基本化学仪器的辨识,故A为三颈烧瓶,B为恒压滴液漏斗,C为球形冷凝管,D为温度计,E为圆底烧瓶,F为直形冷凝管,G为锥形瓶。
(8)恒压滴液漏斗与普通分液漏斗相比,有一个连通分液漏斗和反应容器的恒压管,它可以平衡气压,便于液体顺利滴下,防止滴加的液体挥发损失,也可以防止漏斗中的液体与空气中的氧气、水蒸气、二氧化碳等发生反应而损失。
(9)根据反应原理和各物质的物理性质,氢氧化钠溶液与呋喃甲醛不互溶,该反应在两相中进行,机械搅拌可以增大两相的接触面积,加快反应速率。
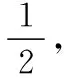
(11)步骤⑥中称量呋喃甲酸的质量需要精确到0.001 g,故选择的仪器应该为电子天平或分析天平。
【设问方向三:对实验试剂的选取和使用】
(12)实验中应使用新蒸馏的呋喃甲醛,其原因是________________。
(13)步骤②中选用乙醚作为萃取剂的原因是________________。
(14)步骤④中无水硫酸镁的作用是________,
其作用原理为________,蒸馏醚层获取呋
喃甲醇前必须过滤的原因是________________。
(15)滴定过程中使用的指示剂是____________,其原因是________。
其滴定至终点的现象是________。
【分析及参考答案】
(12)根据题干信息中呋喃甲醛的性质“在空气中易被氧化变色”,可得出:久置的呋喃甲醛会被空气中的氧气氧化为呋喃甲酸,而使反应物不纯。
(13)本题考查萃取剂的选用原则,选用乙醚作萃取剂的原因为以下三点:①乙醚与水不互溶;②呋喃甲醇在乙醚中溶解度比在水中大;③呋喃甲醇与乙醚不反应。
(14)本题考查无水盐作为干燥剂的原理,无水硫酸镁的作用是除去有机物中少量的水,其原理是无水硫酸镁可与游离水形成结晶水合物从而将水除去;因结晶水合物不稳定会受热分解出水蒸气,与产物同时蒸出,导致产物不纯,故蒸馏前必须过滤。
(15)本题考查酸碱中和滴定时指示剂的选择,使用的指示剂是酚酞溶液,其原因是呋喃甲酸钾是一个强碱弱酸盐,达到滴定终点时溶液显碱性,故使用酚酞试剂作为指示剂可以减少滴定终点的误差。滴定终点的判断方法是滴入最后一滴氢氧化钾标准溶液后,锥形瓶内溶液的颜色由无色变为浅红色且半分钟内不恢复。
【设问方向四:对实验步骤、现象的理解和解释】
(16)步骤①中,在反应过程中控制反应温度在8~12℃之间的方法是________。
(17)步骤②中得到的暗红色液体,用乙醚萃取后得到的物质是________(写名称和结构简式)。每次分液时,乙醚层应该从分液漏斗的________(填“上口”或“下口”)倒出。
(18)步骤④中,水浴蒸馏乙醚时,尾接管(牛角管)的m端口应连接橡胶管并深入到水槽底部,其目的是________________________;在开始加热前应先________,再开始加热,判断乙醚已经蒸馏完全的依据是________________。
(19)步骤⑤中,提纯呋喃甲酸的方法为________(填方法名称),加入活性炭的目的是________________。如未停止加热,直接加入活性炭可能导致的后果是________。
活性炭的用量应有所控制,若加入过量活性炭可能导致的后果是________________。
(20)步骤⑤中,滤液冷却至室温后,继续冰水浴冷却的目的是________________;烘干温度为80~85℃,温度过高可能造成的后果是________________。
【分析及参考答案】
(16)该反应放热,如想控制反应温度,应该将三颈烧瓶适当浸在冰水浴中,保证反应温度在8~12℃之间。
(18)乙醚沸点较低,且与空气混合后遇明火会燃烧,故应将牛角管的m端口连接橡胶管并深入到水槽底部,其目的是减少乙醚挥发到空气中,与空气混合遇明火爆炸;蒸馏操作的顺序是先通入冷凝水,再开始加热;当牛角管末端无液体滴出或温度计示数略有下降后继续上升时可表明乙醚已经蒸馏完全。
(19)根据步骤⑤中的描述,该提纯方法为重结晶;活性炭具有多孔性,其作用是对产品进行脱色;活性炭的孔道中吸附有气体,若未停止加热直接加入活性炭会使吸附的气体瞬间受热膨胀,引起暴沸造成危险;由于活性炭的吸附性是没有选择性的,故加入活性炭过多会导致产品被活性炭吸附,降低产量。
(20)因呋喃甲酸的溶解度随温度降低而减小,故冷却至室温后,继续冰水浴冷却的目的是降低呋喃甲酸的溶解度,尽可能多的获得产品,增大产率;根据题干中信息,呋喃甲酸超过100℃干燥容易升华,造成产率降低。
【设问方向五:对实验数据的分析和处理】
(21)简述如何量取0.1 mol呋喃甲醛?
________。
(22)由实验相关信息和数据可计算出
①呋喃甲酸的纯度为________;
②呋喃甲酸的产率为________;
③呋喃甲醇的产率为________(计算结果均保留三位有效数字)。
【分析及参考答案】
(21)根据表格信息,经过计算,0.1 mol呋喃甲醛的体积为0.1×96÷1.16 mL=8.28 mL,应该使用10 mL量筒量取8.3 mL呋喃甲醛液体。
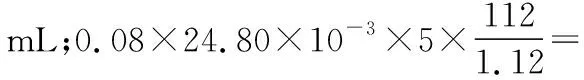
【设问方向六:对实验设计方案的改进和创新】
(23)乙醚完全蒸出后若采用常压蒸馏呋喃甲醇,继续加热前应将蒸馏装置(如图b所示)中的________(填仪器名称)换成________(填仪器名称),若无对应仪器进行更换,一个简单的操作是________,
加热到达所需温度前,应将________(填仪器编号)更换为另一干净的相同仪器,收集________℃的馏分可得到产品。
(24)蒸馏呋喃甲醇时也可以采用减压蒸馏装置(如图c所示),H是一根毛细玻璃管,其作用是________;
减压蒸馏的作用是________。
(25)趁热减压过滤装置如图d所示,将n端接入真空泵,减压过滤和常压过滤相比其优点是________;
趁热减压过滤的目的是____________________;趁热减压过滤需要使用双层滤纸,因在过滤过程中单层滤纸容易破裂,其原因是________。
【分析及参考答案】
(23)呋喃甲醇的沸点为171℃,当液体的沸点超过140℃时,为防止冷凝管炸裂,应将直形冷凝管换成空气冷凝管;若没有空气冷凝管,应停止向直形冷凝管中通水,并将冷凝管中残留的水排尽后用作空气冷凝使用;接收馏分前应更换新的干净的锥形瓶,以确保收集的馏分纯净;呋喃甲醇的沸点为171℃,故收集产品时温度计示数应为171℃。
(24)本题考查的是减压蒸馏的基本原理,毛细玻璃管的作用是提供气化中心;因为液体的沸点随压强的减小而降低,故减压蒸馏的作用是在较低温度下蒸馏出沸点较高的馏分,防止温度过高造成有机物分解。
(25)减压过滤的原理是减小抽滤瓶中的压强,在大气压的作用下,将液体快速过滤,故与常压过滤相比,其优点是加快过滤速度;趁热减压过滤的目的是需要分别进行考虑的:趁热是为了防止产物在过滤时析出,影响产量,而减压是为了加快过滤速度,过滤是为了除去不溶性的杂质;使用双层滤纸是因为高温下酸性溶液对滤纸有较强腐蚀作用,若使用单层滤纸容易造成透滤。
纵观历年高考化学实验综合题,虽呈现方式可能不尽相同,但考查的核心知识相对稳定。内容上一般以物质的制备、性质的探究等为载体,主要考查化学方程式的书写、实验基本操作的描述和实验方案的设计优化等。命题选取的反应原理既源于教材又高于教材;试题考查要求重视对实验基本操作和基本能力的考查,将实验方法渗透于试题中,增加对实验设计和实验评价的考查力度;设问上具有由易到难的梯度,既有对教材知识的考查,又有对实验综合内容的考查。针对高考试题,教师引导学生备考时要注重解决问题或解题的思维模型,注重寻找原理依据,掌握基本方法,分析思路过程,注重对语言描述等几个方面的训练,以求在备考过程中达到事半功倍的效果。


