控制变量法在高考探究实验中的应用及教学启示
广东 骆 涛 苏章顺
1.问题的提出
化学是一门以实验为基础的自然科学,《普通高中化学课程标准(2017年版2020年修订)》(以下简称《课程标准》)建议开展以化学实验为主的多种探究活动,《课程标准》提出了学科核心素养和学业质量水平两个重要概念及其评价指标标准,同时也对学生的实验能力也提出了新的要求:促进实验教学从实验内容向实验思维转变。化学是研究物质的组成、结构、性质、转化及其应用的自然科学。物质转化的过程、物质性质的表现往往受到多种因素的影响,实验研究过程中必须面对多个变量的共同作用,因此控制变量法成为重要的研究方法。
控制变量法是指根据研究需要,运用一定手段,主动干预或控制事物发展的过程,在特定条件下探索客观规律的一种方法。在化学实验中,控制变量法就是把多因素影响的问题变成多个单因素影响的问题,每一次只改变其中某一个因素,控制其余几个因素不变,从而研究被改变的这个因素对事物的影响,然后分别研究其他因素的影响,最后综合解决问题,其运用体现在找出变量、明确目标变量、实施变量控制、观察实验现象的一系列过程中。
2.控制变量法在高考探究实验题中的应用示例
高考真题中注重考查考生的科学探究与创新意识,主要有探究外部影响、探究物质组成和探究物质转化的微观过程三种考查角度。
【例1】(2019·北京卷·28节选)化学小组实验探究SO2与AgNO3溶液的反应。
(1)实验一:用如图1所示装置(夹持、加热仪器略)制备SO2,将足量SO2通入AgNO3溶液中,迅速反应,得到无色溶液A和白色沉淀B。
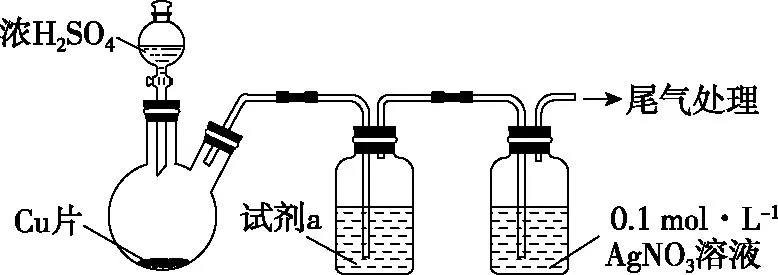
图1
(2)对体系中有关物质性质分析得出:沉淀B可能为Ag2SO3、Ag2SO4或二者混合物(资料:Ag2SO4微溶于水;Ag2SO3难溶于水)。
实验二:验证B的成分

①写出Ag2SO3溶于氨水的离子方程式:________________。
②加入盐酸后沉淀D大部分溶解,剩余少量沉淀F。推断D中主要是BaSO3,进而推断B中含有Ag2SO3。向滤液E中加入一种试剂,可进一步证实B中含有Ag2SO3。所用试剂及现象是________。

②H2O2溶液,产生白色沉淀


【例2】(2018·北京卷·28节选)实验小组制备高铁酸钾(K2FeO4)并探究其性质。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持装置略)

图2
(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:

表1
ⅰ.由方案Ⅰ中溶液变红可知a中含有________离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能由____________________产生(用方程式表示)。
ⅱ.方案Ⅱ可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是________。

理由或方案:________。

ⅱ.排除ClO-的干扰
②> 溶液酸碱性不同




【例3】(2021·广东省学业水平选择性考试·17节选)含氯物质在生产生活中有重要作用。1774年,舍勒在研究软锰矿(主要成分是MnO2)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为chlorine(中文命名“氯气”)。
(4)某合作学习小组进行以下实验探究。
①实验任务 通过测定溶液电导率,探究温度对AgCl溶解度的影响。
②查阅资料 电导率是表征电解质溶液导电能力的物理量。温度一定时,强电解质稀溶液的电导率随溶液中离子浓度的增大而增大;离子浓度一定时,稀溶液电导率随温度的升高而增大。25℃时,Ksp(AgCl)=1.8×10-10。
③提出猜想 猜想a:较高温度的AgCl饱和溶液的电导率较大。
猜想b:AgCl在水中的溶解度S(45℃)>S(35℃)>S(25℃)。
④设计实验、验证猜想 取试样Ⅰ、Ⅱ、Ⅲ(不同温度下配制的AgCl饱和溶液),在设定的测试温度下,进行表2中实验1~3,记录数据。

表2
⑤数据分析、交流讨论 25℃的AgCl饱和溶液中,c(Cl-)=________mol·L-1。
实验结果为A3>A2>A1。小组同学认为,此结果可以证明③中的猜想a成立,但不足以证明猜想b成立。结合②中信息,猜想b不足以成立的理由有________。
⑥优化实验 小组同学为进一步验证猜想b,在实验1~3的基础上完善方案,进行实验4和5。请在答题线上完成表3中内容。

表3
⑦实验总结 根据实验1~5的结果,并结合②中信息,小组同学认为猜想b也成立。猜想b成立的判断依据是________。

⑥45 Ⅱ 45
⑦A3>B2>B1
【试题分析】本题从探究外部条件影响的角度,以小组合作探究为活动方式,目的是探究温度对物质溶解度的影响,相应的必备知识包括“影响电解质溶液导电能力的因素”和“影响溶解度的因素”,需获取的新信息是“电导率的概念和影响因素”,考查考生运用控制变量的思维分析实验、设计实验的能力。
通过回顾“影响电解质溶液导电能力的因素”或阅读题干中关于电导率影响因素的信息,可知电导率影响因素包括测试温度和离子浓度,温度升高、离子浓度增大均可导致溶液导电能力(电导率)增大,且AgCl的溶解度随温度升高而增大,可以迅速判断实验1、2、3中两个变量共同作用导致溶液电导率增大,本组实验没有控制变量,因而不能证明猜想b。接下来由学生进行控制变量的实验设计,通过控制相同测试温度,比较不同温度下配制的AgCl饱和溶液(不同浓度的AgCl溶液)的电导率达成实验目的,但是本题中存在一个不易察觉的认知陷阱,当测试温度低于AgCl溶液的配制温度时,AgCl饱和溶液会析出部分溶质,导致溶液的浓度发生改变而变成该测试温度下的饱和溶液,无法保证实验按预想进行也就不可能顺利得出不同温度条件下的溶解度差异的结论。
【方法点拨】本题通过电导率的比较探究AgCl在水中的溶解度受温度的影响情况,即探究外部条件的影响。首先要找到主要的外部影响因素;再分析温度对体系的影响是否唯一,本题中温度同时影响了电导率和溶解度,即温度影响电导率和温度影响溶解度是两组变量;最后判断变量是否得到控制,本题中表2中该组实验没有控制变量,因此结论不合理。在外部条件影响的分析中,首先要找到影响实验结果的关键外部条件,通常为温度、浓度、压强、酸碱性、催化剂等,以及条件对体系的影响;然后分析这些外部条件是否能成为变量,若多个条件对同一物质造成影响,则多个条件成为变量,若一个条件对多种物质造成影响,则多种影响成为变量;最后判断变量是否得到控制。
3.高考化学学科二轮复习建议
一轮复习是重温巩固基础知识,特点是面面俱到,但是不深入,难点基本不深挖,而二轮复习就是在一轮复习夯实的基础上拔高提分,进行攻坚克难,重点突破。在新高考中,作为综合题中的必考题型,探究实验出现的概率极大,而控制变量法又是高中阶段重要的实验探究方法。所以在二轮复习中教师需要将控制变量法的实验探究类试题作为一个重要的专题引领学生进行突破。无论是探究物质组成,探究物质转化的微观过程,还是探究外部条件的影响,其重要的实验思维都是找出多个变量,分析变量是否唯一或控制唯一变量,观察现象得出结论,因此培养学生“控制变量”的思维和“控制变量”的实验设计能力是教师化学教学和高考备考的重要内容。二轮复习可以从以下几个方面开展教学备考实践。
3.1 构建“控制变量法”的思维模型
控制变量法起源于《控制论》,目的性是“控制”概念的最本质属性。可见在实验中实施控制变量法离不开对实验目的进行分析,“明确实验目的”是控制变量思维模型的第一步。第二步要在分析实验目的的过程中,找出并列的或是干扰的变量,也就是找变量。第三步是对变量实施控制,外部条件可以直接进行设定,物质组分则需加入合适试剂进行规避。最后一步是观察并描述实验现象。

图3 “控制变量法”的思维模型
3.2 回归教材实验,在熟悉情境中落实“控制变量法”的思维模型和实验设计
要真正掌握控制变量法,除了构建思维模型,还需掌握控制变量的基本方法,也是实验设计的方法,包括单组法、等组法、轮组法,以列表的形式进行呈现。如果在陌生情境中对学生进行实验设计的训练,情境的陌生性无疑增大了难度,因此教师在二轮复习中用好教材实验有利于降低情境陌生度,以教材实验为蓝本进行改编能够有针对性的训练学生实验设计能力。例如人教版必修第一册实验活动3,同周期、同主族元素性质的递变,实验1比较了Cl2、Br2、I2的氧化性,除了按照教材设计的步骤完成实验,还可以进行“探究卤素单质氧化性强弱”的实验,给出实验药品——氯水、溴水、碘水、NaCl溶液、NaBr溶液、NaI溶液,学生分组进行实验,列表设计实验组和对照组,最后评出最简便的实验方法。
再如人教版选择性必修1中“探究反应速率的影响因素”,教师除了按照教材实验一一演示、讲解之外,还可以组织学生依据控制变量法的思维模型进行实验探究,落实“明确实验目的”“找出变量”“控制变量”“观察并描述实验现象”一系列过程。广东省2014、2015年高考实验题均取材自化学反应原理教材中的实验。
3.3 在教学过程和高考真题中发现探究情境,引导学生进行实验探究
二轮复习过程中,随着学生对知识的理解更加深刻,思考更加深入,往往会对教材的内容产生疑问,教师如果把学生的疑惑作为探究的问题,组织学生设计实验进行探究,就能有效地落实实验思维的教学。例如学生在学习胶体制备的实验时,对实验中提出的“煮沸后冷却的蒸馏水”“逐滴加入”“饱和FeCl3溶液”“继续煮沸至红褐色停止加热”等要求感到繁琐和不解,往往会提出质疑,这时教师可以引导学生找出实验描述中的要点作为变量,分组实验对变量进行控制,最后对比各组实验结果印证教材内容。


