浅谈脉动真空灭菌柜脉动灭菌和非脉动灭菌模式的不同及使用要点
蔺建平 郭建军 亢和平 张 渊
(金宇保灵生物药品有限公司,内蒙古 呼和浩特 010111)
0 引言
脉动真空灭菌柜由于使用范围广、操作安全等优点,在制药行业中被越来越多的使用,它不仅可以用于液体类物品的灭菌(对热不敏感的溶液如MEM溶液等)、玻璃类用品用具的灭菌(各类血清瓶,取样瓶,吸管等),还可以用于不锈钢类用品用具的灭菌(反应器附属用品用具如取样T阀,离线过滤器等),而且针对不同的灭菌物品可以选择不同的灭菌方式,作为制药行业生产线中的重要灭菌设备,直接影响脉动灭菌柜的利用率和企业单位的直接能源成本。该文针对某公司所使用型号中的一种SHINVAXG1.DWT型脉动真空灭菌柜的工作原理、不同灭菌方式以及灭菌常用物品时的注意事项进行了详细介绍和建议。
1 制药行业常用的灭菌方法及微生物灭菌原理
1.1 常用灭菌方法概述
常用灭菌方法如图1所示。
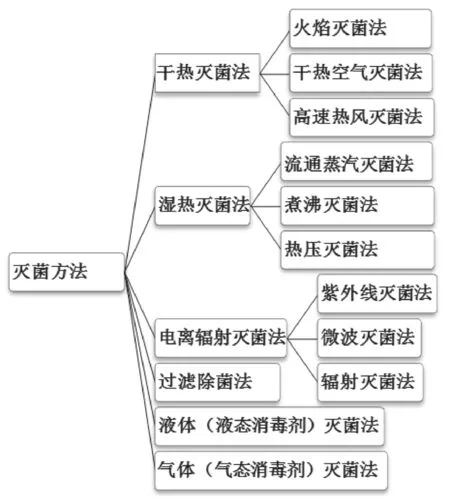
图1 常用灭菌方法
1.2 灭菌基本原理
高压蒸汽灭菌的原理是利用热蒸汽穿透细胞使其蛋白质等物质变性而起到灭菌作用。高温高压灭菌,不仅可杀死一般的细菌、真菌等微生物。对芽孢、孢子也有杀灭效果,是最可靠、应用最普遍的物理灭菌法。主要用于能耐高温的物品,如培养基溶液、蔗糖奶粉保护剂等一些溶液及丁基胶塞、搪瓷制品等制药行业常用物品的灭菌。
2 设备使用前关键事项的准备及要求
2.1 蒸汽
蒸汽的质量、压力直接影响灭菌的效果,所以使用前必须要保证纯蒸汽的质量和压力,纯蒸汽压力应控制在0.3MPa~0.5MPa,压力过低不能保证灭菌程序的顺利进行;压力过高灭菌柜出于安全原因,程序会自动退出,无法灭菌。打开纯蒸汽,在蒸汽进入夹层之前,应先将管道中的冷凝水排放干净。
2.2 软化水
打开软化水阀,为真空泵和冷凝器用水做准备。若水源压力低于0.1MPa,则不能启动设备运行真空泵。 为及时方便观察软化水的压力,建议在进灭菌器的水管道上安装一块0~0.6MPa量程的压力表,便于观看进水压力。
2.3 灭菌效果检测
灭菌效果的检测是评价其灭菌方法是否合理、灭菌效果是否可靠的必要手段。 常规的检测方式分为化学检测、生物检测、物理检测三大类。
利用化学指示剂在一定温度与作用时间条件下受热变色或变形的特点,以判断是否达到灭菌所需要求。
该原理是将一定量已知耐热参数的耐热孢子接入被灭菌的物品中,在预定的灭菌条件下灭菌,以验证灭菌是否达到要求。常用的生物指示剂为嗜热脂肪芽孢杆菌Bacillusstereathernophilus,其常规微生物耐热参数值为121℃(1.5min~3.0min)。
物理验证是对设备灭菌的温度、压力等指标进行验证。就是在灭菌时通过直观地观察灭菌全过程的时间、温度、压力等相关参数,以判断是否达到灭菌的要求。化学检测、生物检测、物理检测这三种方法有着各自不同的目的和意义,因此不可互相替代,应互相结合使用。
3 SHINVAXG1.DWT型脉动真空灭菌柜的非脉动灭菌(液体程序)和脉动灭菌(织物程序)原理及实例
3.1 脉动灭菌(液体程序) 模式下的灭菌及灭菌效果验证
非脉动灭菌(液体程序)模式下的灭菌主要是依靠蒸汽的重力,当纯蒸汽进入内室时将内室的冷空气从排气口逐渐置换出去,使内室温度逐渐升高,尽可能减少温度死角,从而达到灭菌目的。
将待高压验证的MEM溶液分别分装在带有棉塞的1.5万mL血清瓶中,每瓶建议分装5000mL~6000mL,分装完后用一层硫酸纸和两层牛皮纸包扎瓶口并装锅,灭菌柜建议装量是单层满载量的50%~100%。
灭菌温度:116℃~120℃。灭菌时间:900s~1800s。置换时间:2400s。内室压力限度:93kPa~115kPa。
注意事项如下。1)用1.5万mL血清瓶盛装MEM溶液时为保证灭菌效果,不宜装量太多,5000mL~6000mL为宜,瓶口一定要使用透气的棉塞外加硫酸纸和牛皮纸包扎或使用无纺布包扎,切勿使用橡胶胶塞密封瓶口,防止因溶液高压时瓶内液体体积膨胀而发生爆瓶或蹦塞现象,影响灭菌效果。2)容器内液体装量建议不超过容器容积的80%。3)使用液体程序对MEM溶液进行灭菌时,在排汽结束后严禁开真空泵抽空,避免发生爆瓶及液体沸腾。4)液体程序置换时间的设定宜长不宜短,如果置换时间设置过短,将影响MEM溶液的升温,进而可能会导致溶液灭菌不彻底。5)使用液体程序灭菌时,灭菌结束后请确认内室压力略低于当地大气压(建议参考设备安装时厂家设定的灭菌柜在开门状态下屏幕显示的内室压力值为准)时再开门,防止高压后的液体因内外压差过大,导致蹦塞或溶液飞溅,影响灭菌结果。6)灭菌结束点开门,等真空泵运行结束后请勿立即开大锅门,等待5min~10min再开大锅门,要给高压锅内外留有一定的缓冲时间。
备注说明:下面灭菌效果验证中使用的3种无菌检验用培养基分别按各自培养基的使用说明配制并分装在6分管中,每支分装6mL~8mL,盖上胶塞经116℃,1800s高压灭菌后无菌检验合格备用。
检验过程:将高压灭菌后的MEM溶液(在室温放置24h,然后移至层流罩(局百环境)下用5mL无菌注射器取样,并分别接种硫乙醇酸盐流体培养基2支、 胰酪大豆胨液体培养基1支和酪胨琼脂培养基2支,每支接种0.2mL,分别在25℃(硫乙醇酸盐流体培养基、 胰酪大豆胨液体培养基和酪胨琼脂培养基各一支)和37℃(硫乙醇酸盐流体培养基和酪胨琼脂培养基各一支)条件下培养7天,每天观察并记录检验结果。
检验结果:观察7天,无菌检验培养基中均无菌落生长,无菌检验合格。
检验过程:在高压灭菌后的 MEM 溶液中加10%胎牛血清后贴壁培养MDBK细胞,并37℃培养3天,每天观察细胞是否染菌。检验结果:3天后细胞生长良好,显微镜镜检细胞轮廓清晰,视野干净,未见杂菌。
在高压灭菌MEM溶液时选择3个温度可能最低的点分别放置生物指示剂,常用的生物指示剂嗜热脂肪芽孢杆菌Bacillusstereathernophilus,其常规微生物耐热参数值为121℃(1.5min~3.0min)。一同灭菌,灭菌结束后将灭菌后的生物指示剂及时取出并置于56℃培养箱中培养 48h,随后取出培养后的生物指示剂, 观察安瓿的内容物颜色,并与生物指示剂照片进行比较观察。检验结果:48h培养后的生物指示剂颜色呈紫红色且澄清, 说明该灭菌过程可有效杀灭孢子菌。
重复上述验证,连续三次,结果均符合要求。
3.2 脉动灭菌(织物程序) 模式下的灭菌及灭菌效果验证
采用机械强制脉动真空的排除方式, 程序运行后,首先进入的是脉动阶段,真空泵运转将设备内室气体及冷凝水经抽空阀由真空泵抽出。当内室压力达到脉动下限时,抽空阀关闭,停止抽空。当内室压力达到脉动上限时,抽空阀再次开启,又开始抽真空。这样直至达到设定脉动次数。脉动次数达到后,抽空阀关闭,真空泵停止。经多次抽真空多次注入蒸汽,彻底消除灭菌室内的冷点,保证了可靠的灭菌效果。一般一次完整的灭菌程序建议脉动三次:一般情况,脉动上限为80kPa,脉动下限为-80kPa。抽空一次,排出量为80%;当抽空二次时,排出量为96%;当抽空三次时,排出量理论值可达99.2%。
将待高压验证的丁基胶塞分别分装在无纺布袋中,每袋建议装500~1000个,分装完后用线绳捆扎无纺布袋口并装锅,灭菌柜建议装量是单层满载量的50%~100%。
灭菌温度:121℃;灭菌时间:3600s;脉动次数:3次;干燥脉动次数:2次;干燥上限设定:+60kPa;干燥下限设定:-60kPa;干燥上限等待时间:60s;干燥下限等待时间:60s;内室压力限度:11kPa~120kPa。
注意事项如下。1)丁基胶塞用自制的无纺布袋盛装,装量不宜太大,太大会影响灭菌效果,建议每袋500~1000个为宜。2)装锅时请勿靠近高压锅两侧的进汽口,离进汽口太近影响升温。3)装锅时请勿堵塞前后门附近的排汽口,防止高压时冷凝水不能及时排出而导致开锅后湿包。4)装锅时盛装丁基胶塞的无纺布袋不宜过于堆积,堆积过多将影响中间物品的灭菌效果,建议盛装高压锅单层容量的50%~100%。
检验过程:将高压灭菌后的丁基胶塞取一袋置于层流罩(局百环境)下,无菌取袋子中央的一个胶塞置于提前无菌过滤备用的10%血MEM溶液瓶中,盖好瓶盖上下颠倒摇匀3min~5min,再用5mL无菌注射器取样,并分别接种硫乙醇酸盐流体培养基2支、 胰酪大豆胨液体培养基1支和酪胨琼脂培养基2支,每支接种0.2ml,分别在25℃(硫乙醇酸盐流体培养基、 胰酪大豆胨液体培养基和酪胨琼脂培养基各一支)和37℃(硫乙醇酸盐流体培养基和酪胨琼脂培养基各一支)条件下培养7天,每天观察并记录。检验结果:观察7天,无菌检验培养基中均无菌落生长,无菌检验合格。
检验过程:用方法一中使用的10%血MEM溶液贴壁培养MDBK细胞,并37℃培养3天,观察细胞是否染菌。检验结果:3天后细胞生长良好,显微镜镜检细胞轮廓清晰,视野干净,未见杂菌。
在高压灭菌丁基胶塞时选择3个温度可能最低的点分别放置生物指示剂(常用的生物指示剂嗜热脂肪芽孢杆菌Bacillusstereathernophilus,其常规微生物耐热参数值为121℃(1.5min~3.0min))。一同灭菌,灭菌结束后将灭菌后的生物指示剂及时取出并置于56℃培养箱中培养 48h,随后取出培养后的生物指示剂, 观察安瓿的内容物颜色,并与生物指示剂照片做比较观察。检验结果:48h培养后的生物指示剂颜色呈紫红色且澄清,说明该灭菌过程可有效杀灭孢子菌。
重复上述验证,连续三次,结果均符合要求。
4 SHINVAXG1.DWT型脉动真空灭菌柜的非脉动灭菌和脉动灭菌模式的不同对比
4.1 升温方式不同
非脉动灭菌模式下的程序升温主要是通过改变灭菌程序参数里的置换时间来实现的,置换是在纯蒸汽进入内室时通过重力将内室的冷空气从排汽口逐渐置换出去,使内室温度升高,尽可能减少温度死角,置换时间的长短跟待灭菌物品的负载量有关,也跟待灭菌物品的导热性能有关,要综合考虑,根据负载量以及内室疏水温度达标的时长(温度达到 100℃~105℃,且疏水温度不再波动)设定置换时间。
采用非脉动灭菌模式下的置换方式升温较缓慢,主要适用于升温较慢的液体培养基或用硫酸纸和牛皮纸包扎的桶瓶等用品用具的灭菌。
主要是通过脉动真空泵反复抽至真空实现的,真空泵运转将设备内室气体及冷凝水经抽空阀由真空泵抽出,抽真空后内室再注入纯蒸汽,从而实现内室升温的目的,彻底消除灭菌室内的冷点,保证了可靠的灭菌效果。一般情况,脉动上限为80kPa,脉动下限为-80kPa。抽空一次,排出量为80%;当抽空二次时,排出量为96%;当抽空三次时,排出量理论值可达99.2%,所以建议一次完整的灭菌程序一般脉动三次。
脉动式灭菌模式下的脉动式升温速度较快,主要适用于可以快速升温的物品,例如制药行业分装用丁基胶塞、无菌服、陶瓷泵等灭菌。
4.2 夹层与内室的排汽方式不同
非脉动灭菌模式下的液体程序,在灭菌过程结束后,慢排疏水阀打开,内室蒸汽经过慢排疏水阀慢速排出,使内室压力缓慢下降,从而防止爆瓶和液体过度沸腾溢出,达到内室排汽的目的。
该模式下的灭菌阶段结束后,程序转入排汽阶段。排汽气动阀打开,开始排汽。当内室压力下降到一定程度时,冷凝水阀打开,开始进水;真空泵开始运转,使排汽速度加快。
5 使用脉动真空灭菌柜需要注意的其他事项
需要注意的其他事项如下。1)使用前需要检查电器箱上方是否有液体滴漏,防止人员触电。2)关锅门时应将门轻轻推至与前封板靠近的位置,再按下关门按钮,切勿用力过猛,防止撞坏行程开关。3)关门时要密切关注门升降情况,如有异常,立即取消操作(取消操作只需再次按压同一按钮),查看故障原因,并排除。4)脉动真空灭菌柜属于特种设备,相关人员必须持证上岗。
6 结语
脉动真空灭菌柜在制药行业扮演着非常重要的角色,如何规范、正确、高效地使用该设备非常重要,每个基层管理人员和专业操作人员必须熟练掌握。随着GMP要求的不断提高,设备也在不断更新换代,这就要求设备使用人员要与时俱进,不断学习和总结,提高自身的理论水平和专业技能。

