医院制剂活血散质量标准提高研究
赵颖 李文 陈宇

[摘要]目的综合多项指标评价活血散组方药味黄柏质量,全面提升活血散的质量标准。方法综合黄柏的薄层鉴别结果及含量测定结果,评价黄柏的质量;运用指纹图谱技术评价多批次制剂质量、批间稳定性,全过程控制活血散的质量标准。结果薄层斑点显色清晰前五是S1、S2、S4、S12、S14;巴马汀含量前五是S13、S1、S8、S14、S4;小檗碱含量前五是S3、S15、S12、S7、S10。活血散的指纹圖谱及含量测定方法各项方法学验证良好,平均相似度为0.901,相似度良好。结论黄柏质量研究为活血散制剂的质量控制提供了参考,建立了活血散HPLC指纹图谱。
[关键词]活血散;黄柏;小檗碱;巴马汀;指纹图谱技术
[中图分类号]R286.0 [文献标识码]A [文章编号]2095-0616(2022)05-0078-04
Study on the improvement of quality standard of hospital preparation of blood-quickening powder
ZHAO Ying1 LI Wen2 CHEN Yu3
1. Department of Pharmacy,Nanjing Hospital of Chinese Medicine,Jiangsu,Nanjing 210022,China;2. Department of Education,Nanjing Hospital of Chinese Medicine,Jiangsu,Nanjing 210022,China;3. Nanjing University of Chinese Medicine,Jiangsu,Nanjing 210046,China
[Abstract] Objective To evaluate the quality of medicinal ingredient of phellodendron chinense in prescription of blood-quickening powder by combining several indexes,so as to comprehensively improve the quality standard of the blood-quickening powder. Methods The quality of the medicinal ingredient of phellodendron chinense was evaluated by combining the results of thin-layer identification and content determination of phellodendron chinense. In addition,the fingerprint spectra technology was used to evaluate the batch-to-batch stability of the quality of multiple batches of the preparation and to control the quality standard of the blood-quickening powder in the whole process. Results The top five thin-layer spots with clear color development were S1,S2,S4,S12 and S14. The top five with palmatine content in order were S13,S1,S8,S14 and S4,and the top five with berberine content in order were S3,S15,S12,S7 and S10. The fingerprint spectra and content determination methods of blood-quickening powder were well-validated in all methods,with a good average similarity of 0.901. Conclusion The study of the quality of phellodendron chinense provides a reference for the quality control of the preparation of blood-quickening powder,and helps to establish high- performance liquid chromatography (HPLC)fingerprint spectra of blood-quickening powder.
[Key words] Blood-quickening powder;Phellodendron chinense;Berberine;Palmatine;Fingerprint spectra technology
医院的制剂由于具有安全、有效等优势,因此在临床治疗中起到很大的作用。随着我国经济社会的进步、科技的发展,人民群众对于药品的使用要求也愈加严格。部分医院的制剂还存在着产品质量和标准化技术水平不高等问题,制约了医院制剂的发展。本研究以医院制剂活血散为例,通过系统的实验研究,确定组方药味产地,全面提升医院制剂质量标准,有一定的社会效益和经济效益[1-11]。活血散由黄柏、半枝莲、土鳖虫、地肤子等7味中药组成,功效为活血化瘀、消肿止痛。用于骨折、骨裂、软组织挫伤等跌打损伤诸症。本研究对活血散品质提升开展研究。
1 材料与仪器
1.1 仪器
Agilent 1260高效液相色谱仪(安捷伦公司);KQ- 500E型超声波清洗器(昆山市超声仪器有限公司);sp-30e型全自动数控薄层液体光学液相色谱图像测量点样仪(北京上海科哲生化科技有限公司);KQ-300DE型数控超声仪(昆山市超声仪器有限公司),MS205DU十万分之一电子天平(梅特勒-托利多集团)。
1.2 试药
小巢碱(购自中国药品质量鉴定监督研究院,批号:110713-201613)、巴马汀(购自中国科学院附属成都生物研究所,批号:must-20022610)。乙腈、甲醇为色谱纯(TEDIA公司),石油醚、乙酸乙酯、乙醇、磷酸等为分析纯,水为纯净水。
1.3 药材
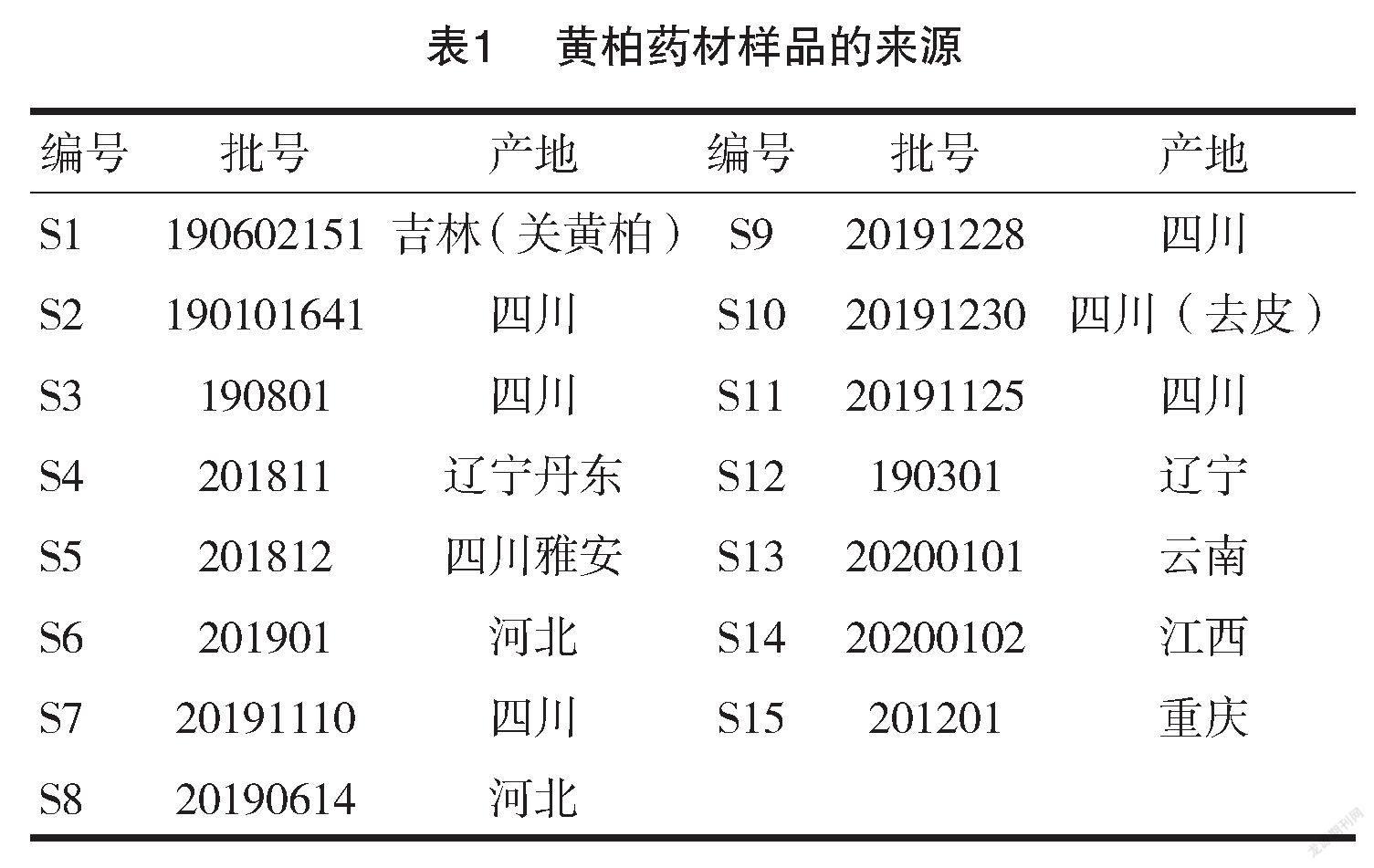
黄柏[12]药材来源见表1。活血散药材来源见表2。
2 方法与结果
2.1 原药材黄柏实验研究
2.1.1 鉴别 取15批黄柏样品的粉末各0.2 g,加入乙酸乙酯20 ml,超声处理30 min,滤过,滤液浓缩至l ml,作为供试品溶液。将15批供试品溶液,点样于同一硅胶G薄层板上,展开剂石油醚(60~90℃):乙酸乙酯为1:1,展开,取出,晾干,显色,显色剂为硫酸乙醇溶液(5.7 ml硫酸和94.3 ml 乙醇配制溶液),105℃加热。15批黄柏薄层色谱见图1,可以看出S1、S2、S4、S12、S14显现斑点颜色最深;S3、S5、S6、S7、S8、S9、S10、S11、S13、S15 斑点辨识度低。
2.1.2 含量测定
2.1.2.1 色谱条件[13-14] 以十八烷基硅烷键合硅胶为填充剂;以乙睛为流动相A,以0.1%磷酸溶液(加入磷酸二氢钠使其达到0.02 mol/L的浓度)为流动相B,按表3进行梯度洗脱;检测波长为345 nm 理论板数按盐酸小巢碱峰计算应不低于4000。
2.1.2.2 对照品溶液的制备 精密稱取适量巴马汀、小巢碱,用甲醇定容,巴马汀、小巢碱浓度分别为0.112、0.067 mg/ml,作为对照品储备溶液。
2.1.2.3 供试品溶液的制备 取15批黄柏粉末约0.2g,加入60%乙醇40~50 ml容量瓶中,超声45 min,加60%乙醇至刻度,滤过,取续滤液,即得。
2.1.2.4 方法学考察 ①线性关系考察:取巴马汀、小巢碱对照品溶液,进样体积分别为1、2、5、10、15.20 μl,以浓度为横坐标(X),峰面积为纵坐标(Y),得回归方程,见表4。
②精密度试验:分别取巴马汀、小巢碱对照品溶液,连续进样5次,记录峰面积。结果表明,巴马汀和小巢碱的峰面积RSD分别为2.32%和1.25% (n=5),具有较好的准确性。
③重复性试验:取供试品溶液S1,连续进样5次,记录峰面积。结果表明,巴马汀和小巢碱峰面积的RSD分别为1.12%和1.75%(n=5),重复性好。
④稳定性试验:取供试品溶液S1,分别在0、2、4、8、16、24 h进样,记录峰面积。结果表明,巴马汀和小巢碱峰面积的RSD分别为1.84%和1.62%(n=6)表明溶液在24 h内稳定性好。
⑤不同批次黄柏的含量测定:取15批次黄柏样品,分别按上述供试品溶液得制备方法进行制备,进样,记录峰面积,计算含量,结果见表5。
根据含量数据得,S13、S1、S8、S14、S4以上5味样品巴马汀含量最高,S3、S15、S12、S7、S10以上5味样品小巢碱含量最高。
2.2 活血散实验研究
2.2.1 鉴别 取15批活血散样品粉末各1g,加入乙酸乙酯50 ml,超声处理30 min,滤过,滤液浓缩至1 ml,作为供试品溶液。分别取上述15批次供试品溶液10 μl,点样于同一硅胶G薄层板上,展开剂石油醚(60~90℃):乙酸乙酯为1:1,展开,取出,晾干,喷硫酸乙醇溶液(5.7 ml硫酸和94.3 ml 乙醇配制溶液),105℃加热至显色,结果见图2,可以看出H4、H5、H10、H12、H13显现斑点颜色最深;H1、H6、H7、H15显现斑点但颜色较浅;H2、H3、H8、H9、H11、H14显现斑点颜色适中。
2.2.2 活血散的含量测定
2.2.2.1 色谱条件 同2.1.2.1
2.2.2.2 对照品溶液的制备 精密称取适量小巢碱,用甲醇定容,制成0.067 mg/ml小巢碱溶液,作为对照品储备溶液。
2.2.2.3 供试品溶液的制备 取15批活血散粉末约0.28,加入60%乙醇40~50 ml容量瓶中,超声45 min,加60%乙醇至刻度,滤过,取续滤液,即得。
2.2.2.4 方法学考察 ①精密度试验:取小巢碱对照品溶液,连续进样5次,记录峰面积。结果表明,小巢碱的峰面积RSD为2.01%(n=5),具有较好的准确性。
②重复性试验:取供试品溶液H1,连续进样5次,记录峰面积。结果表明,小巢碱峰面积的RSD分别为1.52%(n=5),重复性好。
③稳定性试验:取供试品溶液H1,分别在0、2、4、8、16、24 h进样,记录峰面积。结果表明,小巢碱峰面积的RSD分别为1.98%(n=6),表明溶液在24 h内稳定性好。
2.2.3 活血散的指纹图谱建立
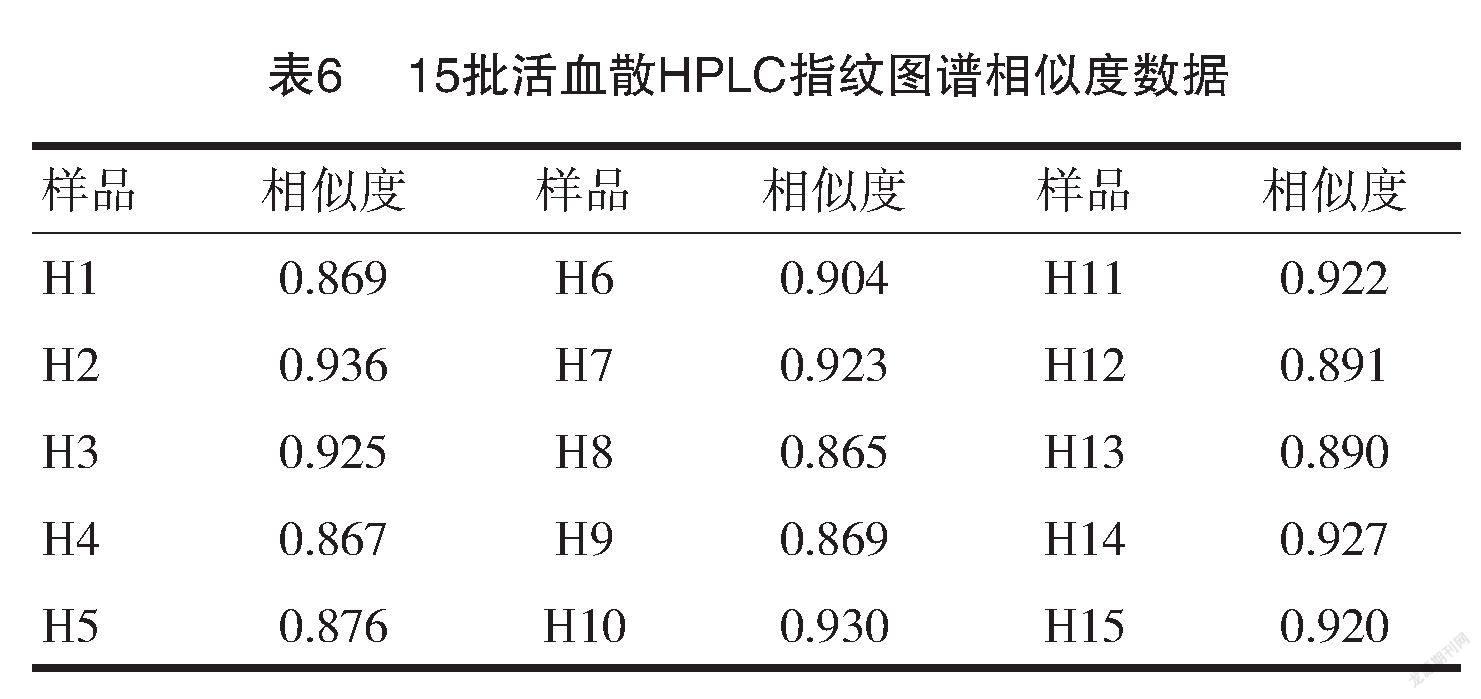
2.2.3.1 指纹图谱的建立[13-14] 将之前制备好的15批活血散的供试品溶液样品制成高效液相色谱图,格式为AIA,然后导入软件“中药色谱指纹图谱相似度评价系统2012版”进行指纹图谱的制作,采用H1活血散色谱图作为对照谱图;时间窗宽度为0.10,15批样品的指纹图谱,见图3~4。将指纹测定结束后所有捕获15批指纹样本的分析数据分别综合采用了随机指纹分析图谱相似度综合评价分析系统和随机生成的指纹对照表和指纹分析图谱分别对其进行相似度分析评价,结果情况详见参数表6。
2.2.3.2 色谱峰的指认[15] 通过高效液相色谱仪测定活血散样品和对照品的含量,记录样品的色谱时间图,分析测定各色谱峰的平均值。指定了1个点的色谱峰,3号为小檗碱,见图5。
3 讨论
黄柏流动相的选择:曾考察乙睛:磷酸溶液(1:1)(每100毫升加十二烷基磺酸钠0.l g)为流动相的效果,由于流动相中含有离子对,配置过程中含有不溶性沉淀,极有可能损伤色谱柱,故最终未选择该流动相。活血散的薄层鉴別:制备供试品溶液时,活血散取样量偏少导致最终点样时浓度偏低,得到的色谱图不清晰。稀碘化铋钾显色剂放置时间过长,容易导致显色效果差。加热时间太短,斑点显色不清晰。
[参考文献]
[1]金鹏飞,刘凤琴,刘建中,等.医院制剂的现状分析及发展建议[J].中国药学杂志,2014,49 (4):348-350.
[2]袁瑞玉,陈凌亚,周晓芳.新医改形势下医院制剂室的发展策略[J].卫生经济研究,2015(5):50-52.
[3]沈萍.如何提高医院制剂质量的探讨[J].中国医药科学,2012,2(16):173-174.
[4]马佩杰,沈伟,张妍,等.医院制剂质量标准存在的问题分析及对策探讨[J].中国医学伦理学,2015,28(3):353-355.
[5]赵电红,梁红元,谢来洪,等.运用PDCA循环模式促进医院制剂质量管理的持续改进[J].中国药事,2016,30(10):1037-1042.
[6]杨炳火,周芙琼,朱维娜,等.超高效液相色谱-质谱联用法测定不同粒径活血散透皮吸收液中4种成分含量[J].医药导报,2017,36(9):1033-1037.
[7]高妍,周海芳,刘朵,等.黄柏化学成分分析及其药理作用研究进展[J].亚太传统医药,2019,15(4):207-209.
[8]国家药典委员会.中华人民共和国药典:一部[M].北京:中国医药科技出版社,2020:318.
[9]可维,马春辉,季宇彬.不同产地川黄柏HPLC指纹图谱的研究[J].上海中医药大学学报,2008(1):62-65.
[10]谢明全.炮制对黄柏中3种生物碱含量的影响[J]. 中国药房,2010,21(15):1419.
[11]唐艳梅,叶萌,向丽,等.HPLC测定黄柏中盐酸小檗碱、盐酸巴马汀和盐酸药根碱[J].西药学杂志,2006,21(3):265-267.
[12]赵颖,周芙琼,朱维娜,等.活血散的质量标准研究[J].中国药房,2016,27(15):2114-2116.
[13]李凤丽,李进,吴娇.指纹图谱技术在中药领域研究中应用现状[J].天津药学,2014,26(3):52-57.
[14]刘静,刘燕,于健东,等.跌打活血散HPLG-DAD-ELSD双通道指纹图谱分析[J].中国药事,2016,30(9):924-931.
[15]屈爱桃,覃洁,雷文秀,等.黄柏薄层色谱指纹图谱研究[J].内蒙古医学院学报,2006(3):174-177.

