脱硫液组成对EDTA-Fe稳定性和选择性的影响
黄佩武,徐勋达,潘 威,余国贤*
(1.江汉大学 光电材料与技术学院,湖北 武汉 430056;2.武汉国力通能源环保股份有限公司,湖北 武汉 430206)
0 引言
气相硫化氢不仅会引起设备和管路的腐蚀、催化剂的中毒,而且对人体有害,燃烧产物污染大气[1−4]。湿法氧化还原脱硫法由于直接将硫化氢转化为硫磺,具有吸收和再生反应速率快、环境友好等优点,目前是煤气脱硫中应用最广泛的一类脱硫方法,如PDS法、ADA法、栲胶法、络合铁法等[5−6],其中络合铁法具有脱硫选择性高、流程简单、无污染、脱硫剂廉价易得等优点,是一种绿色环保型湿法氧化还原脱硫技术。近年来,络合铁法被广泛应用于天然气、煤气等含硫化氢气体的净化中。络合铁法脱硫过程中会导致络合铁脱硫催化剂的稳定性和选择性降低,增加催化剂消耗。针对该问题,本文建立了脱硫系统模型,通过实验研究了络合铁脱硫液组成对络合铁催化剂稳定性和选择性的影响,为工业络合铁脱硫系统提升络合铁催化剂的稳定性和选择性提供参考。
1 实验材料与方法
1.1 主要实验原材料
氯化铁,国药集团化学试剂有限公司;乙二胺四乙酸二钠,西陇科学股份有限公司;碳酸钠,国药集团化学试剂有限公司;碳酸氢钠,成都市科隆化学品有限公司;硫代硫酸钠,国药集团化学试剂有限公司;邻菲啰啉,国药集团化学试剂有限公司;氮气和硫化氢,武汉纽瑞德气体有限公司。所有试剂均为分析纯。
1.2 吸收/再生实验
图1为络合铁脱硫化氢吸收/再生实验装置示意图。来自氮气钢瓶经过气体流量计的氮气和来自硫化氢钢瓶经过气体流量计的硫化氢进入气体混合罐,从气体混合罐输出的含有硫化氢的混合气体经过一个三通阀进入自制鼓泡吸收玻璃管(内径4 cm,高150 cm,离底部10 cm处有一砂芯气体分布器),在鼓泡吸收管离底部50 cm设置了取样口,鼓泡吸收的液位控制在100 cm,三通阀的另外一端连接空气压缩机,管路上安装了气体流量计,控制再生空气流量。吸收后的尾气通入一个1 000 mL装满质量分数为10%的氢氧化钠溶液的洗气瓶。

图1 络合铁脱硫化氢吸收/再生实验装置示意图Fig.1 Schematic diagram of experimental device for hydrogen sulfide removal by iron complexation absorption/regeneration
将氯化铁、乙二胺四乙酸二钠、碳酸氢钠、碳酸钠、硫代硫酸钠等物质按照一定的比例配制成所需脱硫液,用0.2 mol/L氢氧化钠溶液调节脱硫液的pH为8.5。将配制好的脱硫液倒入吸收/再生实验装置中,静止液位控制在100 cm,通过水浴控制脱硫液温度为40℃,用0.5 L/min来自氮气钢瓶的氮气和0.02 L/min来自硫化氢钢瓶的硫化氢进入混合罐混合后的含硫化氢气体进行吸收实验,气相吸收可看成平推流,控制吸收硫化氢为Fe总摩尔数的20%,即络合铁转化为络合亚铁的比例为总铁的40%;吸收硫化氢至电位不再变化后进行再生,使用2 L/min的空气鼓泡对脱硫液进行再生实验,恢复至初始电位。此为1次吸收/再生实验,如此循环50次,每10次实验后取样分析脱硫液参数。
吸收和再生表观气速远低于0.05 m/s,符合平推流假设,可忽略气体返混的影响,便于考察脱硫液组成,如碱度值、EDTA/Fe摩尔比、总铁浓度及硫代硫酸盐浓度,对于EDTA−Fe作为脱硫催化剂的稳定性和选择性的影响。
1.3 分析方法
1.3.1 总铁分析方法 采用邻菲罗啉分光光度法测定总铁。
1.3.2 EDTA分析方法 采用Agilent 1200高效液相色谱仪(配有二极管阵列检测器)测定EDTA含量,色谱柱:Agilent TC−C18,5μm,150 mm×4.6 mm;流动相:A表示0.03 mol/L乙酸钠溶液和0.02 mol/L四丁基溴化铵水混合液,用磷酸调节pH=4;B表示甲醇;VA/VB(体积分数)=75/25。流速:1.0 mL/min;进样量:20μL;柱温:25℃;检测波长:254 nm。
1.3.3 碱度值分析方法 取脱硫液2 mL于150 mL烧杯中,加入50 mL蒸馏水,使用雷磁PHS−25型pH计指示溶液的pH,使用0.1 mol/L的硫酸标准液将溶液pH滴定至4.0。记下体积V1,mL。总碱度=(0.1 mol/L*V1)/2 mL。
1.3.4 硫代硫酸根分析方法 取2 mL脱硫液于250 mL烧杯中,加入50 mL蒸馏水,用pH=6的缓冲溶液(醋酸钠和冰醋酸配制)调节溶液pH为弱酸性,加入3 mL淀粉指示剂(10 g/L),摇匀后使用0.2 mol/L的碘液滴定溶液至蓝色为终点,记下体积V2,mL。C(S2O32−)=(112 g/mol*V2*0.1 mol/L)/2 mL。
1.3.5 硫酸根含量分析方法 取5 mL脱硫液于150 mL烧杯中,加20 mL蒸馏水和15 mL丙酮,充分混合后,用0.1 mol/L的盐酸调节混合液pH为1.7,滴加3滴0.1%偶氮氯磷Ⅲ指示剂,然后用0.05 mol/L氯化钡标准溶液滴定至溶液呈蓝色为终点。记下滴定体积V3,mL。C(SO42−)=(96 g/mol*0.05 mol/L*V3)/5 mL。
1.3.6 氧化还原电位分析方法 采用a1pha—pH800型PH/ORP控制变送器测定脱硫液的氧化还原电位。
2 结果与讨论
络合铁脱硫技术的基本原理是通过弱碱性的水溶液将气相H2S吸收并转化为HS−,脱硫液中的Fe3+Ln−将HS−氧化为单质硫,同时自身被还原成Fe2+Ln−,再生过程中通过鼓空气,Fe2+Ln−被空气中的氧气氧化为Fe3+Ln−,实现再生循环吸收[7−10]。本文讨论了脱硫液碱度值、EDTA/Fe摩尔比、总铁浓度及硫代硫酸盐浓度对脱硫催化剂EDTA−Fe稳定性和脱硫选择性的影响。
2.1 络合铁脱硫液碱度值对脱硫催化剂稳定性和选择性的影响
2.1.1 络合铁脱硫液碱度值对脱硫催化剂稳定性的影响 图2给出了脱硫溶液碱度值对催化剂稳定性的影响。硫化氢在水中的溶解度并不大,脱硫溶液需要加入碳酸钠或氨水等形成一定碱度值,促进气相硫化氢进入脱硫液形成HS−。由图2可知,脱硫液5种碱度值下,随着吸收/再生循环次数从0增加到50,EDTA的降解率均随吸收/再生循环次数增加而增加;随着脱硫液碱度值的增加,EDTA的降解率依次降低。
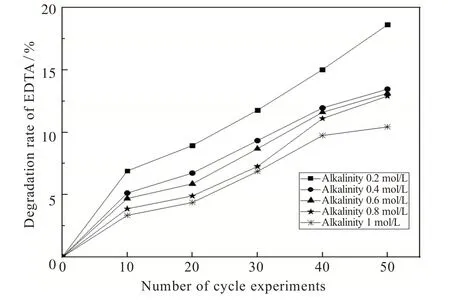
图2 EDTA降解率与脱硫液碱度值的关系Fig.2 Relationship between EDTA degradation rate and alkalinity value of desulphurization solution
络合铁吸收硫化氢后富液中存在大量络合亚铁,溶液中的络合亚铁鼓空气再生为络合铁,在这个过程中会产生羟基自由基和双氧水,化学方程式如下:

(1)式和(2)式是络合铁脱硫再生过程的副反应,类似于Fenton试剂,产生的羟基自由基具有很强的氧化性能,能将EDTA氧化降解为一系列分子量更低的氨基羧酸类络合剂,最终降解为二氧化碳、水和氨等[11−12]。另外,络合状态的亚铁离子,在脱硫液中存在以下化学反应:

碱度值越高,脱硫剂溶液提供OH−的能力越强。根据Fenton试剂产生羟基自由基的原理,比如(2)式,OH−能跟络合亚铁或游离的亚铁结合,这将抑制过氧化氢分解为羟基自由基。碱度值越高,络合铁或络合亚铁同OH−形成络合物的浓度越高,络合亚铁离子或游离亚铁离子的浓度越低,产生(2)式中的副反应的速率就更低,系统中的羟基自由基浓度就会更低,EDTA降解就少。
2.1.2 络合铁脱硫液碱度值对脱硫催化剂选择性的影响 表1给出了脱硫液的碱度值对脱硫选择性的影响。由表1可知,随着脱硫液碱度值从0.2 mol/L增加到1.0 mol/L,EDTA−Fe的脱硫选择性从97.81%降低到95.84%,副盐只生成了硫代硫酸盐,在分析误差允许范围内没有检测到硫酸根。络合铁脱除硫化氢生成硫磺的途径为[13]:硫化氢经脱硫液吸收后,与络合铁反应首先生成S22−,S22−通过一系列的聚合反应生成S92−,然后S92−与H+结合形成稳定的S8,简要步骤如下:
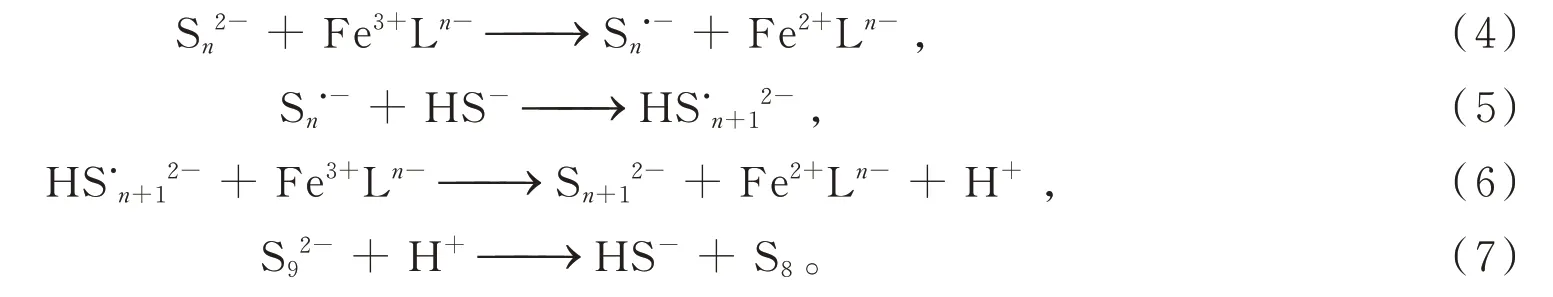
由(4)~(7)式可知,硫磺的生成机理实质为多硫化物离子的聚合反应而来。然而,脱硫过程中产生的Sn2−可以被溶解氧氧化为S2O32−,降低脱硫过程中氢硫化物的转化速率[14]。同时,Kleinjan等[15]研究了Sn2−与O2的反应,并提出动力学经验式
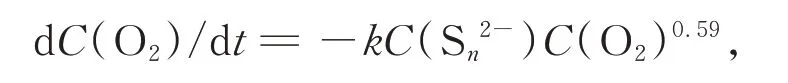
式中,C(O2)和C(Sn2−)分别表示O2和Sn2−的浓度,k表示反应速率常数,该式证明溶解氧对氢硫化物在向硫单质转化时存在抑制作用。夏涵等[16]通过对东平湖水体中溶解氧的测定,发现pH大于8时,pH与溶解氧的增加成正相关。脱硫液的碱度值越高时,系统提供OH−的能力越大,溶液中溶解氧的浓度必然增加,更高的氧气浓度更容易将系统中的Sn2−氧化为S2O32−,所以随着脱硫液碱度值的增加,表现出脱硫选择性的降低。

表1 脱硫液碱度值对脱硫选择性的影响Tab.1 Influence of alkalinity value of desulphurization solution on desulfurization selectivity
2.2脱硫液中EDTA/Fe摩尔比对脱硫催化剂稳定性和选择性的影响
2.2.1 脱硫液中EDTA/Fe摩尔比对脱硫催化剂稳定性的影响 图3给出了脱硫溶液中EDTA/Fe摩尔比对催化剂稳定性的影响。铁离子作为脱硫的催化剂,在碱性溶液中无法单独稳定存在,螯合剂的功能是防止不溶性铁化合物的形成,而不影响铁进行还原和氧化的能力,使用EDTA与其络合,使得铁离子更加稳定,增加了铁离子在水中的溶解性。由图3可知,脱硫液5种EDTA/Fe摩尔比值下,随着吸收/再生循环次数从0增加到50,EDTA的降解率均随吸收/再生循环次数增加而增加;随着脱硫液EDTA/Fe摩尔比的增加,EDTA的降解率依次增加。
Saelee等[17]建立了EDTA−Fe降解速率方程,其研究表明EDTA−Fe与羟基自由基的降解反应类似一级反应,根据一级反应的特点,其反应速率与反应物的浓度呈正比。实验中各种脱硫溶液中总铁浓度并未减少且一致,在达到相同的总铁转化率下,Fe2+Ln−量也是一定的,由反应式(2)可知,其产生的羟基自由基量并未减少。随着溶液中EDTA/Fe摩尔比的增加,EDTA浓度也随着增加。羟基自由基产生量没变,EDTA浓度增加,根据一级反应特点,其降解速率将加快。因此,在总铁浓度不变的情况下,随着EDTA/Fe摩尔比的增加,EDTA的降解率也随之增加。

图3 EDTA降解率与溶液EDTA/Fe摩尔比的关系Fig.3 Relationship between EDTA degradation rate and EDTA/Fe molar ratio of solution
2.2.2 脱硫液中EDTA/Fe摩尔比对脱硫催化剂选择性的影响 表2给出了脱硫液中EDTA/Fe摩尔比对脱硫选择性的影响。由表2可知,随着脱硫液EDTA/Fe摩尔比从1增加到2,EDTA−Fe的脱硫选择性从96.89%降低到96.32%,副盐只生成了硫代硫酸盐,没有检测到硫酸根。EDTA/Fe摩尔比的增加导致脱硫选择性稍稍降低,可能同EDTA增加导致溶解氧的增加有关。

表2 EDTA/Fe摩尔比对脱硫选择性的影响Tab.2 Effect of EDTA/Fe mole ratio on desulfurization selectivity
2.3 脱硫液中总铁浓度对脱硫催化剂稳定性和选择性的影响
2.3.1 脱硫液中总铁浓度对脱硫催化剂稳定性的影响 图4给出了脱硫溶液中总铁浓度对催化剂稳定性的影响。EDTA−Fe在碱性溶液中与HS−反应从而达到脱除硫化氢的目的,总铁浓度在一定程度上代表了其处理硫化氢的能力。由图4可知,脱硫液4种总铁浓度下,随着吸收/再生循环次数从0增加到50,EDTA的降解率均随吸收/再生循环次数增加而增加;随着脱硫液总铁浓度的增加,EDTA的降解率依次增加。
脱硫液保持EDTA/Fe的摩尔比一致,改变总铁浓度。随着总铁浓度的增加,达到一定转化率时,溶液中Fe2+Ln−浓度也随之增加,由副反应(2)可知,产生的羟基自由基数量也随之增加,在EDTA/Fe摩尔比不变的情况下,EDTA浓度随着总铁浓度的增加而增加,所以溶液中的羟基自由基和EDTA的浓度都随着总铁浓度的增加而增加。根据EDTA和羟基自由基的反应类似一级反应的特点,两种参与反应的物质浓度都在增加,势必导致其降解反应的速率增加,所以EDTA的降解率随着总铁浓度的增加而增加。

图4 EDTA降解率与溶液总铁浓度的关系Fig.4 Relationship between EDTA degradation rate and total iron concentration in solution
2.3.2 脱硫液中总铁浓度对脱硫催化剂选择性的影响 表3给出了脱硫液总铁浓度对脱硫选择性的影响。随着脱硫液总铁浓度从0.5 g/L增加到2 g/L,EDTA−Fe的脱硫选择性从97.14%降低到96.13%,副盐只生成了硫代硫酸盐,没有检测到硫酸根。随着总铁浓度的增加,在达到相同转化率的情况下,其处理硫化氢的量也随之增加,所以产生硫磺的量也随之增加,前面提到硫磺是多硫化物离子通过聚合反应产生,更多硫磺的产生需要更多的多硫化物离子,EDTA−Fe(Ⅲ)脱除硫化氢后变为EDTA−Fe(Ⅱ),随着总铁溶度的增加,其氧化成EDTA−Fe(Ⅲ)的需氧量随之增加,因此系统中所需多硫化物离子和氧气量都在提升,其接触的机会大大增加,多硫化物被氧化成硫代硫酸盐的趋势也大大增加,所以随着总铁浓度的增加,脱硫选择性稍有降低。
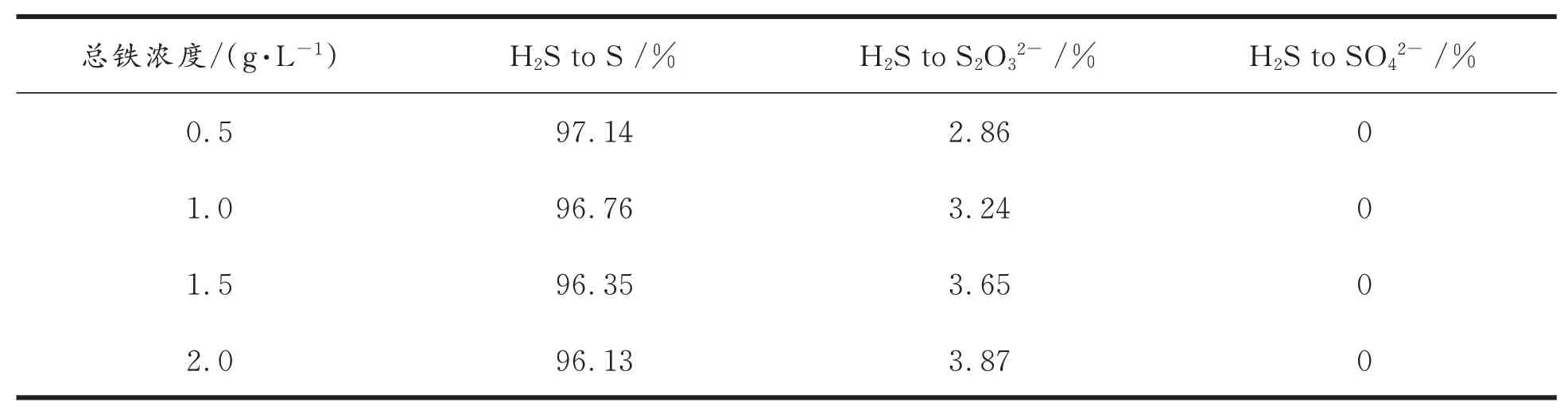
表3 总铁浓度对脱硫选择性的影响Tab.3 Influence of total iron concentration on desulfurization selectivity
2.4 脱硫液中硫代硫酸钠浓度对脱硫催化剂稳定性和选择性的影响
2.4.1 脱硫液中硫代硫酸钠浓度对脱硫催化剂稳定性的影响 图5给出了脱硫溶液中硫代硫酸钠浓度对催化剂稳定性的影响。由于羟基自由基的产生,配体存在降解现象,硫代硫酸钠常常作为抗氧化剂添加到脱硫液中。由图5可知,EDTA的降解率随吸收/再生循环次数增加而增加;随着脱硫液中硫代硫酸钠浓度的增加,EDTA的降解率依次降低。
一般认为是羟基自由基导致了EDTA的降解,硫代硫酸钠作为一种常见的自由基清除剂[18],与羟基自由基有很好的亲和力,有利于抑制EDTA的降解,提高脱硫催化剂的稳定性。与其他自由基清除剂相比,硫代硫酸钠具有一定的优势,硫代硫酸钠在与羟基自由基作用后,通过反应可以部分再生,其清除羟基自由基的原理及部分再生原理如下:

在实验范围内,硫代硫酸盐对EDTA的降解起到了显著抑制作用,同时随着浓度的增加,抑制EDTA降解的效果更好。

图5 EDTA降解率与溶液中硫代硫酸钠浓度的关系Fig.5 Relationship between EDTA degradation rate and sodium thiosulfate concentration in solution
2.4.2 脱硫液中硫代硫酸钠浓度对脱硫催化剂选择性的影响 表4给出了脱硫液中硫代硫酸钠浓度对脱硫选择性的影响。随着脱硫液硫代硫酸钠浓度从0增加到80 g/L,EDTA−Fe的脱硫选择性从96.76%增加到97.01%,前面提到脱硫过程中硫代硫酸盐的形成是由于多硫化物离子被氧气氧化,溶液中含氧量越高越有利于硫代硫酸盐的生成。饶胡敏等[19]研究表明,随着水中盐度的增加,水体中溶解氧浓度呈现下降趋势。随着硫代硫酸钠浓度的增加,脱硫液中的盐度也随之增加,所以脱硫液中溶解氧的含量随之下降,多硫化物离子被氧化成硫代硫酸根的趋势减小,所以表现出脱硫选择性随着硫代硫酸钠的增加而增加。同时系统中检测到了硫酸根离子,根据物料守恒定律,得出产生的硫酸根离子为另加的硫代硫酸钠被氧气氧化而来,具体如下:

由于硫代硫酸根浓度增加,造成其氧化成的硫酸根离子增多。
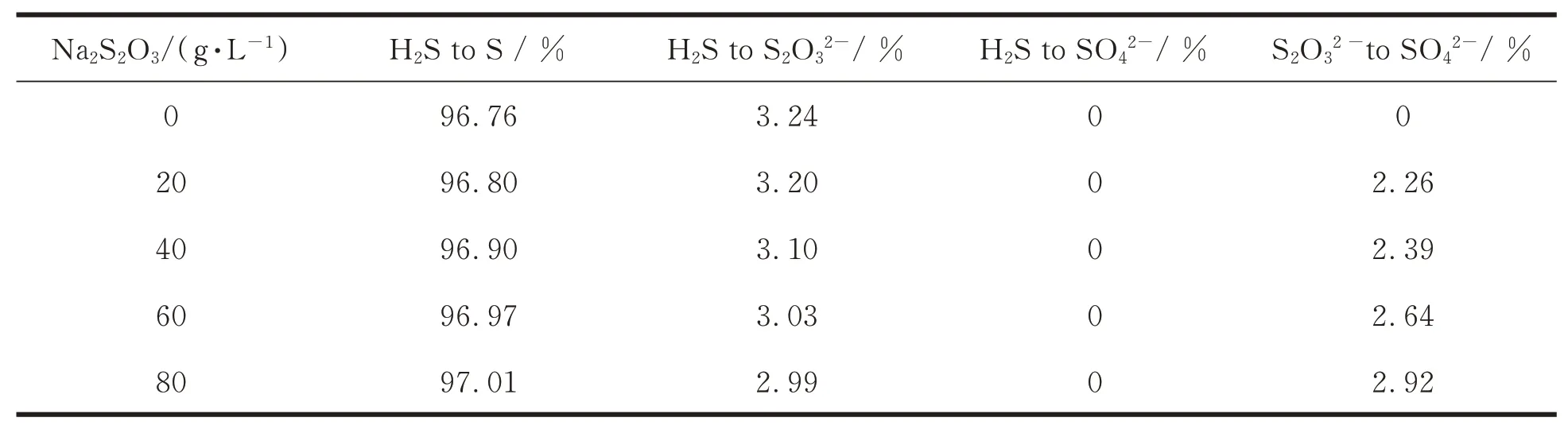
表4 硫代硫酸钠浓度对脱硫选择性的影响Tab.4 Influence of sodium thiosulfate concentration on desulfurization selectivity
3 结论
1)随着脱硫液中碱度值的增加,增加了脱硫液中的溶解氧浓度,因而降低了EDTA的降解率,降低了EDTA−Fe脱硫体系的选择性。
2)在EDTA−Fe脱硫系统中,EDTA/Fe摩尔比的增加导致再生过程中EDTA降解率增加,脱硫体系选择性降低,同降解反应速率增加有关。
3)在EDTA−Fe脱硫系统中,总铁浓度增加导致再生过程中EDTA降解率增加,脱硫体系选择性降低,同增加了再生中羟基自由基有关。
4)在EDTA−Fe脱硫系统中,硫代硫酸钠浓度的增加会减缓EDTA的降解,增加脱硫选择性,这主要是因为硫代硫酸根具有非常好的羟基自由基清除作用。

