三黄连散对靶动物(罗非鱼)的安全性试验
孙钰博,禹方晓,韦英益,于美玲,梁万文,李 旻,覃志彪*,胡庭俊*
(1.广西大学动物科学技术学院,广西南宁 530005;2.广西壮族自治区水产科学研究院,广西南宁 530021)
罗非鱼蛋白质含量较高[1],肉质白嫩,且富含人体所需的8种必需氨基酸,享有“白肉三文鱼”“21世纪之鱼”等美称。罗非鱼养殖要求低,近年来已成为养殖、加工、出口的水产新星。但养殖户操作不良或水体环境恶劣,常导致罗非鱼群暴发细菌性疾病。代表性病原菌包括无乳链球菌、海豚链球菌和嗜水气单胞菌,以无乳链球菌最为典型[2]。养殖户常为预防此类疾病而在水体和饵料中滥用抗生素,导致药残严重超标、出货优品率下降等问题。因此,找到低药残、低污染、纯天然绿色的中草药迫在眉睫。
黄连、黄芩和大黄均具有清热燥湿、泻火解毒的功效。其中,黄芩的临床抗菌性更优,且不产生抗药性[3]。三黄连散由广西大学动物科学技术学院药理实验室自主研发,是黄连、黄芩和大黄等中药配伍制成的复方中草药散剂,可应用于预防罗非鱼无乳链球菌病[4-6]。本试验在前期研究的基础上,进行三黄连散对靶动物(罗非鱼)的安全性评价,为三黄连散的临床应用提供依据。
1 材料与方法
1.1 试验材料
1.1.1 试验药物
三黄连散由广西大学动物科学技术学院研制,山西首爱动物药业有限公司中试生产(批号:20170703,规格:每克含黄芩苷不少于80 mg,包装:100 g/袋)。
1.1.2 试验饲料
罗非鱼膨化配合饵料403(百洋产业投资集团股份有限公司生产,编号:Q/BYS 003—2019,净含量25 kg/袋);水产药物及饵料专用黏合剂(北京鑫洋水产高新技术有限公司生产,净含量250 g/袋)。
1.1.3 试验动物
150尾罗非鱼,每尾重50~100 g,临床健康,未检出无乳链球菌等致病菌,购自广西水产研究所罗非鱼养殖基地。试验前进行场地适应性饲养7 d。每日投喂饲料量按鱼体重的3%称取,每日投喂2次(9:00、18:00)。
1.2 给药方式
采用与临床应用相同的给药途径,拌饵投喂。饵料粉碎,取相应重量的三黄连散与等重量黏合剂混合,加适量水搅拌,与饵料搅拌混匀。阴干8 h,分装后密封保存于塑料袋,4℃保存。
1.3 试验设计
选取已经过适应性饲养7 d且规格相同的罗非鱼150尾,随机分为5组,分别为对照组以及1、3、5、10倍剂量组,每组3个重复,每个重复10尾鱼,分别饲养于400 L的塑料桶中。试验期14 d。连续饲喂7 d后停止投药,只投喂基础饲料。于试验第8、第15 d采样。试验期间饲养条件不变。具体分组处理见表1。

表1 三黄连散靶动物安全性试验分组及处理Tab.1 Grouping and treatment of safety test of three coptis isolated target animals
1.4 样品前处理
每尾鱼血液样本分为2份:0.50 mL血液加抗凝剂EDTA-K2混匀,立即测定全血常规生理指标;剩余血液保存于无菌EP管,4℃静置过夜,3 000 r/min离心10 min,取血清,分装标记,-80℃保存,以测定血清生化指标。采集肝、脾,以10%福尔马林固定,应用于病理组织学检查。
1.5 测定指标及方法
1.5.1 临床症状
试验期间观察记录各组罗非鱼的临床表现和采食情况等。若试验期间罗非鱼出现临床病理变化或死亡等异常情况,详细记录情况出现时间、数量和临床症状等,解剖死亡鱼并确定死亡原因。
1.5.2 生长性能
试验开始前和给药后的第8、第15 d,分别称量记录罗非鱼的体重。采血后处死鱼,采摘完整的肝脏和脾脏进行称重并记录,计算肝脏指数脾脏和指数。

1.5.3 血液生理指标的测定
取抗凝全血检测白细胞计数(WBC)、血红蛋白浓度(HGB)、淋巴细胞(LY)、粒细胞(GRAN)、红细胞计数(RBC)、红细胞比容(HCV)、平均红细胞体积(MCV)、红细胞分布宽度变异指数(RDW-CV)、平均红细胞血红蛋白量(MCH)、血小板计数(PLT)和平均红细胞血红蛋白浓度(MCHC)指标,均使用全自动血细胞计数仪。
1.5.4 血液生化指标的测定
取离心后的血清检测丙氨酸氨基转移酶、总蛋白、天门冬氨酸氨基转移酶、白蛋白、总胆固醇、肌酐、总胆红素、甘油三酯、血尿素氮和碱性磷酸酶指标,均采用南京建成试剂盒测定,操作步骤参照说明书。
1.5.5 病理组织学检查
取10%的福尔马林固定后的肝、脾,包埋切片、HE染色,镜检,观察脏器内中各细胞形态的变化。
1.6 数据统计与分析
试验数据采用SPSS 18.0软件进行单因素方差分析。结果以“平均值±标准差”表示,P<0.05表示差异显著,P<0.01表示差异极显著。
2 结果与分析
2.1 三黄连散对罗非鱼体重及器官指数的影响(见表2、表3)
由表2可知,给药7 d后各组的增重率、脾脏指数和肝脏指数均无显著差异(P>0.05)。
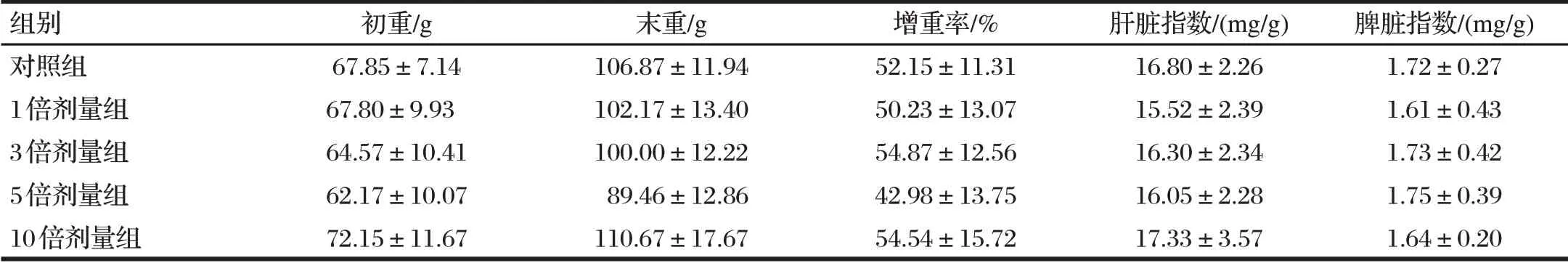
表2 给药7 d对罗非鱼体重及脏器指数的影响Tab.2 Weight and organ indexes after seven days of administration
由表3可知,停药7 d后,与对照组相比,3倍剂量组和10倍剂量组罗非鱼的增重率均显著降低(P<0.05)。各组初重、末和肝脏、脾脏指数均无显著差异(P>0.05)。
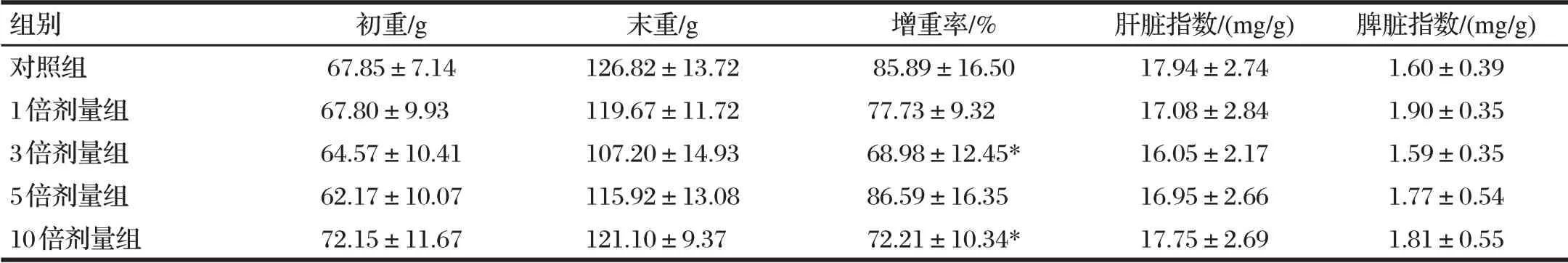
表3 停药7 d对罗非鱼体重及脏器指数的影响Tab.3 Weight and organ indexes after seven days of withdrawal
2.2 三黄连散对罗非鱼血液生理指标的影响(见表4、表5)
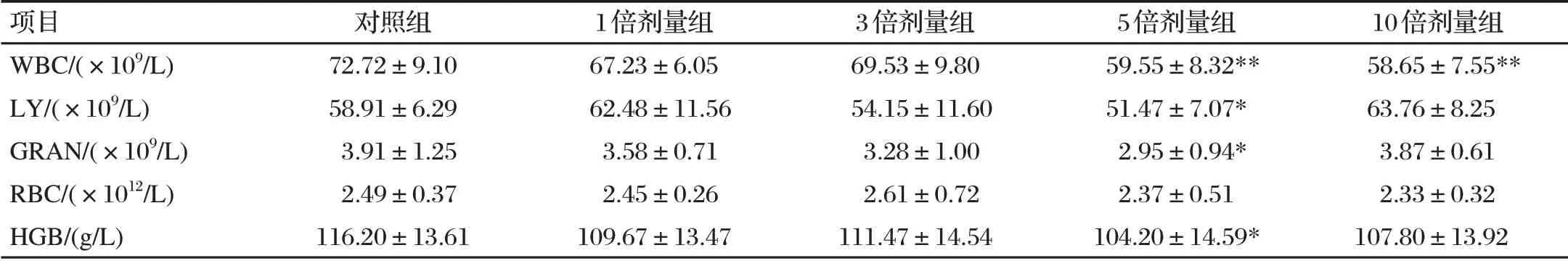
表5 停药7 d对罗非鱼血液生理指标的影响Tab.5 Blood physiological indexes after seven days of withdrawal
由表4可知,给药7 d后,与对照组相比,1倍剂量组、5倍剂量组和10倍剂量组的GRAN和MCH均显著降低(P<0.05),各剂量组的MCV均极显著降低(P<0.01),各剂量组的MCHC均极显著升高(P<0.01)。
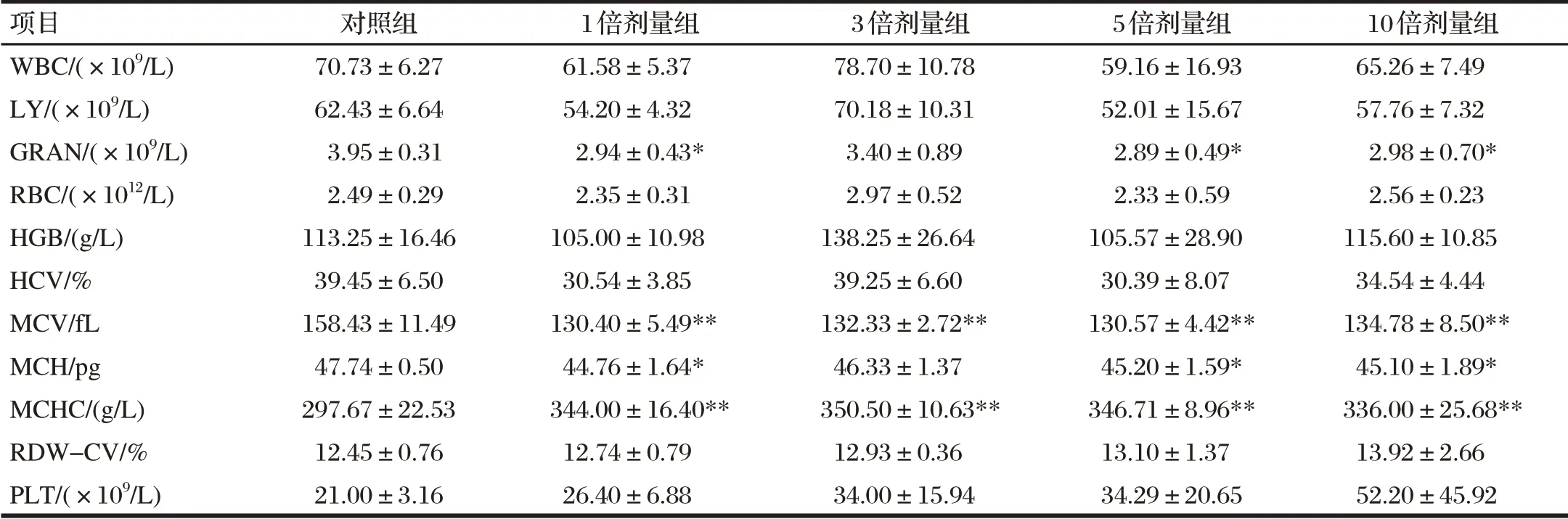
表4 给药7 d对罗非鱼血液生理指标的影响Tab.4 Blood physiological indexes after seven days of administration
各组WBC、LY、RBC、HGB、HCV、RDW-CV、PLT均无显著差异(P>0.05)。
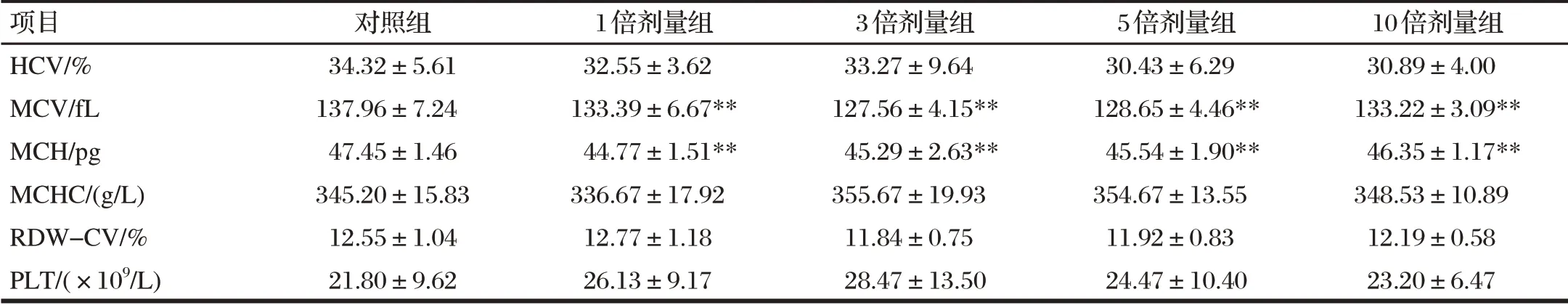
续表5 停药7 d对罗非鱼血液生理指标的影响Tab.5(continue)Blood physiological indexes after seven days of withdrawal
由表5可知,与对照组相比,停药7 d后,5倍剂量组和10倍剂量组的WBC均极显著降低(P<0.01);各剂量组的MCV和MCH均极显著降低(P<0.01);5倍剂量组的LY、GRAN和MCHC均显著降低(P<0.05)。
2.3 三黄连散对罗非鱼血液生化指标的影响(见表6、表7)
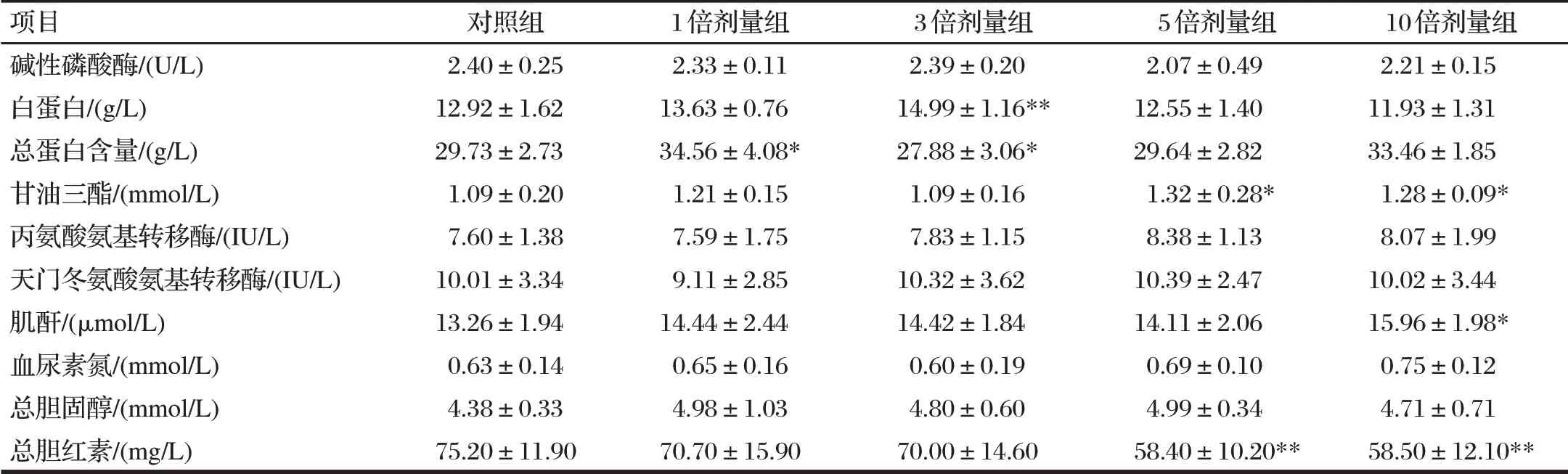
表7 停药7 d对罗非鱼血液生化指标的影响Tab.7 Blood biochemical indexes after seven days of withdrawal
由表6可知,与对照组相比,给药7 d后,5倍剂量组的白蛋白含量极显著升高(P<0.01),10倍剂量组的总蛋白含量极显著升高(P<0.01)。
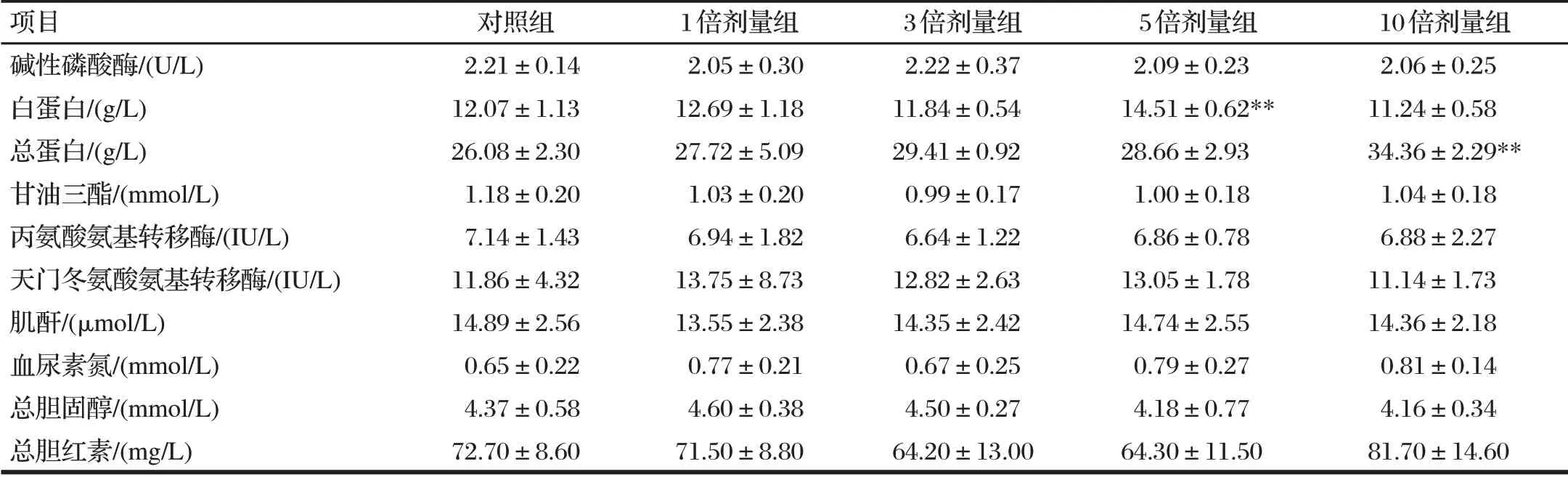
表6 给药7 d对罗非鱼血液生化指标的影响Tab.6 Blood biochemical indexes after seven days of administration
各组碱性磷酸酶、丙氨酸氨基转移酶、天门冬氨酸氨基转移酶的活性以及甘油三酯、肌酐、血尿素氮、总胆固醇、总胆红素的含量均无显著差异(P>0.05)。
由表7可知,与对照组相比,停药7 d后,3倍剂量组的白蛋白含量极显著升高(P<0.01);1倍剂量组总蛋白含量显著升高(P<0.05),3倍剂量组的总蛋白含量显著降低(P<0.05);5倍剂量组和10倍剂量组的甘油三酯的含量显著升高(P<0.05),1倍剂量组数值有所增高,但差异不显著(P>0.05);5倍剂量组和10倍剂量组的总胆固醇含量极显著降低(P<0.01);10倍剂量组肌酐含量显著升高(P<0.05)。
各组碱性磷酸酶、丙氨酸氨基转移酶、天门冬氨酸氨基转移酶的活性及血尿素氮、总胆固醇的含量则均无显著差异(P>0.05)。
2.4 组织切片结果(见图1~图4)
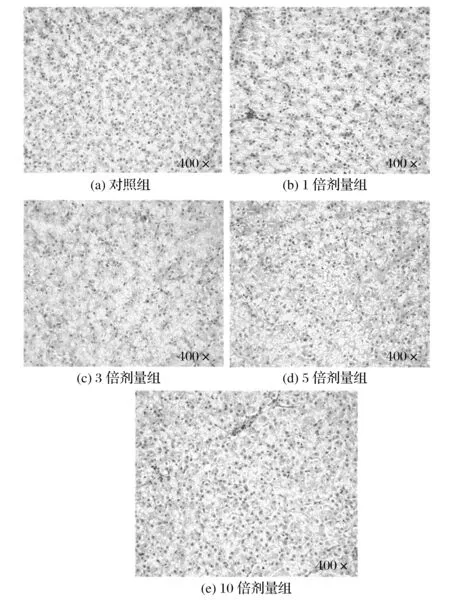
图1 给药7 d罗非鱼肝脏病理组织学结果Fig.1 Histopathological results of liver of tilapia after seven days administration
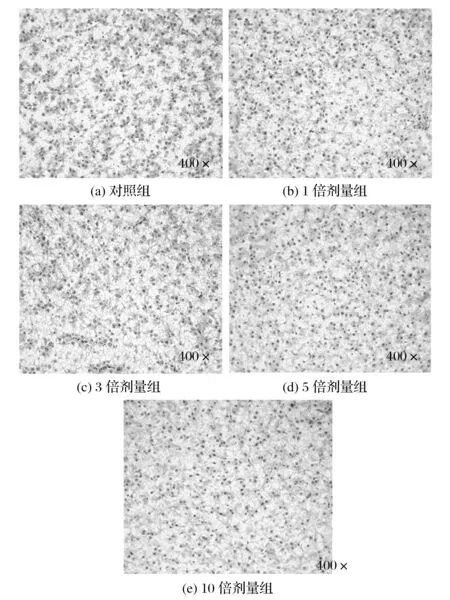
图2 停药7 d罗非鱼肝脏病理组织学结果Fig.2 Histopathological results of liver of tilapia after seven days of withdrawal
由图1~图4可知,于给药7 d和停药7 d后解剖罗非鱼,经眼观和组织病理学检查发现,三黄连散各剂量组脏器均无明显眼观病变,病理组织切片未发现药物引起的细胞毒性变化。
3 讨论
链球菌病一直是罗非鱼养殖户面临最大的难题[7],其中以无乳链球菌感染首当其冲。目前,渔业高密度养殖的环境下,无乳链球菌病初期病症不明显,很可能造成难以估计的损失。因此,养殖户为节约成本,多选择大剂量、大面积地泼洒抗生素类药物,导致链球菌的多重耐药现象日趋严重[8]。近年来,有关部门严令禁止饲料中添加抗生素,要求生产企业生产仅可添加中药类促生长类饲料添加剂;在多重因素的影响下,进一步促进了中兽药制剂的研发。
多种中草药有效成分均具有良好的抗菌效果,能够提高动物的生长性能。陈奇等[9]研究发现,不同剂量的山豆根多糖对人工感染罗非鱼链球菌病具有不同程度抵抗效果,可有效降低罗非鱼感染无乳链球菌后的病死率。徐晴等[10]研究发现,黄芩素对感染鼠伤寒沙门氏菌的小鼠具有明显的治疗作用。薛芳翰等[11]研究发现,黄芩素对鼠伤寒沙门氏菌的生长繁殖具有显著抑制作用,可能与药物干扰细菌细胞膜通透性有关。王宁等[12]研究发现,黄芪提取物对常见的金黄色葡萄球菌、大肠杆菌和沙门氏菌等致病菌具有较明显的体内外抑菌作用。倪建腾等[13]研究发现,黄连、黄芩体外对鲍曼不动杆菌具有一定的抑制作用。阿木古楞等[14]研究发现,石榴皮、诃子、黄芩等3味蒙药对金黄色葡萄球菌和大肠杆菌综合抑菌效果均可达到极度敏感或高度敏感的程度。张照红[15]研究发现,大黄、黄芩和党参等7种中药制成的复方制剂,连续饲喂罗非鱼45 d,可表现显著增重作用。兽用中草药制剂发展前景广阔,为水产养殖的防病、治病提供了新思路。
三黄连散是由广西大学药理实验室自主研发,经过中兽医辨证论治、科学配伍研制而成的中兽药复方制剂。靶动物安全试验通过饲喂罗非鱼不同剂量的三黄连散,检测器官指数、血液生理指标、血液生化指标和病理组织学细胞形态的变化,得到三黄连散对罗非鱼的临床影响情况。
本研究中,罗非鱼各器官指数结果显示,与对照组相比,各剂量组罗非鱼的肝脏指数和脾脏指数均无显著差异,表明三黄连散对罗非鱼脏器无明显毒副作用。
本研究中,罗非鱼的血液生理指标显示,与对照组相比,各三黄连散剂量组罗非鱼的平均红细胞体积均显著降低,表明罗非鱼代谢能力增强[16];给药期间各剂量组的平均红细胞血红蛋白浓度均极显著升高,表明罗非鱼血液氧气运输量增加[17-18]。
本研究中,罗非鱼的血液生化指标显示,与对照组相比,停药前后1、5、10倍剂量组的总蛋白含量均显著升高,且总蛋白含量随中药剂量升高而增加,表明三黄连散可促进机体代谢速度及蛋白质的吸收与合成[19]。停药前各剂量组总胆固醇含量未见明显增高,表明使用三黄连散不会引起罗非鱼体内脂肪堆积[20],对脂质代谢造成压力[21]。停药7 d后,5、10倍剂量组总胆红素含量均显著降低,但丙氨酸氨基转移酶、天门冬氨酸氨基转移酶和碱性磷酸酶的活性等均无显著差异,表明三黄连散对罗非鱼肝脏功能无不良影响[22]。停药前后,1、3、5倍剂量组血尿素氮和肌酐含量均无显著差异,表明三黄连散对罗非鱼的肾脏功能无不良影响。
本试验病理组织学结果显示,停药前后各剂量组肝脏组织结构完整,肝脏细胞清晰可见,与对照组比均无明显的病理变化,表明三黄连散对代谢和免疫无影响。停药前后各剂量组与对照组的脾脏组织切片上均存在少量含铁血黄素,与黄明[23]的试验结果相似,可能与红细胞的生长和凋亡有关。病理切片显示无其他明显的病理变化和细胞毒性变化,表明三黄连散对罗非鱼对造血和免疫无影响。结合停药前后的各项检测指标数据分析表明,1~10倍推荐剂量的三黄连散对罗非鱼无不良影响。
4 结论
以三黄连散临床推荐剂量的1、3、5、10倍,连续给药7 d及停药7 d后,各剂量组罗非鱼均未出现临床病理变化,且脏器指数、血液生理指标、血液生化指标和病理组织学结果与对照组相比均无显著差异。研究表明,三黄连散在1~10倍推荐剂量下连续饲喂安全可靠。

