人工液胸在内科胸腔镜术前准备中的应用价值
卢志斌 罗莉 罗林紫 肖阳宝
内科胸腔镜在呼吸系统疾病,特别是胸膜疾病中具有重要的诊断价值[1-2]。其一般使用穿刺鞘管(trocar)将外界与胸腔连通,但要确保胸腔镜安全进入胸腔还需要有足够的胸腔内空间,若肺脏未萎陷、胸腔内液体量或空间不足,则进镜会增加脏层胸膜损伤的风险。故有研究推荐在内科胸腔镜术前实施人工气胸以形成隔离缓冲带,并有效扩大手术操作空间,但这一方式也会产生皮下气肿、疼痛、呼吸困难,甚至气体栓塞等严重并发症[3]。人工液胸类似于人工气胸,既往主要用于膈顶或肝脏肿瘤消融治疗的辅助超声定位,效果良好[4-5],但目前尚缺乏应用于内科胸腔镜手术条件的报道。故笔者通过整理分析内科胸腔镜活检术前实施和未实施人工液胸准备患者的临床资料,对人工液胸探查胸腔情况和创造胸腔操作条件的能力进行评估,为其在临床中的应用及推广提供依据。
资料和方法
一、研究对象
回顾性分析2014年5月至2019年11月因胸腔积液或胸膜疾病入住湖南省胸科医院并行内科胸腔镜手术的163例患者的临床资料。以2017年1月我院内镜中心将人工液胸作为内科胸腔镜活检术前准备为节点,将2014年5月至2016年12月前未实施内科胸腔镜术前人工液胸准备的48例患者作为对照组,将2017年1月至2019年11月实施了内科胸腔镜术前人工液胸准备的115例患者作为观察组。
163例患者中,男性126例,女性37例,年龄范围为14~82岁,平均年龄为(49.0±16.4)岁。通过胸腔超声测定,胸膜厚度为4~18 mm,其中102例未见胸膜明显增厚(≤5 mm);95例存在中度以上的胸腔粘连,25例为轻度粘连,43例未探及明显分隔或光带影,由于轻度及以下的粘连对胸腔影响较小,故纳入无胸腔粘连组。通过CT图像测定,胸膜厚度为3~15 mm,36例患者未见胸膜明显增厚(≤5 mm);119例发生胸腔粘连(在胸腔内发现条索影或包裹性胸腔积液),44例未发现胸腔粘连(胸腔积液呈弧形、新月形、半月形影,且未见明显条索影或包裹附壁现象)。两组患者在性别、年龄、术前胸膜厚度及胸腔粘连程度的差异均无统计学意义(表1)。

表1 内科胸腔镜术前评估指征在两组患者间的分布情况
纳入标准:(1)胸腔积液原因不明者;(2)各种原因引起的非严重胸膜粘连需行松解术者;(3)急性脓胸需早期治疗者。排除标准:(1)胸膜广泛粘连,无胸膜操作空间者;(2)慢性脓胸且形成钙化纤维板者;(3)大量胸腔积液或影像学提示胸腔无粘连者;(4)严重心肺功能不全者;(5)难以纠正的出凝血功能障碍者;(6)极度衰竭不能承受手术者;(7)并发肺包虫、囊虫病等疾病者。
二、术前评估指标
1.胸腔积液量:积液量对内科胸腔镜的手术效果有直接影响。中量以上的胸腔积液可在脏壁两层胸膜间形成一定的缓冲隔离带,是行内科胸腔镜的理想条件,术前胸腔积液量应维持在既不会引起患者不适,也不会增加术中脏层胸膜损伤风险的程度。故根据本中心经验,当胸腔超声和(或)胸部CT提示胸腔积液深度<20 mm或无胸腔积液时(图1,2),应当实施人工液胸。
2.胸膜厚度:胸膜厚度通常采用胸腔B超或胸部CT测量,其正常厚度约为1~2 mm,超过3 mm考虑为胸膜增厚。但目前并没有明确的胸膜厚度分级标准,故本研究结合患者特点并参照《WS 288—2017肺结核诊断》[6],以>5 mm为胸膜增厚,≤5 mm 或无法测量为非胸膜增厚(图3,4)。
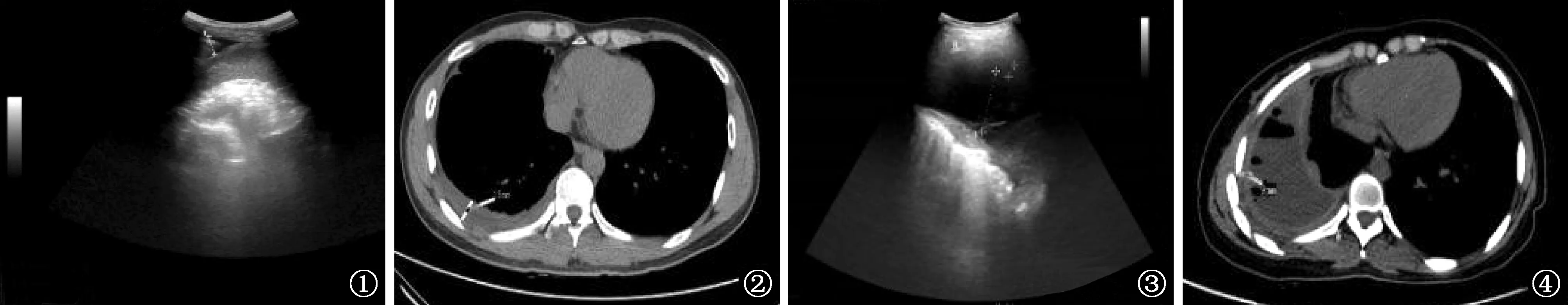
图1 超声见少许胸腔积液 图2 CT见少许胸腔积液 图3 超声见胸膜增厚 图4 CT见胸膜增厚
3.胸腔粘连程度:通常采用超声和CT检查联合评估胸腔是否存在粘连[7-9],以胸腔内有条索影或积液呈现明显包裹分隔、密度不均匀、局部有钙化等为胸腔粘连(图5~8);以胸腔积液呈弧形、新月形或半月形影,密度均匀,呈均一低回声低密度影为非胸腔粘连。考虑影像学检查对胸腔有无粘连可能存在一定的判断偏差,本研究最终以内科胸腔镜镜下直视可见粘连确认粘连分组。

图5 超声见包裹分隔 图6 超声见分隔光带及片絮状回声 图7 CT见胸腔内条索影 图8 CT见积液包裹附壁粘连
三、器械和操作方法
1.器械:一次性无菌留置引流导管(广州艾贝尔医疗器械有限公司)、一次性使用无菌注射器(60 ml)、内科胸腔镜(LTF-240,日本Olympus株式会社,外径为7 mm,工作孔道为2.8 mm)。
2.术前准备:完善术前常规检查,向家属交代胸腔穿刺、人工液胸的手术过程及风险,签署知情同意书。
3.人工液胸术:术前通过超声引导于积液最低点处下行胸腔穿刺,置入胸腔引流管。预热500 ml生理盐水至37 ℃,引流管三通接头连接60 ml注射器,推注生理盐水进入胸腔。人工液胸的注液量因患者体型及病灶部位按需注入,一般采取前50 ml缓慢(1~3 ml/s)注入,中间200 ml快速(10~15 ml/s)注入,后250 ml缓慢(1~3 ml/s)注入,总量不超过500 ml,如因注入量偏多而引起患者出现刺激、压迫症状(咳嗽、呼吸困难、局部胀痛等)则可及时负压抽吸。术后可经留置闭式引流管完全清除剩余生理盐水。
4.内科胸腔镜检查:患者取健侧卧位,予以镇静镇痛+局部麻醉后于腋前线与腋后线间的第4至第8肋区域以体表标记作为穿刺鞘管进入部位行内科胸腔镜检查。其中,观察组应避开肋间的胸腔置管于B超定位胸膜滑动征最明显处作标记,对照组于B超定位胸腔积液最深且胸膜滑动征最明显处作标记。
四、评价指标
通过对两组患者相关资料进行比较,对人工液胸实施的操作成功率、操作有效率和进胸时肺损伤率进行评估。其中,操作成功率指成功实施人工液胸操作的患者数占该组总患者数的比例;操作有效率指在内科胸腔镜手术中成功取得理想组织标本,并最终取得病理支持诊断的患者数占该组总患者数的比例;进胸时肺损伤率指通过穿刺鞘管突破壁层胸膜时,由于各种原因造成脏层胸膜和(或)肺部损伤的患者数占总患者数的比例。
五、统计学处理
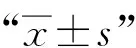
结 果
一、疾病诊断
163例患者中,经内科胸腔镜活检后病理直接确诊141例(86.5%),分别为观察组106例(92.2%)、对照组35例(72.9%),两组病理直接确诊率的差异有统计学意义(χ2=10.757,P=0.001);22例(13.5%)结合临床资料综合判断后确诊。其中,诊断为结核性胸膜炎者95例(58.3%),分别为观察组71例,对照组24例;诊断为非结核性胸膜疾病者68例(41.7%),分别为癌性胸腔积液33例(20.2%;观察组22例,对照组11例)、纤维素性胸膜炎34例(20.9%;观察组21例,对照组13例)、乳糜胸1例(观察组)。
二、两组患者实施效果分析
1.人工液胸操作成功率:观察组患者人工液胸操作均获得成功,其中,114例(99.1%)患者首次即获得成功,仅1例因置管后引流管堵塞而无法实施胸腔注液,拔除原管重新置管后操作也获得成功。
2.内科胸腔镜操作有效率:观察组患者中,112例患者内科胸腔镜操作有效,有效率为97.4%。3例无效患者中,1例为进胸后发现胸膜增厚僵硬,转外科行手术治疗,考虑晚期脓胸纤维板形成;2例为胸腔结构不清,进镜至壁层胸膜后考虑继续操作的风险较大,终止操作,术后综合诊断为结核性脓胸。对照组患者中,41例患者内科胸腔镜操作有效,有效率为85.4%。7例无效患者中,1例为晚期脓胸,纤维板形成,转外科行手术治疗;另6例均为脏壁两层胸膜粘连严重,进镜分离时造成肺损伤,且未能进一步分离至胸腔积液腔,终止操作。两组操作有效率差异有统计学意义(χ2=6.481,P=0.011)。
3.内科胸腔镜致肺损伤率:14例患者在穿刺鞘管置入过程中肺部受损,其中观察组5例(4.3%),对照组9例(18.8%),两组间差异有统计学意义(χ2=7.206,P=0.007)。
三、实施人工液胸的并发症情况
观察组平均生理盐水注入量为(371.8±110.3) ml,注水过程中共计有27例(23.5%)出现不适,经处置后均缓解。其中,有7例出现轻中度咳嗽,吸氧后缓解;1例出现胸壁皮下包块而停止操作,平卧休息6 h 后缓解;11例出现注水侧胸腔局部疼痛,调整体位及呼吸频率后缓解;8例患者在注水400 ml时出现呼吸困难,停止操作,采取坐位及吸氧治疗后缓解。未出现与人工液胸操作相关的皮下气肿、血胸、感染、针道转移、皮下气肿、空气栓塞等严重并发症。
讨 论
结核性胸膜炎是渗出性胸腔积液的常见原因[10-11],常有纤维蛋白沉积、附着,多发生胸腔内纤维粘连、包裹等手术不利因素[12],增加了胸腔镜操作相关并发症的风险。
自1968年Rudy等[13]创立人工气胸造影术以来,人工气胸就被用于结核病的治疗,但因其可能发生气体栓塞等严重并发症[14],且术后皮下气肿与术前行人工气胸有相关性[15],其在内科胸腔镜的术前应用中一直存在争议。为获得良好的彩色多普勒超声探测视野,有学者向胸腔内注入液体,成功地将人工液胸应用于临床相关治疗中[16-17],具有简单易行、可重复操作的特点。而且,在评估内科胸腔镜手术效果时,人工气胸需胸部X线或CT复查,而人工液胸采用彩色多普勒超声评估即可,避免了患者的重复射线暴露,依从性明显提高。因此,人工液胸可使胸腔积液条件从无或少量转变为中到大量,更利于直接置入穿刺鞘管;并可以通过推注时感受到的阻力、注入和抽出液体情况、患者不适反应判断胸膜腔的粘连程度、包裹分隔的软硬度情况,指导手术方案。
我中心开展人工液胸以来取得了良好的效果。首先,实施人工液胸患者组的病理直接确诊率明显高于未实施组患者,提示术前人工液胸的干预可能对手术结果有积极作用,虽然病理结果的好坏与手术操作的熟练度、留取标本的部位和方式、疾病的种类、病情的进展程度等更有关联,但目前并无大样本多中心研究否认术前准备对手术结果的影响,需行进一步研究来论证。但笔者推测,人工液胸可能是利用水的流动性渗透到各个角落,随着积液量的增加,胸腔压力增大,对于胸腔狭小、外压、粘连、分隔等可起到一定的柔性扩张作用,创造了更好的手术视野和操作条件,从而提高了诊断效率。其次,本研究人工液胸的操作成功率高达100.0%,进一步说明其简单易行,更利于穿刺鞘管置入。虽然研究中1例患者为二次操作成功,但与引流管堵塞有关,不涉及手术操作问题。最后,观察组行内科胸腔镜操作的有效率明显高于对照组,肺损伤率明显低于对照组,说明人工液胸为内科胸腔镜手术提供了更积极的手术条件,安全有效。
现行内科胸腔镜诊疗规范[3]中推荐少量胸腔积液的患者术前应行人工气胸,虽然存在皮下气肿、空气栓塞等较严重并发症,但因发生率较低,不少医院还一直使用人工气胸。而人工液胸的操作可达到与人工气胸相近的胸腔效果,且在安全性方面更具优势[18]。本研究中,实施人工液胸的患者未见皮下气肿、血胸、感染、针道转移、空气栓塞等严重并发症,在注水过程中有27例(23.5%)出现了轻中度咳嗽、胸壁皮下包块、注水侧胸腔局部疼痛、呼吸困难等并发症,经简单对症治疗后均可较快缓解。笔者认为并发症的出现可能与人工液胸在早期开展时操作不熟练、液体注入速度过快、对液胸建立终点经验值不明确等有关,在经过一定的实践积累后,发现控制注液速度,通过先慢(1~3 ml/s)后快(10~15 ml/s)再慢(1~3 ml/s)的方式,可以增加操作耐受度,并能够有效探知胸腔情况;输注的液体最好加温至接近体温的37 ℃,能进一步减少异物对胸膜的刺激;同时建议在操作前后进行彩超检查,做到术前预估注液量、术后评估液胸建立情况,目前我中心每例患者平均注入(371.8±110.3) ml液体即可达到理想状态,如能配备床旁彩超实时监测,则能进一步提高工作效率。
对于发病初期的患者,其积液量较多且胸腔粘连程度低,是行内科胸腔镜的最佳时机,术前可不行人工液胸;对于病程较长、胸腔积液治疗后反复增长,特别是渗出性积液者,由于纤维蛋白渗出沉着于胸膜表面,并于胸膜纤维化进程中在脏壁层间形成网格状粘连[19],极易造成穿刺鞘管入腔受限、操作困难或肺部损伤等[15],丧失了行内科胸腔镜的最佳手术时机[20],此类患者建议术前行人工液胸改善胸腔条件。
根据本中心的经验和临床观察,当注水无阻力、回抽顺畅、患者未诉不适时,提示胸腔粘连较少、分隔较薄、脏壁两层胸膜易分离;当注水阻力大、可注水量少、回抽困难,且注水后出现明显不适时,提示胸腔内粘连严重、包裹分隔坚韧、肺脏贴壁固定可能性大,手术风险较高;若抽吸出絮状白色物则提示胸腔内粘连可能为近期形成或疏松易于清理等[21]。由于手术采取健侧卧位,积液会不可避免地向纵膈侧聚集,在进胸处可能会缺乏积液覆盖导致肺部损伤,故认为人工液胸可能对于胸腔积液少或无且胸腔存在粘连并在局部形成包裹分隔的患者更有优势。但如果积液较易流动,也说明胸腔内粘连程度并不严重,此类患者即使不进行术前干预也很少发生并发症。
综上所述,人工液胸作为内科胸腔镜术前的胸腔准备,具有良好的可重复操作性,可有效探知胸腔情况,能有效提高操作有效率,减少操作过程中的肺损伤,安全性高,有临床推广价值。
利益冲突所有作者均声明无利益冲突
作者贡献卢志斌:数据收集及整理、统计学分析、论文撰写;罗莉:数据收集、统计学分析、论文修改;罗林紫:数据收集、统计学分析;肖阳宝:研究指导、论文修改

