MnFe2O4-还原氧化石墨烯活化过硫酸氢钾降解罗丹明B
王 欣, 姚 变, 程 浩, 乔 旭, 吴 丹
(沈阳化工大学 环境与安全工程学院, 辽宁 沈阳 110142)
高级氧化技术(AOPs)由Glaze等[1]提出,是指利用光、电、热等方式产生强氧化性的自由基(例如OH·)将难降解的结构复杂的大分子有机物氧化成低毒甚至无毒的小分子,或者直接将其矿化为CO2、H2O、无机矿物盐等无机物.相较于传统的氧化法,AOPs对于高毒性、可生化性差的有机废水具有较强的适应性,与常规的物化、生化法相比有明显的技术优势.因此,高级氧化技术在实际废水处理中具有较好的应用潜力.
本文采用水热法制备了MnFe2O4-RGO催化剂,并以罗丹明B为目标污染物,探究了MnFe2O4-RGO对PMS的活化性能,研究了反应体系的条件对RhB降解性能的影响规律.
1 实验部分
1.1 试剂与表征
氯化锰(MnCl2·4H2O)、石墨粉、聚乙烯吡咯烷酮(PVP,K-30)、铁氰化钾(K3[Fe(CN)6])、过硫酸氢钾(KHSO5)、高锰酸钾(KMnO4)、双氧水、无水乙醇、浓硫酸均为天津科密欧化学试剂有限公司提供;超纯水.
采用超高分辨场发射扫描电镜 Quanta 200 FEG 对所制备样品进行微观形态观察分析,工作电压 5 kV; 采用 X-射线衍射仪 D8 Advance 测试样品的晶体结构.
1.2 催化剂的制备
1.2.1 氧化石墨烯(GO)的制备
将23 mL浓硫酸缓缓倒入装有1 g石墨粉的250 mL烧杯中,将该烧杯置于冰水混合物中,少量多次加入3 g高锰酸钾,超声6 h.加入186 mL超纯水和10 mL双氧水,离心分离后,用质量分数为5%的HCl洗涤3次,经干燥后得到GO.
1.2.2 MnFe2O4的制备
MnFe2O4的制备以参考文献[11]为依据,并对铁锰比进行改良.溶液A:MnCl2·4H2O(1.487 g)和PVP(0.3 g)搅拌溶解于C2H5OH与H2O的混合溶液中(C2H5OH与H2O均为25 mL).溶液B:0.825 g K3[Fe(CN)6]搅拌溶解于C2H5OH与H2O的混合溶液中(C2H5OH与H2O均为25 mL).将溶液A和溶液B混和均匀,放入120 ℃鼓风干燥箱保温12 h,洗涤干燥后,在450 ℃下煅烧1 h.
1.2.3 MnFe2O4-RGO的制备
取0.06 g GO溶于60 mL超纯水中,超声12 h后取21 mL GO溶液备用.称取0.3 g MnFe2O4,加入21 mL GO溶液和14 mL去离子水中搅拌30 min,在120 ℃下保温15 h,离心分离干燥后得到黑色粉末,即为MnFe2O4-RGO.
1.3 降解RhB实验
采用质量浓度为9.6 mg/L的RhB溶液作为目标污染物.将一定量的催化剂加入到100 mL RhB溶液中,在不停搅拌下加入一定量的过硫酸氢钾,开始计时,每隔10 min取2 mL样品,经离心分离后取上清液,采用紫外-可见分光光度计测其在波长554 nm处的吸光度.
2 结果与讨论
2.1 MnFe2O4-RGO催化剂的表征
图1是MnFe2O4-RGO样品的SEM照片.由图1可知:RGO呈现出带有褶皱的半透明薄层状结构[10];MnFe2O4呈无规则的颗粒状结构,分散于RGO表面;MnFe2O4粒径大约为0.1 μm,RGO粒径约为1.5 μm.

图1 MnFe2O4-RGO样品的SEM照片Fig.1 SEM image of MnFe2O4-RGO sample
图2为MnFe2O4-RGO样品的XRD谱图.
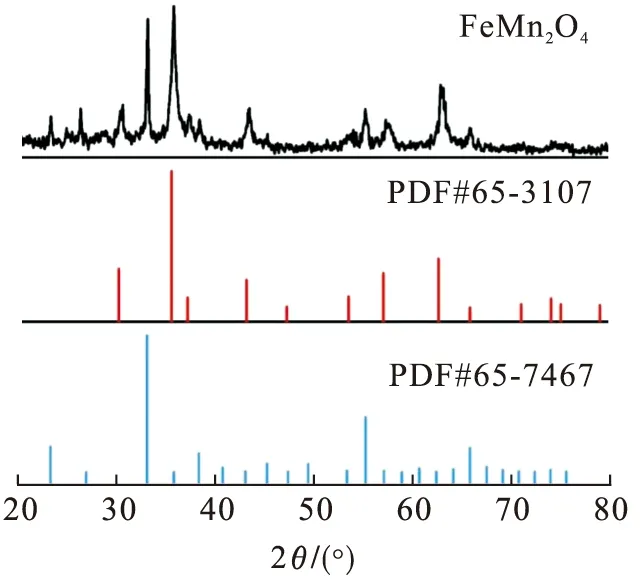
图2 MnFe2O4-RGO样品的XRD曲线Fig.2 XRD pattern of MnFe2O4-RGO sample
由图2可知:在30.2°、34.88°、35.4°、43.1°和63.5°处的衍射峰分别对应MnFe2O4的(220)、(222)、(311)、(400)和(440)晶面,与标准PDF卡片NO.65-3107和NO.65-7467吻合度较高.煅烧后MnFe2O4各个特征衍射峰与标准卡片一一对应,说明经过煅烧所制备的催化剂为多孔MnFe2O4.
2.2 RGO对MnFe2O4-RGO催化活性的影响
为了探究RGO对MnFe2O4-RGO催化活性的影响,实验制备了一系列不同RGO掺杂量的MnFe2O4-RGO样品,记作x% MnFe2O4-RGO(x%为RGO的质量分数).图3为不同催化剂活化过硫酸氢钾对RhB的降解效果曲线.降解反应条件为MnFe2O4-RGO投加量0.25 g/L、c(KHSO5)=0.15 mmol/L、T=25 ℃、pH=7.
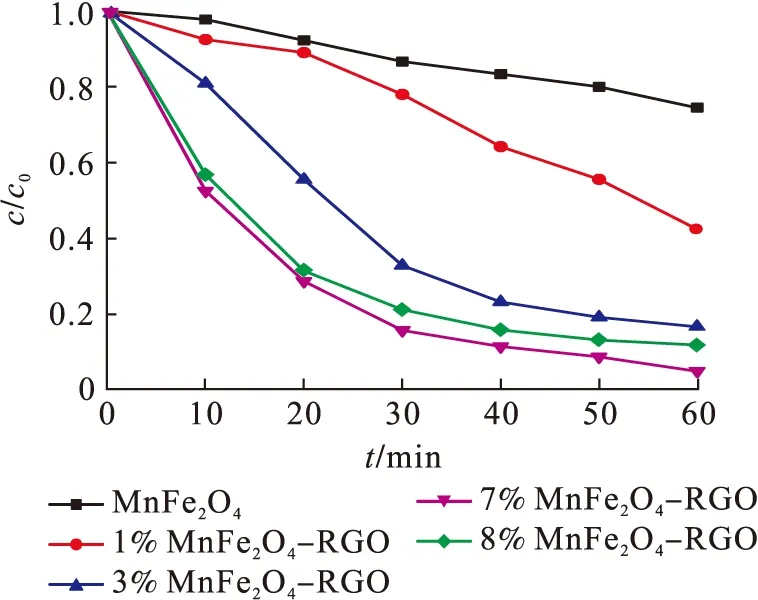
图3 不同催化剂反应体系下RhB的降解效果Fig.3 Degradation effect of RhB under different catalyst reaction systems
由图3可知MnFe2O4-RGO降解效率显著高于MnFe2O4.原因是掺杂了RGO后,RGO表面携带的大量官能团(—OH、—COOH等)产生的静电斥力促进了催化剂在溶液中的分散性.同时,由于RGO具有较大的比表面积,为活化过硫酸氢钾降解RhB提供了更多的活性位点,使RhB的降解效率明显提高.当RGO的掺杂质量分数分别为1%、3%、7%、8%时,RhB的去除率分别为57%、83%、95%、88%.可见随着RGO掺杂量的增加,MnFe2O4-RGO的降解能力也在不断提高.但当RGO掺杂质量分数为8%时,MnFe2O4-RGO的降解率出现下降,这可能是由于RGO掺杂量过大时,部分MnFe2O4被RGO包裹住,使RGO和MnFe2O4的协同作用下降,导致降解效率下降.综上,RGO的最适宜掺杂质量分数为7%.
2.3 pH对MnFe2O4-RGO催化活性的影响
催化降解RhB的实验条件同2.2节,探究MnFe2O4-RGO催化剂在不同pH(pH=3、5、7、10)条件下对RhB的降解效果,如图4所示.
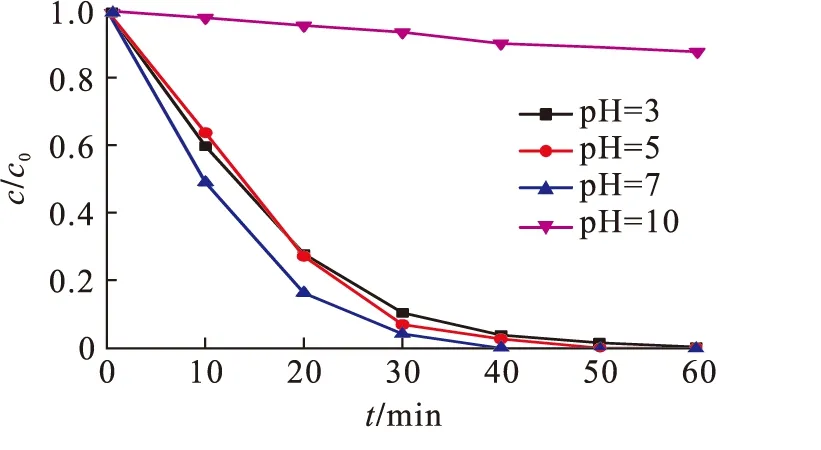
图4 pH对RhB降解效果的影响Fig.4 Effect of pH on the degradation of RhB
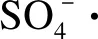
2.4 温度对MnFe2O4-RGO催化活性的影响
催化降解RhB的实验条件同2.2节,考察了不同温度(25、30、40、50 ℃)条件下,催化剂对RhB降解效果的影响,结果如图5所示.
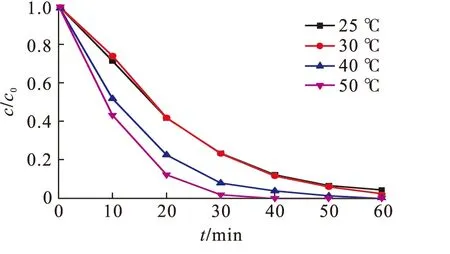
图5 温度对RhB降解效果的影响Fig.5 Effect of temperature on RhB degradation
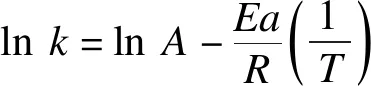
2.5 PMS投加量对MnFe2O4-RGO催化活性的影响
在实际工业处理印染废水时,PMS的投加量直接影响水处理成本,投加量对污水处理过程具有重要意义.笔者探究了不同过硫酸氢钾浓度对MnFe2O4-RGO降解RhB的影响,结果如图6所示.
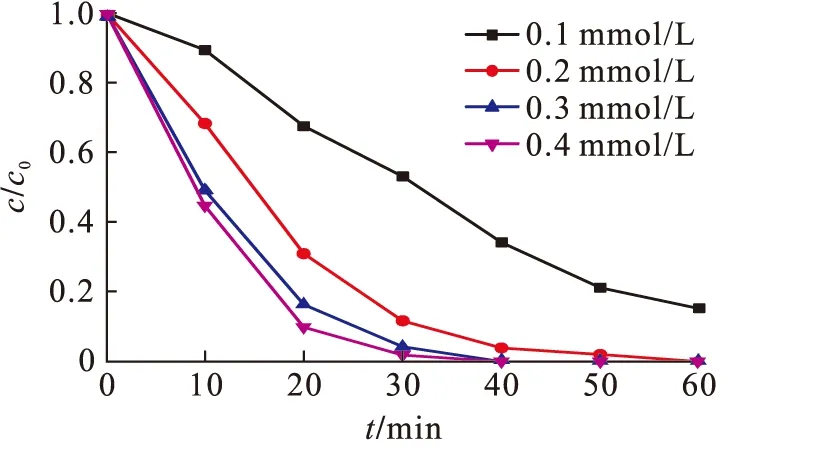
图6 过硫酸氢钾对降解反应的影响Fig.6 Effect of potassium persulfate on degradation reaction
当溶液中过硫酸氢钾浓度从0.1 mmol/L增加至0.4mmol/L,RhB的降解率不断提高.当浓度为0.1 mmol/L时,RhB的去除率为85%,未全部降解;当过硫酸氢钾浓度为0.3 mmol/L和0.4 mmol/L时,RhB均在40 min降解完成.考虑经济因素,0.3 mmol/L为最优PMS浓度,此时n(RhB)∶n(KHSO5)=1∶15.
2.6 MnFe2O4-RGO投加量对降解RhB的影响
催化降解RhB的实验条件同2.2节,考察了MnFe2O4-RGO投加量对RhB降解效率的影响,结果如图7所示.由图7知:在MnFe2O4-RGO投加量为0.1、0.25、0.5 g/L时,RhB降解效率随MnFe2O4-RGO剂量的増加而提高.当进一步增加MnFe2O4-RGO投加量至0.75 g/L和1 g/L时,RhB降解效率不再提高,表明当MnFe2O4-RGO的投加量为0.25 g/L时已经为PMS提供了充足的反应活性位点,投加量过大会加速消耗反应体系中的PMS,使得降解率下降.MnFe2O4-RGO的最佳投加量为0.25 g/L.
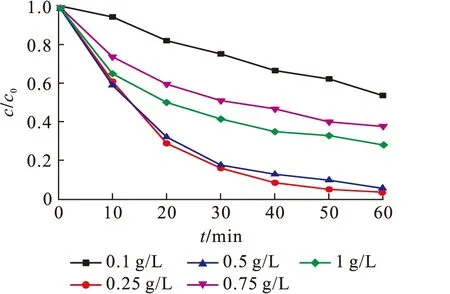
图7 MnFe2O4-RGO投加量对RhB降解的影响Fig.7 Effect of MnFe2O4-RGO dosage on RhB degradation
2.7 无机阴离子对RhB降解的影响

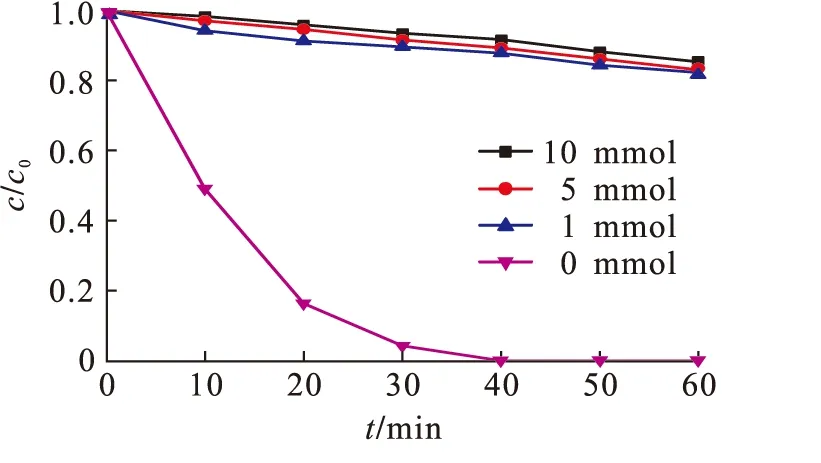
图对RhB降解的影响Fig.8 Effect of on the degradation of RhB
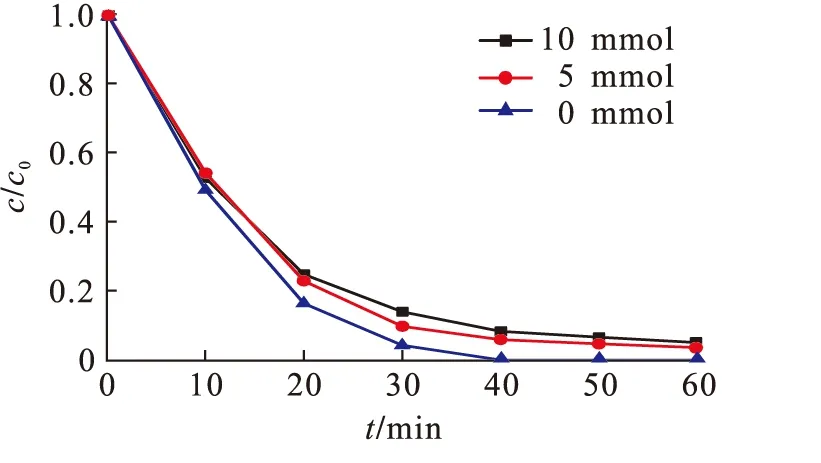
图9 Cl-对RhB降解的影响Fig.9 Effect of Cl-on the degradation of RhB
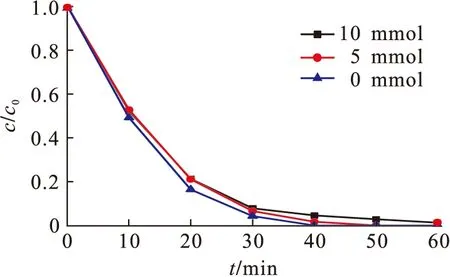
图对RhB降解的影响Fig.10 Effect of on the degradation of RhB
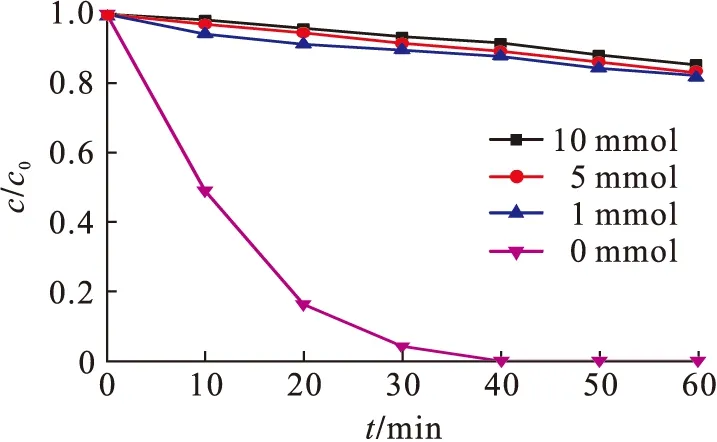
图对RhB降解的影响Fig.11 Effect of the degradation of RhB
2.8 MnFe2O4-RGO的稳定性
考察了MnFe2O4-RGO的稳定性,如图12所示.对样品MnFe2O4-RGO进行5次循环利用,MnFe2O4-RGO对RhB的降解效果没有明显下降,证明该催化剂结构稳定,适用于实际废水处理.
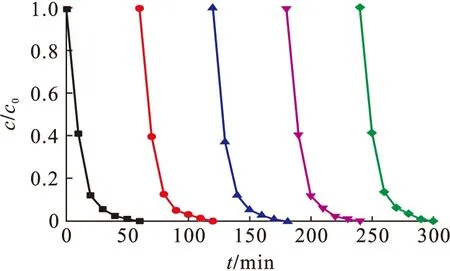
图12 MnFe2O4-RGO降解RhB的重复利用效果Fig.12 Reuse effect of MnFe2O4-RGO degrading RhB
3 结 论
通过水热法制备了MnFe2O4-RGO复合催化剂,探究了MnFe2O4-RGO/PMS体系对RhB的降解性能,系统研究了各要素对降解RhB的影响规律,得到了如下研究结果:
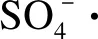
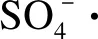
(3) 本研究为实际的染料废水处理提供了一种有效的的理论方法,具有较好的研究价值和应用前景.

