聚焦复分解反应
陈铖铖
复分解反应属于化学基本反应类型,是酸、碱、盐之间发生的重要反应。复分解反应在判断物质能否共存和物质的检验、除杂、鉴别中具有重要应用,是中考考查的重点和难点。
考点速览
考点1:复分解反应的概念
两种化合物互相交换成分,生成另外两种新的化合物,这类反应叫作复分解反应。反应表达式:AB + CD → AD + CB。
考点2:复分解反应发生的条件
只有当两种化合物互相交换成分,生成物中有气体或沉淀或水生成时,复分解反应才可以发生。
考点3:常见的复分解反应类型
常见的复分解反应类型有酸和碱的反应、酸和盐的反应、酸和金属氧化物的反应、碱和盐的反应、盐和盐的反应。
考点4:利用复分解反应的条件判断离子(或物质)能否共存
若离子之间能结合生成水或气体或沉淀,则离子之间不能共存。离子共存这类题型中常见的隐含条件有三种情形:(1)酸性条件型;(2)碱性条件型;(3)无色条件型。注意Cu2 +(蓝色)、Fe2 + (浅绿色)、Fe3 + (黄色)、MnO[-4](紫红色)是有色离子。
考点5:物质的检验、鉴别和除杂
利用离子之间的反应可进行检验、鉴别和除杂。例如,可以用稀硝酸和硝酸钡来检验硫酸根。碳酸根和碳酸氢根的检验方法是一样的,可以用稀盐酸和澄清石灰水来检验,若需对二者进行鉴别,可以分别向两种溶液中加入氯化钙溶液,能产生白色沉淀的为碳酸根。若需除去氯化钠溶液中的少量碳酸钠,溶液中的杂质离子为碳酸根离子,可采用沉淀法(加入氯化钙溶液)或化气法(加入稀盐酸)将碳酸根除去。
应用提升
例1 (2021·湖北·仙桃)某无色溶液滴入酚酞后显红色,在其中可能大量存在的离子组是( )。
A. Na+、K+、CO[2-3]、Cl- B. Na+、NH[+4]、Cl-、NO[-3]
C. K+、Fe3+、NO[-3]、Cl- D. K+、Ba2+、CO[2-3]、NO[-3]
答案:A
例2 (2021·湖北·恩施)某公司生产的融雪剂由NaCl、CaCl2、Na2CO3和CuSO4中的一种或两种物质组成。小洁同学将该融雪剂加水溶解,得到无色溶液,向该溶液中加入K2CO3溶液,有白色沉淀生成。由此可知,该融雪剂的组成可能是( )。
A. CuSO4、NaCl B. Na2CO3、NaCl
C. CaCl2、NaCl D. CuSO4、CaCl2
答案:C
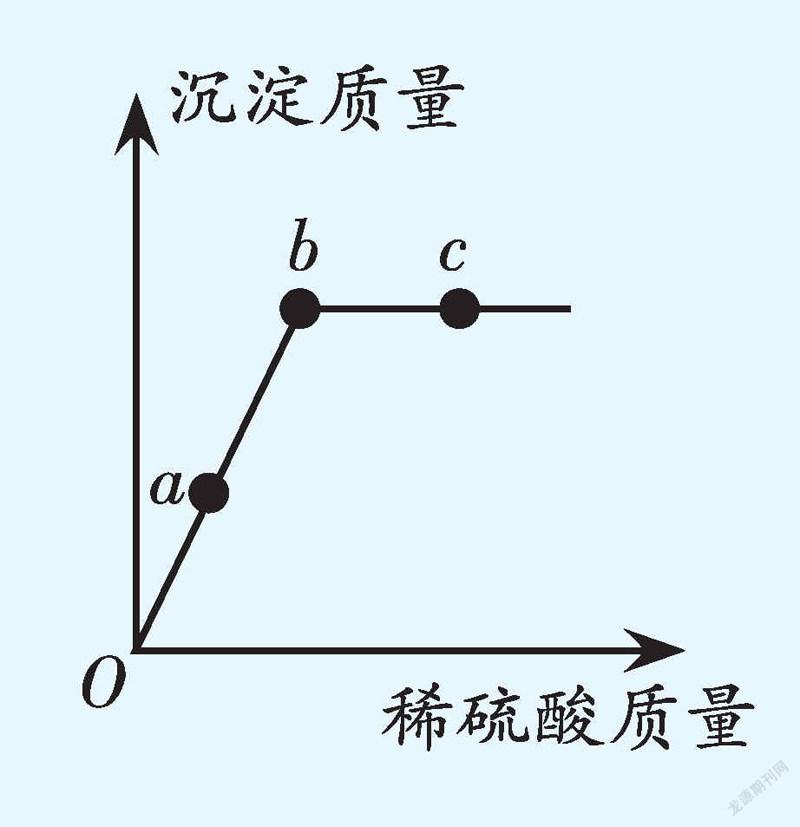
例3 (2021·广西·河池)现有NaOH和BaCl2的混合溶液,向其中逐滴加入稀硫酸,生成沉淀质量与加入稀硫酸质量的变化关系如图所示。下列说法错误的是( )。
A. 滴至a点时,溶液中可能只进行一个化学反应
B. 滴至b点时,溶液中一定不含BaCl2
C. 滴至b点时,溶液中的pH一定等于7
D. 滴至c点时,溶液的pH可能等于7,也可能大于7或小于7
答案:C
(作者單位:辽宁省实验中学分校)

