紫外光高级氧化技术降解安赛蜜的研究进展
殷超,刘亚利
(南京林业大学 土木工程学院,江苏 南京 210037)
近年来,药品、个人护理产品、人工甜味剂等新兴污染物,通过污水、垃圾渗滤液等方式进入水环境,引起了科学界的高度重视[1-2]。安赛蜜是一种应用较为广泛的人工甜味剂,因具有甜度高、生产成本低、不含热量等优势,其全球消费量持续稳定增长[3]。此外,安赛蜜很难通过代谢系统被人体吸收,导致其在水中的浓度达到90 μg/(人·d),远高于药品和个人护理品的浓度[4-5]。安赛蜜在水环境中不断累积,对生态系统和人类健康产生潜在威胁[6-8]。
目前,活性炭吸附、生物降解、高级氧化等技术被用来降解去除水中的安赛蜜[9-11]。其中,基于紫外光辐射衍生的高级氧化技术是一种很有前途的污水处理技术,通过生成强氧化自由基来处理有机物。本文介绍了紫外光分别联合过氧化氢、二氧化钛、芬顿、臭氧、氯化氨和过硫酸盐降解安赛蜜的机理,并对降解过程中的不利因素和副产物进行了综合分析,确定了紫外光/过硫酸盐是降解安赛蜜较好的方法。
1 安赛蜜的性质和分布
1.1 安赛蜜的性质
安赛蜜是一种由人工合成或通过提取天然物质进行二次加工而成的甜味剂[12]。从化学结构来看,安赛蜜的热和酸稳定性好、难以降解。并且辛醇-水分配系数(logKow)为-1.33,具有较高的溶解度(270 g/L)[12-13]。尽管当前研究表明,每天摄入 15 mg/L 的安赛蜜不会对人体造成危害,但是孕妇食用大量含安赛蜜的食品会导致高血糖、胎儿生长受限[14]。小白鼠服用安赛蜜4周后,它的短期记忆和认知功能、肠道微生物和体重受到严重影响[15]。特别是在自然光照射下,安赛蜜的降解副产物乙酰乙胺更持久、毒性是本身的500倍[16]。此外,安赛蜜与三氯蔗糖、腐殖酸等有机物共存,会加重对藻类生长的抑制作用[17]。然而,与国外相比,我国对安赛蜜及其代谢中间产物的长期毒理性、协同毒理性等方面的研究还有待进一步深入。
1.2 安赛蜜在水环境中的分布
由于安赛蜜具有极性高、结构稳定、难降解等特性,普通的物理方法和生物降解只能使其部分矿化。因此,安赛蜜几乎是以完整的化合物形式从污水厂直接进入水环境中[18]。据报道,欧洲各河流和湖泊中的安赛蜜浓度均在ng/L至μg/L数量级[19-20]。浙江省的地表水中安赛蜜的浓度为0.15~0.85 μg/L[21]。此外,安赛蜜可以通过污水灌溉、管道渗漏、粪肥返田、污泥施肥等方式渗入地下水[22]。Yang等[23]调查了我国华南地区的东江流域,检测到地下水中安赛蜜浓度最高为4 580 ng/L。而加拿大地下水中检测到的安赛蜜浓度超过20 μg/L,远高于我国[20]。越来越多的研究表明,安赛蜜是持久性最强的,在水环境中分布最广的人工甜味剂[24]。
2 紫外光催化氧化技术研究
2.1 紫外光催化氧化技术机理与优势

基于UV衍生的高级氧化技术非常具有潜力。UV辐射可以诱发氧化剂/催化剂发生能级跃迁产生电子-空穴对,从而产生大量氧化活性基团[29]。为了进一步分析UV催化氧化降解安赛蜜的效率,分别介绍 UV与过氧化氢(H2O2)、二氧化钛(TiO2)、芬顿(Fenton)、臭氧(O3)、氯化氨(NH2Cl)和过硫酸盐(PS)等催化剂/氧化剂产生的协同机理。
2.2 单独UV降解
紫外光作为光源,不仅可以起到杀菌消毒的作用,而且具有效率高、预热时间短、成本低等特点[30-31]。安赛蜜暴露在UV的辐射下,基于结构中的发色团在波长<290 nm时的吸收能力,可以吸收光子并激发,产生一系列光物理变化和光化学变化,达到降解的目的。安赛蜜的UV转化产物至少有10个,现已知的包括氨基磺酸、硫酸盐、羟基化的乙酰磺胺和异乙酰磺胺等,其中氨基磺酸、硫酸盐是安全的,但是羟基化的乙酰磺胺和异乙酰磺胺的毒理学并不明确。然而,安赛蜜对UV吸收有限,受pH、安赛蜜初始浓度和UV波长影响较大,并且反应时间较长[32]。因此,单独使用UV降解安赛蜜不适合实际应用。
2.3 UV/H2O2
在UV的辐射下,H2O2中的O—O键断裂,分解生成两个·OH,见式(1),同时·OH的产生又促进了H2O2的二次反应[33]。然而,H2O2的摩尔吸光系数较低,转化率<10%,需要加入高浓度的H2O2才能产生足够多的·OH。为了研究H2O2浓度对安赛蜜的降解速率的影响,在目标污染物溶液中加入不同浓度的H2O2。据研究表明,在pH值为3.0,安赛蜜浓度为30 μmol/L,UV照射时间为120 min的条件下,安赛蜜的去除率随着H2O2的浓度增加而上升,然而上升到一定程度,去除效果不再明显[24]。这是因为过多的H2O2会导致·OH的清除和过氧化氢离子(HO2·)的形成,见式(2)。
因此,当 H2O2的浓度过低时,产生的·OH不足,从而使其对目标物的降解速率较低。当 H2O2的浓度过高时又会发生抑制效应,因为过量的 H2O2与·OH反应生成比·OH活性低的HO2·,进而与目标污染物竞争·OH,见式(3)。
H2O2+UV→ 2HO·
(1)
H2O2+HO·→ HO2·+H2O
(2)
HO·+HO2·→ H2O+O2
(3)
2.4 UV/TiO2

(4)
h++OH-→·OH
(5)
h++H2O →·OH+H+
(6)
UV/TiO2对安赛蜜的水溶液处理60 min后,最大矿化度为57%,总去除率>99%[35]。即使对于安赛蜜废水,UV/TiO2作用30 min也能使其去除率 >84%,在2 h内实现完全光矿化,比单独TiO2催化所需时间更短[36]。此外,有研究表明,当UV照射120 min时,安赛蜜的降解率随TiO2剂量的增加而升高。然而,值得注意的是,TiO2存在量子产率低、缺乏可见光利用率等缺点,为了使安赛蜜的光降解率最大化,需要大量的紫外灯辐射,从而增加了操作成本,限制了UV/TiO2大规模工程应用化[37]。最近,Wang等[24]采用紫外线发光二极管(UV-LED)作为光源,在低pH环境下,UV-LED/TiO2处理 120 min 后,安赛蜜的去除率不仅达到97%,而且有效缩短了预热时间、降低成本低[25]。然而,在UV/TiO2过程中会伴有副产物的生成。当安赛蜜用量为400 mg/L,与TiO2质量比为1∶2时,UV辐射19 h后,极易出现安赛蜜副产物,比母体化合物毒性更强,这种副产物对胚胎发育影响重大[38]。
2.5 UV/Fenton
芬顿法是在酸性条件下,亚铁离子(Fe2+)催化H2O2,使其分解产生·OH与三价铁离子(Fe3+),同时生成的Fe3+和H2O2又还原成Fe2+和氢过氧自由基(·OOH),保证Fe2+的再生,使反应能持续进行,见式(7)、式(8)[39]。
Fe2++H2O2→ Fe3++·OH+OH-
(7)
Fe3++H2O2→ Fe2++H++·OOH
(8)
光芬顿工艺对安赛蜜的降解结果表明,在酸性(pH=3)条件下,UV/H2O2/Fe2+系统产生的·OH实现了安赛蜜的完全降解[7]。但是UV辅助的光芬顿技术对安赛蜜的降解过程非常受pH和H2O2∶Fe2+等因素影响,这是因为芬顿体系需要在酸性的环境下防止Fe3+沉淀。因此,在中性条件下,安赛蜜的去除率<10%[7]。为此,Law等[40]在光芬顿系统中添加氧化还原介体(D,L-巯基琥珀酸),通过加速铁氧化还原循环来强化芬顿体系,以提高中性环境的降解率。然而,光芬顿工艺的运行成本较高、设备复杂,而且反应后溶液中残留的 Fe2+易造成二次污染。因此,使用光芬顿时,需要综合考虑UV与芬顿法的协同作用。
光芬顿降解安赛蜜形成的副产物,取决于光的波长。通过短波UVC、中波UVB以及长波UVA分别辐射,转化物大不相同,但是大部分是无害的。根据Law等[40]的研究分析,UV降解安赛蜜确实会产生有毒副产物,但是UV不是诱导安赛蜜副产物具有毒性的原因,而是由于处理效果不同,光芬顿系统有更高的产·OH率来使有毒副产物转化为无毒的。
2.6 UV/O3

O3联合UV(UV/O3)是污水处理厂应用比较广泛的催化体系。首先,O3的光解产生O·,而后 O·与H2O反应生成·OH(直接促进O3分解),见式(9)、式(10)。其次,O3能够与H2O分子反应生成O2与H2O2,然后H2O2的O—O键断裂,分解生成 2个·OH(间接),见式(11)、式(12)。
直接:
O3+UV → O2+O·
(9)
O·+H2O → 2·OH
(10)
间接:
O3+H2O → O2+H2O2
(11)
H2O2+UV → 2·OH
(12)

2.7 UV/NH2Cl
UV/氯化铵(UV/NH2Cl)是一种新兴的高级氧化工艺,可以产生反应性氯物质(RCS)和·OH去除微污染物。用NH2Cl代替Cl2可以减少消毒副产物(DBP)的形成,例如三卤甲烷。并且NH2Cl本身具有高稳定性,可以起持久的消毒作用。NH2Cl在UV的辐射下,光解生成酰胺基(H2N·)和氯基(Cl·),它们的氧化还原电位分别是0.6 V和 2.7 V。Cl·可以和OH-进一步反应生成强氧化剂自由基·OH,随后解离的ClOH-·与Cl-反应生成其他的RCS。见式(13)~式(15):
NH2Cl+UV → H2N·+Cl·
(13)
Cl·+OH-→·OH+ClOH-·
(14)
ClOH-·+Cl-→ RCS
(15)
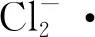
UV/NH2Cl与单独UV降解相比,产生的副产物更多,且大部分带有毒性。归因于处理安赛蜜过程中生成大量有毒氯化副产物(例如卤代醇)。而且安赛蜜会转化生成卤代乙酰胺(HAcAms),据报道,HAA具有潜在的致癌性[44]。
2.8 UV/PS
(16)
(17)
(18)
(19)
经研究表明,UV与PS联用对人工甜味剂表现出显著的去除效果[47]。UV/PDS主要通过氧化、羟基取代、水解和水合4种途径实现对安赛蜜的降解[48]。Fu等[49]通过实验和建模证明UV活化的PDS对污水厂出水中安赛蜜的去除率达 99.93%[48]。Xu等[50]在中性pH条件下,使用 2.520 mmol/L 的PDS,通过 UV的活化作用降解 0.126 mmol/L 的人工甜味剂,60 min后反应体系TOC去除率可高达93%。并且UV/PDS对纯水中安赛蜜的降解速率约是 UV/H2O2的4倍[48,51]。

3 对比分析
总体来说,UV/H2O2、UV/O3、UV/TiO2、光芬顿、UV/NH2Cl以及UV/PS均对安赛蜜有显著的降解作用,但在各自的反应体系中仍存在着缺点。在UV/H2O2体系中,H2O2用量不好把控。在UV/O3体系中,O3容易与水中的溴离子发生反应形成致癌物溴酸盐。在UV/TiO2体系中,TiO2的光生电子产量低,反应转化速率较慢。过多的TiO2会增加溶液浊度,从而降低UV的利用率,而且在一定条件下会生成毒性更强的副产物。在UV/Fenton体系中,受pH值的影响很大,在中性或者碱性水质中,安赛蜜几乎没有被降解。在UV/NH2Cl体系中,过量的NH2Cl会清除自由基,而且反应体系容易生成有毒氯化合物和有毒安赛蜜副产物。

4 未来发展方向
(2)研究表明一些光催化氧化降解安赛蜜的过程中会形成比母体化合物更持久、毒性更强的中间产物或副产物,因此需要综合评估光催化氧化副产物对生态环境的毒理性。
(3)目前,光催化氧化对安赛蜜的研究多集中在单一物质方面,而对实际污水的研究相对较少,有必要研究污水中有机物、无机物等对光催化降解安赛蜜的协同/抑制机理进行深入研究。
5 结论

——人-时间资料率比分析与SAS实现

