气相色谱法测定食用林产品有机磷农药残留基质效应研究
邬能英黄安香王忠伟柏文恋罗国波张福安
(1.贵州省林业科学研究院,贵州 贵阳 550000;2.贵州一航生态农牧科技开发有限公司,贵州 铜仁 565100)
食用林产品是指依托于森林、林木、林地生产以及经过初级加工,可供人类直接或间接食用的植物、菌类和其制成品等[1]。随着我国食用林产品市场需求量不断增加,人工种植的食用林产品大量涌现,如竹笋、花椒、刺梨、核桃和油茶等。在种植生产食用林产品的过程中,为了避免病虫害及提高产量和质量,人们大量使用农药,很多农药属于剧毒物,滥用导致农药残留量超标,从而影响食用林产品的质量安全,进一步危害人的身体健康[2],农药残留的精准测定及控制成为食品安全最重要的工作。
近年来,农药检测分析残留技术发展迅猛,气相色谱法[3]、液相色谱-串联质谱法[4]及气相质谱法[5]等检测手段也发展相对成熟,然而食用林产品品种繁多,基质干扰效应带来的假阳性结果给检测工作带来一定的难度。如何避免基质效应的干扰,成为提高检测准确率的重要手段。基质的复杂性常对分析物的分析过程有显著的干扰,从而影响分析结果的准确性,这种现象称为基质效应[6]。根据基质对检测信号响应值的不同影响,可将其分为基质增强效应和基质减弱效应。关于基质效应的产生机理目前尚未清楚,黄宝勇[7]等认为,产生基质效应与待测物的化学结构与性质、样品基质的种类和浓度、待测物在样品基质中的浓度、检测器和接口类型以及进样技术等因素有关。易盛国等[8]研究结果表明,基质含水量越多,基质效应越弱,含糖类、油脂和蛋白质越多,基质效应越强。基质效应普遍存在于气相色谱、液相色谱和质谱联用等农药残留分析过程中,是影响分析结果准确性的一种主要因素[9,10]。目前在水果和蔬菜等样品的农药残留基质效应研究较多[11],对食用林产品如刺梨、竹笋、核桃等的农药残留检测基质效应少有报道。因此,本文采用气相色谱法分析了11种有机磷农药在刺梨、竹笋、核桃、花椒和油茶的基质效应,希望为食用林产品有机磷农药残留检测提供参考,提高检测结果的准确性。
1 材料与方法
1.1 试剂与材料
标准品甲基对硫磷(C8H10O5NPS)、杀螟硫磷(C9H12NO5PS)、乐果(C5H12NO3PS2)、倍硫磷(C10H15O3PS2)、乙酰甲胺磷(C4H10NO3PS)、氧乐果(C5H12NO4PS)、二嗪磷(C4H4N2O)、杀扑磷(C6H11N2O4PS3)、伏杀硫磷(C12H15ClNO4PS2)、马拉硫磷(C10H19O6PS2)、甲基嘧啶磷(C11H20N3O3PS)标准溶液浓度均为1000μg·mL-1(天津农业农村部环境质量监督检测测试中心);丙酮(CH3COCH3,色谱纯)和乙腈(C2H3N,色谱纯,美国Sigma-Aldrich);氯化钠(NaCl,分析纯)。竹笋、花椒、刺梨、核桃和油茶样品均采于成熟期。
1.2 仪器与设备
Agilent-8890气相色谱仪,色谱柱包括DB-1701(长度30m、内径0.250mm、膜厚1.00μm)和DB-1(长度30m、内径0.250mm、膜厚0.25μm)(Agilent中国有限公司);ME802/02型电子天平在(梅特勒-多利多仪器上海有限公司);KQ2200E型超声清洗器(昆山市超声仪器有限公司);XW-80A型漩涡混合器(上海精科实业有限公司);N-EVAP 112型氮吹仪(青岛陆零玖环保科技有限公司);T25 ECD SO25型匀浆机(上海书培实验设备有限公司)。
1.3 气相色谱条件
升温程序为150℃保持2min,以8℃·min-1速度升至250℃,并保持14min,运行时间28.5min;进样口温度220℃,不分流方式进样,进样量为1μL,检测器温度300℃,载气(氮气)流速60mL·min-1,燃气(氢气)流速75mL·min-1,助燃气(空气)流速100mL·min-1,色谱柱型号为DB-17和DB-1。
1.4 空白基质的提取
5种不同食用林产品样品的空白基质提取具体如下。称取25.0g粉碎样品于100mL烧杯中(刺梨、核桃和油茶先加10mL水,其余步骤相同),加入50mL乙腈,用匀浆机匀浆(2000rpm,2min),将匀浆好的溶液用滤纸过滤,滤液全部收集到装有4g氯化钠的100mL具塞量筒中,盖上塞子,剧烈振荡2min,于室温中静置30min,使水相和乙腈相充分分层。取上层乙腈溶液10mL于100mL烧杯中,将烧杯放在50℃的氮吹仪上,并将氮气缓缓通入烧杯内,吹近干,加入2mL丙酮,并将其放入超声清洗器中超声3min。将超声之后的溶液全部转移到10mL刻度离心管中,用丙酮洗涤烧杯3次(每次1mL)并将洗涤液全部转入离心管中,定容至5mL,在旋涡混合器上涡旋0.5min,用0.2μm滤膜过滤,上机检测样品,未检出图1中所列的11种农药,则该样品称为干净样品,并将此次提取的样品溶液作为基质实验所用溶剂。
1.5 储备液的配制
11种有机磷农药分别为甲基对硫磷、杀螟硫磷、乐果、倍硫磷、乙酰甲胺磷、氧乐果、杀扑磷、二嗪磷、伏杀硫磷、马拉硫磷和甲基嘧啶磷,溶液原始浓度均为1000μg·mL-1。逐级稀释成浓度为10μg·mL-1的标准储备液,后续根据实验要求配制成所需要的工作溶液。
1.6 实验设计
用色谱级的丙酮作为溶剂所配制的标液,称之为溶剂标液。分别用竹笋、花椒、刺梨、核桃和油茶的空白基质(上机检测,样品中甲基对硫磷、杀螟硫磷、乐果等11种有机磷农药残留均未检出)作溶剂所配制的标液,称之为基质标液。溶剂标液和基质标液的质量浓度相同,且采用同一标准储备液进行配制。乙酰甲胺磷、氧乐果、杀扑磷、二嗪磷、马拉硫磷、伏杀硫磷、甲基嘧啶磷、杀螟硫磷、甲基对硫磷、乐果和倍硫磷标准曲线质量浓度分别为0.1μg·mL-1、0.2μg·mL-1、0.4μg·mL-1、0.6μg·mL-1、0.8μg·mL-1、1.0μg·mL-1和2.0μg·mL-1,使用GC-FPD进行检测,伏杀硫磷所用色谱柱为DB-1,其余农药指标所用色谱柱均为DB-17。添加回收试验:准确称取25.0g剁碎的样品,加入1mL 10μg·mL-1的农药标准品溶液,按照1.3中方法进行处理,添加水平重复5次,并用GC-FPD检测,计算回收率和相对标准偏差。
1.7 基质效应的计算
本文的基质效应(Marix Effects,ME)计算公式[9]:
式中,A表示基质标准曲线斜率;B表示溶剂标准曲线斜率;当ME﹥0时,表示基质对待测物有基质增强效应;当ME﹤0时,为基质减弱效应;-20%≤ME≤20%,可认为该基质没有基质效应;若其值在20%~50%,则表明该基质有中等基质效应;若超过-50%或50%,则表明基质效应很强。
2 结果分析
2.1 11种有机磷类农药的气相色谱图
11种有机磷农药标准品气相色谱图如图1所示,按照1.3气相色谱条件检测,其出峰时间分别为乙酰甲胺磷10.158min、氧乐果12.446min、甲基对硫磷15.418min、杀螟硫磷15.927min、杀扑磷18.969min、伏杀硫磷14.146min、二嗪磷12.157min、甲基嘧啶磷14.404min、马拉硫磷15.472min、乐果14.126min和倍硫磷15.627min。检测伏杀硫磷的色谱柱为DB-1,其余10种农药指标用的色谱柱为DB-17,乙酰甲胺磷和甲基对硫磷为一对混标,氧乐果和杀扑磷为一对混标,其余都为单标,进样量均为1μL 0.2μg·mL-1的标准溶液。
2.2 基质效应分析
2.2.1 竹笋中农药残留基质效应
竹笋中5种农药的基质效应实验数据如表1所示。甲基对硫磷(Parathion-methyl)、乙酰甲胺磷(Acephate)、杀螟硫磷(Fenitrothion)、氧乐果(Omethoate)和杀扑磷(Methidathion)在竹笋基质中的基质效应分别为-19.60%、-15.01%、4.981%、18.63%和2.530%,其中,甲基对硫磷和乙酰甲胺磷为基质减弱效应,其余,3种农药为基质增强效应。据文献报道[12],当基质效应均落在20%≤ME≤20%范围内时,可认为该基质没有基质效应,可用标准曲线进行定量分析。这与易盛国[12]等的研究结果比较相一致,样品含水量越高,基质效应越弱,这是由于越多的水分可以在一定程度上稀释基质共萃物的浓度,从而使基质效应降低。
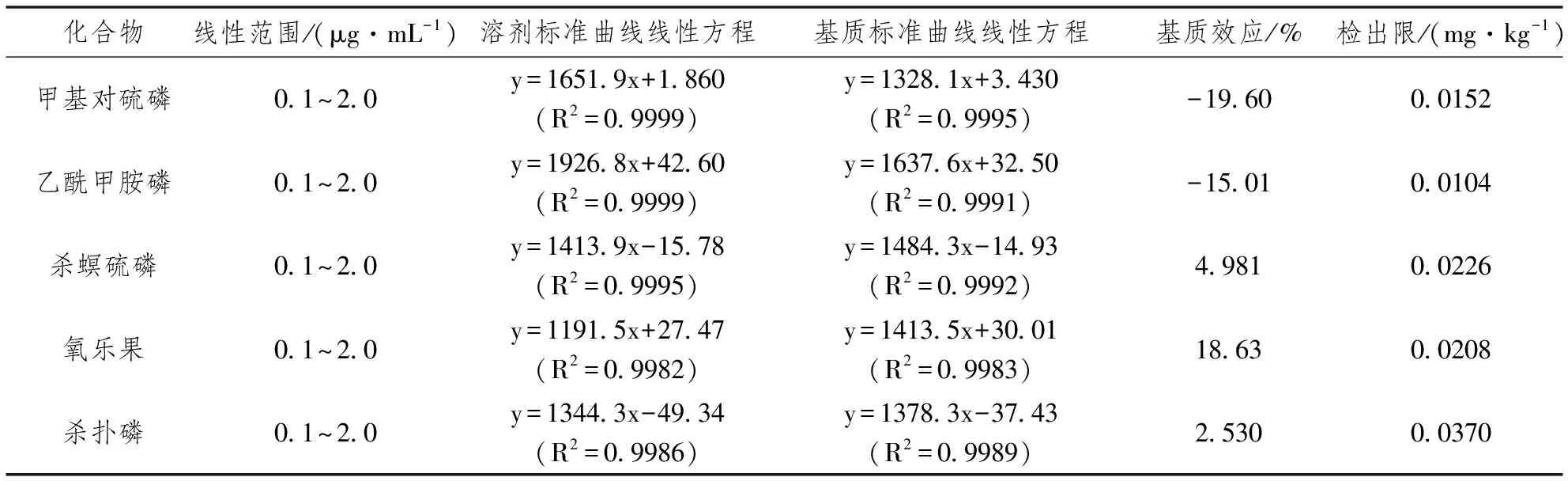
表1 5种农药在溶剂与竹笋基质溶液中的线性范围、标准曲线、相关系数、基质效应和检出限
2.2.2 花椒中农药残留基质效应
花椒中5种农药的基质效应实验数据如表2所示,乙酰甲胺磷(Acephate)、二嗪磷(Diazinon)、马拉硫磷(Malathion)、伏杀硫磷(Phosalone)和甲基嘧啶磷(Pirimiphos-methyl)在花椒基质中的基质效应分别为-22.36%、11.90%、16.32%、10.01%、-1.368%,其中,乙酰甲胺磷和甲基嘧啶磷为基质减弱效应;其余3种农药为基质增强效应。由于乙酰甲胺磷基质效应落在-50%~20%,则表现为中等程度的基质干扰效应,因此花椒样品采取基质加标进行定量检测,以减少基质效应对检测结果的干扰[13]。
2.2.3 刺梨、核桃和油茶中农药残留基质效应

表2 5种农药在溶剂与花椒基质溶液中的线性范围、标准曲线、相关系数、基质效应和检出限
刺梨、核桃和油茶中7种农药的基质效应实验数据如表3所示,甲基对硫磷(Parathion-methyl)、杀螟硫磷(Fenitrothion)和乐果(Dimethoate)在刺梨基质中基质效应分别为65.30%、80.32%和60.31%;二嗪磷(Diazinon)和伏杀硫磷(Phosalone)在核桃基质中的基质效应分别为53.27%和32.56%;倍硫磷(Fenthion)和乐果(Dimethoate)在油茶基质中的基质效应分别为81.32%和80.10%。伏杀硫磷在核桃基质中的基质效应为32.56%,在20%~50%,则表现为中等基质效应,其余基质效应均>50%,则表现为强基质效应。这与Gillespie[14]和易盛国[8]等的研究结果相类似,对于糖类(刺梨)、油脂(油茶、核桃)和蛋白质(核桃)含量越高的样品,基质效应越强,这是由于糖类、油脂和蛋白质属于不易挥发性物质,此类物质容易富集在进样口的活性位点并占据活性位点,从而减少农药的吸附量。因此,稀释样液浓度及采取基质加标进行定量检测,以减少基质效应对检测结果的干扰。
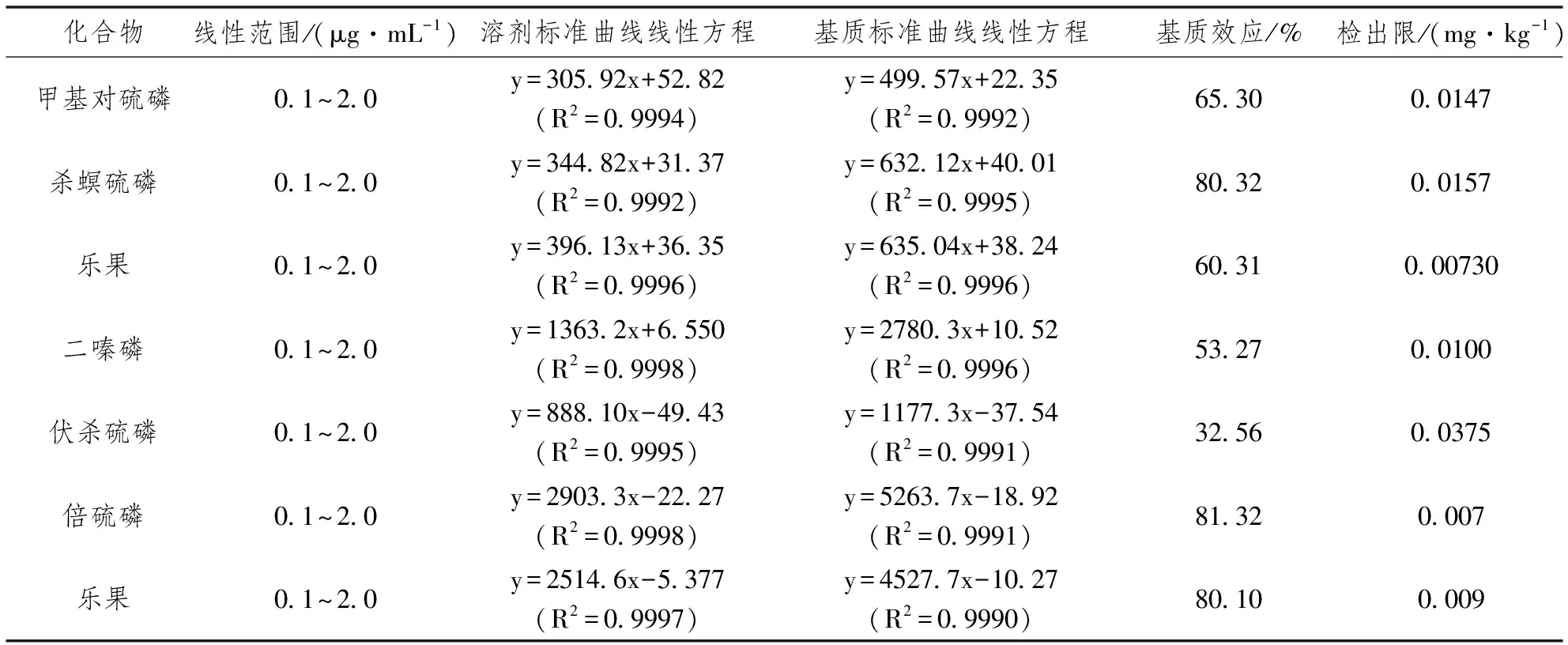
表3 7种农药在溶剂与刺梨、核桃和油茶基质溶液中的线性范围、标准曲线、相关系数、基质效应和检出限
2.3 方法学验证
2.3.1 线性范围和检出限
以基质标液质量浓度0.1μg·mL-1、0.2μg·mL-1、0.4μg·mL-1、0.6μg·mL-1、0.8μg·mL-1、1.0μg·mL-1和2.0μg·mL-1进行测定,每个浓度测定3次,峰面积取平均值,以质量浓度为横坐标,峰面积为纵坐标绘制标准曲线。结果表明,所测的11种有机磷类农药,在各自样品基质中均呈良好线性关系,线性相关系数(R2)均>0.998。11个农药化合物检出限范围为0.007~0.0375mg·kg-1。11种有机磷类农药的线性范围、标准曲线线性方程、线性相关系数和检出限见表1~3,以信噪比S/N=3确定检出限。
2.3.2 回收率与相对标准偏差
采用空白基质(核桃、刺梨、油茶、竹笋和花椒)进行添加回收实验,实验结果如图2所示。图2a表示二嗪磷和伏杀硫磷在空白核桃基质中的平均回收率,平均回收率为105.7%~106.3%,相对标准偏差为2.1%~3.5%;图2b表示甲基对硫磷、乐果和杀螟硫磷在空白刺梨基质中的回收率,平均回收率为82.9%~88.0%,相对标准偏差为1.0%~1.4%;图2c表示乐果和倍硫磷在空白油茶基质中的平均回收率,平均回收率为105.3%~107.0%,相对标准偏差为1.0%~1.5%;图2d表示乙酰甲胺磷、二嗪磷、甲基嘧啶磷、马拉硫磷和伏杀硫磷在空白花椒基质中的平均回收率,平均回收率为78.2%~105.0%,相对标准偏差为1.0%~1.8%;图2e表示甲基对硫磷、氧乐果、杀螟硫磷、杀扑磷和乙酰甲胺磷在空白竹笋基质中的平均回收率,平均回收率为82.1%~103.0%,相对标准偏差为1.0%~1.7%。即11种有机磷类农药在食用林产品空白基质中的平均回收率为78.2%~107.0%,相对标准偏差为1.0%~3.5%。按照残留准则回收率在70%~110%允许范围内,相对标准偏差≤15%,同时,这与Gillespie[14]等在研究高脂肪含量样品,使用含样品基质的标准溶液校正后回收率在103%左右相类似,故该方法满足分析要求。
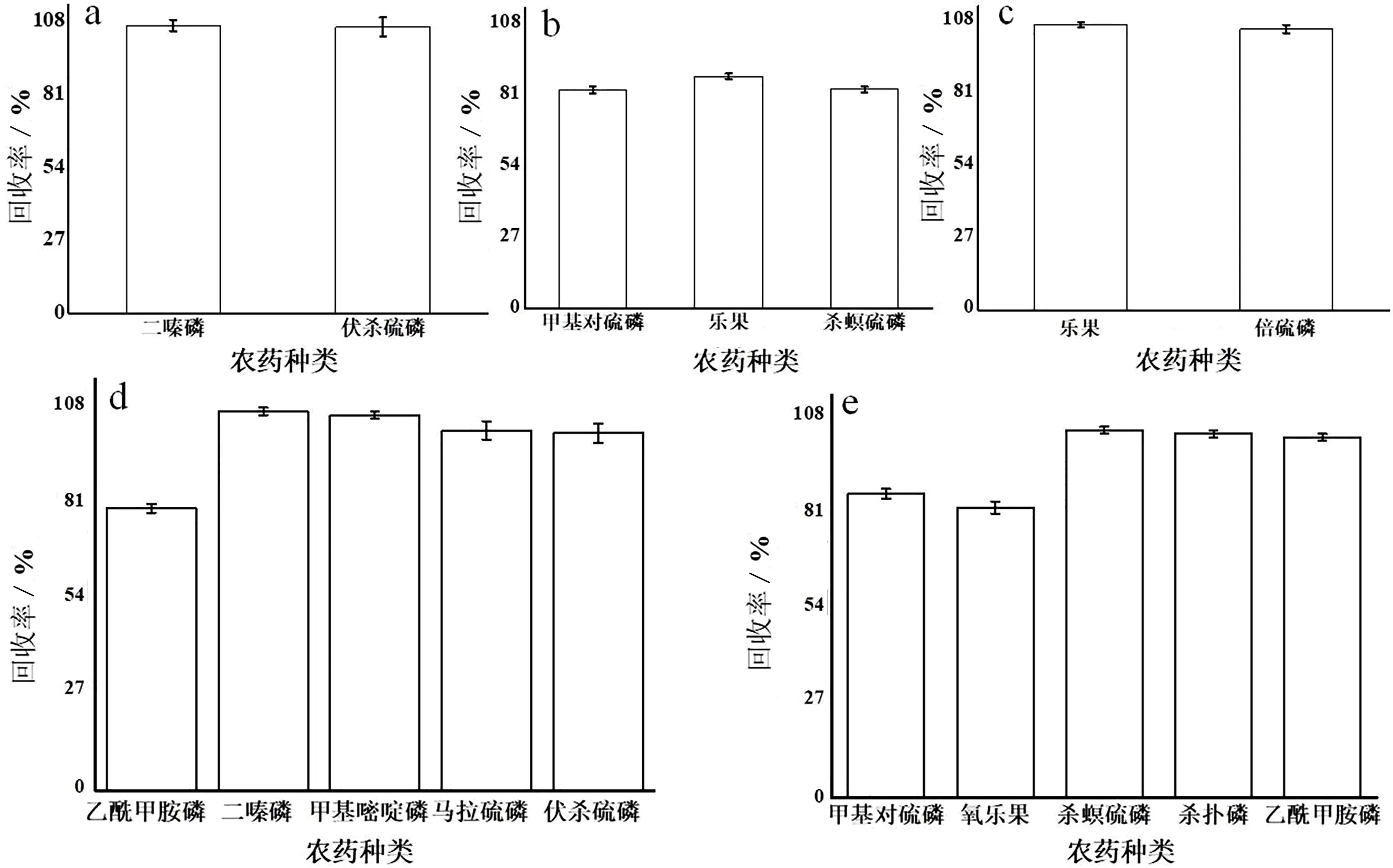
图2 11种有机磷类农药在不同基质中的回收率柱状图
2.4 实际样品的检测
采用本方法对成熟期的85批次竹笋、80批次花椒、55批次刺梨、93批次核桃和91批次油茶中农药残留进行了检测,共检出农药1种。其中,刺梨、核桃和油茶均未检出相对应的农药,竹笋样品中检出乙酰甲胺磷,含量范围为0.001~0.1mg·kg-1;花椒样品中检出乙酰甲胺磷,含量范围为0.015~0.045mg·kg-1。实验结果可知,两者均未超过我国的最大残留限量标准(GB-2763-2019)。
3 讨论
Zrostlikova J[15]等研究总结含有以下基团或特征结构的化合物常常表现出较强的基质效应:P=O、-O-CO-NH、-OH、-N=和-NH-CO-NH-等,如乙酰甲胺磷、氧乐果和马拉氧磷等,其中农药极性越强越容易产生基质效应。有机磷类农药大部分含有P=O或P=S基团,这些基团属于极性基团,共轭给电子,使得极性变大,存在此类基团的农药更容易被进样口活性位点所吸附,从而在气相色谱分析中引起较强的基质效应[16]。
4 结论
本研究选择了5种代表性的食用林产品,通过基质加标的方法消除基质效应,并用气相色谱法测定食用林产品中的11种农药残留。在0.1~2.0μg·mL-1范围内线性良好,检出限为0.007~0.0375mg·kg-1。该方法定量准确、灵敏度高、前处理简单且方法自动化程度高,适用于食用林产品农药残留定性分析,为提高有机磷农药在食用林产品中的残留检测准确性提供一定实际的参考价值。

