不同梗死相关动脉完全闭塞的非ST段抬高型心肌梗死患者临床特征分析
肖文颖,汪宇,张佳雨,史骏,刘新兵,冯六六
随着急性心肌梗死诊疗手段的进步,越来越多的患者得以在心肌梗死急性期接受及时的再灌注治疗。研究显示,2017年ST段抬高型心肌梗死(ST segment elevation myocardial infarction,STEMI)患者中接受直接经皮冠状动脉介入术(percutaneous coronary intervention,PCI)者占比为42.2%,较2016年(38.9%)进一步提升,且PCI后患者死亡率稳定在较低水平(0.23%)[1]。与STEMI患者相比,非ST段抬高型心肌梗死(non-ST elevated myocardial infarction,NSTEMI)患者由于缺乏特异性心电图改变,临床症状不典型,其早期介入时机的选择常受到影响。目前认为NSTEMI的病理机制主要是动脉粥样硬化斑块破裂引起非闭塞性冠状动脉血栓形成[2],其梗死相关动脉(infarct-related artery,IRA)并未完全闭塞[3]。但随着对IRA认识的不断深入,研究发现,34%的NSTEMI患者存在IRA完全闭塞[4],且此类患者的预后与STEMI患者相似,但其临床前驱症状常不典型。本研究旨在分析不同IRA完全闭塞的NSTEMI患者前驱症状、心电图、冠状动脉造影(coronary arteriography,CAG)的特点,以期更早、更好地识别此类患者,尽早开通闭塞血管,改善患者预后。
1 对象与方法
1.1 研究对象 选取2018年3月至2021年3月入住上海市杨浦区市东医院心脏重症监护室(Coronary Care Unit,CCU)并经24 h内CAG证实IRA完全闭塞的NSTEMI患者79例为研究对象。纳入标准:(1)符合《第4版心肌梗死全球统一定义(2018)》[5]中NSTEMI的诊断标准:①缺血性胸痛持续时间≥30 min;②血清心肌肌钙蛋白(cardiac troponin,cTn)水平高于参考值上限第99百分位值,且cTn有上升和/或下降的动态变化;③心电图上并未出现ST段抬高,仅表现为ST段压低和/或T波倒置。(2)IRA符合以下中的1项:病变可以解释心电图演变,局部有新鲜血栓影,干预后症状明显缓解。排除标准:梗死后心绞痛、瓣膜病或心肌病、急性心包炎、脑血管出血性疾病等。本研究经上海市杨浦区市东医院伦理委员会审批通过,且所有患者签署了知情同意书。
1.2 研究方法
1.2.1 一般资料收集 收集患者一般资料,包括年龄、性别、吸烟史(一生中连续或累积吸烟6个月或以上定义为吸烟)、高血压史、糖尿病史、PCI史。
1.2.2 前驱症状收集 收集患者前驱症状,包括典型胸痛和非典型胸痛,后者包括气促、头晕、晕厥、消化道症状等。
1.2.3 心电图检查 所有患者入院后10 min内完成首份心电图(十八导联)检查,记录新出现的病理性Q波、ST段偏移、T波倒置、完全性左束支传导阻滞(complete left bundle branch block,CLBBB)发生情况。
1.2.4 CAG检查 所有患者入院24 h内经股动脉或桡动脉途径完成CAG检查。由经验丰富的固定介入团队分析CAG检查的影像资料。统计患者三支病变发生率、病变位置、右冠状动脉(right coronary artery,RCA)优势型发生情况及侧支循环情况。结合冠状动脉解剖学特点,将病变位置分为近段、中段和远段。大部分心肌血供来源于RCA判断为RCA优势型。采用Rentrop分级(0~3级)评价侧支循环形成情况,0级为无侧支循环,1、2、3级为存在侧支循环,其中2、3级为侧支循环良好。根据患者IRA,将其分为RCA组(33例)、左回旋支(left circumflex artery,LCX)组(26例)和左前降支(left anterior descending branch,LAD)组(20例)。
1.3 统计学方法 使用SPSS 21.0统计学软件进行数据处理。计量资料以(±s)表示,多组间比较采用单因素方差分析,组间两两比较采用LSD-t检验;计数资料以相对数表示,组间比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 一般资料 三组年龄、性别及有吸烟史、高血压史、糖尿病史、PCI史者所占比例比较,差异无统计学意义(P>0.05),见表1。
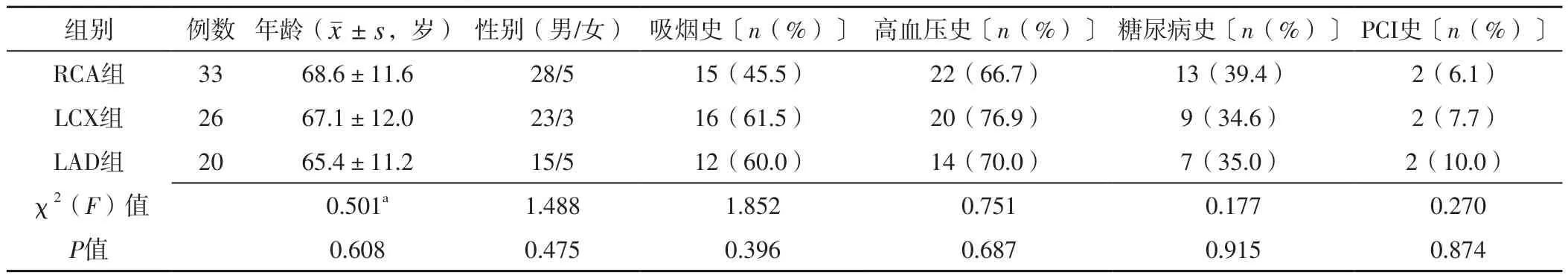
表1 三组一般资料比较Table 1 Comparison of general data among the three groups
2.2 前驱症状 三组前驱症状比较,差异无统计学意义(χ2=0.003,P=0.998),见表2。
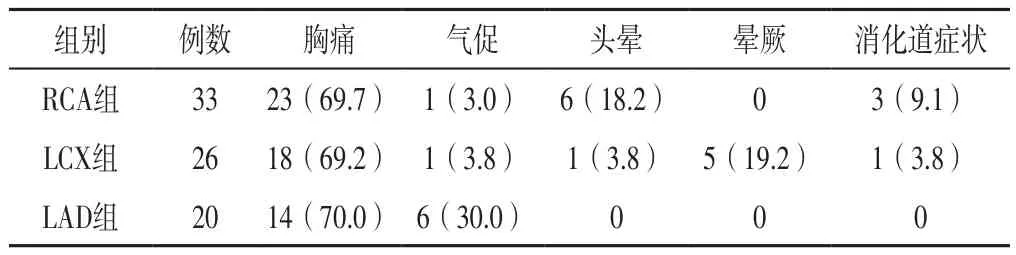
表2 三组前驱症状比较〔n(%)〕Table 2 Comparison of prodromal symptoms among the three groups
2.3 心电图检查结果 三组新出现的病理性Q波、ST段偏移、T波倒置、CLBBB发生率比较,差异无统计学意义(P>0.05),见表3。
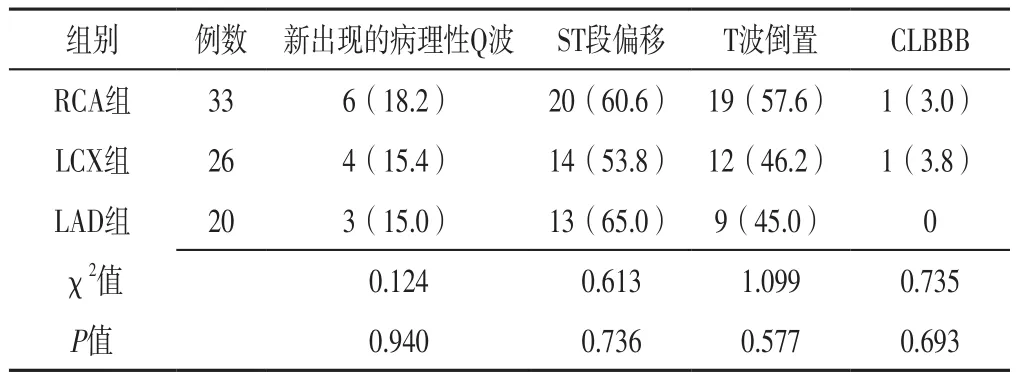
表3 三组心电图检查结果比较〔n(%)〕Table 3 Comparison of ECG results among the three groups
2.4 CAG检查结果 三组三支病变、RCA优势型发生率比较,差异无统计学意义(P>0.05);三组病变位置、侧支循环良好率比较,差异有统计学意义(P<0.05)。LCX组侧支循环良好率低于RCA组,差异有统计学意义(P<0.05);LAD组病变位置为近段者所占比例高于LCX组,病变位置为远段者所占比例低于LCX组,差异有统计学意义(P<0.05),见表4。
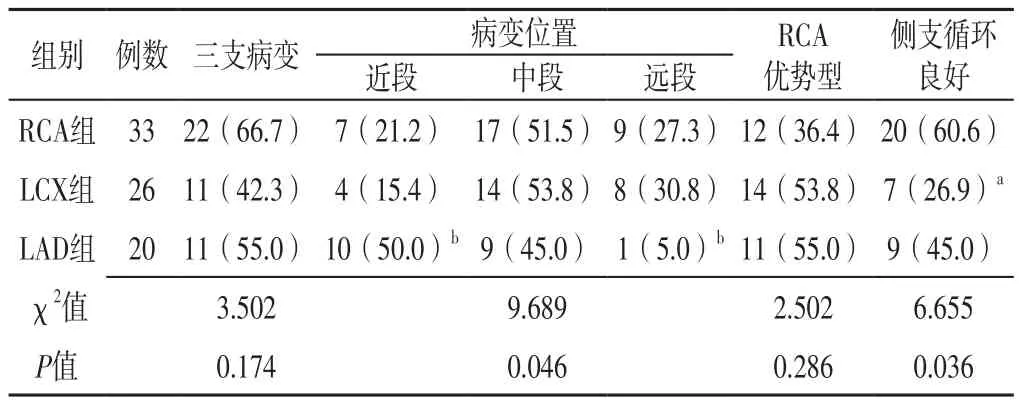
表4 三组CAG检查结果比较〔n(%)〕Table 4 Comparison of CAG results among the three groups
2.5 非典型胸痛患者病变位置 前驱症状为气促的患者多见于LAD近段完全闭塞,前驱症状为头晕的患者多见于RCA近段完全闭塞,前驱症状为晕厥的患者均见于LCX完全闭塞,前驱症状为消化道症状的患者多见于RCA远段完全闭塞,见表5。
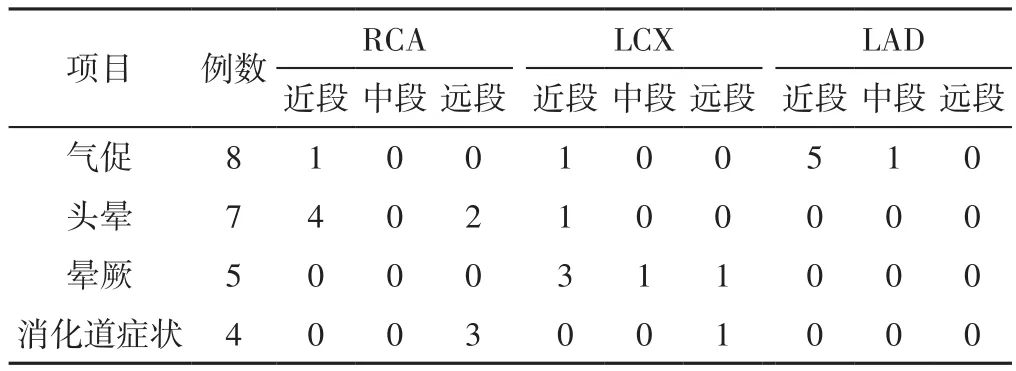
表5 非典型胸痛患者病变位置(例)Table 5 Lesion location in patients with atypical chest pain
3 讨论
调查显示,NSTEMI患者占心肌梗死患者的比例不断增加,从1995年的1/3升高到2015年的1/2以上,由于早期血管造影的应用(从9%增加到60%)和首次住院期间PCI比例的增加(从12.5%增加到67.0%),使得NSTEMI患者6个月死亡率明显降低(从17.2%降至6.3%)[6]。但研究发现,与STEMI患者相比,NSTEMI患者的远期预后更差[7]。与IRA未完全闭塞的NSTEMI患者相比,IRA完全闭塞的NSTEMI患者的不良心血管事件发生率及死亡率更高[8]。本研究旨在分析不同IRA完全闭塞NSTEMI患者前驱症状、心电图、CAG的特点。
既往临床实践显示,CAG检查显示IRA已完全闭塞,但心电图检查未见ST段抬高的情况并不少见,这在LAD、LCX和RCA中均可出现,其中LCX发生率更高[6]。本研究79例IRA完全闭塞的NSTEMI患者中,RCA、LCX、LAD完全闭塞者分别占41.8%(33/79)、32.9%(26/79)、25.3%(20/79),与上述研究结果不同,提示在关注LCX完全闭塞的同时,也需要早期识别RCA、LAD完全闭塞。
本研究结果显示,三组新出现的病理性Q波、ST段偏移、T波倒置、CLBBB发生率比较无统计学差异,提示不同IRA完全闭塞NSTEMI患者的心电图改变仍缺乏明显的特异性。究其原因,本研究样本量较小,心电图资料收集的尚不够全面及细化,此外,心电图改变可能受到闭塞血管直径、血供范围、侧支循环及心室传导阻滞等多种因素影响。但也有研究显示,ST段下移的深度(是否≥1 mm)及ST段压低导联数(是否>6个)可反映病变狭窄程度,受损范围越大,ST段压低越多,ST段压低导联数越多[9]。VIVES-BORRÁS等[10]研究发现,由于侧支循环不同,LCX近端闭塞多表现为STEMI,远段闭塞多表现为ST段压低,而在ST段无变化患者中钝缘支闭塞所占比例较高。左束支主要由前降支室间隔支供血,小部分接受右冠状动脉后降支供血。研究发现,合并左束支阻滞的心肌梗死患者中IRA绝大部分位于LAD近中段[11]。在临床实践中,IRA完全闭塞的NSTEMI患者由于缺乏特征性的临床表现及ECG特征,极易被临床医师忽视,延误最佳再灌注治疗时机。因此,还需要积累更多的临床经验,以期探索对IRA完全闭塞的NSTEMI具有较高灵敏度和特异度的ECG指标,并早期确诊IRA完全闭塞的NSTEMI患者。
既往研究发现,NSTEMI患者常合并糖尿病、高血压、高脂血症等疾病,以多支血管病变为主,长期预后差[12]。本研究结果显示,三组三支病变发生率比较无统计学差异,但均>40%,提示IRA完全闭塞的NSTEMI患者的血管条件较差,需要引起足够的重视。闭塞位置与患者病情严重程度和预后密切相关。本研究结果显示,RCA组、LCX组病变位置主要为中段,LAD组病变位置主要为近段,提示IRA完全闭塞的常见部位可能为非远段,故患者缺血心肌的面积较大,从而影响预后。本研究结果还显示,LAD组病变位置为近段者所占比例高于LCX组,病变位置为远段者所占比例低于LCX组,造成此差异的原因可能为侧支循环代偿不同。研究显示,NSTEMI患者侧支循环形成率明显高于STEMI患者,其机制可能与病变血管的固定狭窄较重、管腔内血流缓慢且压力低,利于侧支循环建立与开放有关[6]。本研究结果显示,LCX组侧支循环良好率低于RCA组,提示LCX完全闭塞的患者病情较为凶险。亦有研究显示,与RCA完全闭塞患者相比,LCX完全闭塞患者的心肌梗死面积更大,左心室功能异常率更高[13]。
老年人合并高血压、糖尿病、高脂血症的发生率及有PCI史者占比较高,随着我国二级预防策略的深入开展,血管紧张素转换酶抑制剂/血管紧张素受体阻滞剂、β-受体阻滞剂、钙通道阻滞剂、抗血小板药物等的广泛使用可能会减少NSTEMI患者中典型胸痛症状者占比,而非典型胸痛症状者占比不断增多。目前,非典型胸痛症状与闭塞部位之间的关系尚缺乏相关研究。本研究结果显示,三组前驱症状比较无统计学差异,且RCA组、LCX组、LAD组中分别有30.3%、30.8%、30.0%患者的前驱症状为非典型胸痛,提示有相当部分的NSTEMI患者容易被漏诊,延误首次心肌酶和心电图检测时间,直接影响预后。
本研究结果显示,前驱症状为气促的患者多见于LAD近段完全闭塞,分析原因,LAD沿右心室-左心室的室间隔上(前室间沟)走行,绕心尖切迹后到后室间沟,供应心肌为心脏前壁、左心室前侧壁、室间隔前2/3,供血面积大,当其发生闭塞时,心脏舒缩力明显减小或不协调,左心室泵血功能明显受损,出现气促、呼吸困难等表现,当左心室舒张期末压继续增高,肺毛细血管平均压超过25 mm Hg(1 mm Hg=0.133 kPa),渗出血管外的液体在肺间质蓄积,进而外渗到肺泡内,形成肺水肿,因而临床上以急性左心衰竭为主要表现的心肌梗死患者不占少数[10]。
本研究结果显示,前驱症状为头晕的患者多见于RCA近段完全闭塞,分析原因,RCA供应的心肌包括右心室,当其发生闭塞时,尤其是近中段,可引起右心室梗死,右心室收缩功能的锐减易导致左心室回心血量减少,左心室充盈不足,引起心排血量降低,大脑灌注不足,从而出现头晕等症状。
心源性晕厥是由于心排血量突然降低引起急性脑缺血发作而诱发的晕厥。急性心肌梗死患者由于梗死区心肌电生理呈不均一改变,电活动极不稳定,易产生恶性心律失常,如室性心动过速、心室颤动等,并且Bezold-Jarish反射可引起严重的窦性心动过缓或高度房室传导阻滞,导致血压下降,从而引起晕厥。本研究结果显示,前驱症状为晕厥的患者均见于LCX完全闭塞,分析其原因:首先,根据冠状动脉的走行特点,LCX参与了左心室心肌侧壁、后壁和下壁的供血,当LCX发生闭塞时,血供不足,左心室功能严重受损,心排血量随之下降,进而引发晕厥。其次,窦房结动脉可以起源于RCA主干,也可以起源于LCX[14]。本研究中LCX病变位置主要为中段,不能排除患者闭塞区累及窦房结动脉,从而出现缓慢型心律失常,诱发晕厥。
本研究结果显示,前驱症状为消化道症状的患者多见于RCA远段完全闭塞,分析其可能的原因有:冠状动脉走行和迷走神经分布。RCA沿右心房-右心室的房室沟入心脏后部,走行于后室间沟附近的为房室结支和后降支,即RCA远段供应心脏后部心肌。此外,RCA供应的心肌包括右心室、左心室下壁、左心室后壁、室间隔后1/3[15]。RCA远段发生闭塞时,所支配的心肌缺血缺氧,心排血量减少,脏器灌注不足,造成胃肠道循环紊乱,甚至合并肠系膜栓塞,从而产生腹痛等症状。迷走神经传入纤维感受器多分布在心脏下壁表面,该区域心肌梗死时,心肌细胞释放酸性代谢产物,刺激神经末梢感受器并传至中枢神经系统的网状结构,最后通过传出神经协调运动引起恶心、呕吐等症状。另外,心脏下壁靠近膈肌,坏死物质可刺激膈神经,诱发膈肌痉挛,也会产生消化道症状。
综上所述,不同IRA完全闭塞的NSTEMI患者前驱症状均以典型胸痛为主,但前驱症状为气促的患者多见于LAD近段完全闭塞,前驱症状为头晕的患者多见于RCA近段完全闭塞,前驱症状为晕厥的患者均见于LCX完全闭塞,前驱症状为消化道症状的患者多见于RCA远段完全闭塞;不同IRA完全闭塞NSTEMI患者心电图检查结果无特异性;LCX完全闭塞NSTEMI患者CAG检查结果较差,其病情可能较为凶险。但本研究样本量较小,尤其是前驱症状为非典型胸痛患者非常少,选择偏倚可能较大,代表性有限,且对患者心电图资料收集的不够全面、充分,后续应扩大样本量以进一步验证本研究结论。
作者贡献:肖文颖进行文章的构思与设计、文章的可行性分析,文献/资料收集、整理,撰写论文;张佳雨、史骏、刘新兵、冯六六进行资料收集、整理;肖文颖、汪宇进行论文的修订,负责文章的质量控制与审校,对文章整体负责、监督管理。
本文无利益冲突。

