1株副猪嗜血杆菌血清4型的分离鉴定及耐药性分析
王同兆,张付贤,雷连成,2
(1.长江大学动物科学学院,荆州 434023;2.吉林大学动物医学学院,长春 130062)
副猪嗜血杆菌病是由副猪嗜血杆菌(Haemophilusparasuis,Hps)引发的、以猪多发性纤维素性浆膜炎和关节炎为特征的全身感染性疾病,严重危害仔猪和青年猪的健康。Hps是一种条件致病菌,广泛存在于猪的上呼吸道[1],在猪遭受饲养管理不当、天气变化、长途运输等应激条件时易引起发病。此外,当猪感染其他疾病导致免疫力减退时,也易引起Hps感染,特别是在免疫抑制性疾病的作用下,导致猪群高发病率和高死亡率[2-3]。
已发现的Hps有15种血清型,其中血清1、2、3、4、5、8、10、12、13、14和15型具有较强的致病性,而血清4和5型在中国最流行[4]。Hps不同血清型或不同菌株间交叉保护力低,有明显的地方特异性,不同地区分离的相同血清型菌株的毒力和抗原性可能不同[5]。由于临床上滥用抗生素预防和治疗副猪嗜血杆菌病,导致中国大部分省市Hps产生耐药性[6]。目前,国内外对Hps的报道越来越多,呈急骤上升趋势。Hps单独感染可导致猪群发病,临床上发现其与多种细菌如多杀性巴氏杆菌(Pasteurellamultocida,Pm)、猪链球菌(Streptococcussuis,SS)、胸膜肺炎放线杆菌(Actinobacilluspleuropneumoniae,APP)等,与多种致病性病毒如猪圆环病毒2型(Porcine circovirus type 2,PCV2)、猪繁殖与呼吸综合征病毒(Porcine reproductive and respiratory syndrome virus,PRRSV)等多重混合感染[7-8],是导致保育阶段仔猪死亡率升高的主要原因,其在全球范围内广泛流行与致病性、耐药性的不断加重严重影响养猪业的健康发展,带来了巨大的经济损失[9]。2020年12月,河南省漯河某猪场的仔猪暴发呼吸道疾病,经抗生素治疗后效果不显著,病死猪剖检可见胸腔积液、肺脏肉样变、淋巴结肿大等症状。为了阐明引起此次仔猪呼吸道疾病的主要细菌性病原,采集2~3月龄具有典型呼吸道症状仔猪的口鼻拭子和病死猪的病变器官,通过病原菌的分离培养、染色观察、卫星试验、PCR等方法鉴定引起仔猪呼吸道症状的主要病原体为Hps,并对分离菌株的血清型、致病性和耐药性等进行了研究,以期为临床上Hps感染的精准施治和合理用药提供理论依据,为有效防控Hps及其相关疾病提供参考。
1 材料与方法
1.1 病料
采集河南省漯河某猪场2~3月龄、具有呼吸道症状仔猪的口鼻拭子60份;无菌采集病死猪的胸腔积液8份、淋巴结28份,以及病变肺脏、肝脏和脾脏共21份。
1.2 试验动物
30只体重为18~20 g的BALB/c小鼠,购自湖北宜昌三峡大学,Pm、SS、APP、Hps、PCV2、PRRSV等病原检测均为阴性。
1.3 主要试剂
脑心浸液培养基(brain heart infusion,BHI)购自Oxoid公司;特级马血清、革兰染色剂、琼脂、D-氨基葡萄糖均购自北京索莱宝生物科技有限公司;Taq酶购自宝生物工程(大连)有限公司;烟酰胺腺嘌呤二核苷酸(NAD)购自Biofoxx公司;病毒DNA/RNA提取试剂盒购自天根生化科技(北京)有限公司;药敏纸片购自杭州微生物试剂有限公司;金黄色葡萄球菌CVCC 25923由河南科技学院预防兽医学实验室惠赠。
1.4 呼吸道疾病病原的鉴定
1.4.1 病料核酸的提取 取送检肺脏约300 mg,经灭菌过的研磨器匀浆后用300 μL无菌PBS稀释后转移至1.5 mL离心管中,按照病毒基因组提取试剂盒操作说明提取病料的DNA/RNA,利用FastKing gDNA Dispelling RT SuperMix试剂盒进行反转录,获得的cDNA样品于-20 ℃保存备用。
1.4.2 呼吸道疾病病原的PCR鉴定 以从病料中提取的DNA与反转录的cDNA为模板,参照文献[10-11]中引物(表1),分别扩增Pm、SS、APP、Hps、PCV2、PRRSV的特异性基因,PCR产物进行1.5%琼脂糖凝胶电泳检测。

表1 猪呼吸道病原检测引物信息
1.5 细菌分离鉴定
1.5.1 病原分离培养 取病猪的胸腔积液、病变肺脏、肝脏和脾脏等组织,在超净工作台中分别接种于含5%马血清、20 μg/mL NAD[12]的固体BHI培养基上进行病原的分离培养,在37 ℃、5% CO2培养箱中培养24~48 h。
1.5.2 病原菌染色观察 观察培养基上生长细菌的菌落形态,挑取表面光滑、针尖大小的菌落进行革兰染色、镜检[13]。
1.5.3 卫星试验 将分离并纯化的菌种均匀划线接种于绵羊血平板上,在平板的中心垂直划线接种金黄色葡萄球菌CVCC 25923,置于37 ℃、5% CO2培养箱中培养48 h,观察平板上菌落是否有卫星菌落生长与溶血现象[14-15]。
1.5.4 V因子依赖性试验 将分离菌株纯培养物分别接种BHI、BHI+5%马血清、BHI+5%马血清+20 μg/mL NAD的液体培养基,置于37 ℃、5% CO2培养箱中培养24 h,观察培养基的浑浊度[16]。
1.5.5 PCR鉴定 利用Hps的鉴定引物vanY-F/R对有卫星现象的菌落进行PCR鉴定。PCR扩增体系20 μL:模板1 μL,2×PCR Mix 10 μL,上、下游引物(10 μmol/L)各1 μL,ddH2O 7 μL。PCR扩增条件:94 ℃预变性5 min;94 ℃变性30 s,58 ℃退火30 s,72 ℃延伸1 min,共35个循环;72 ℃延伸10 min。取5 μL PCR反应产物使用1.5%琼脂糖凝胶电泳进行检测,80 V恒压电泳50 min。
1.5.6 16S rDNA鉴定 利用通用引物27F:5′-AGAGTTTGATCCTGGCTCAG-3′与1492R:5′-TACGCTACCTTGTTACGACTT-3′进行PCR扩增。PCR反应体系20 μL:模板1 μL,2×PCR Mix 10 μL,上、下游引物(10 μmol/L)各1 μL,ddH2O 7 μL。PCR反应条件:94 ℃预变性5 min;94 ℃变性30 s,55 ℃退火30 s,72 ℃延伸1 min,共35个循环;72 ℃延伸10 min。PCR扩增产物送生工生物工程(上海)股份有限公司武汉测序部进行测序;利用NCBI BLAST工具对测序结果进行比对分析,并用Mega-X工具构建系统进化树。
1.5.7 Hps血清型分型 参照Howell等[17]引物对分离菌株进行多重PCR鉴定,引物序列见表2。PCR扩增体系20 μL:模板1 μL,2×PCR Mix 10 μL,引物Mix(50 μmol/L)3 μL,ddH2O 6 μL。PCR反应条件:94 ℃预变性5 min;94 ℃变性30 s,58 ℃退火30 s,72 ℃延伸1 min,共35个循环;72 ℃延伸10 min。PCR产物进行1.5%琼脂糖凝胶电泳检测,80 V恒压电泳50 min。
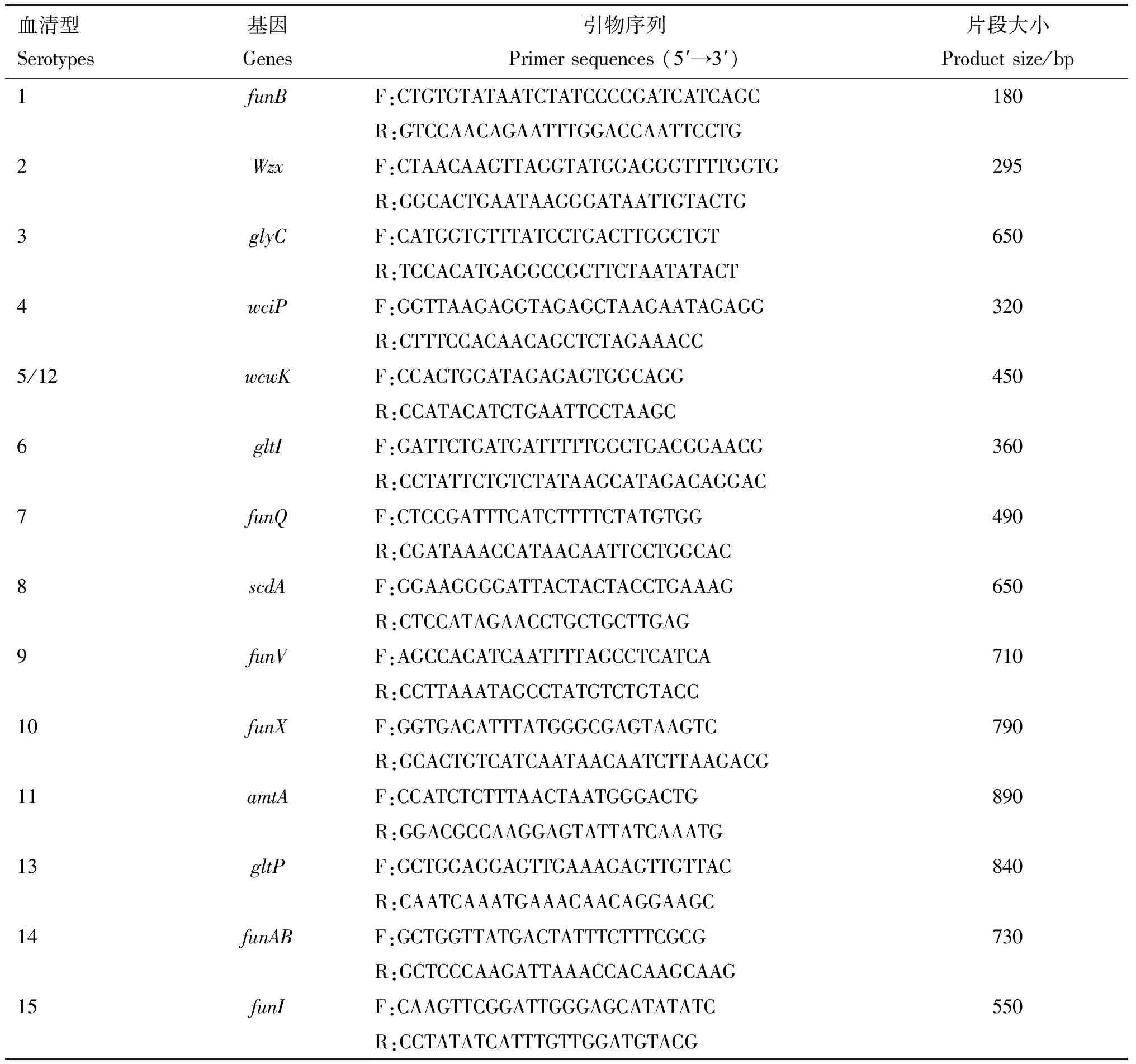
表2 Hps分型引物信息
1.6 动物致病性试验
将培养至对数生长期的Hps以无菌PBS重悬至终浓度分别为4.2×1012、4.2×1011、4.2×1010、4.2×109及4.2×108CFU/mL;将30只BALB/c小鼠随机分为6组,每组5只,其中5个感染组分别腹腔注射不同稀释度的Hps 0.2 mL,对照组注射同体积的无菌PBS。观察各组小鼠的临床症状,并对死亡小鼠进行剖检。采集死亡小鼠的血液、心脏、脑、脾脏、肺脏、肾脏、肝脏及腹水等样品,在固体BHI培养基上划线分离,并对分离到的菌落进行PCR鉴定。
1.7 分离菌株的药敏试验
用无菌接种环挑取单菌落接种于含5%马血清、20 μg/mL NAD的BHI液体培养基中,37 ℃恒温摇床培养5~6 h,用无菌棉签蘸取菌液均匀涂布于平板上。采用Kirby-Bauer(K-B)纸片扩散法[18],选取四环素、环丙沙星等11种抗菌药为试验药物,于37 ℃、5% CO2培养箱中培养24 h,测量抑菌圈直径,并参考流感嗜血杆菌NCTC 8468与ATCC 49766的质控标准判定Hps的耐药性。
2 结 果
2.1 呼吸道疾病病原的鉴定结果
从采集的病料中提取DNA/RNA,以提取的DNA与反转录的cDNA为模板进行呼吸道疾病病原的PCR鉴定,PCR产物经1.5%琼脂糖凝胶电泳显示,泳道8有约302 bp的条带,与Hps阳性对照大小一致(图1);其他病原检测均为阴性,推测该猪场仔猪的呼吸道疾病可能由Hps感染造成。
2.2 致病菌分离鉴定
2.2.1 致病菌培养特性 将病料划线接种于含血清和NAD的BHI固体平板后,生长出无色透明、表面光滑的微小菌落(图2A);纯培养的细菌革兰染色形态为革兰阴性杆菌,多单个存在,呈球杆、长杆状,部分以短链排列成丝状分布(图2B),符合Hps的基本形态特征。
2.2.2 卫星试验 将金黄色葡萄球菌与分离菌株垂直划线接种于绵羊血平板,培养后发现分离菌株只生长在金黄色葡萄球菌培养物周围,越靠近金黄色葡萄球菌的分离菌株,生长状态越好,呈现典型的“卫星现象”,且未发现溶血活性(图2C)。
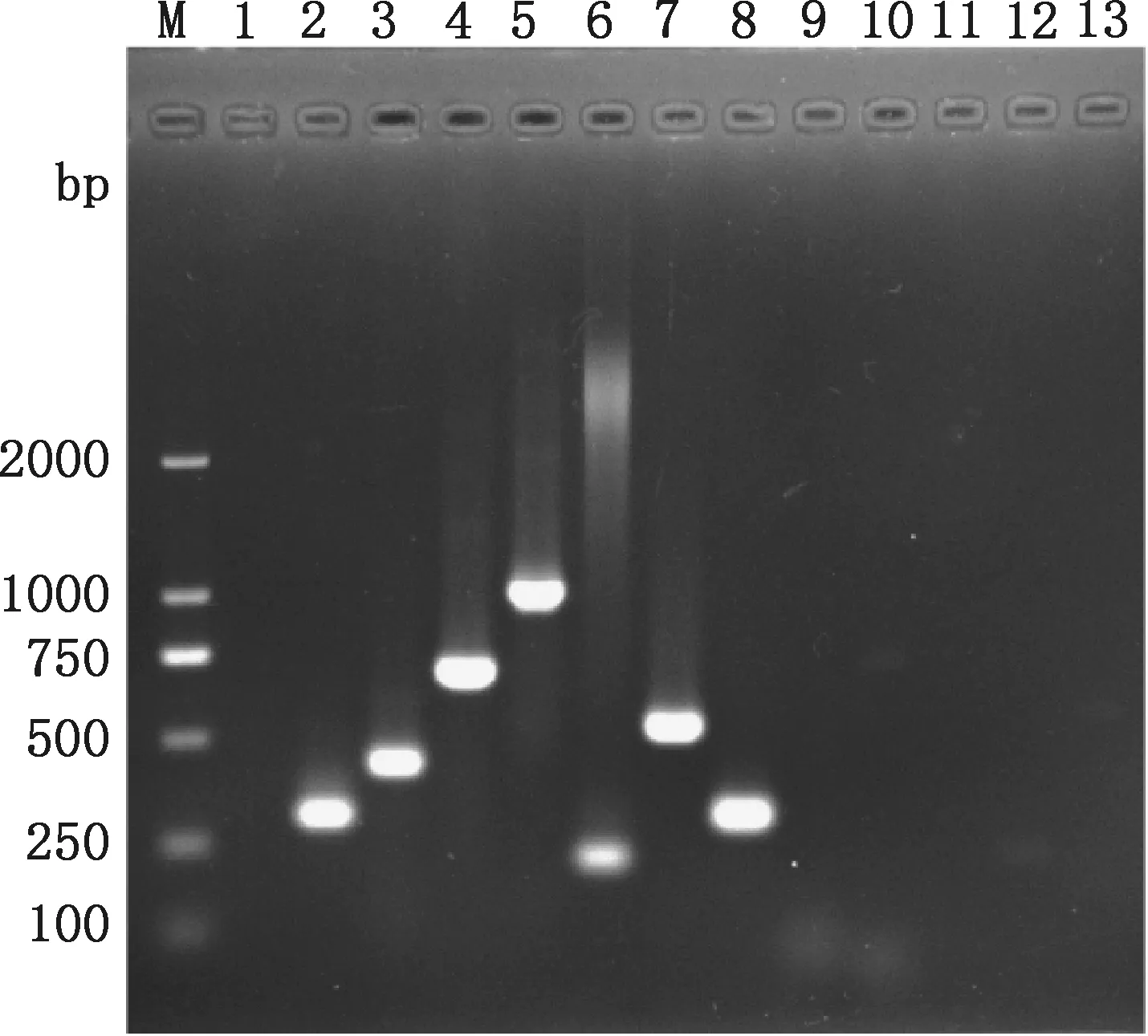
M,DL2000 DNA Marker;1,Hps阴性对照;2~7,Hps、APP、SS、Pm、PRRSV、PCV2阳性对照;8~13,样品Hps、APP、SS、Pm、PRRSV、PCV2病原检测M,DL2000 DNA Marker;1,Hps negative control;2-7,Hps,APP,Pm,PRRSV and PCV2 positive control,respectively;8-13,Sample pathogen detection of Hps,APP,SS,Pm,PRRSV and PCV2,respectively图1 病料的PCR鉴定Fig.1 PCR identification of the sample
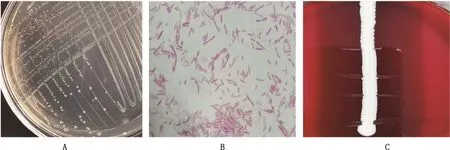
A,分离菌株菌落形态;B,分离菌株革兰染色(1 000×);C,分离菌株的卫星现象A,Colony morphology of the isolated strains;B,Gram staining of the isolated strains(1 000×);C,Satellite phenomenon of the isolated strains图2 分离菌株形态学鉴定Fig.2 Morphological identification of the isolates
2.2.3 V因子依赖性试验 将分离菌株的纯培养物分别接种BHI、BHI+5%马血清、BHI+5%马血清+20 μg/mL NAD的液体培养基,结果发现,分离菌株在不含V因子的BHI和BHI+5%马血清培养基中不生长,而在含有V因子的培养基中大量增殖(图3A),说明该分离菌的生长依赖V因子。
2.2.4 PCR鉴定 利用Hps的特异性引物对有卫星现象与V因子依赖的菌落进行PCR鉴定,结果显示,从分离菌基因组DNA中扩增出302 bp的特异性条带(图3B),与预期大小相符,说明分离菌株为Hps。
2.2.5 16S rDNA基因序列分析 以分离菌株DNA为模板,利用通用引物27F、1492R扩增分离菌株的16S rDNA并进行测序,测序结果比对发现,分离菌株序列与GenBank中收录的Hps参考株基因序列的相似性为97%~98%。系统进化树分析发现,分离菌株与Hps P462/03株处于同一分支(图4),证实分离菌株为Hps,命名为LH-20201220。

1,BHI;2,BHI+5%马血清;3,BHI+5%马血清+20 μg/mL NAD;M,DL2000 DNA Marker;4,阳性对照;5,分离菌株1,BHI;2,BHI+5% horse serum;3,BHI+5% horse serum +20 μg/mL NAD;M,DL2000 DNA Marker;4,Positive control;5,Isolates图3 V因子依赖性试验(A)与PCR鉴定(B)结果Fig.3 Results of V factor dependent test (A) and PCR identification (B)

图4 分离菌株16S rDNA序列的系统进化树Fig.4 Phylogenetic tree of 16S rDNA sequence of the isolate
2.2.6 分离菌血清型鉴定 利用Hps血清分型引物对分离菌LH-20201220进行多重PCR鉴定,结果显示,在约320 bp处扩增出清晰的特异性条带(图5A),与血清4型阳性对照大小相符;以血清4型特异性引物对分离菌LH-20201220的亚型进行重复鉴定,结果显示,在约320 bp处出现特异性条带(图5B),与多重PCR鉴定结果一致,确定分离菌LH-20201220为Hps血清4型菌株。
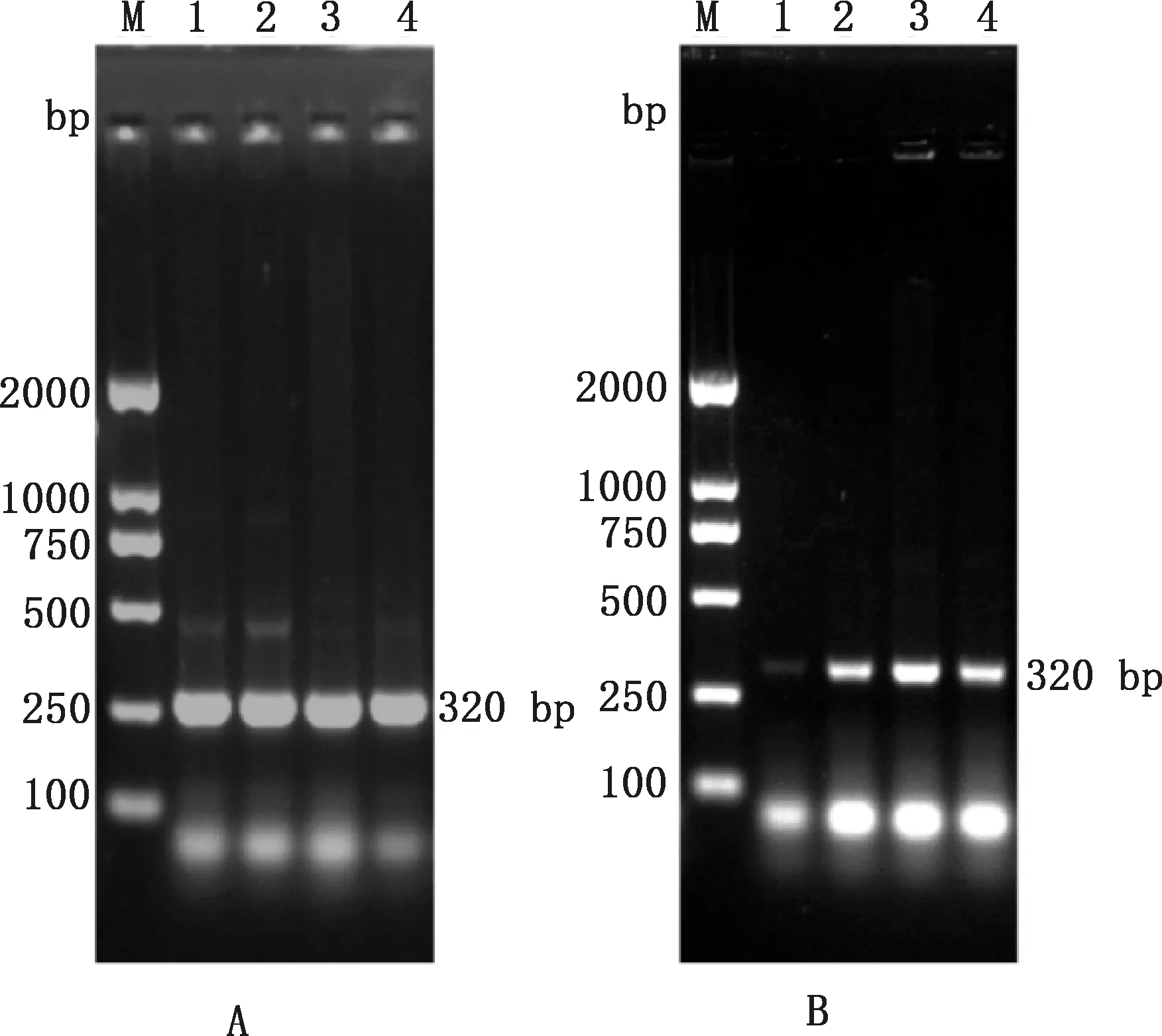
①A,多重PCR鉴定;B,血清4型PCR鉴定。②M,DL2000 DNA Marker;1~3,分离菌株;4,阳性对照①A,Multiple PCR identification;B,Identification of serotype 4.②M,DL2000 DNA Marker;1-3,Isolates;4,Positive control图5 分离株血清型鉴定Fig.5 Serotype identification of the isolate
2.3 分离菌株的致病性试验
将纯培养的分离菌株LH-20201220分别腹腔注射试验组小鼠,在感染后2 h,试验组小鼠均出现被毛凌乱、呼吸急促、扎堆畏寒等症状,对照组小鼠未出现异常变化;在感染后8 h,4.2×1012和4.2×1011CFU/mL组小鼠全部死亡,4.2×1010、4.2×109及4.2×108CFU/mL组小鼠活动性降低、厌食、呼吸急促、被毛凌乱无光泽;在感染后72 h,4.2×
1010、4.2×109及4.2×108CFU/mL组小鼠的临床症状有所缓解,5 d后基本恢复正常。
剖检死亡小鼠发现,感染Hps小鼠的肺脏、肝脏、脾脏、心脏和脑组织均有不同程度出血,以肺脏最为明显;肠壁变薄、透明,局部有出血。无菌采集死亡小鼠的心脏、脑、脾脏、肺脏、肾脏、肝脏、腹水等样品在固体BHI培养基上划线培养,肉眼可见无色透明、表面光滑的微小菌落,经PCR检测为Hps血清4型(图6),与感染菌株一致。
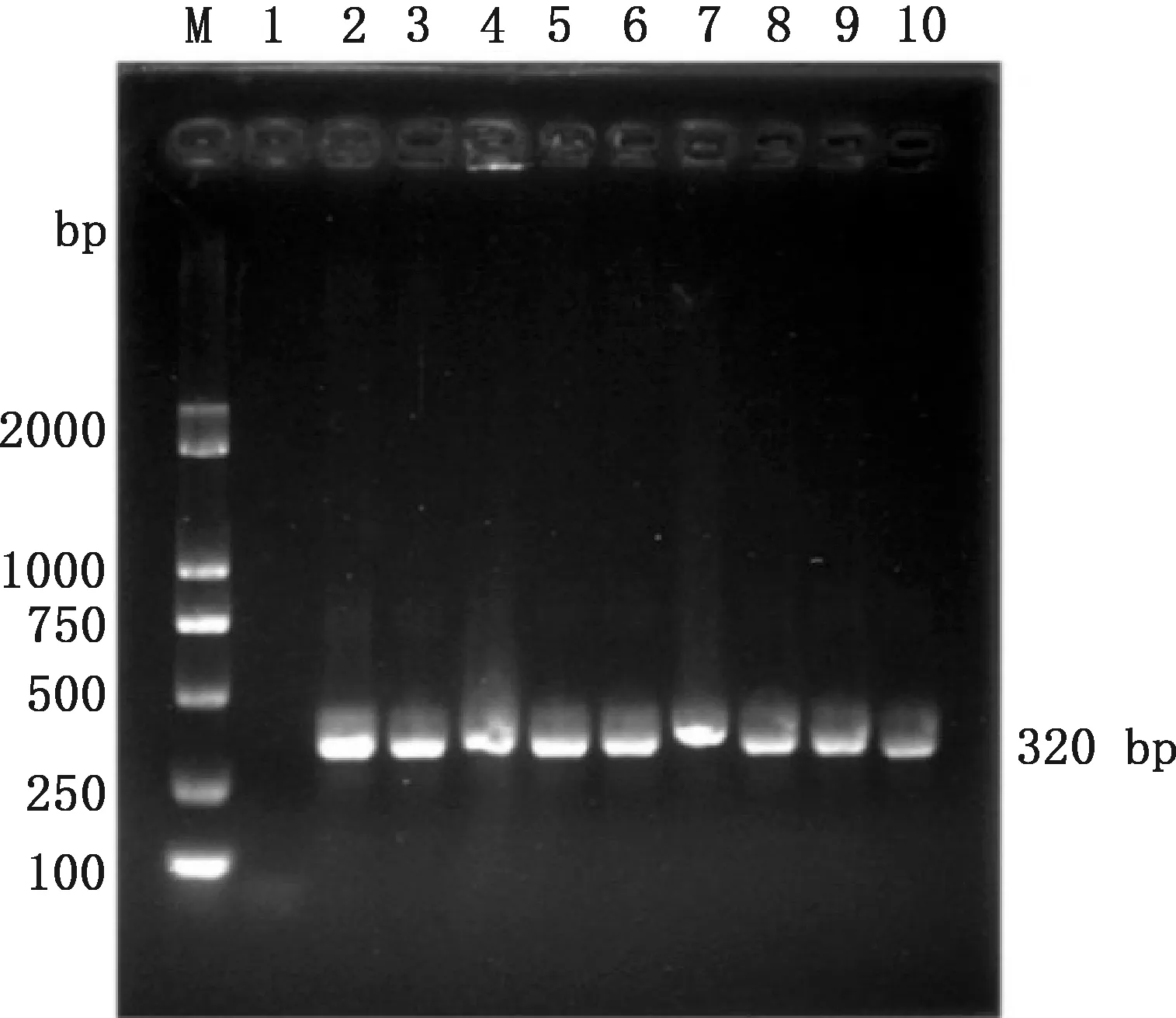
M,DL2000 DNA Marker;1,阴性对照;2,阳性对照;3,血液;4,心脏;5,肝脏;6,肺脏;7,脾脏;8,肾脏;9,脑;10,腹水M,DL2000 DNA Marker;1,Negative control;2,Positive control;3,Blood;4,Heart;5,Liver;6,Lung;7,Spleen;8,Kidney;9,Brain;10,Ascites图6 Hps感染小鼠各脏器的病原分离鉴定Fig.6 Isolation and identification of pathogens from various organs in Hps-infected mice
2.4 分离菌株耐药性试验
将药敏纸片贴附于平板上培养24 h后,测量抑菌环直径,依据流感嗜血杆菌NCTC 8468与ATCC 49766的质控标准判定分离菌株的耐药性情况,结果显示,分离菌株LH-20201220对红霉素、氨苄西林、头孢美唑、阿莫西林高度敏感,对四环素、环丙沙星、复方新诺明耐药,对氧氟沙星、氯霉素、利福平、亚胺培南为中度敏感(表3)。
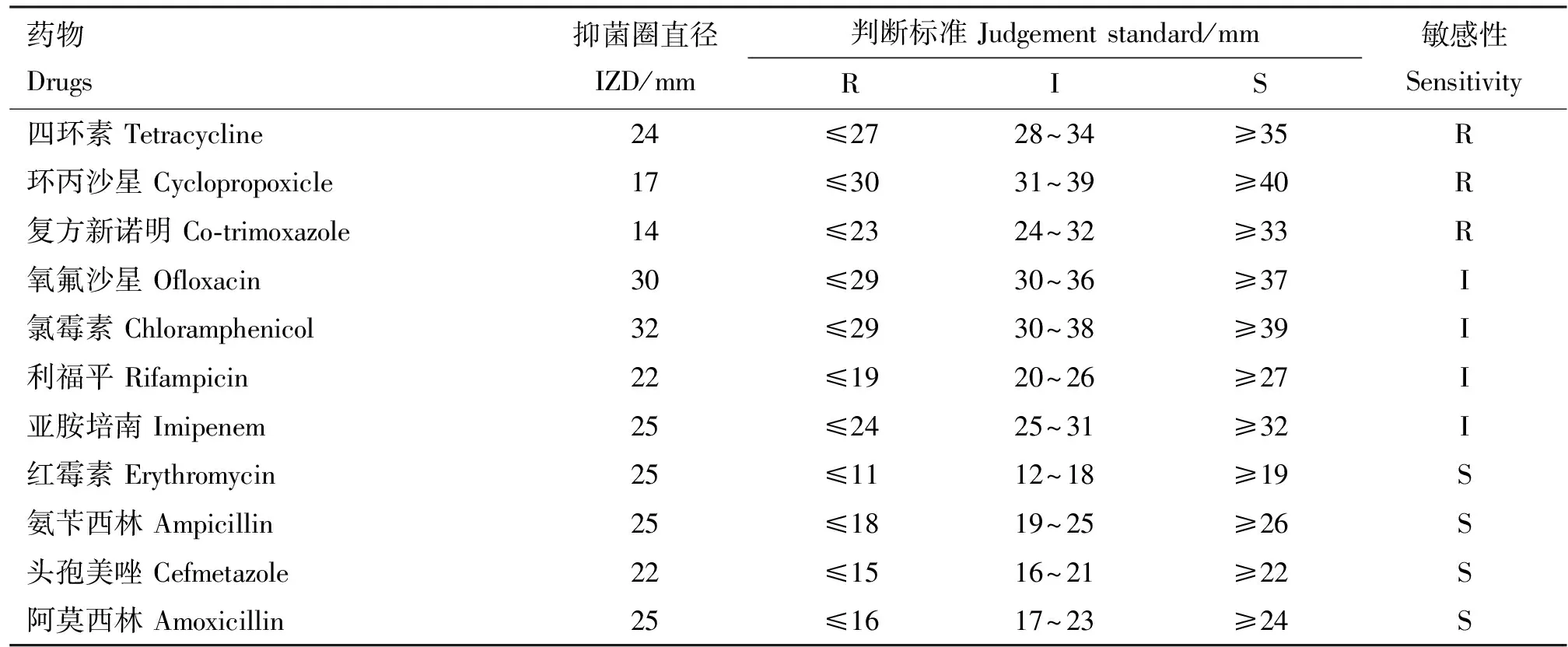
表3 药敏试验结果
3 讨 论
Hps广泛存在于猪的上呼吸道,它可以分解呼吸道上皮细胞的紧密连接蛋白而越过黏膜屏障,最终引起全身性感染,甚至穿透血脑屏障引起脑膜炎[19]。当Hps其他病原混合感染时,易造成猪群大面积发病,且Hps耐药菌株随着规模化和集约化养殖的发展而日趋流行,增加了猪群病情确诊和防治的难度,给生猪养殖带来较大的经济损失,引起了行业内的广泛关注[3,20]。目前,Hps的鉴别方法主要有染色镜检、卫星生长现象与PCR检测等。本试验使用PCR检测方法对采集的病料进行呼吸道疾病病原的检测发现,河南省漯河猪场仔猪的呼吸道疾病疑似由Hps引起,经革兰染色镜检、卫星生长试验、V因子依赖型试验和16S rDNA基因PCR扩增及序列分析验证,确定分离菌株为Hps。Hps血清型众多,按照传统的琼脂扩散血清分型方法可将Hps分为15种血清型。Howell等[17]根据不同血清型Hps菌株荚膜基因座的变异特点设计的多重PCR分型方法,可以较为准确地鉴别出Hps的不同血清型,优于传统的血清学方法。本研究利用该方法对分离菌株进行了血清型鉴定,确定分离菌株为Hps血清4型,这与丁文文等[5]2019年得出的河南地区主要流行的Hps为血清4型的结果一致。
Hps因血清型与流行地区的差异,其致病性也存在差异,近年来不断有Hps流行情况的调查研究,但对具体菌株的致病性研究较少。本研究利用试验小鼠分析分离株LH-20201220的致病性,结果表明,该分离菌株有较强的致病性,高剂量感染可导致小鼠死亡;剖检结果显示,感染组小鼠出现多器官损伤,且能从脑、肺脏、肝脏等器官中分离到感染菌株,这也证实了Hps能透过血脑屏障引起脑部感染,为后续Hps血清4型致病机制的研究提供了参考依据。
目前,对Hps的防治主要通过疫苗接种与药物治疗,但由于众多的血清型之间缺乏有效的交叉免疫保护,尚无可以预防多种血清型感染的多价疫苗[21]。同时,由于抗生素的滥用和耐药菌株的出现[22],Hps感染时用药不当将造成猪群大规模发病,给养殖场造成巨大经济损失,所以针对性地选择敏感药物进行Hps治疗就显得尤为重要[23]。本试验采用纸片法筛选了分离菌株Hps的敏感药物,发现其对红霉素、氨苄西林、头孢美唑、阿莫西林高度敏感,对环丙沙星等药物耐药,对氧氟沙星等中度敏感,与Zhao等[24]在2018年发现的Hps对洛美沙星、左氧氟沙星、诺氟沙星、环丙沙星均呈低耐药水平的结果有一定的出入,说明Hps的耐药性存在时间与空间上的差异性。根据本研究药敏试验结果选用敏感药物对发病猪群进行治疗,取得了良好的治疗效果。因此,在Hps发病时可根据药敏试验结果选取高敏药物进行治疗,在临床用药遵循使用小剂量敏感药物的原则,防止耐药性的发生和提高治疗效果。本研究结果表明,分离菌株在临床上具有较强的致病性和耐药性,提示应加强动物源Hps的流行病学调查和耐药性监测,为进一步系统性防控该病奠定基础。
4 结 论
本试验成功分离出1株Hps血清4型,与Hps参考株基因序列的相似性为97%~98%;分离菌株Hps可致感染小鼠多个器官不同程度出血,甚至死亡;分离菌株Hps对红霉素、氨苄西林、头孢美唑、阿莫西林敏感,对四环素、环丙沙星、复方新诺明耐药。

