细胞穿透肽增强氨基糖苷类抗生素杀菌作用的方法
石舒婷 王妍

摘 要:为验证细胞穿透肽能否增强氨基糖苷类抗生素杀菌作用,选用具代表性的3种氨基糖苷类抗生素(妥布霉素、卡那霉素及链霉素)处理平台期大肠杆菌。在特定抗生素处理浓度和处理时间下,进行平台期大肠杆菌杀伤效果组间比较,用ANOVA算法分析试验结果差异性;并使用NPN染色法探究细胞穿透肽增强氨基糖苷类抗生素杀菌作用机制。结果表明:细胞穿透肽预处理可以极显著增强妥布霉素、卡那霉素及链霉素杀灭平台期大肠杆菌,且细胞穿透肽对大肠杆菌細胞外膜造成轻微破坏。
关键词:氨基糖苷类抗生素;多肽;耐药
中图分类号:S 858.28 文献标志码:A 文章编号:0253-2301(2022)01-0012-06
DOI: 10.13651/j.cnki.fjnykj.2022.01.003
Method of Enhancing the Bactericidal Action of Aminoglycoside Antibiotics by Cell Penetrating Peptides
SHI Shu-ting, WANG Yan*
(Fujian Provincial University Key Laboratory of Cellular Stress Response and Metabolic
Regulation/College of Life Science, Fujian Normal University, Fuzhou, Fujian 350108, China)
Abstract: In order to verify whether the cell penetrating peptides could enhance the bactericidal action of aminoglycoside antibiotics, three representative aminoglycoside antibiotics (tobramycin, kanamycin and streptomycin) were selected to treat Escherichia coli at plateau phase. Under the specific antibiotic treatment concentration and treatment time, the killing effect of Escherichia coli at plateau phase was compared between groups, and the differences of experimental results was analyzed by using the ANOVA algorithm. Then, the NPN staining method was used to explore the mechanism of cell penetrating peptides enhancing the bactericidal action of aminoglycoside antibiotics. The results showed that the pretreatment with cell penetrating peptides could extremely significantly enhance tobramycin, kanamycin and streptomycin to kill Escherichia coli at plateau phase, and the cell penetrating peptides could slightly damage the cell outer membrane of Escherichia coli.
Key words: Aminoglycoside antibiotics; Polypeptide; Drug resistance
自Fleming[1]发现第一种抗生素(青霉素),其在人类社会健康和经济发展中占有重要地位[2],在农业和畜牧养殖业发展中亦拥有不可磨灭的功绩。近年来,随着临床和养殖业中抗生素的广泛应用,细菌耐药问题在全球范围内引起高度关注[3],找到解决细菌耐药问题的方案至关重要[4]。
目前,全球对细菌耐药采用的防治对策大致可归结为三类:一是建立健全监管机制,控制抗生素滥用:世界卫生组织[4]及其成员国已制定相应计划及政策[5];二是加快新型抗生素研发:包括针对抗MDR革兰氏阴性菌的新型四环素、多粘菌素[6]、darobactin[7]等[8]。新型抗生素虽已取得临床前良好试验效果,然至今尚未获得批准上市,且新型抗生素研发速度总体呈现下降趋势[9];三是改善抗生素治疗措施:包括抗生素联合给药[10]、“老药新用”[11]以及改变抗生素处理条件[12]。传统抗生素使用已有大量研究数据支持,其重新使用可能是应对细菌耐药问题的有效方法。部分氨基糖苷类抗生素(妥布霉素、卡那霉素及链霉素)拥有丰富临床研究数据,其杀菌机制主要是通过与细菌核糖体30 s亚基结合[13],使其发生读码错误。
近来,学者们陆续发现一些具有穿透细胞膜或核膜能力的氨基酸序列,其序列长度一般不超过30个氨基酸,统称为细胞穿透肽[14]。经改造和修饰,细胞穿透肽甚至可以携带多种物质运送至细胞内特定位置。故利用细胞穿透肽破膜改变细菌药物主动外排机制,可以降低细菌耐药性,增强氨基糖苷类抗生素杀菌。本研究选用1种只含13个氨基酸的细胞穿透肽,命名为CMP[15]。CMP能够破坏细菌细胞外膜,提高胞内抗生素浓度水平。通过使用CMP预处理平台期大肠杆菌,可以增强传统氨基糖苷类抗生素(妥布霉素、卡那霉素及链霉素)杀菌效果,即使用更低浓度氨基糖苷类抗生素和更短处理时间达到与以往相同甚至更好的杀菌效果。此方法极大减少氨基糖苷类抗生素使用浓度和作用时间,符合当前应对细菌耐药防治策略趋势。
1 材料与方法
1.1 试验材料
本研究选用大肠杆菌K12 BW25113菌株,细胞穿透肽(CMP)序列:KFFKFFKFFKGSG(杭州丹港生物科技有限公司,多肽经过严格质量检测,含质谱分析报告和HPLC分析报告,多肽纯度在80%以上。)
1.2 主要试剂及试验溶液
LB液体培养基(每1 L水包含10 g蛋白胨、10 g氯化钠、5 g酵母粉)、LB固體培养基(每1 L水包含10 g蛋白胨、10 g氯化钠、5 g酵母粉、10 g琼脂)、0.01 mol·L-1 PBS溶液(每1 L水包含8 g氯化钠、0.2 g氯化钾、1.44 g磷酸氢二钠、0.24 g磷酸二氢钠)、超纯水,以上溶液均经过高压灭菌锅121℃,30 min湿热高压灭菌。其中LB固体培养基灭菌完成后,倒入无菌培养皿中待其凝固即可使用。
妥布霉素(25 mg·mL-1)、卡那霉素(50 mg·mL-1)、链霉素(100 mg·mL-1),以上氨基糖苷类抗生素储液均用超纯水配置,并使用0.22 μm滤膜过滤除菌。
NPN荧光染料储液(1 mmol·L-1),超纯水配置,避光保存。
1.3 抗生素对平台期大肠杆菌杀菌效果检测
从-80℃冰箱挑取保藏的BW25113大肠杆菌,37℃,220 r·min-1,摇床过夜活化,之后1∶1000接种至含有20 mLLB液体培养基的摇瓶中,摇床37℃,220 r·min-1,培养至平台期(16~24 h)。取500 μL细菌置于EP管中,13000 r·min-1离心3 min,吸取上清(旧LB)置于无菌器皿内,用500 μL0.01 mol·L-1 PBS溶液重悬菌体,静置5 min,再次离心去上清。
用500 μL超纯水重悬菌体,各个处理样品中加入CMP(终浓度10 μmol·L-1)混匀,室温下静置处理5 min,离心去上清。加入旧LB培养基,移至玻璃摇菌管中并加入抗生素,摇床37℃,220 r·min-1振荡处理,每1、3、5 h取样50 μL,离心去上清,加入500 μLPBS重悬清洗5 min,再次离心去上清,用50 μLPBS重悬,进行10倍浓度梯度稀释。将稀释好的菌液滴于正常LB平板上测试细菌存活情况。
1.4 细胞穿透肽(CMP)对大肠杆菌外膜破坏检测
从-80℃冰箱活化菌株BW25113,1∶1 000转接至LB液体培养基中,摇床(37℃,220 r·min-1)培养至平台期。取100 μL菌液置于EP管中,13000 r·min-1,3 min离心去上清,将沉淀重悬于相同体积的PBS中,静置5 min,再次离心去上清,后用同体积超纯水重悬沉淀,将CMP(终浓度为10 μmol·L-1)加入处理,同时向细菌溶液中加入等量PBS作为空白对照组处理5 min。离心去上清,将沉淀重悬于同体积PBS中。而后用PBS将菌液稀释至约为1×108 CFU·mL-1。移至黑色EP管,将5 μL NPN荧光染料(终浓度10 μmol·L-1)添加到黑色EP管中,避光孵育,使用紫外荧光分光光度计在激发波350 nm和发射波长420 nm条件下,0、5、10 min监测NPN荧光强度。
2 结果与分析
2.1 细胞穿透肽(CMP)增强氨基糖苷类抗生素对平台期大肠杆菌的杀菌效果
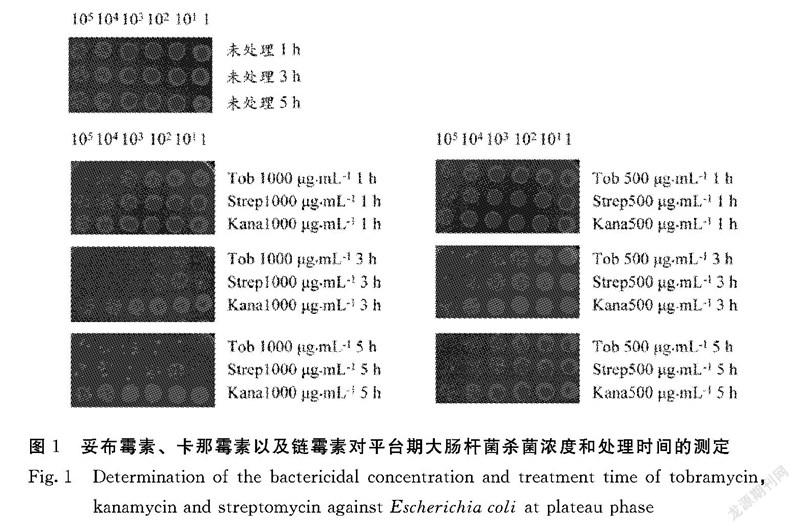
2.1.1 妥布霉素、卡那霉素以及链霉素对平台期大肠杆菌杀菌浓度和处理时间测定 首先,本研究将平台期大肠杆菌用妥布霉素(Tob)、卡那霉素(Kana)以及链霉素(Strep)进行单独杀菌处理,处理终浓度为1000 μg·mL-1和500 μg·mL-1,由图1可知:除卡那霉素终浓度为500 μg·mL-1时处理平台期大肠杆菌1、3和5 h均没有杀菌效果外,其余2种抗生素在处理平台期大肠杆菌3 h和5 h后都对细菌造成2~4个数量级杀伤效果。
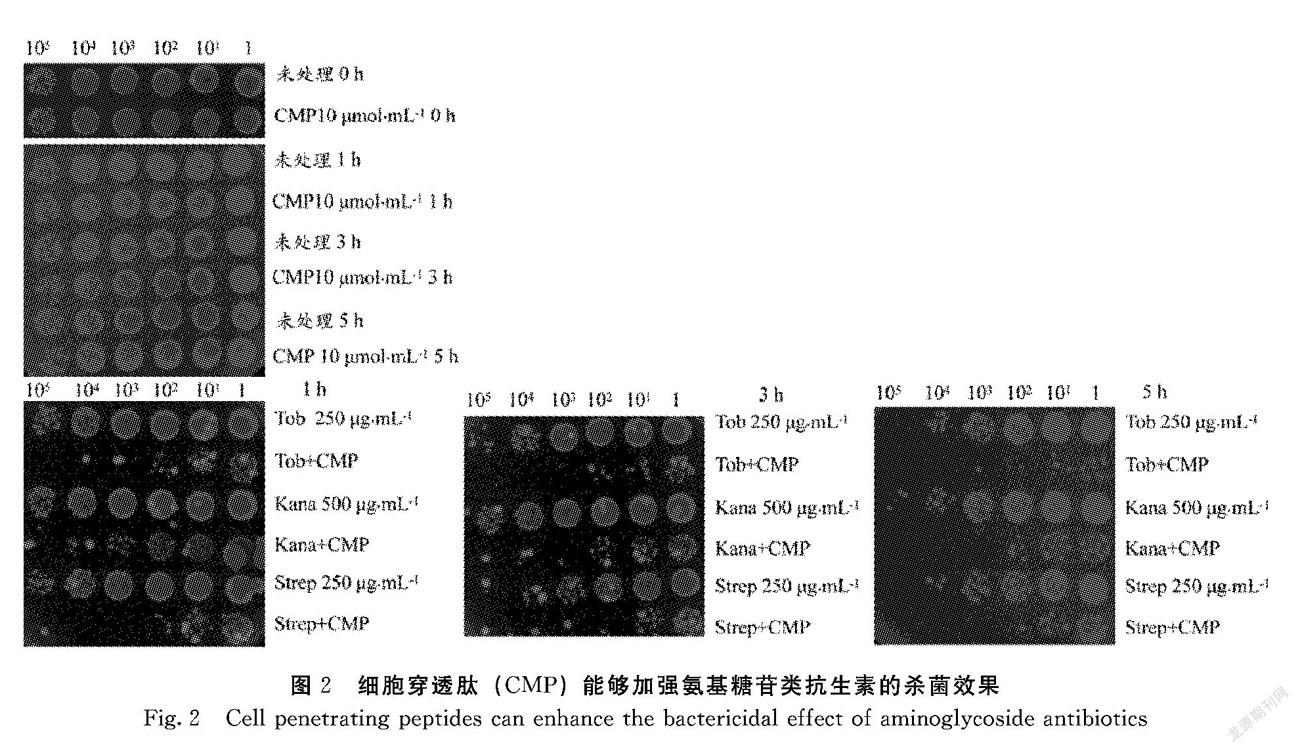
2.1.2 细胞穿透肽(CMP)能够加强氨基糖苷类抗生素杀菌效果 根据上述结果,将卡那霉素处理终浓度定为500 μg·mL-1,妥布霉素和链霉素处理终浓度下调至250 μg·mL-1。根据以往试验结果,细胞穿透肽(CMP)预处理终浓度为10 μmol·L-1。由图2可知,单独使用终浓度10 μmol·L-1CMP处理平台期大肠杆菌,在1、3和5 h内均无杀伤效果,故排除CMP自身杀菌情况。CMP预处理后,细菌在1 h便被终浓度为250 μg·mL-1妥布霉素杀伤4~5个数量级,相同浓度下单独妥布霉素处理组没有表现出对细菌杀伤。在3、5 h时,单独妥布霉素处理组对细菌表现2个数量级杀伤,但CMP预处理组在3、5 h时对细菌表现出4个数量级杀伤。卡那霉素和链霉素杀菌情况亦是如此。
2.1.3 特定浓度细胞穿透肽(CMP)处理后氨基糖苷类抗生素杀菌效果的定量分析 综上,优化试验条件,进行3次独立试验完成定量分析。3次独立试验所使用CMP预处理终浓度为10 μmol·L-1,妥布霉素终浓度为125 μg·mL-1,卡那霉素终浓度为500 μg·mL-1,链霉素终浓度为125 μg·mL-1,取样时间为1、3 h。图3A为其中1次试验表型结果展示,图3B是3次独立试验所得数值定量统计分析。由图3B可知,与试验对照组相比,CMP预处理组的3种抗生素均表现出对平台期大肠杆菌更强的杀菌作用。在1 h内,CMP预处理情况下,妥布霉素杀4个数量级、链霉素杀2个数量级、卡那霉素杀1个数量级;在3 h内,CMP预处理情况下,妥布霉素和链霉素表现出对平台期细菌4个数量级杀伤,卡那霉素亦达到对细菌3个数量级杀伤。根据试验结果得出结论,CMP预处理可以促进氨基糖苷类抗生素杀菌作用,并且效果极其显著。
2.2 CMP通过破坏细胞膜增加传统氨基糖苷类抗生素杀菌效果
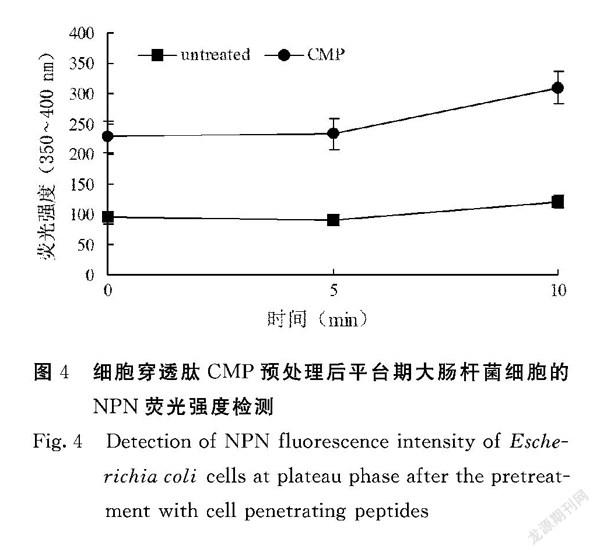
利用NPN熒光染料对CMP处理过的细菌进行染色,以验证CMP是否破坏细胞膜。由图4可知,起始时(0 min)CMP预处理组荧光强度高于对照组,在随后5、10 min检测中,NPN荧光强度一直呈上升趋势,且数值增加幅度大;反观对照组,荧光强度初始处于较低状态,随2次监测强度略微上升,不排除部分细菌自然发生一个外膜损伤造成上升现象。由此可得,CMP预处理造成细菌外膜破坏,且该破坏是轻微不致死的,不破坏细胞膜生物结构。
3 结论与讨论
抗生素发展应用与细菌耐药性产生,是一种密不可分的关系,细菌耐药性随抗生素广泛应用而愈演愈烈[16],新药研发难以跟上细菌自身耐药性发展的脚步[17]。本研究从促进传统抗生素杀菌效果的理念出发,利用细胞穿透肽CMP对细菌进行短时间预处理,增强氨基糖苷类抗生素杀菌效果。以妥布霉素为例,单独抗生素处理的平台期大肠杆菌,在妥布霉素终浓度为1000 μg·mL-1处理1 h的条件下被杀灭2个数量级,而经CMP预处理的细菌,终浓度为125 μg·mL-1妥布霉素处理相同时间,被杀灭3~4个数量级。在相同处理时间内,抗生素浓度下降8倍之多,且杀菌效果不减反增。其余2种抗生素亦展现此种增效现象。本试验结果表明,通过细胞穿透肽预处理是一种有效增强氨基糖苷类抗生素杀菌的方法。通过荧光染料NPN发现CMP轻微破坏细胞外膜,故推测其增强抗生素杀菌效果的机制是通过破坏细菌药物主动外排机制,提高胞内抗生素水平,从而展现更强的杀菌效果。
从生态学看来,现代抗生素临床及农业畜牧业等方面的广泛应用[18]为细菌创造一个与自然进化相似且更为苛刻严峻的生存环境[19],此种情况频繁发生势必增加细菌耐药性基因的进化速度、传播速度以及富集速度[20]。因此,在达到相同杀菌效果的同时,迂回降低抗生素处理浓度,减缓细菌耐药情况发生,特别是对于早期开发的一些经典抗生素,通过对其杀菌方法“回炉重造”,让经典抗生素再一次为人类所用,于当今细菌耐药性问题而言不失为一种颇有前景的解决方法。
参考文献:
[1]FLEMING A.On the antibacterial action of cultures of a penicillium, with special reference to their use in the isolation of B.inflfluenzae[J].Bulletin of the World Health Organization, 1929, 79 (8): 780-790.
[2]胡永飞,朱宝利.细菌耐药专刊序言[J].生物工程学报 2018, 34(8): 1201-1204.
[3]杜鹃,谢峻,郑颖城,等.《抗生素耐药:全球监测报告 2014》解读与反思[J].华南国防医学杂志, 2014, 28(8): 814-817.
[4]WEINER L M, WEBB A K, LIMBAGO B, et al.Antimicrobial-Resistant Pathogens Associated With Healthcare-Associated Infections: Summary of Data Reported to the National Healthcare Safety Network at the Centers for Disease Control and Prevention, 2011-2014[J].Infection Control & Hospital Epidemiology,2016, 37(11): 1288-1301.
[5]KITANO H, TEISHIMA J, SHIGEMURA K, et al.Current status of countermeasures for infectious diseases and resistant microbes in the field of urology[J].International Journal of Urology, 2019, 26(12): 1090-1098.
[6]OTSUKA Y.Potent Antibiotics Active against Multidrug-Resistant Gram-Negative Bacteria[J].Chemical & Pharmaceutical Bulletin,2020, 68(3): 182-190.
[7]YU I, MEYER K J,IINISHI A, et al.A new antibiotic selectively kills Gram-negative pathogens[J].Nature, 2019, 576: 459-464.
[8]ZHANEL G G, LAWSON C D, ZELENITSKY S, et al.Comparison of the next-generation aminoglycoside plazomicin to gentamicin, tobramycin and amikacin[J].Expert Review of Anti-infective Therapy, 2012, 10(4):459-473.
[9]LEVIN, STUART.The crisis in antibiotic resistance[J].Infectious Diseases in Clinical Practice,1993, 2(1): 53.
[10]FASS R.Comparative in vitro activities of beta-lactam-tobramycin combinations against Pseudomonas aeruginosa and multidrug-resistant gram-negative enteric bacilli[J]. Antimicrobial Agents and Chemotherapy,1982, 2(1):1003-1006.
[11]CHEN F, DI H, WANG Y, et al.Small-molecule targeting of a diapophytoene desaturase inhibits S.aureus virulence[J].Nature Chemical Biology, 2016, 12(3):174-179.
[12]ZHAO Y, LV B, SUN F, et al.Rapid Freezing Enables Aminoglycosides To Eradicate Bacterial Persisters via Enhancing Mechanosensitive Channel MscL-Mediated Antibiotic Uptake[J].mBio, 2020, 11(1).
[13]郑卫.氨基糖苷类抗生素研究的新进展[J].国外医药抗生素分册,2005,26(3):10.
[14]VIVè E, BRODIN P, LEBLEU B.A truncated hiv-1 tat protein basic domain rapidly translocates through the plasma membrane and accumulates in the cell nucleus[J].Journal of Biological Chemistry, 1997, 272(25):160-170.
[15]TINCHO M B, MORRIS T, MEYER M, et al.Antibacterial Activity of Rationally Designed Antimicrobial Peptides[J].International Journal of Microbiology, 2020(2):1-9.
[16]鐘艾玲, 田敏, 刘艳全, 等.氨基糖苷类抗生素的耐药机制研究进展 [J].中国抗生素杂志, 2019, 44(4): 5.
[17]BLAIR J, WEBBER M A, BAYLAY A J, et al.Molecular mechanisms of antibiotic resistance[J].Nature Reviews Microbiology, 2015, 13(1): 42-51.
[18]李昕,曾洁,王岱,等.细菌耐药耐受性机制的最新研究进展[J].中国抗生素杂志,2020,45(2):113-120.
[19]DISSMANN E, IGLAUER E.Clinical causes of bacterial resistance in pulmonary tuberculosis[J].Der Tuberkulosearzt, 1961, 15: 233.
[20]LEVIN-REISMAN I, RONIN I, GEFEN O, et al.Antibiotic tolerance facilitates the evolution of resistance[J].science, 2017, 355(6327): 826-830.
(责任编辑:柯文辉)
收稿日期:2021-12-05
作者简介:石舒婷,女,1996年生,硕士研究生,主要从事细菌耐药研究。
通信作者:王妍,女,1987年生,博士,副教授,主要从事细菌外膜蛋白生成研究(E-mail:wangyan@fjnu.edu.cn)。
基金项目:福建省科技厅基金青年创新项目(2018J05056)。
3488501908250

