半导体纳米材料的电离辐射合成综述
赵彩凤 杨亚辉 罗 琳 于卫东 谢洪科 张乐平 张 勇周毅吉 武小芬 邵 颖 邵 赛 王克勤
1(湖南省农业科学院核农学与航天育种研究所 长沙 410125)
2(湖南农业大学 资源环境学院 长沙 410128)
3(湖南师范大学 化学化工学院 长沙 410081)
能源危机和环境污染是阻碍社会经济发展的两大关键问题,如何解决这两个问题对实现可持续发展和维护生态环境和谐具有重要战略意义。半导体纳米材料是吸收和转化太阳能的关键所在,开发高效经济的光催化剂材料是解决目前太阳能转化利用问题的关键途径之一。光催化技术在利用太阳光能光解水制氢和光催化深度降解环境污染物方面得到广泛的关注和迅猛的发展,成为全球性研究热点[1-3]。
半导体纳米材料的合成技术在当前纳米材料研究中占有极为重要的地位,半导体纳米材料的制备方法因材料的应用目的和制备过程不同而不同。表1重点介绍了几种国内外的半导体纳米材料的制备方法,并分析这些方法各自的优缺点。辐射合成一般在室温下进行,合成方法简单,易操作,反应试剂绿色环保,合成的半导体材料纯度高,反应活性位点多。目前主要使用辐射源为γ射线,加速电子或重离子。同时,在相同实验条件下,得到的纳米颗粒尺寸、形貌及其性能差异较小。对辐射方法进行改进甚至可以实现快速辐射生产大量的微米级或纳米级材料,这使得它们在工业规模上的应用具有广阔的前景[4]。
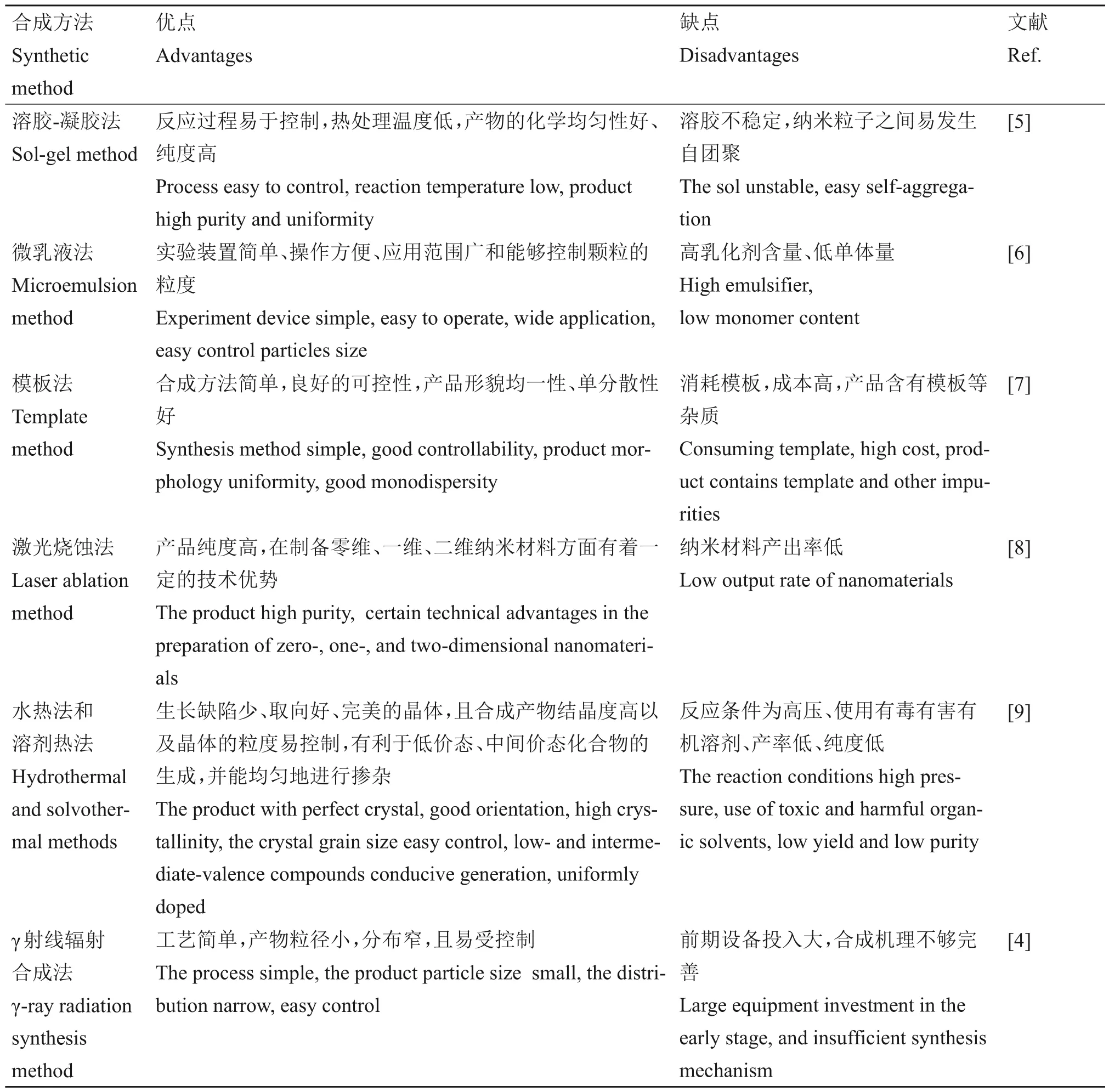
表1 半导体纳米材料的合成方法Table 1 Synthesis methods of semiconductor nanomaterials
根据辐射源性质,通过辐射分解、光解、撞击和光热效应机制,辐射诱导合成贵金属沉积、化合物和聚合物半导体纳米材料[10](图1)。半导体纳米材料的辐射改性主要包括:金属氧化物[11-12](TiO2、WO3、ZnO、Cu2O、CuO、Mn3O4等)、金属硫(硒)化物[13-14](CdS、ZnS、PbS、NiS、CdSe 等)、聚合物[15](g-C3N4)、表面贵金属沉积[16]及空位缺陷半导体纳米材料[17-19]的辐射改性。本文重点在于阐述辐射合成各种形貌及特征的半导体纳米材料的研究进展。

图1 贵金属沉积、化合物和聚合物半导体纳米材料的辐射诱导合成示意图[5]Fig.1 Schematic illustration of radiation-induced synthesis and modification of noble metal deposition,compound and polymer semiconductor nanomaterials[5]
1 半导体纳米材料电离辐射的机制
1.1 金属氧(硫、硒)化物半导体纳米材料的电离辐射合成机制
辐射合成金属氧化物,即将金属离子转化为氧化物,包括金属氧化态的转变(即辐射还原)。辐照不同溶液可制备无定形或结晶氧化物。应用辐射诱导方法已成功制备复杂结构的纳米粒子,如石榴石、尖晶石或钙钛矿[20-21]。
金属离子与OH-等中间体的反应可能导致热力学不稳定的氢氧化物形成,氢氧化物随后衰变为氧化物[22-23],(式1)。

一些金属单质(Fe、Ni、Co、Cu、Zn 等)能与溶解氧反应形成氧化物,(式2)。
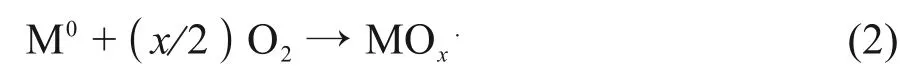
氧系数x取决于金属氧化物的稳定性,如氧化Cu0会产生CuO0.67,这是一种Cu2O的缺陷结构。当金属在溶液中以氧基的形式存在时(如VO2+),也可以通过辐射还原直接形成氧化物,(式3)。

硫化物半导体纳米材料由于具有重要的光电性能,从其材料的制备、表征到应用,一直都是人们研究的热点。辐射法制备纳米硫化物的反应过程一般比较复杂,Eager[24]、Buxton[25]和Elliot[26]等分别于1965 年、1984 年和1990 年相继报道了Na2S2O3在γ 射线辐照下可均匀地释放出S2-离子。Johnston[27]报道了γ 射线辐照CS2可产生硫自由基(S‧)。Hayes 等[28]报道了γ 射线辐照硫醇可产生HS-,由于巯基乙醇也有-SH官能团,因此可以推测巯基乙醇也有可能产生HS-,HS-继续电离释放出S2-。S2-/S.与金属离子结合,即得硫化物半导体材料。上述反应机理见式(4)~(11)。辐射法制备纳米金属硒化物的合成机理与硫化物半导体的制备类似。

1.2 贵金属沉积半导体纳米材料的电离辐射合成机制
水溶液吸收电离辐射导致水的辐射分解。式(4)辐射分解过程中,部分吸收的能量被消耗,形成反应中间体,进行多种反应[29-30]。
水的辐射分解得到强氧化性的羟基自由基(OH‧)和强还原性的水合电子,‧OH的氧化电位为E0=+2.73 V[31]。的还原电位为E0=-2.87 V,强还原电位基本可以还原水溶液中的金属离子,同时,添加‧OH 清除剂,如HCOO-或醇类(异丙醇),将加速辐射还原效应[32]。
甲酸盐离子清除‧OH和氢自由基(H‧)反应见式(12)、(13)。
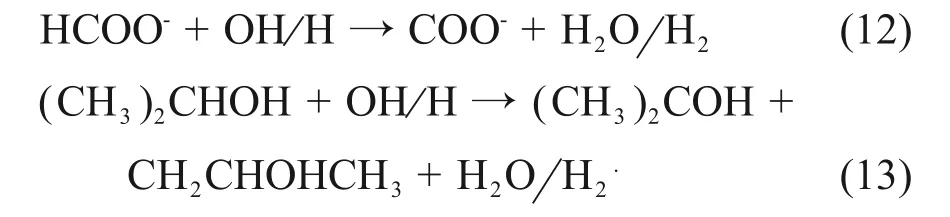
速率常数分别为3.2×109L/(mol·s)和2.1×108L/(mol·s)。反应产物是强还原性的二氧化碳离子自由基COO-。异丙醇与‧OH/H‧自由基主要发生抽氢反应,进攻α位。其中的产物之一((CH3)2COH)具有还原性。
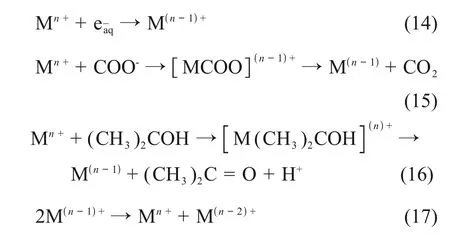
部分金属离子M(n-1)将发生歧化反应,然后经过、COO-、(CH3)2COH 连续的还原反应得到M0金属单质,并在溶液中聚集沉淀,从而得到表面贵金属沉积半导体纳米材料。
1.3 空位缺陷型半导体纳米材料的电离辐射合成机制
金属氧化物半导体氧空位的形成,主要是通过辐解的作用。在辐射场中,辐射水溶液产生还原性粒子(如、COO-、(CH3)2COH 等),可以将高价的过渡金属还原成低价态,同时产生氧空位。同时,添加OH‧清除剂如HCOO-或醇类(异丙醇、乙醇等)将加速辐射还原效应[14]。
非金属聚合物半导体产生空位缺陷主要是在辐射场中,具有一定能量的重离子(He+、Ar+、Au+等)将经过一系列的碰撞过程而逐渐损失能量,而靶原子会从晶格位置射出,留下空位。在经历系列的级联碰撞过程后,由于离子辐照的非化学选择性,可同时产生多种类型的空位。
2 金属氧(硫、硒)化物半导体纳米材料的电离辐射合成
2.1 金属氧化物半导体纳米材料
近年来,通过不同类型的电离辐射(如γ 射线、加速重离子或电子)对水体系进行辐照,制备了多种纳米金属氧(硫、硒)化物。通常,吸收剂量高达数十kGy。在合成各种氧(硫、硒)化物时,必须添加表面活性剂、自由基清除剂,以及进行溶液脱氧等步骤。吸收剂量、pH 和表面活性剂的改变对氧化物纳米颗粒的形貌和尺寸大小有显著影响。
辐射法制备氧化亚铜纳米晶的研究报道较多。近年来,许多文献报道了在水溶液中通过辐射还原铜(II)盐可以成功地制备出各种铜氧化物[22]。添加表面活性剂可以控制纳米颗粒的尺寸/形状。已有文献研究了在异丙醇和多种表面活性剂(PVA、SDS 等)、甲酸盐自由基清除剂的作用下,硫酸铜在射线和电子束照射下,辐射引发合成了立方晶结构氧化亚铜。在硫酸铜、异丙醇、表面活性剂(SDS)的醋酸盐缓冲液(pH=4.0~4.5)中,采用γ射线法合成了纳米晶氧化亚铜,粒径为14 nm[22]。通过γ 射线辐照脱氧油包水乳剂,乳剂里含有Triton X-100、正己醇、环己烷及铜溶液,得到尺寸可控的八面体氧化亚铜纳米晶,不存在其他相[22]。Zhou 等[35]研究了表面活性剂对纳米颗粒化学成分的影响。采用电子束(2 MeV)辐照分别含有PVA、SDS、麸质或聚乙二醇(PEG)的表面活性剂水溶液体系,合成铜纳米粒子,添加PVA 时得到铜和氧化亚铜的混合物。纳米粒子的化学组成也会受到前驱体浓度的影响。在含有硫酸铜或甲酸铜的水溶液中,在异丙醇或PVA 的情况下,用γ 射线或电子束辐照,制备了大粒径(250 nm)单晶八面体氧化亚铜纳米颗粒,然而,降低铜盐浓度会导致主要形成金属铜粒子[23]。电离辐射也应用于氧化物半导体纳米颗粒的改性,Shinde 等[6]应用电子束辐射对连续离子层吸附反应(SILAR)合成的CuO 薄膜进行辐照改性,研究结果表明,吸收剂量在0~30 kGy,CuO 薄膜的形貌从纳米薄片(0 kGy)、混合纳米颗粒/纳米层(10 kGy)、相互连接的纳米颗粒状(20 kGy),到玫瑰纳米结构(30 kGy)。经过20 kGy辐照改性的CuO 薄膜,形成了相互连接的纳米颗粒形貌,具有更高的充电/放电效果,最高电容达511 F/g,在超级电容器中具有一定的应用空间(图2)。

图2 不同剂量辐射改性CuO样品的TEM图像:(a)0 kGy;(b)10 kGy;(c)20 kGy;(d)30 kGy[6]Fig.2 TEM images of pristine and irradiated CuO sample at different doses:(a)0 kGy;(b)10 kGy;(c)20 kGy;(d)30 kGy[6]
另一种常用辐射法制备的材料是氧化锌(六角纤锌矿结构)。用60Co γ 射线辐照碱性胶束溶液成功制备了单晶ZnO[7]。也有报道通过直接辐射合成制备过氧化锌的方法[21]。使用电离辐射(γ射线或e-射线)辐射含有甲酸锌和过氧化氢的水溶液,用于制备该化合物。Hu等[36]报道了一种在室温和常压下,通过γ射线辐射一步法制备单分散均匀的大尺寸ZnO 单晶六棱柱。通过辐照ZnSO4·7H2O、NaOH、十六烷基三甲基溴化铵(CTAB)的异丙醇水溶液,吸收剂量100 kGy,剂量率50 Gy/min,得到白色沉淀ZnO。场发射扫描电子显微镜(FESEM)图像显示产物由边缘为(230±10)nm 的六角形棱柱组成,长度可达8.5 μm,同时,高分辨透射电镜(HRTEM)进一步证实了ZnO 为六方单晶。形成这种单晶六棱柱的主要原因是CTAB是一种阳离子表面活性剂,与亲水盐共存时易形成棒状胶束。
辐射法也已成功制备了Mn3O4、Co3O4、Fe2O3等半导体纳米材料。Said 等[37]提出了一种利用γ射线辐照含有表面活性剂前驱体溶液,制备单分散均匀的罗盘状Mn3O4纳米晶。通过辐照MnSO4·H2O及CTAB异丙醇水溶液,吸收剂量80 kGy,剂量率50 Gy/min,得到Mn3O4纳米晶。TEM及HRTEM图像结果显示,样品为单分散均匀的罗盘状单晶,中间宽度为80 nm,长度为200 nm。CTAB 的存在是单晶罗盘状的Mn3O4纳米晶形成的关键因素。通过γ 射线辐照CoSO4溶液得到Co3O4纳米胶体粒子,研究了氧化物形成的机理。分析颗粒形成与辐照时间的关系,结果表明颗粒从Co(OH)2演化为CoOOH,最后演化为200 nm Co3O4纳米颗粒[38]。将制备的Fe(OH)3或FeOOH 溶胶在pH=5 进行γ 射线辐照。观察到菱形三氧化二铁α-Fe2O3(pH=3~5)[39-40]。
2.2 金属硫化物半导体纳米材料
随着对辐射机理(中间产物、自由基等)的深入研究,可控粒径及形貌的硫化物半导体也随着发展。在硫醇存在的情况下,γ射线辐照诱导聚集形成镉和锌硫化物[8]。制备的颗粒非常小,受吸收剂量和剂量率的影响较大,CdS 小于1.0 nm,ZnS 约为1.5 nm。Hu等[41]通过两步辐照得到高度分散的NiS(PbS)空心球。首先,将含40%甲基丙烯酸甲酯(MMA)单体的乙醇水溶液在室温下放入γ射线辐射场中辐照,得到透明的聚甲基丙烯酸甲酯(PMMA)凝胶;其次,将PMMA 凝胶分成0.5 cm×1.0 cm 或更小的薄片,然后将其放入含有CS2和NiSO4·6H2O [Pb(CH3COO)2·3H2O]的乙醇溶液中,达到溶胀平衡后,再次放入60Co γ射线辐射场,当反应全部完成时,可以得到亚微米级的NiS(PbS)。本实验成功合成中空球的关键在于控制辐射诱导PMMA 降解为MMA 单体,MMA不溶于水,在溶液中以油滴形式存在。CS2也不溶于水,容易附着在MMA油滴的表面。从而,这些油滴形成油包水反应中心。FESEM及TEM结果显示,样品由直径为500 nm 的均匀单分散空心球组成。Abdelhak 等[42]采用γ 射线辐照含有PVP 水溶液制备了单分散ZnS纳米球。辐照ZnCl2、Na2S2O3·5H2O及PVP 水溶液,吸收剂量为133.06 kGy,即可得到白色沉淀物ZnS。FESEM结果表明,ZnS由平均直径约120 nm 的多层单分散纳米球组成。随着吸收剂量增加(66.53 kGy、99.79 kGy、133.06 kGy 和166.33 kGy),纳米球的直径也相应地增加。
2.3 金属硒化物半导体纳米材料
金属硒化物在结构和化学性质上与相应的硫化物类似,其能带隙一般在0.3~3.0 eV,是重要的直接带隙半导体材料。硒源的选择是辐射合成的关键,不仅需要能够溶解于水体系,而且必须是能够缓慢地释放Se-。文献中报道的常用的硒源有硒脲、硒化氢或者有机硒、二硒化碳等,但这些硒源一般都难于获得且价格昂贵[43]。随着辐射研究的不断深入,目前常用的硒源为Na2SeSO3。研究发现,不同的辐射源得到的CdSe 纳米颗粒存在差异。在叔丁醇存在的情况下,分别采取两种不同的高能射线合成CdSe 纳米颗粒,发现在电子束辐照下,CdSe 容易被氧化发生逆反应。而通过γ射线辐射合成的CdSe 纳米颗粒,不易发生逆反应,归因于两种合成过程中剂量率的巨大差异,导致了纳米颗粒晶体结构和尺寸的显著不同[9](图3)。同时,采用模板亦可制备不同形貌的CdSe半导体纳米材料。Choudhary[43]等以聚乙烯吡咯烷酮(PVP)或聚丙烯酰胺(PAM)水凝胶为模板,在室温下辐照制备了硒化镉(CdSe)空心结构和纳米球。CdSe 中空结构孔径为25~180 nm,壁厚为3~7 nm;CdSe纳米空心球孔径为40~50 nm,壁厚为3~5 nm。该研究中选择合适的水溶性聚合物作为软模板是成功合成CdSe 中空结构和纳米球的关键。

图3 EB辐射后CdSe纳米粒子的可逆形成和分解,以及γ辐射单向合成CdSe纳米粒子示意图:(I)起始溶液;(II)在辐射下产生的CdSe溶胶;(III)分解的CdSe溶胶[9]Fig.3 Schematic representation showing the reversible formation and decomposition of CdSe nanoparticles upon EB irradiation and one way formation upon γ irradiation:(I)the starting reagent solution;(II)CdSe sol produced upon irradiation;(III)decomposed CdSe sol[9]
3 贵金属沉积半导体纳米材料的电离辐射合成
3.1 Ag沉积半导体纳米材料
电离辐射合成可以得到纯度高、粒径小、分布窄的贵金属,目前电离辐射合成的贵金属主要包括Ag、Au、Ir 等(表2)。贵金属均匀地分布在半导体纳米材料上,能够和半导体形成异质结复合材料,并且贵金属的存在能够优化半导体材料表面电子结构,提高导电性能,贵金属与半导体材料之间形成的欧姆接触能够产生局部电场,形成能垒,抑制光生载流子的复合。此外,贵金属Ag、Au 等一般具有局部表面等离子体共振效应(LSPR),可以极大地提高半导体材料的可见光响应能力,进而有效地提高了半导体材料的光电性能。

表2 在表面活性剂存在下γ射线辐射诱导合成贵金属纳米颗粒的合成参数Table 2 Summary of the synthetic parameters for γ-ray radiation-induced synthesis of metal NPs in the presence of surfactants
贵金属沉积半导体纳米材料合成的关键因素包括:足够的氢氧根自由基清除剂,一定量的络合剂,保持体系惰性气氛和碱性,处理样品时在低温真空中干燥。利用γ射线引发辐射化学反应可方便地与溶胶-凝胶过程相结合,成功地制备贵金属沉积半导体纳米材料。室温条件下,在具有锐钛矿结构的氧化钛基质中,溶胶-凝胶法和γ 辐射法的复合可合成晶体银的纳米复合材料。第一步,通过溶胶-凝胶法制备氧化钛;随后,通过辐射还原制备5 nm银纳米颗粒,并负载在其表面。经过γ射线辐照、洗涤和干燥后,获得了纳米复合材料,该材料由锐钛矿基质和银纳米颗粒组成,银纳米颗粒尺寸分布较窄[52]。Zhang 等[44]研究表明,在γ 射线辐照下,Ag@还原氧化石墨烯@TiO2纳米管阵列复合材料的光催化活性增强。其中一个原因是材料在γ射线退火下,部分Ti4+被还原为Ti3+,产生了Ti3+缺陷。同时,在γ 射线辐照下,AgNO3被还原成Ag 单质,均匀分散在TiO2纳米管阵列表面,有助于载流子的分离,从而光催化活性提高。
3.2 其他贵金属沉积半导体纳米材料
在PVA 和异丙醇的存在下,通过18 kGy γ 射线辐照,制备了包含金、铂和钯纳米粒子的复合材料[53]。铁氧化物(c-Fe2O3)分散在贵金属盐水溶液中,可观察到纳米复合物的形成。采用电子加速器制备了4 nm 金-铁氧化物纳米复合材料[54]。与射线法合成金纳米粒子相比,电子束法合成金纳米粒子更小。Shi等[11]创新性地使用60Co γ 辐照法在石墨相氮化碳和铂纳米颗粒之间构建了界面电子传输通道,提出一种基于金属载体相互作用制备氮化碳基载铂(CN/Pt)纳米复合材料用于燃料电池催化剂的方法(图4)。研究人员将制备的CN/Pt纳米复合材料作为电催化剂应用于氧还原反应(ORR)中,发现其塔费尔斜率小,四电子转移路径快,氧还原性能远优于商业Pt/C 和大多数报道的g-C3N4基电极。实验结果表明,PtNPs 与g-C3N4之间通过金属-载体相互作用能够实现快速电荷转移,从而证明了采用γ辐照技术可有效构建界面电子传输通道,这一策略能有效提高g-C3N4电催化性能。此类CN/Pt 纳米复合材料合成方法简便、环保,且可大规模普及。辐射法制备贵金属沉积半导体纳米材料,具有贵金属离子与半导体结合紧密、贵金属粒径小、均匀分散在半导体材料表面的优点,从而相对于传统方法制备得到半导体材料光电性能大大的提升。
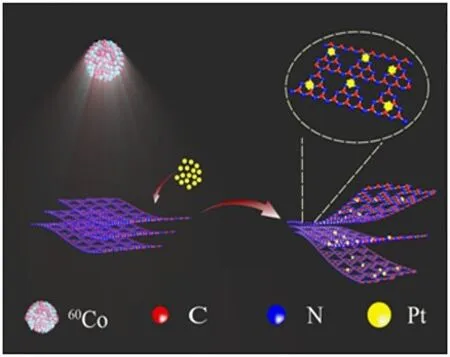
图4 γ辐照法制备CN/Pt纳米材料示意图[11]Fig.4 Diagram of the preparation procedure of CN/Pt[11]
4 空位缺陷半导体纳米材料的电离辐射合成
4.1 金属氧化物空位缺陷型半导体纳米材料
非计量化学比的半导体材料在光催化、光电催化以及太阳能电池中得到广泛的研究和应用,缺陷结构对空穴和光生电荷的产生、分离和迁移以及界面反应都具有重要影响。大部分学者认为[55-56]在合适的数量范围内,缺陷可以起到电荷分离的效果,然而超过一定范围内,则会变成电子-空穴的复合中心,因此缺陷工程是构筑高反应活性半导体纳米材料最为行之有效的方法之一。
TiO2作为典型的金属氧化物半导体,其辐射产生空位缺陷的研究已有文献报道。Lamo 等[55]研究了γ辐射对工业用TiO2光催化剂的影响,结果表明,TiO2氧空位的含量并不随吸收剂量而增加。Samet 等[56]利用γ 射线辐射合成Cu 掺杂的TiO2纳米粒子,并用于降解有机污染物。研究表明,与未掺杂的光催化剂相比,Cu 掺杂的TiO2光催化剂粉末的加入显著提高了污染物的降解率。这可能是在γ 射线辐射合成过程中,Cu 掺杂TiO2同时产生了氧空位。Zhao 等[14]利用γ 射线辐照诱导锐钛矿TiO2产生氧空位和Ti3+缺陷,并高效光催化降解有机污染物(图5(I))。本研究采用γ射线辐照TiO2乙醇/水溶液,反应体系与已有文献报道固体粉末体系相差较大,故辐射后的TiO2光催化剂性能也不一致。对辐照后的TiO2光催化剂进行了XRD、Raman、UV-vis、TEM、SEM测试,发现γ射线辐射能够同时产生表面及体相氧空位及Ti3+缺陷,材料的稳定性好。经过49.5 kGy 辐照的TiO2光催化剂,对RhB 光催化降解速率是未辐照(对照)的30 倍,对苯酚光催化降解速率是未辐照的20 倍。同时,光催化剂具有良好的稳定性,经过5次循环实验,光催化降解性能基本不变。辐射源不同,其电离能力、穿透力等不同,电子束穿透力相对于γ 射线穿透力弱,产生的空位缺陷存在于表面,然而电离能力相对γ射线较强,产生的空位缺陷较丰富。Huang 等[12]利用电子束辐射得到表面含氧空位的二氧化钛纳米棒并应用于光解水制氢研究。本文采用能量为0.1 MeV 的高能电子束(EBI)对TiO2纳米棒阵列的表面结构进行了修饰。结果表明,与原始TiO2相比,EBI-TiO2光阳极的光电化学(PEC)光解水制氢活性明显增强,这是由于EBI在TiO2纳米棒阵列表面引入了丰富氧空位(VO)。通过控制吸收剂量可以方便得到不同表面VO的浓度,从而进一步影响PEC 性能。改性后的TiO2在没有掺杂或助催化剂的情况下,光电流密度明显提高,约为原始TiO2的2倍。该项工作系统地研究了EBI辐射改性对光催化材料中电荷分离和迁移的影响机制。WO3(2.5~2.8 eV)具有一定的可见光响应能力和较长的空穴传输距离,是一种具有应用潜力的光电转化半导体材料。在电化学N2固定中,Du等[13]利用γ射线辐照调节WO3纳米片的界面电子态,用于抑制析氢反应。γ射线辐射在WO3纳米片表面构造缺陷结构,即氧空位,利用高角度环形暗场扫描透射电子显微镜(HAADF-STEM)在原子尺度上清晰地观察到这些表面缺陷结构。
4.2 非金属聚合物空位缺陷型半导体纳米材料
随着半导体材料研究范围的不断拓宽,非金属聚合物半导体研究成为热点。2009 年,Wang等[57]首次将g-C3N4作为一种半导体催化剂,用于光解水制氢。这一突破性进展将g-C3N4研究推向新的高潮,有关g-C3N4研究层出不穷。目前文献报道的利用化学法在g-C3N4引入空位,反应条件苛刻,只能单一地引入C空位或是N空位,同时还会引入杂质元素。利用辐射法引入空位缺陷,g-C3N4放入氦离子辐射场中,具有一定能量的He+将经过一系列的碰撞过程而逐渐损失能量,而靶原子会从晶格位置射出,留下空位。在经历系列的级联碰撞过程后,由于离子辐照的非化学选择性,石墨相氮化碳中将同时引入C、N 空位[10]。Guo 等[10]用离子辐照技术实现了石墨相氮化碳的缺陷控制形成。通过氦离子辐照,实现了C、N空位的同时引入,并通过控制吸收剂量,可以控制引入的空位缺陷含量,从而实现了光催化产氢性能的优化提高。通过不同注量的He+(总剂量:8.625×1013cm-2、17.250×1013cm-2、34.500×1013cm-2、86.250×1013cm-2)注入到涂覆在FTO上的石墨相氮化碳纳米片中,制备出了具有一系列空位浓度的石墨相氮化碳纳米片。采用XPS、EPR表明C、N空位成功引入,同时进行PEC 测试和产氢性能测试,结果表明,中等空位浓度的样品的光催化产氢量是原始石墨相氮化碳纳米片(对照)的2.7倍,表现出最优的性能。DFT理论计算显示,C空位的引入导致了石墨相氮化碳的带隙缩减,从而帮助提高可见光吸收,而N 空位则引入了一个缺陷能级。因此,C、N空位缺陷共掺杂确实能够有效帮助提高石墨相氮化碳的光电催化和光催化产氢性能。该部分研究表明,离子辐照是一种有效提高二维材料光电催化和光催化水分解性能的方法(图5(Ⅱ))。本方法也适用于其他半导体光催化剂、能源转化和材料研究领域。

图5(I)γ射线辐射诱导锐钛矿TiO2产生氧空位和Ti3+缺陷并高效光催化降解有机污染物[14];(Ⅱ)可控He+离子辐照C/N空位协同增强g-C3N4纳米片的可见光驱动析氢[10]Fig.5 (I)γ-ray induced formation of oxygen vacancies and Ti3+defects in anatase TiO2 for efficient photocatalytic organic pollutant degradation[14];(Ⅱ)C/N Vacancy Co-enhanced visible-light-driven hydrogen evolution of g-C3N4 nanosheets through controlled He+ion irradiation[10]
5 影响半导体纳米材料形成过程的因素
影响半导体纳米材料辐射合成的主要因素:溶解氧、pH、稳定剂、络合剂、吸收剂量和剂量率及载体和纳米复合材料。
溶液中有溶解氧存在时,水合电子和H 自由基转化为HO2和O2-离子自由基。另外,溶解氧可以直接氧化许多金属单质。因此,溶液辐照必须通入氮气或氩气进行通气排氧。通常情况下,在样品辐照前使用简单的通气排氧,并不测定残余氧浓度。贵金属,尤其是银离子的辐射还原研究最多。虽然银离子很容易被辐射还原成由零价原子组成的胶体纳米团簇,但它们往往相当不稳定,必须在辐照前对溶液进行彻底的脱氧。
由于半导体纳米粒子辐射合成的第一步通常是辐射还原,因此通常需要将辐射溶液的pH 提高,促进辐射还原过程。5~50 nm铜纳米粒子的辐射诱导合成[36],是在pH为5~9的范围内,对硫酸铜、异丙醇和PVA的脱氧水溶液进行电子束辐照。通过辐照六氯铂酸、聚丙烯酸和异丙醇的脱氧水溶液(NaOH 将pH 调整为4.5),对铂离子进行辐射还原,得到2.5~35 nm的Pt纳米粒子[58]。
pH 的改变对氧化物纳米颗粒的形貌和尺寸大小、氧化物的化学计量比[40]有显著影响。在硫酸铜、异丙醇、表面活性剂(SDS)的醋酸盐缓冲液(pH=4.0~4.5)中,采用γ 射线法合成了纳米晶氧化亚铜,粒径为14 nm。对比没有在缓冲溶液进行的反应,pH 反应后降低至3.0~3.5,得到的产物为铜和氧化亚铜的混合物。3 个竞争反应同时存在:辐射还原;亚铜离子的歧化反应;氢氧化亚铜分解为氧化亚铜。在醋酸盐缓冲溶液及较高的pH值下,只会发生氢氧化亚铜形成过程,然后迅速分解为氧化亚铜。将制备的Fe(OH)3或FeOOH 溶胶在pH=5 时进行γ 射线辐照。观察到菱形三氧化二铁α-Fe2O3(pH=3~5)[40]。
聚合物稳定剂(如十二烷基硫酸钠(SDS)[59-60]、聚乙烯醇[61-63]、壳聚糖[64-65]、牛血清白蛋白[66]或聚乙烯吡咯烷酮)的存在会显著影响纳米粒子的化学稳定性、尺寸分布和所需的吸收剂量。络合剂(包括乙二胺四乙酸(EDTA)、柠檬酸、十二烷基硫酸钠等)的添加是另外一个影响辐射合成纳米粒子尺寸大小及形貌的因素。
除了研究聚合物稳定剂影响外,还有一些研究侧重于探讨剂量和/或剂量率对纳米颗粒大小的影响。分别对γ射线、电子加速器、C6+离子电离辐射进行研究,发现剂量(率)对粒径影响是随着剂量(率)的增加,粒径减小,粒径分布变窄,这种变化规律与辐射化学产额有关[67]。辐射化学产额是电离辐射与物质相互作用的化学效能(效果大小),为每吸收100 eV能量所引起变化的分子数表示,单位为mol·J-1。
负载到材料的纳米颗粒具有宽pH 稳定性。与合成纳米颗粒一样,辐射合成法的固有优势是使用无害且廉价的水做试剂,合成尺寸和分布可控的纳米颗粒[68]。与上述合成纳米颗粒不同的是,载体上的纳米颗粒可以从溶液中简单分离出来,干燥后直接使用。金属纳米粒子可以很容易地通过辐射还原沉积在各种固体载体上[68]。半导体载体包括各种材料,如二氧化钛[52]、氧化铝[69]、氧化铈[70]、或氧化铁[54]。
6 结论
总结了不同种类半导体纳米材料的电离辐射合成。辐照体系主要由前驱体、有机溶剂、稳定剂及络合剂组成。基本原理是利用电离辐射水溶液,产生辐解产物与前驱体化合物的反应。由于半导体纳米粒子辐射合成的第一步通常是辐射还原,溶解氧是半导体纳米材料合成的关键因素,通常需要通气排氧;其次,通常需要提高辐照原溶液的pH,方可得到性能优越的半导体纳米材料。稳定剂、络合剂、吸收剂量和剂量率可用于调控半导体纳米粒子的大小和形貌,一般随着吸收剂量(率)的增大,纳米粒子的尺寸变小,且分布变窄。半导体纳米粒子的电离辐射合成一般在室温下进行,操作简单方便,能耗低,可制备多种半导体纳米材料,从金属氧(硫、硒)化物、聚合物、贵金属沉积到空位缺陷半导体纳米粒子。
目前,应用电离辐射合成半导体纳米粒子的方法成为研究热点,但距工业化应用还存在一定距离。(1)电离辐射合成半导体纳米粒子机理研究尚不清楚,目前,电离辐射合成纳米粒子过程中间体难以测定,导致机理研究困难。采用脉冲辐射技术可初步研究纳米颗粒的反应和形成机理。(2)电离辐射合成半导体纳米粒子缺陷研究有待完善。高能射线由于能量强,穿透力强,可能会导致半导体纳米粒子的缺陷。一部分缺陷可能提高纳米粒子的性能,然而,过量的缺陷可能降低纳米粒子的性能。因此研究半导体纳米粒子缺陷将推动该领域的发展。(3)应用电离辐射合成单原子分散的贵金属沉积半导体纳米材料亟待发展。应用化学法得到的贵金属纳米颗粒一般情况下易于团聚,形成团簇和纳米颗粒。通过电离辐射在半导体纳米材料上负载单原子分散的贵金属催化剂将具有一定研究价值。辐射方法将有望对纳米技术做出重大的贡献,并且辐射诱导合成的纳米颗粒和纳米材料将迎来蓬勃发展。
作者贡献说明赵彩凤是本综述文献收集的执行人,完成文献分析,论文初稿的写作;杨亚辉、罗琳、于卫东参与综述设计和文献归纳;谢洪科、张乐平、张勇、周毅吉、武小芬、邵颖参与文献资料的讨论;邵赛、王克勤是项目的构思者及负责人,指导综述的撰写与修改。全体作者都阅读并同意最终的文本。

