色氨酸和苏氨酸衍生化红曲红色素的稳定性研究
何贝贝,刘彩,陈莎,高梦祥,李利
(长江大学生命科学学院,湖北 荆州 434025)
红曲色素是由红曲菌发酵产生的一种安全的天然色素,已作为着色剂列入GB 2760—2014《食品安全国家标准食品添加剂使用标准》,允许用于乳、糕点、饼干、熟肉制品等食品类别中。红曲色素是一种混合物,包括红、黄、橙3类色素组分,其中红曲橙色素中的红斑红曲素和红曲玉红素化学性质比较活泼,可与伯胺发生亲氨基反应,生成红曲橙色素衍生物(orange Monascus pigment derivates,OMPDs)[1-3]。OMPDs在颜色上为红色,属于红曲红色素范畴[4]。目前报道的49种不同结构的天然红曲红色素化合物中,至少有26种为与氨基酸发生反应而生成的OMPDs[5],这类红曲红色素称之为氨基酸衍生化的红曲红色素。
研究表明,氨基酸衍生化的红曲红色素具有多种生物活性[6-9],在食品方面具有很好的应用前景。其中,色氨酸衍生化的红曲红色素(red Monascus pigments derived with Trp,Trp-RMPs)和苏氨酸衍生化的红曲红色素(red Monascus pigments derived with Thr,Thr-RMPs)对肥胖的预防和干预功效显著,可用于开发减肥功能性食品[9-14]。肥胖是一种以脂肪在体内过度积累为特征的疾病,在全世界范围内普遍存在并呈快速增加的趋势,能引发糖尿病、高血压、心血管疾病及小肠癌等多种疾病[9,14]。研究表明,抑制脂质代谢过程中的关键酶是降脂减肥的有效途径之一,如抑制脂肪酶可减少肠道对膳食脂肪的水解吸收,抑制羟甲基戊二酸单酰辅酶A(3-hydroxy-3-methyl glutaryl coenzyme A,HMG-CoA)还原酶能减少体内胆固醇的合成[10-13,15]。Trp-RMPs和 Thr-RMPs通过参与不同的脂质代谢途径,达到预防和干预肥胖的效果,其中,Trp-RMPs具有较高的脂肪酶抑制活性,能使肥胖小鼠的体重、皮下脂肪及肝脏脂肪含量等显著减少[10],而Thr-RMPs具有较高的HMG-CoA还原酶抑制活性,能显著降低C57BL/6小鼠血清中的总胆固醇水平和动脉粥样硬化指数[12]。
在功能性食品中,食品作为功效成分的载体,其pH值范围多为3.5~7.0[16],在加工过程中,通常需要巴氏杀菌等热处理过程。而红曲色素作为一种天然色素,容易受pH值、温度等环境因素影响而发生颜色改变或降解[2,17-20]。为了解 Trp-RMPs和 Thr-RMPs两种红曲色素对pH值和温度的耐受性,本研究通过体外衍生化反应,用化学半合成的方法制备Trp-RMPs和Thr-RMPs,研究其在常见食品pH值范围内的pH稳定性和热稳定性,为富含Trp-RMPs和Thr-RMPs的减肥功能性食品的开发提供参考。
1 材料与方法
1.1 材料与试剂
红曲橙色素:长江大学食品微生物及其产品开发实验室提供,主要含红斑红曲素和红曲玉红素,二者含量比为1∶1.25;苏氨酸、色氨酸(均为分析纯):天津市福晨化学试剂厂;甲醇、甲酸、磷酸二氢钾、磷酸氢二钠(均为分析纯):国药集团化学试剂有限公司;乙腈(色谱纯):美国天地有限公司;C18固相萃取柱:天津市宝津科技有限公司。
1.2 仪器与设备
紫外可见分光光度计(TU1900):北京普析通用仪器有限责任公司;高效液相色谱仪(LC1200):美国安捷伦公司;液相色谱质谱联用仪(TripleTOF 5600+):美国AB Sciex公司。
1.3 方法
1.3.1 Trp-RMPs和Thr-RMPs的制备
色氨酸和苏氨酸与红曲橙色素的亲氨基反应参照刘彩等[19]的方法,反应体系含50%甲醇,8 mmol/L色氨酸或苏氨酸,0.1 mg/mL红曲橙色素,反应条件为30℃、250 r/min、2 h。反应结束后,加入去离子水,将反应液中甲醇调至20%,用C18固相萃取柱进行净化,最终用90%甲醇洗脱,洗脱液在40℃、100 r/min条件下进行旋转蒸发干燥、称重,加入一定量的去离子水溶解,制备2 g/L色素衍生物的水溶液。该色素衍生物于4℃避光保存备用,临用前用去离子水稀释至色价(2.0±0.1)U/mL,色价的计算参考刘彩等[19]的方法用最大吸收波长处的吸光值A计算,色价/(U/mL)=A×稀释倍数。
1.3.2 Trp-RMPs和Thr-RMPs的高效液相色谱分析
红曲色素的高效液相色谱(high performance liquid chromatography,HLPC)分析条件参照刘彩等[19]的方法,具体如下。
色谱柱:Inertsil ODS-3(250 mm× 4.6 mm,5 μm);柱温:30 ℃;进样量:10 μL;检测器:二极管阵列检测器(diode array detector,DAD);检测波长:300nm~600nm;监测波长:380、470、520nm。流动相A相:乙腈(含0.1%甲酸),B相:酸水(含0.1%甲酸);梯度洗脱条件为0 min~ 18 min,15%A ~ 80%A;18 min ~ 30 min,80%A;30 min ~ 31 min,80%A ~ 15%A;31 min ~ 40 min,15%A,流速:1.0 mL/min。
1.3.3 Trp-RMPs和Thr-RMPs的液相色谱质谱联用分析
红曲色素的液相色谱质谱联用(liquid chromatography/mass spectrometry,LC/MS)分析条件参照刘彩等[19]的方法,具体如下。
色谱柱:Kinetex 2.6 μm F5(100 mm × 2.1 mm);柱温:30℃;流动相:A相为酸水(含0.1%甲酸),B相为乙腈;梯度洗脱条件:0 min~1 min,95%A;1 min~8 min,95%A~15%A;8 min ~ 9 min,15%A;9 min ~9.1 min,15%A ~ 95%A;9.1 min ~ 11 min,95%A;流速:0.2 mL/min;进样量:10 μL;DAD 检测波长:300 nm ~600 nm;离子源:电喷雾电离,正离子模式;扫描范围:质荷比(m/z)100~ 1 000;电喷雾电压:5 500 V;离子源温度:550℃;雾化气压力379kPa;辅助气压力379kPa;气帘气压力172 kPa。
1.3.4 不同pH值条件下Trp-RMPs和Thr-RMPs的颜色变化分析
将色价为(2.0±0.1)U/mL的Trp-RMPs或Thr-RMPs水溶液与0.1 mol/L的柠檬酸-磷酸盐缓冲液(pH 3、pH 5、pH 7)以体积比为1∶1的比例混合,25℃避光放置10 min,观察溶液颜色的变化情况,并在350 nm~500 nm范围内扫描紫外可见吸收光谱,分析光谱的形状和最大吸收波长的变化情况。
1.3.5 不同pH值条件下Trp-RMPs和Thr-RMPs的热稳定性分析
将色价为(2.0±0.1)U/mL的Trp-RMPs或Thr-RMPs水溶液与0.1 mol/L的柠檬酸-磷酸盐缓冲溶液(pH 3、pH 5、pH 7)以体积比为 1∶1 的比例混合,置于密封玻璃瓶中,分别在40、60、80℃下避光加热处理,根据降解速度间隔取样,其中40℃时间隔5 h或10 h取样,60℃时间隔1 h或2 h取样,80℃时间隔0.5 h或1 h取样。测定红曲红色素的浓度和残留率。
采用分光光度法测定红曲红色素浓度。配制系列浓度(5 mg/L~30 mg/L)的Trp-RMPs或 Thr-RMPs水溶液,在最大吸收波长处测定吸光值A,以浓度C为横坐标,以吸光值A为纵坐标绘制标准曲线,得到线性回归方程。根据待测样品的吸光值,通过线性回归方程计算Trp-RMPs和Thr-RMPs的浓度。

式中:Ct为样品热处理t小时后和处理前的红曲红色素浓度,mg/L;C0为样品处理前的红曲红色素浓度,mg/L。
根据红曲红色素的残留率,计算一级动力学反应的速率常数(k)和半衰期(t1/2)公式如下。

式中:t为热处理时间,h;Ct为样品热处理t小时后和处理前的红曲红色素浓度,mg/L;C0为样品处理前的红曲红色素浓度,mg/L。
1.3.6 数据分析
试验均重复3次,取其平均值,采用Excel 2010进行数据分析。
2 结果与分析
2.1 Trp-RMPs和Thr-RMPs的衍生化制备及分析
在pH 7.0条件下将红曲橙色素分别与色氨酸和苏氨酸进行亲氨基反应,反应完成后溶液的颜色由橙色变成亮红色,其HPLC检测结果见图1。
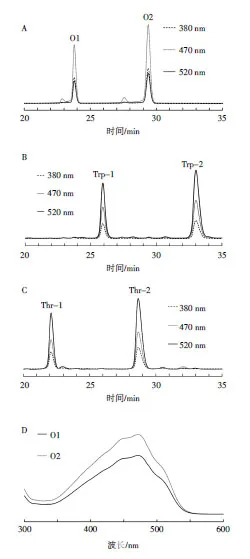
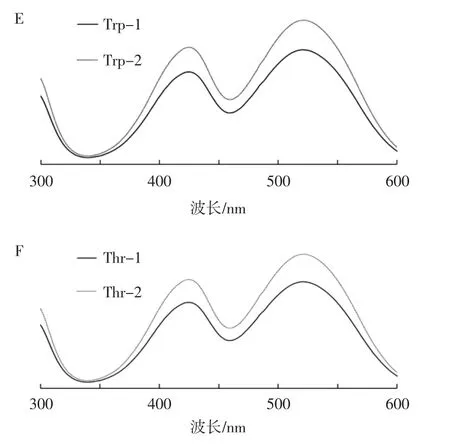
图1 红曲橙色素及其与色氨酸、苏氨酸反应产物的HPLC分析结果Fig.1 The HPLC results of orange Monascus pigments and theirs reaction products with Trp and Thr
由图1可知,色氨酸衍生化的红曲色素溶液中检出了2种主要组分Trp-1和Trp-2(图1B),苏氨酸衍生化的红曲色素溶液中检出了2种主要组分Thr-1和Thr-2(图 1C),在 300 nm~600 nm 波长范围内上述4种组分最大吸收峰均在520 nm左右(图1E和图1F),与观察到的溶液颜色相符。
进一步对色氨酸和苏氨酸衍生化的红曲色素溶液进行了液相色谱质谱联用分析,结果见图2。

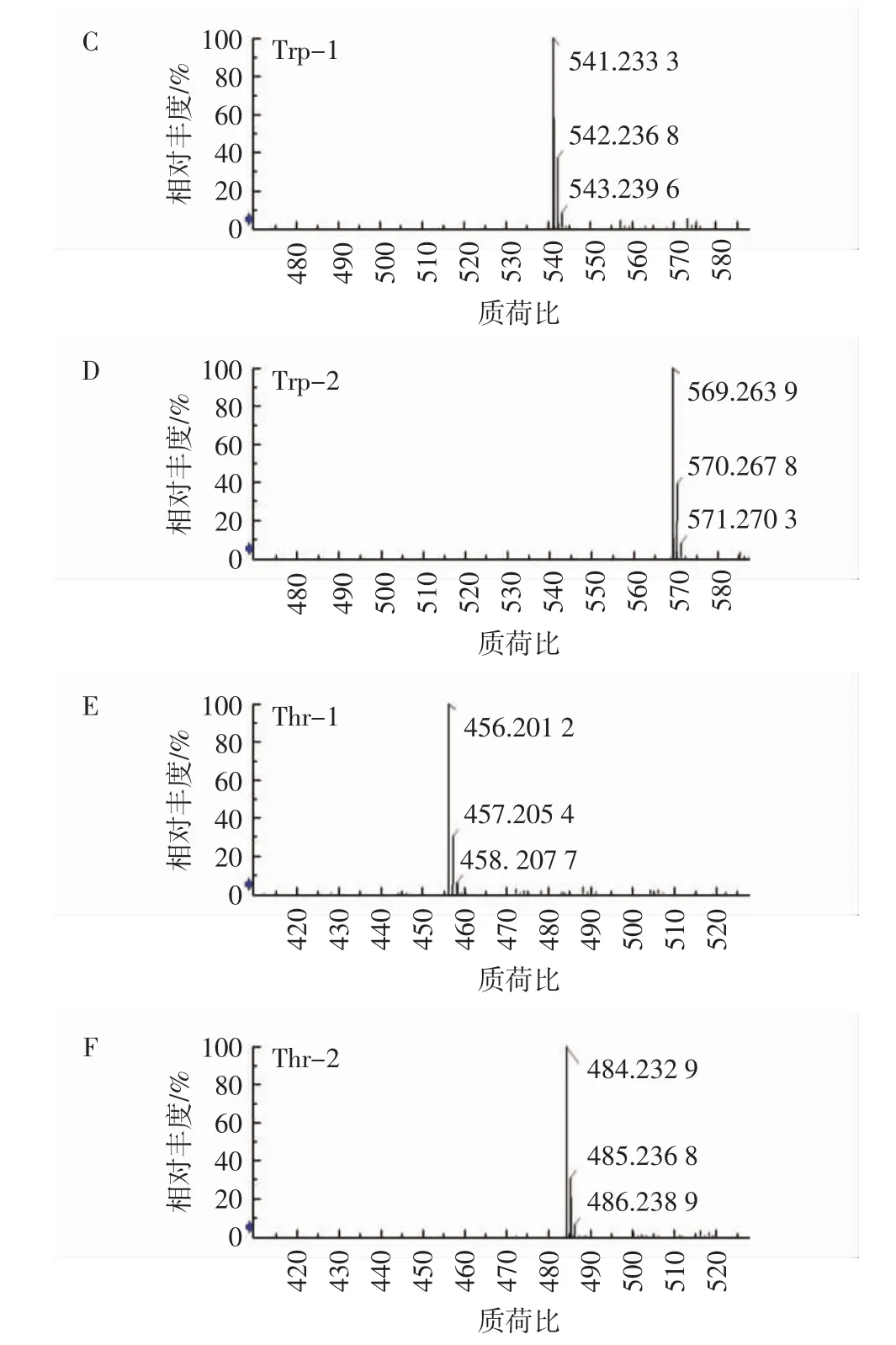
图2 红曲橙色素及其与色氨酸、苏氨酸反应产物中各色素组分的液相色谱质谱联用分析结果Fig.2 The liquid chromatography-mass spectrometry results of orange Monascus pigments and their reaction products with Trp and Thr
由图2C和图2D可知,Trp-1和Trp-2对应的准分子离子[M+H]+峰分别为(m/z)541和569。由图2E和图2F可知,Thr-1和Thr-2对应的准分子离子[M+H]+峰分别为(m/z)456 和 484。
根据亲氨基反应原理[4,21],红斑红曲素(O1)、红曲玉红素(O2)与色氨酸、苏氨酸反应产物的化学结构和分子量见图3。
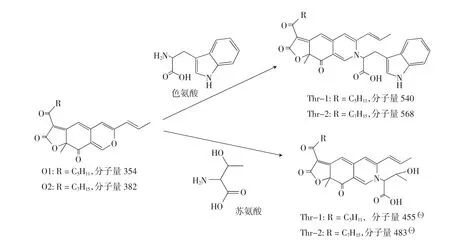
图3 色氨酸、苏氨酸同红斑红曲素(O1)、红曲玉红素(O2)的亲氨基反应产物Fig.3 The products by aminophilic reaction between Trp,Thr and rubropunctain(O1),monascorubrin(O2)
由图3可知,色氨酸与红斑红曲素(O1)、红曲玉红素(O2)的反应产物Trp-1和Trp-2,以及苏氨酸与红斑红曲素(O1)、红曲玉红素(O2)的反应产物Thr-1和Thr-2的分子量与反应液的质谱检测结果相一致(图2),表明该体外亲氨基反应成功地合成了色氨酸衍生化的红曲红色素和苏氨酸衍生化的红曲红色素。
2.2 pH值对Trp-RMPs和Thr-RMPs颜色的影响
为了解Trp-RMPs和Thr-RMPs两种红曲红色素的pH值稳定性,对其在不同pH值条件下的颜色特征进行分析,结果见图4。

图4 Trp-RMPs和Thr-RMPs在不同pH值下的颜色和紫外可见吸收光谱图Fig.4 The ultraviolet-visible spectrum of Trp-RMPs and Thr-RMPs at different pH and color
研究发现,2种主要红曲红色素组分红斑红曲胺和红斑玉红胺的pH值稳定性较差,颜色会随着pH值的变化而发生改变,在pH值小于4时,颜色为紫红色,最大吸收波长为530 nm;在pH值大于6时,颜色为红色,最大吸收波长为502 nm[18]。由图4可知,Trp-RMPs和Thr-RMPs在pH 3~pH 7范围内感官颜色未发生明显变化,均为亮红色;紫外可见吸收光谱的形状和最大吸收波也未发生明显改变,与感官颜色一致。结果表明,Trp-RMPs和Thr-RMPs颜色的pH稳定性优于2种主要红曲红色素组分红斑红曲胺和红斑玉红胺,在常见食品的pH值范围内颜色稳定一致。
2.3 Trp-RMPs和Thr-RMPs在不同pH值下的热稳定性
为进一步研究Trp-RMPs和Thr-RMPs在pH 3~pH 7范围内的热稳定性,其在40、60、80℃热降解曲线见图5~图7,半衰期(t1/2)见图8。

图5 40℃时Trp-RMPs和Thr-RMPs的热降解曲线Fig.5 Thermal degradation curve of Trp-RMPs and Thr-RMPs at 40℃
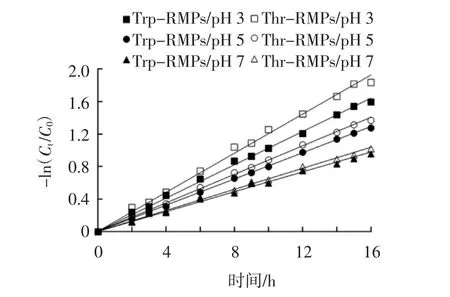
图6 60℃时Trp-RMPs和Thr-RMPs的热降解曲线Fig.6 Thermal degradation curve of Trp-RMPs and Thr-RMPs at 60℃
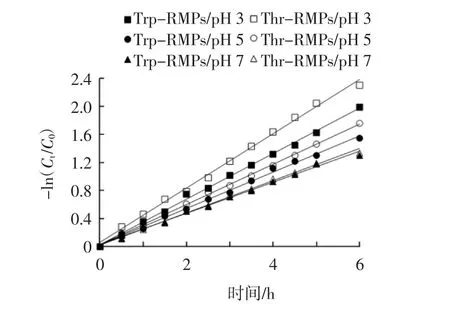
图7 80℃时Trp-RMPs和Thr-RMPs的热降解曲线Fig.7 Thermal degradation curve of Trp-RMPs and Thr-RMPs at 80℃
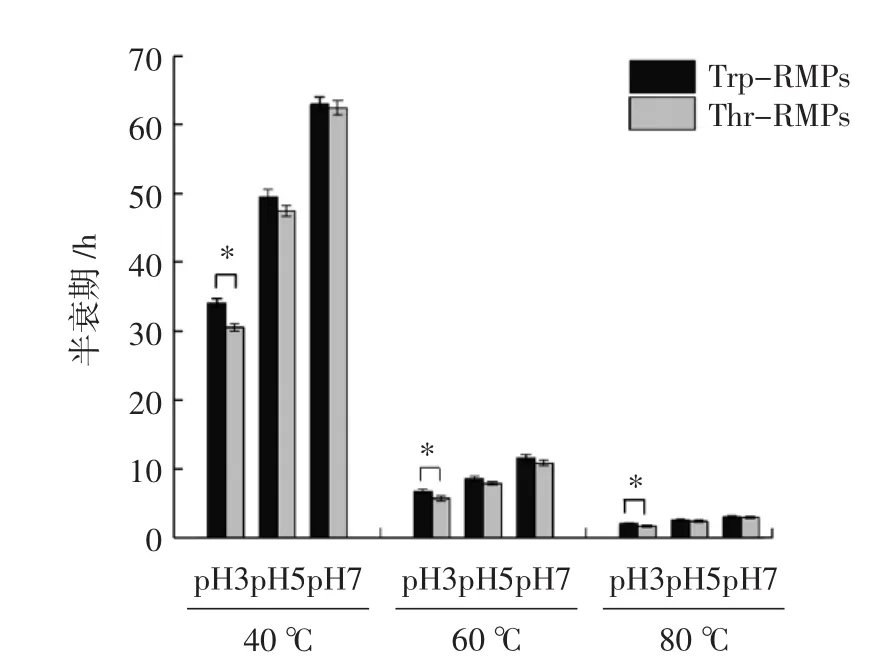
图8 Trp-RMPs和Thr-RMPs在不同pH值和不同温度下的半衰期(t1/2)Fig.8 The half-life of Trp-RMPs and Thr-RMPs at different pH and temperature
由图5~图7可知,在40、60、80℃的避光条件下加热处理,Trp-RMPs和Thr-RMPs会发生不同程度的褪色现象,色素的残留率随加热时间的延长而降低,-ln(Ct/C0)与时间 t呈现良好的线性关系(R2>0.976 4),说明Trp-RMPs和Thr-RMPs的热降解遵循一级反应动力学规律。
由图8可知,Trp-RMPs和Thr-RMPs的半衰期随着温度的升高而急剧下降。40℃时,Trp-RMPs在pH 3、pH 5和pH 7条件下的半衰期依次为34.15、49.51、63.01 h,Thr-RMPs在 pH 3、pH 5 和 pH 7 条件下的半衰期依次为30.54、47.48、62.44 h。当温度从40℃升高至60℃,Trp-RMPs在pH 3、pH 5和pH 7条件下的半衰期分别降低了80.32%、82.69%和81.64%,Thr-RMPs在pH 3、pH 5和pH 7条件下的半衰期分别降低了81.30%、83.38%和82.26%,当温度从40℃升高至80℃,Trp-RMPs在pH 3、pH 5和pH 7条件下的半衰期分别降低了93.91%、94.85%和92.21%,Thr-RMPs在pH 3、pH 5和pH 7条件下的半衰期分别降低了94.47%、95.03%和95.28%。结果表明,高温能加速Trp-RMPs和Thr-RMPs的降解,因此在加工和储藏过程,应避免长时间高温处理。
由图8可知,在相同温度下,Trp-RMPs和Thr-RMPs的半衰期均随着pH值的升高而呈增大趋势,表明pH值对Trp-RMPs和Thr-RMPs的热稳定性有较大影响,在pH 3~pH 7范围内,pH值越高,稳定性越好。pH值为3时,Trp-RMPs的半衰期显著大于Thr-RMPs(p<0.05),此时 Trp-RMPs比 Thr-RMPs更稳定;而在pH值为5和pH值为7时,Trp-RMPs和Thr-RMPs的半衰期无显著差异(p>0.05),二者的稳定性差异不大。
3 结论
利用亲氨基反应,在体外成功合成了两种红曲红色素衍生物:色氨酸衍生化的红曲红色素Trp-RMPs和苏氨酸衍生化的红曲红色素Thr-RMPs。Trp-RMPs和Thr-RMPs呈亮红色,在常见的食品pH值范围内,不随pH值的变化而发生颜色改变。Trp-RMPs和Thr-RMPs对热敏感,热降解符合一级反应动力学模型,40℃~80℃范围内半衰期随着温度的升高而急剧下降,在加工与储藏过程中应避免长时间高温处理。pH值对Trp-RMPs和Thr-RMPs热稳定性的影响显著,在pH 3~pH 7范围内,pH值越高,稳定性越好,更适合应用于弱酸性至中性的食品中。Trp-RMPs的热稳定性在pH 3时显著高于Thr-RMPs,而在pH 5~pH 7时Trp-RMPs和Thr-RMPs的稳定性相差不大。本研究结果可为为富含Trp-RMPs和Thr-RMPs的食品加工提供参考。