基于水热/溶剂热法制备不同形貌LiNi0.8Co0.1Mn0.1O2 锂离子电池正极材料
吴兆国,曹 骏,杨则恒
(合肥工业大学化学与化工学院,可控化学与材料化工安徽省重点实验室,安徽合肥 230009)
锂离子电池因具有高能量密度、 长循环寿命以及较好的安全稳定性,在便携式电器、电动汽车和智能电网存储等许多领域的应用越来越广泛[1-3]。镍钴锰酸锂三元正极材料因具有高的理论比容量而受到广泛关注[4-6]。 但是目前高镍三元正极材料的实际比容量和循环稳定性还难以满足日益发展的电动汽车行业的需求,阻碍了其在锂离子电池市场,特别是动力电池领域的推广应用。因此,如何提升高镍三元正极材料的放电比容量和提高其循环稳定性正成为当下的研究热门[7-8]。
水热法[9-10]制备工艺简单,以水为溶剂,将镍、钴、 锰盐按一定物质的量比配成溶液并加入适量的沉淀剂,在反应釜中加温加压即可生成反应产物。不同水热合成条件可能会对前驱体的晶体成核动力学产生很大的差异, 从而影响正极材料形成过程中晶体生长的主导方向, 最终对材料的电化学性能产生关键影响。水热法制备的正极材料结晶度高、位错密度小、晶体发育完善,因此放电比容量高,具有良好的电化学性能。 溶剂热法[11-12]是在水热法的基础上发展起来的, 与水热反应的不同之处在于所使用的溶剂为有机溶剂而不是水。 溶剂的表面张力改变以及生长环境变化会影响晶粒的成核速率和生长速率,从而形成细小的纳米颗粒,并聚集成球形二次颗粒。 PENG 等[13]以镍、钴、锰乙酸盐为原料,以过硫酸铵为氧化剂, 尿素作为表面活性剂维持溶液中碱性氛围,制备出特殊的纳米网状NCM 前驱体,再经过混锂煅烧得到LiNi1/3Co1/3Mn1/3O2正极材料。由于所制备的材料具有特殊的纳米网状结构,有利于Li+的脱嵌, 使得电化学性能得到提升,0.5C 电流密度下首圈放电比容量高达175 mA·h/g。 但引入表面活性剂,增加了实验所需控制的工艺参数,加大了制备的难度,不如直接对溶剂组分调整便捷。
本工作以六亚甲基四胺为沉淀剂, 分别采用水热和溶剂热法合成Ni0.8Co0.1Mn0.1(OH)2前驱体,再通过高温混锂煅烧获得LiNi0.8Co0.1Mn0.1O2正极材料。通过改变溶剂组分调节溶剂的表面张力控制一次颗粒成核速率和生长速率, 合成了两种形貌不同的Ni0.8Co0.1Mn0.1(OH)2前驱体,经混锂煅烧后得到两种不同形貌的LiNi0.8Co0.1Mn0.1O2正极材料。以水为溶剂合成了一次片状颗粒紧密堆积组成的长方体状LiNi0.8Co0.1Mn0.1O2正极材料,这种独特的结构能通过扩大电化学活性区域抑制Li/Ni 的无序性来增强正极材料的放电比容量和倍率性能。 以乙醇为溶剂合成了具有球形二次颗粒的LiNi0.8Co0.1Mn0.1O2正极材料,相较于其他形状的颗粒,多孔球形颗粒能够减小循环过程中颗粒的应力和应变,提升材料的结构稳定性,从而提高了锂离子电池循环稳定性与可逆性。
1 实验部分
1.1 LiNi0.8Co0.1Mn0.1O2 的制备
将镍、钴、锰乙酸盐按照 n(Ni)∶n(Co)∶n(Mn)=8∶1∶1加入到去离子水中, 在烧杯中配制体积为30 mL 浓度为0.1 mol/L 的过渡金属盐溶液,以六亚甲基四胺作为沉淀剂,将六亚甲基四胺与过渡金属盐按照物质的量比为2∶1 加入到烧杯中。 搅拌溶解之后,将混合溶液倒入50 mL 的聚四氟乙烯内胆中, 再将聚四氟乙烯内胆密封到不锈钢反应釜中,在恒温鼓风烘箱中于200 ℃水热反应12 h。 反应结束后冷却至室温,分别用去离子水和乙醇洗涤3 次除去杂质残留物,最后在 100 ℃条件下干燥 12 h 得到Ni0.8Co0.1Mn0.1(OH)2前驱体,记为 NCM-1。 类似地,将反应溶剂组成更换为体积比为1∶1 的乙醇与水混合溶液, 采用相同的反应条件制得Ni0.8Co0.1Mn0.1(OH)2前驱体,记为NCM-2。 再将反应溶剂更换为无水乙醇,重复上述反应制得 Ni0.8Co0.1Mn0.1(OH)2前驱体,记为NCM-3。
将Li2CO3与上述3 种前驱体按照物质的量比为1.05∶1 称量,并在研钵中充分研磨,然后在管式炉中于O2氛围下分2 步进行煅烧处理,首先以2 ℃/min的升温速率升温至 450 ℃恒温处理 6 h,再以2 ℃/min 的升温速率加热至750 ℃继续恒温处理15 h,得到黑色粉末状LiNi0.8Co0.1Mn0.1O2样品,由前驱体样品NCM-1、NCM-2 和NCM-3 经过上述步骤所制得产物分别记为LNCM-1、LNCM-2 和LNCM-3。
1.2 正极片的制作和电池组装
将制备的LiNi0.8Co0.1Mn0.1O2正极材料与导电剂乙炔黑、黏结剂PVDF(聚偏氟乙烯)按照质量比为8∶1∶1 在研钵中充分研磨混合,将混合物分散于NMP(1-甲基-2-吡咯烷酮)中制成浆料,用刮刀均匀地涂覆在铝箔集流体上。 将涂覆好的电极片在100 ℃真空烘箱中干燥12 h, 用切片机切成直径为12 mm的圆形正极片。 以金属锂为负极,电解液为1 mol/L LiPF6的碳酸乙烯酯+碳酸二甲酯(体积比1∶1)溶液,隔膜选用Celgard 2400 聚丙烯微孔膜。 在氩气气氛的手套箱内按照正极壳、垫片、正极极片、电解液、隔膜、电解液、锂片、垫片、弹簧片从下到上的顺序依次整齐放置组装CR2032 型扣式电池, 最后使用封口机封口。
1.3 样品表征与电池性能测试
采用SU8020 型场发射扫描电子显微镜(FESEM)测试样品的形貌和微观结构;X′PERT PRO MPD 型X 射线衍射仪(XRD)仪对测试样品进行物相分析,Cu Kα 辐射,扫描速度为 4(°)/min,2θ=10°~80°;Agilent 7500 型电感耦合等离子质谱仪(ICPMS)测试样品的元素组成;BTS-5 V/10 mA 型充放电测试仪测试电池充放电性能, 电压窗口为2.8~4.3 V;CHI 660D 型电化学工作站测试电池的循环伏安曲线和交流阻抗。定义电池充放电倍率1C=180 mA/g。
2 结果与讨论
2.1 结构与形貌表征
图1a 是采用不同溶剂制备的 3 种LiNi0.8Co0.1Mn0.1O2正极材料 XRD 谱图。 由图 1a 可见,3 种 LiNi0.8Co0.1Mn0.1O2材料的 XRD 谱图都具有典型的α-NaFeO2六方层状晶体结构, 属R3m 空间群。 因为其中镍含量较高,所以样品的衍射峰与LiNiO2的标准卡片(PDF#74-0919)的特征峰基本吻合,无杂质峰出现。 图 1b~1c 展示了(006)/(102)以及(108)/(110)两组峰的局部放大图,可以清楚看到明显分裂的衍射峰,这说明所制备的样品具有完善的层状结构。 3 种样品的晶胞参数计算结果见表 1,晶格参数c 与 a 的比值也可以反映层状结构完善情况,通常认为c/a≥4.9 表明结晶程度和发育程度良好,由样品 LNCM-1(4.942 3)、LNCM-2(4.942 1)和 LNCM-3(4.933 6)的 c/a 值可以看出3 种样品的晶体过渡金属原子的平均层间距,LNCM-1(c=1.419 21 nm)拥有最大的离子层间距,这会更有利于Li+的嵌入和脱出,这预示LNCM-1 会具有比其他两种材料更高的初始容量[14]。 (003)和(104)衍射峰的强度比可以反映材料的锂镍混排程度,如果 I(003)/I(104)<1.2,则表明材料的锂镍混 排 严重[15-16]。 表 1 显示样品 LNCM-1(1.3827)、LNCM-2(1.3785)和LNCM-3(1.3726)的 I(003)/I(104)均大于 1.2,这表明3 种样品的锂镍混排程度都比较低, 有利于发挥材料的电化学性能。
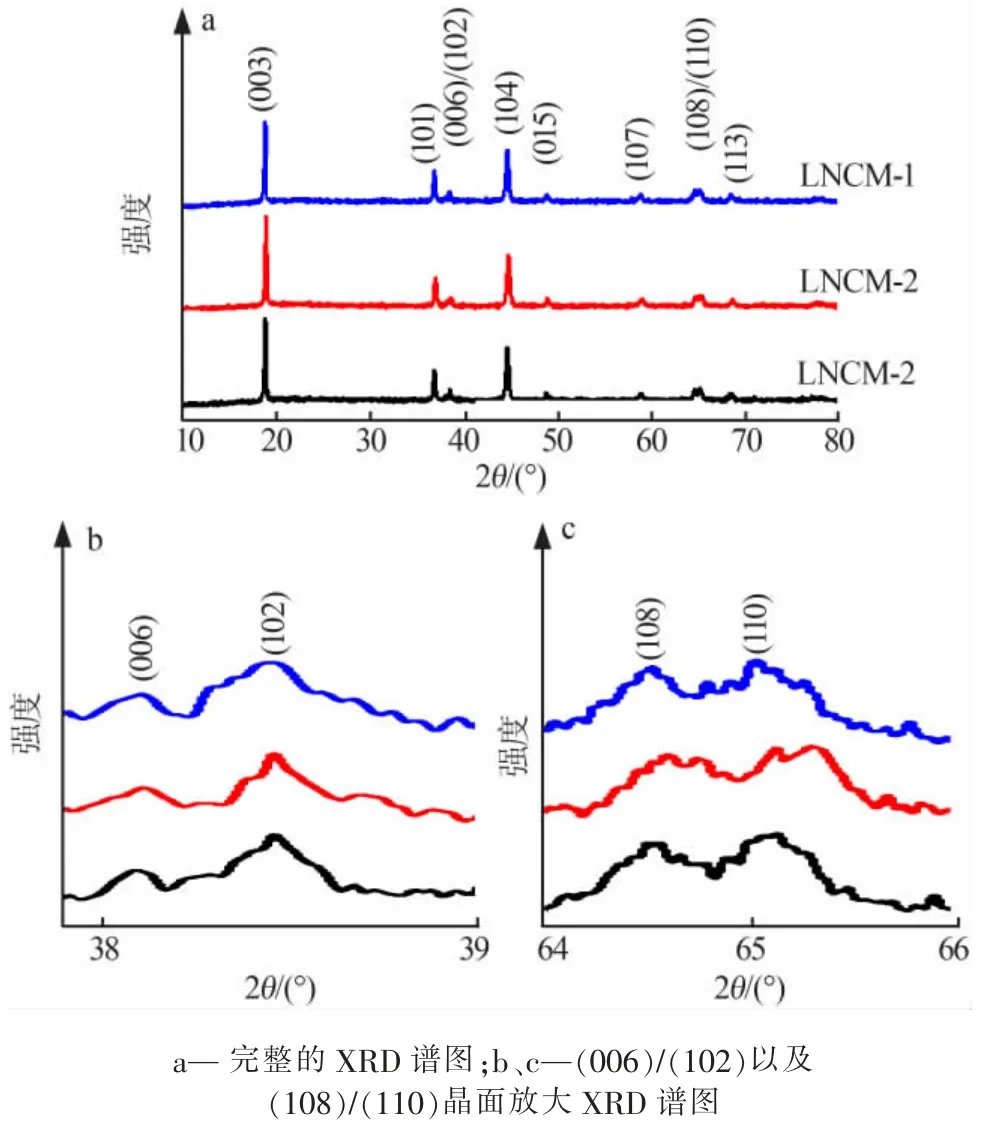
图1 不同溶剂制备的LiNi0.8Co0.1Mn0.1O2 正极材料XRD 谱图Fig.1 XRD patterns of LiNi0.8Co0.1Mn0.1O2 cathode materials prepared in different solvents

表1 不同溶剂制备的LiNi0.8Co0.1Mn0.1O2 正极材料的晶胞参数Table 1 Lattice parameters of different LiNi0.8Co0.1Mn0.1O2 cathode materials in different solvents
图2a~2b 为所合成的NCM-1 前驱体颗粒的FESEM 照片。 由图 2a~2b 可见,在溶剂为去离子水条件下获得的NCM-1 样品是由一次片状颗粒紧密堆积组成的长方体状二次颗粒,颗粒大小较均匀,宽度约为 1 μm,长度约为 2 μm。 图 2c~2d 为乙醇水混合溶液条件下所合成NCM-2 样品的FESEM 照片。由图2c~2d 可见,NCM-2 前驱体是由一次片状颗粒紧密堆积组成的橄榄球形二次颗粒,颗粒大小比较均匀,直径为 1~2 μm,长度为 2~4 μm,相比于NCM-1 前驱体颗粒,一次颗粒片有所增厚,且二次颗粒也明显从长方体状向橄榄球形变化。 图2e~2f为溶剂为无水乙醇条件下所合成的NCM-3 前驱体颗粒的 FESEM 照片, 相比 NCM-1 和 NCM-2 前驱体颗粒,NCM-3 前驱体是由许多一次纳米小颗粒紧密堆积组成球形二次颗粒,直径为2~4 μm。

图2 Ni0.8Co0.1Mn0.1(OH)2 前驱体的 FESEM 照片Fig.2 FESEM images of Ni0.8Co0.1Mn0.1(OH)2 precursor
将溶剂从水更换为乙醇后,由于乙醇具有非常低的介电常数,能有效地降低溶液的表面张力(20 ℃条件下,100 mL 水的表面张力是72.75×10-3N/m,乙醇为22.32×10-3N/m), 表面张力的改变影响一次颗粒的成核速率和生长速率。 在溶剂为去离子水的条件下,先形成大量的纳米片,随后初级粒子自组装成长方体二次颗粒。 当溶剂改变为乙醇时,由于表面张力改变导致的成核速率大大提高,瞬间生成大量的Ni0.8Co0.1Mn0.1(OH)2纳米晶核,有利于小粒径的Ni0.8Co0.1Mn0.1(OH)2一次颗粒的形成,这些一次颗粒随后聚集形成了球形Ni0.8Co0.1Mn0.1(OH)2二次颗粒。控制溶剂组分为乙醇与水体积比为1∶1 时, 此时溶剂表面张力介于纯水溶剂和乙醇溶剂之间, 所得到的产物也呈中间状态,此时Ni0.8Co0.1Mn0.1(OH)2一次颗粒纳米片厚度有所增大,自组装形成的二次颗粒也变为橄榄球形。
图3 为 NCM-1、NCM-2 和 NCM-3 前驱体样品经过混锂煅烧获得的产物 LNCM-1、LNCM-2 和LNCM-3 材料的 FESEM 照片。 由图 3 可以看出,经过混锂煅烧之后, 产物基本保持着前驱体颗粒的形貌特征, 但是经过前驱体的脱水转化和混锂煅烧过程,产物都呈现一定的多孔结构,这有利于电解液扩散,促进锂离子传输。

图3 不同溶剂制备的LiNi0.8Co0.1Mn0.1O2 正极材料的FESEM 照片Fig.3 FESEM images of the LiNi0.8Co0.1Mn0.1O2 cathode materials in different solvents
为了准确地分析所制备3 种样品的化学组成,采用电感耦合等离子质谱仪(ICP-MS)测试了3 种样品的元素组成,所得结果如表2 所示。 ICP-MS 测试结果表明,所制备的 LNCM 样品中 Ni、Co、Mn 3 种元素物质的量比非常接近(8∶1∶1),符合设计要求的总体元素的物质的量比。

表2 不同LNCM 正极材料的ICP-MS 测试结果Table 2 ICP-MS testing results of different LNCM cathode materials
2.2 电化学性能
对所制备的LNCM 材料组装的CR2032 型扣式电池进行电化学性能测试,测试条件为25 ℃、电化学平台为2.8~4.3 V,循环性能测试结果如图4 所示。LNCM-1、LNCM-2 和 LNCM-3 在 0.5 C 的初始放电比容量分别为 189.70、182.95、178.65 mA·h/g。 相较于其他两种材料,由片状一次颗粒紧密堆积成的长方体状LNCM-1 颗粒具有更高的初始放电比容量,这是因为其具有更大的离子层间距,有利于Li+的嵌入和脱出。 在 0.5C 下循环 200 次后,LNCM-1、LNCM-2 和 LNCM-3 的比容量衰减到 132.26、151.13、168.92 mA·h/g,容量保持率分别为 69.72%、82.93%和94.55%。 可以看出,LNCM-3 的容量保持率明显高于另外两种材料, 循环性能的提高是由于多孔球形颗粒相较于其他形状的颗粒能够减小循环过程中颗粒的应力和应变,提升材料的结构稳定性,因为球形颗粒一侧的局部Jahn-Teller 扭曲可以在颗粒的相反侧被相同的扭曲所抵消[17]。
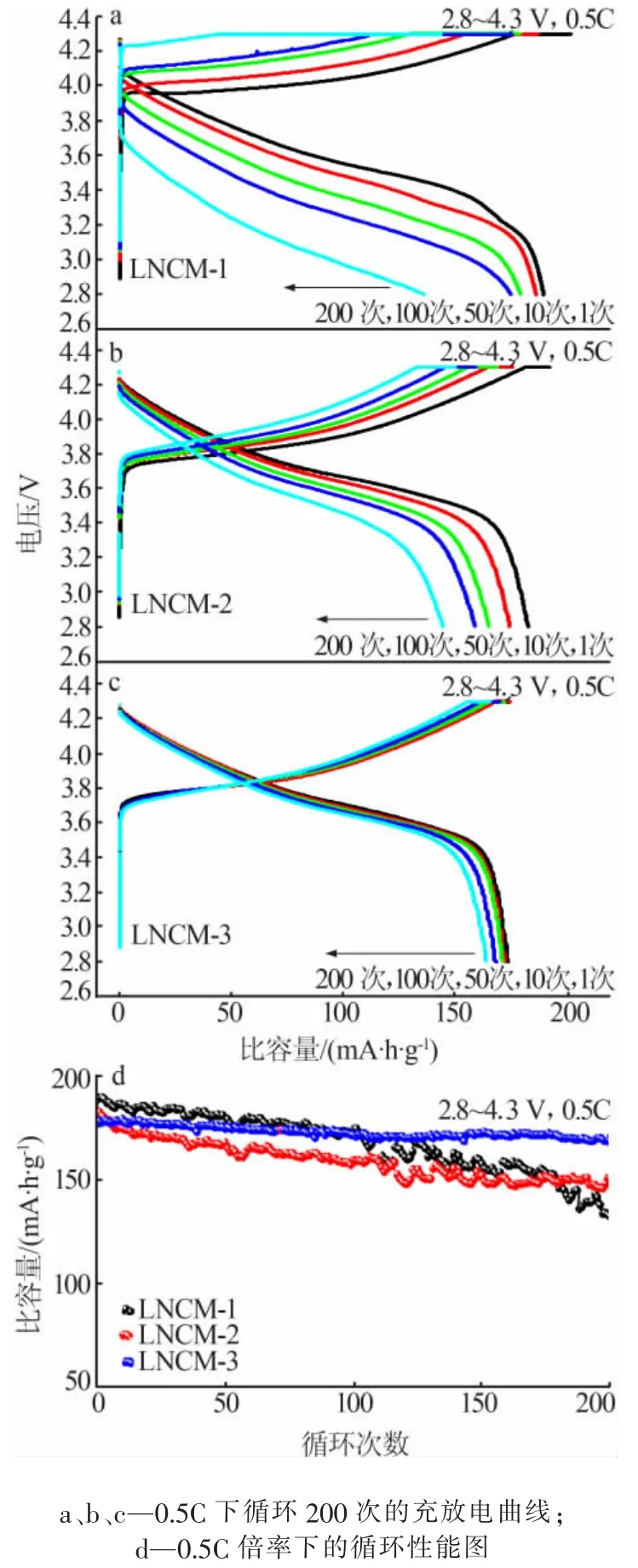
图4 不同 LiNi0.8Co0.1Mn0.1O2 正极材料在25 ℃、2.8~4.3 V电化学窗口下的电化学性能图Fig.4 The cycle performance of different LiNi0.8Co0.1Mn0.1O2 cathode materials at 25 ℃ and 2.8~4.3 V
图5a~5c 为 3 种 LNCM 材料的循环伏安曲线图(CV 图),展示了在扫描速度为 0.1 mV/s 时LNCM-1、LNCM-2 和 LNCM-3 样品的 CV 曲线,3 条CV 曲线都显示了在3.9 V/3.6 V 附近有一对氧化还原峰,对应了Ni2+/Ni3+到Ni4+的氧化还原,表明材料发生从六方相(H)到单斜相(M)的转变。 在4.2 V/4.1 V 的氧化还原峰则对应Co3+向Co4+的电化学氧化。 由图5c 可以看出,球形LNCM-3 样品的CV 曲线后4 次的重合度明显高于LNCM-1 样品,说明球形结构提高了正极材料的循环稳定性与可逆性,LNCM-2 样品的循环稳定性与可逆性则介于上述两样品之间。氧化还原峰的电势差(ΔE)能够表明正极材料的电化学可逆性和极化程度。 LNCM-1 样品的ΔE 为 0.333 V,但 LNCM-3 样品的 ΔE 仅为 0.238 V,说明LNCM-3 样品的电化学可逆性得到改善, 并大幅减少极化程度,这与LNCM-3 极好的循环性能相吻合。 图5d 为3 种LNCM 材料在活化后的交流阻抗图(EIS)。 EIS 图谱中频区半圆在阻抗实部的截距表示电荷转移电阻(Rct)。 图 5d 清楚地显示了 3 种LNCM 材 料 的 电 阻 差 异 ,LNCM-1、LNCM-2 和LNCM-3 样品的 Rct分别为 272.5、275.9、415.1 Ω。表明LNCM-1、LNCM-2 特殊的一次纳米片组装而成的颗粒结构能在高温煅烧过程中形成更多由Ni、Mn等过渡金属原子迁移形成的扩散通道, 有效提高了Li+在正极材料与电解液界面的迁移速率,这将有利于提升其倍率性能。
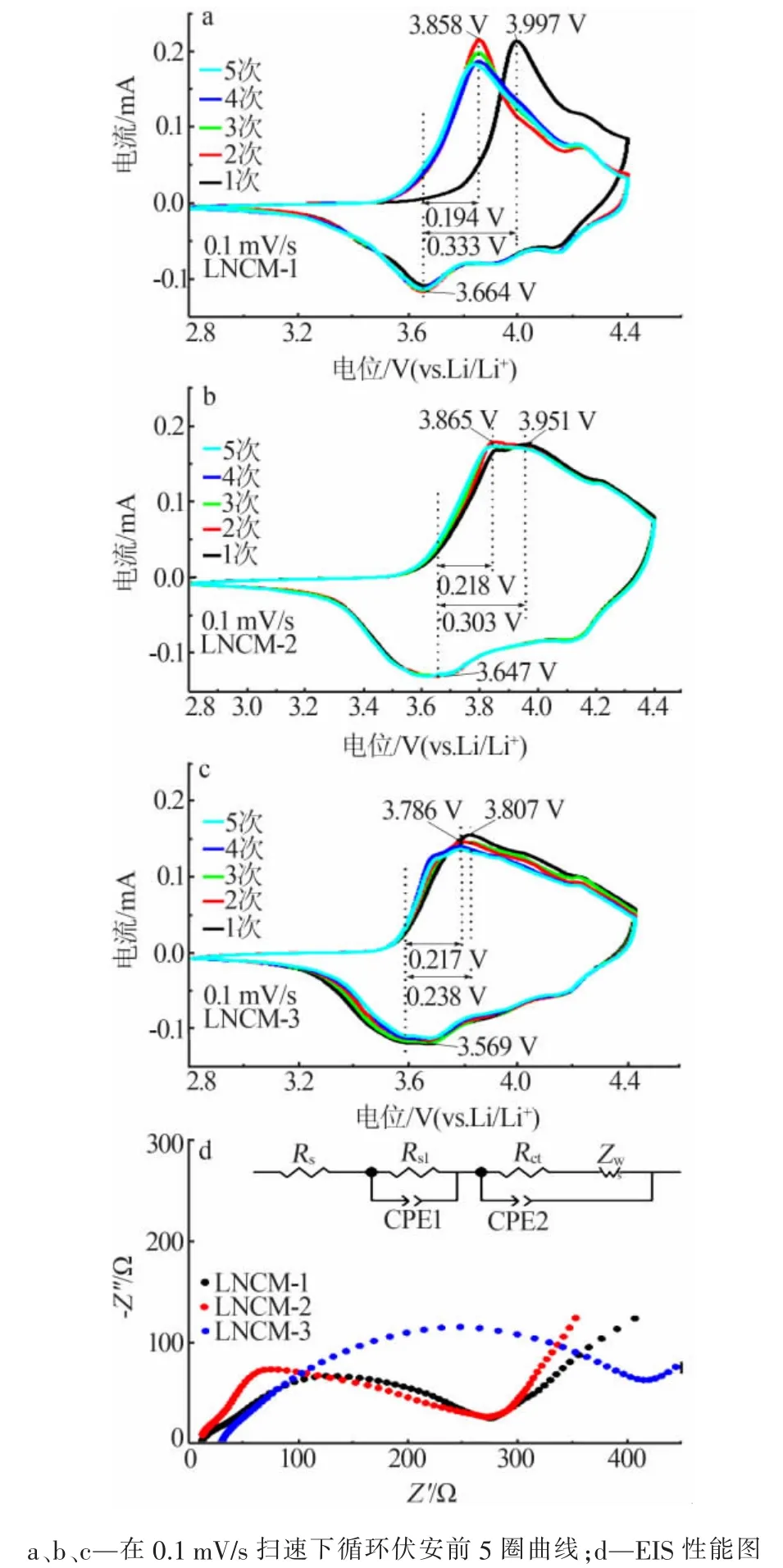
图5 不同LNCM 正极材料的CV 性能图和EIS 性能图Fig.5 CV performance diagrams and EIS performance diagrams of different LNCM cathode materials
图6a~6c 为 3 种 LNCM 材料在 0.1~0.5 mV/s 扫速下的循环伏安曲线图(CV),由3 种LNCM 的CV曲线都可以看到,随着扫描速率提高,氧化还原峰的电势差(ΔE)持续变大,说明样品极化程度增加。
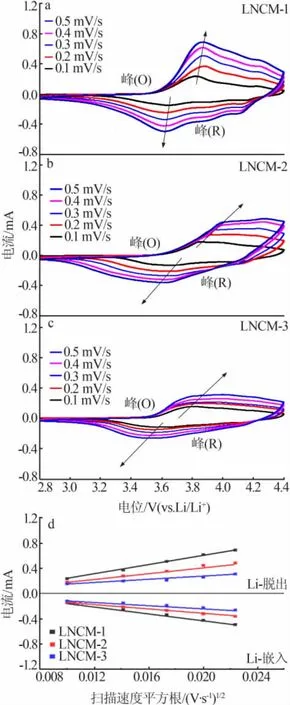
图6 不同LNCM 正极材料在0.1~0.5 mV/s扫速下的CV 图(a~c);不同扫速下峰值电流与扫描速率的平方根的线性拟合(d)Fig.6 CV curves of different LNCM cathode materials at scanning rate of 0.1~0.5 mV/s (a~c);Linear fitting between peak current and square root of scanning rate at different scanning rate(d)
对于扩散控制的可逆电化学反应, 氧化还原峰的峰值电流(Ip)可以通过Randles-Sevcik 方程描述如下:


表3 不同LNCM 正极材料的锂离子扩散速率Table 3 Lithium-ion diffusion rate of different LNCM cathode materials
其中,Ip为峰值电流,A;n 为转移电子数;A为电极片面积,cm2;C0为锂子浓度,mol/cm3;v 为扫描速率,v/s;D 为扩散系数;其他参数视为一个常数,可得到一个关于Ip与v1/2的线性拟合, 由此可以结合图6d得到电极材料中的锂扩散系数。图6d 展示了峰值电流Ip与扫描速度v1/2的线性关系。 LNCM-1 样品具有最大的线性拟合斜率, 表明LNCM-1 样品的Li+扩散系数最大,最易于锂离子的脱出与嵌入,LNCM-1 样品的嵌入扩散系数为 6.97×10-11cm2/s, 分别是LNCM-2 样品的 2.4 倍、LNCM-3 样品的 5.9 倍。 脱出扩散系数为2.56×10-11cm2/s,分别是LNCM-2 样品的1.8 倍、LNCM-3 样品的 2.1 倍。说明 LNCM-1 样品的特殊形貌和微结构更有利于Li+的扩散,这与之前电化学测试中LNCM-1 样品显示出的更高比容量相吻合。
3 结论
以镍、钴、锰乙酸盐为原料,六亚甲基四胺为沉淀剂,通过水热/溶剂热法合成 Ni0.8Co0.1Mn0.1(OH)2前驱体,再结合混锂和高温煅烧获得LiNi0.8Co0.1Mn0.1O2正极材料。 通过改变溶剂组分合成了2 种形貌不同的Ni0.8Co0.1Mn0.1(OH)2前驱体,合成方法方便快捷,重复性好。 以水为溶剂合成的一次片状颗粒紧密堆积组成的长方体状LiNi0.8Co0.1Mn0.1O2正极材料,其特殊的形貌和微结构有利于锂离子扩散迁移, 对提升放电比容量起到了促进作用。 锂离子嵌入扩散系数为6.97×10-11cm2/s, 脱出扩散系数为 2.56×10-11cm2/s,0.5C 下首次放电比容量可达到189.70 mA·h/g。而以乙醇为溶剂制备的球形LiNi0.8Co0.1Mn0.1O2正极材料具有更好的循环性能,0.5C 下循环200 次容量保持率为94.55%。 实验结果表明,采用水热/溶剂热法合成三元材料前驱体, 并结合后续热处理过程可以获得电化学性能优良的LiNi0.8Co0.1Mn0.1O2三元正极材料,为三元材料的制备探索了新的途径。

