用聚吡咯改性电解锰渣去除废水中的六价铬
邵 黎,杨秀端,魏 华,马梦雨,刘衍昌,李 佳
(中南民族大学 资源与环境学院,湖北 武汉 430074)
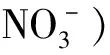
电解锰渣(EMR)的主要成分为由硅、锰、钙、铁、氧和硫元素组成[8]。EMR中含有铁、锰、铝等专性吸附的活性阳离子,使其具有一定吸附性,但用其吸附Cr(Ⅵ)的研究未见报道[9]。EMR成分复杂且分布不均匀,比表面积小,不宜直接用作Cr(Ⅵ)吸附剂。包覆法改性是一种可以在基体表面包覆一层有机聚合物来优化基体材料性能、赋予材料新功能的方法,对基材纯度与表面基团要求较低。试验采用包覆法将PPY包覆在EMR表面制备出复合吸附材料,并用于从废水中吸附Cr(Ⅵ),以期解决电解锰渣的二次利用问题[10-15]。
1 试验部分
1.1 试验材料
锰渣:取自某大型锰生产企业,主要组成见表1。

表1 电解锰渣的主要组成 %
试剂:吡咯(PY)、重铬酸钾(K2Cr2O7)、过硫酸铵(APS)、十六烷基三甲基溴化铵(CTAB)、盐酸、氯化钾、硝酸钾、硫酸钾、碳酸钾,均为分析纯,购于国药集团。
1.2 EMR-PPY的制备
将2 g EMR分散在100 mL去离子水中搅拌0.5 h;添加1 mL PPY和1 g CTAB搅拌0.5 h,再用注射器注入一定量APS溶液,搅拌12 h确保聚合充分,然后洗涤至滤液无色,pH为中性。将聚合物置于烘箱中在60 ℃下干燥6 h,得EMR-PPY复合材料。
1.3 EMR-PPY吸附Cr(Ⅵ)
用重铬酸钾配制Cr(Ⅵ)质量浓度为150 mg/L的模拟废水。取模拟废水50 mL至100 mL锥形瓶中并投加0.05 g EMR-PPY,在一定温度恒温振荡器中振荡一定时间,定时取样,过0.45 μm滤膜后,用国标二苯碳酰二肼分光光度法测量滤液中Cr(Ⅵ)质量浓度,计算Cr(Ⅵ)去除率,计算公式为
(1)
式中:r—Cr(Ⅵ)去除率,%;ρ0—初始Cr(Ⅵ)质量浓度,mg/L;ρ—吸附后滤液中Cr(Ⅵ)质量浓度,mg/L。
Cr(Ⅵ)吸附量计算公式为
(2)
式中:qm—吸附饱和时吸附量,mg/g;m—EMR-PPY加入量,g。
1.4 分析方法
用X射线荧光光谱仪XRF(Zetium)测定EMR组成;用德国Brüker 公司的D8 Advance型X射线衍射仪(XRD)测定电解锰渣及EMR-PPY晶相结构;用德国Brüker公司的傅里叶变换红外光谱(V70)测定吸附前后材料的官能团变化;用紫外分光光度计测定Cr(Ⅵ)浓度;通过扫描电子显微镜(SEM,Hitach SU8010)分析吸附材料表面形貌特征。
2 试验结果与讨论
2.1 改性电解锰渣吸附材料结构表征
2.1.1 XRD表征
EMR、EMR-PPY的XRD分析图谱如图1所示。可以看出:EMR的主要矿物组成为石英、钾锰盐和水合硫酸钙等;EMR-PPY的主要矿物组成为石英,由于EMR颗粒表面掺杂大量PPY导致钾锰盐和水合硫酸钙的特征峰减弱。
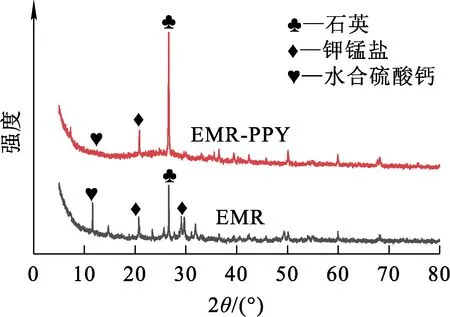
图1 EMR、EMR-PPY的XRD图谱
2.1.2 SEM表征
EMR、PPY、EMR-PPY的表面形貌如图2所示。可以看出:PPY为圆柱状颗粒,并通过颗粒的聚集形成堆积孔;EMR颗粒较大,呈长条状;改性后,EMR表面负载了PPY颗粒,比表面积增大。

图2 PPY(a)、电解锰渣EMR(b)、EMR-PPY(c)、吸附Cr(Ⅵ)后EMR-PPY(d)的SEM照片
2.1.3 BET表征
EMR、EMR-PPY的N2吸附—脱附等温线和孔径大小分布如图3所示。可以看出:EMR、EMR-PPY有相似的N2吸附—脱附等温线,均为Ⅱ型等温线;3个样品均具有不同孔隙结构。
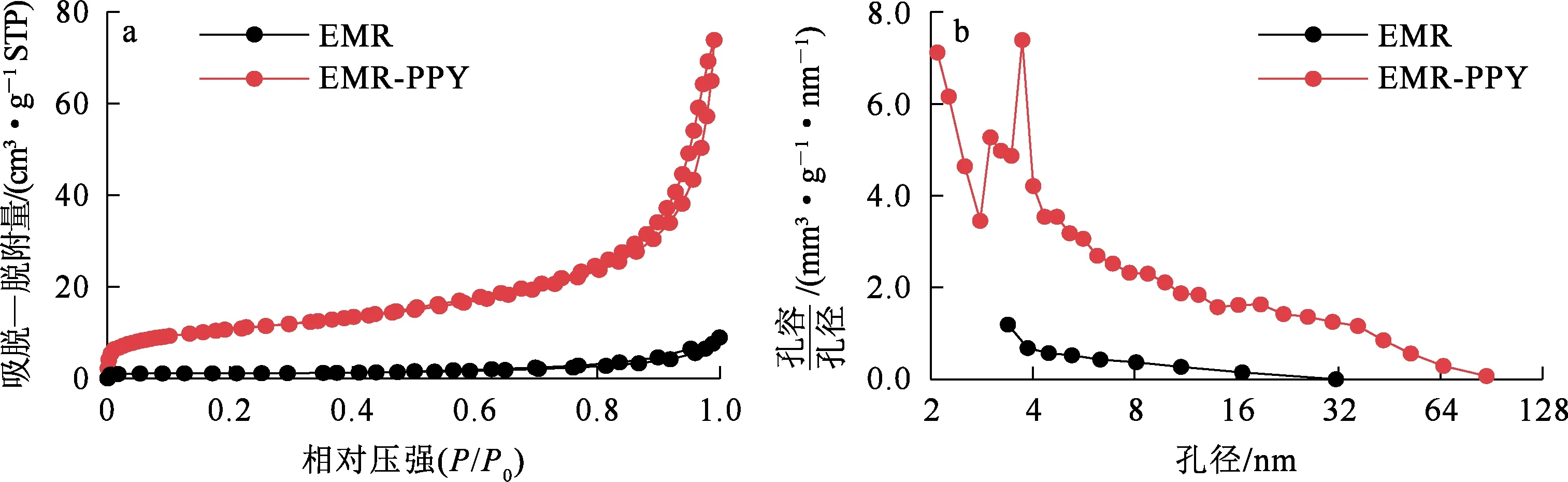
图3 EMR、EMR-PPY的N2吸附—脱附等温线(a)及孔径大小分布(b)
EMR、PPY和 EMR-PPY的比表面积、平均孔径和孔容积见表2。可以看出,EMR-PPY的比表面积和孔容积比EMR扩大了约10倍,说明EMR改性后,其吸附性能得到改善。
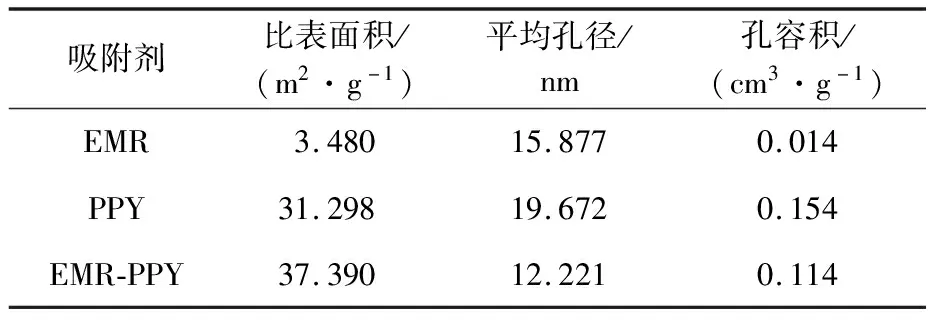
表2 EMR、PPY和EMR-PPY的比表面积、平均孔径和孔容积
2.1.4 FT-IR表征
EMR、EMR-PPY和PPY的FT-IR图谱如图4所示。
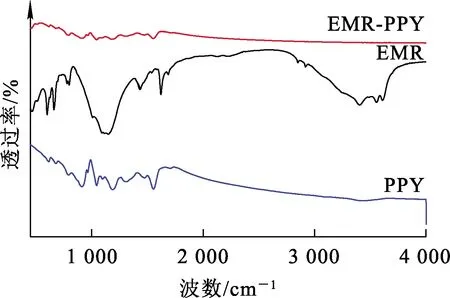
图4 EMR、PPY和 EMR-PPY的FT-IR图谱

2.2 EMR-PPY吸附废水中的Cr(Ⅵ)
2.2.1 吸附动力学
将试验数据用不同的动力学模型进行拟合,以了解吸附材料在不同因素影响情况下对重金属离子的吸附速率变化情况,从而解释吸附过程和吸附机制。
1)准一级动力学模型
(3)
根据式(3)换算得到
qt=qe(1-e-k1t);
(4)
(5)
式中:qe、qt—吸附平衡时和吸附t时间时的吸附量,mg/g;k1—准一级动力学吸附速率常数,min-1。k1可以由lg(qe-qt)对时间t进行线性拟合得到。
2)准二级动力学模型
(6)
式中,k2—准二级动力学平衡速率常数,mg/(g·min)。吸附t时间时,
(7)
积分可得线性方程式
(8)
吸附时间对EMR-PPY吸附Cr(Ⅵ)的影响试验结果如图5所示。
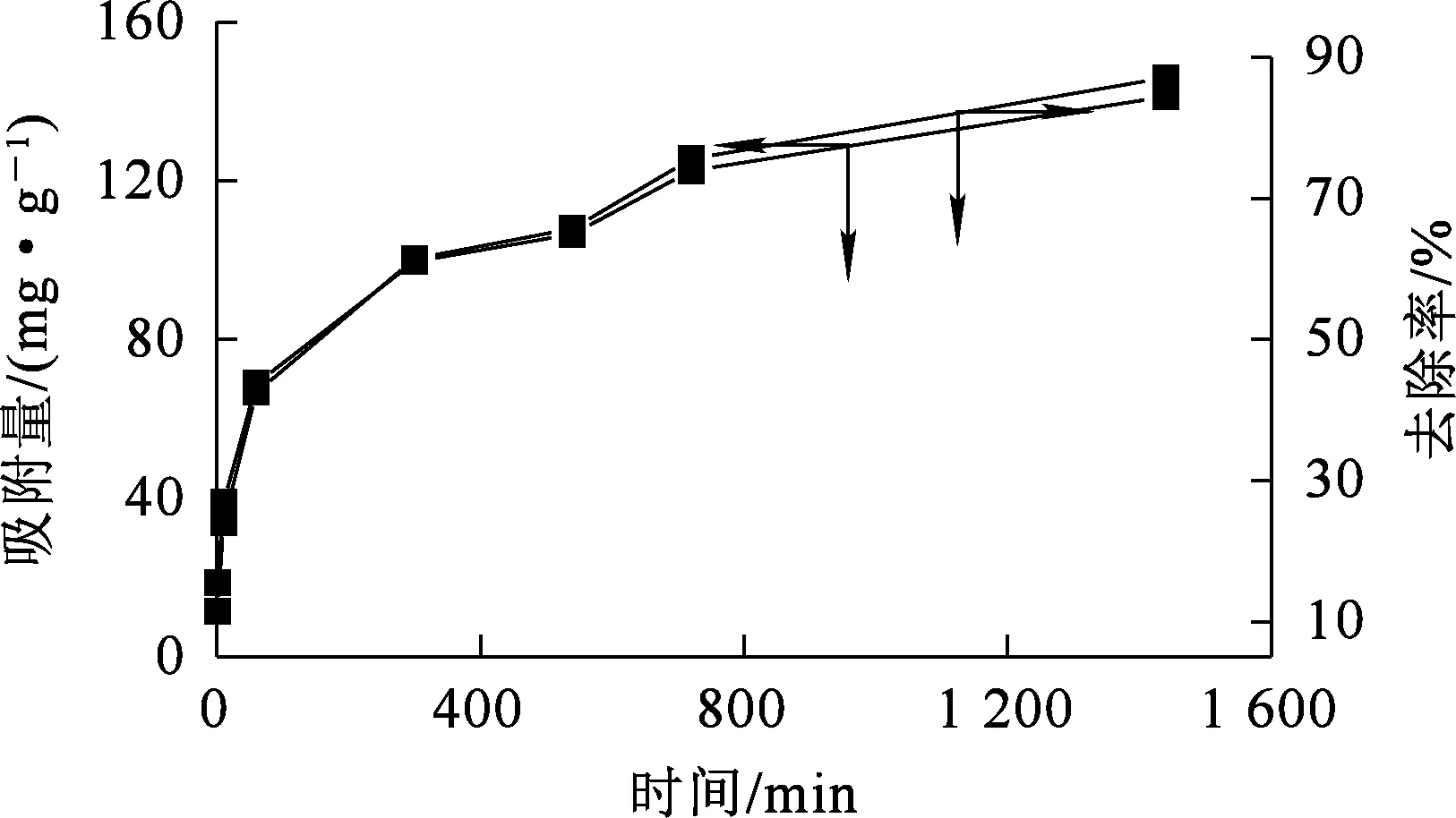
图5 吸附时间对EMR-PPY吸附Cr(Ⅵ)的影响
由图5看出:吸附时间在0~100 min内,EMR-PPY对Cr(Ⅵ)的吸附量和去除率随吸附时间延长而明显升高;吸附800 min后,吸附量和去除率升高幅度都变小。随吸附进行,EMR-PPY对Cr(Ⅵ)吸附更充分,但EMR-PPY表面的吸附位点有限,被Cr(Ⅵ)占据后,吸附时间继续延长,Cr(Ⅵ)吸附量和去除率没有明显变化。
采用准一级动力学模型和准二级动力学模型对EMR-PPY吸附Cr(Ⅵ)的试验数据进行拟合,拟合曲线如图6所示,相关的动力学模型拟合参数见表3。
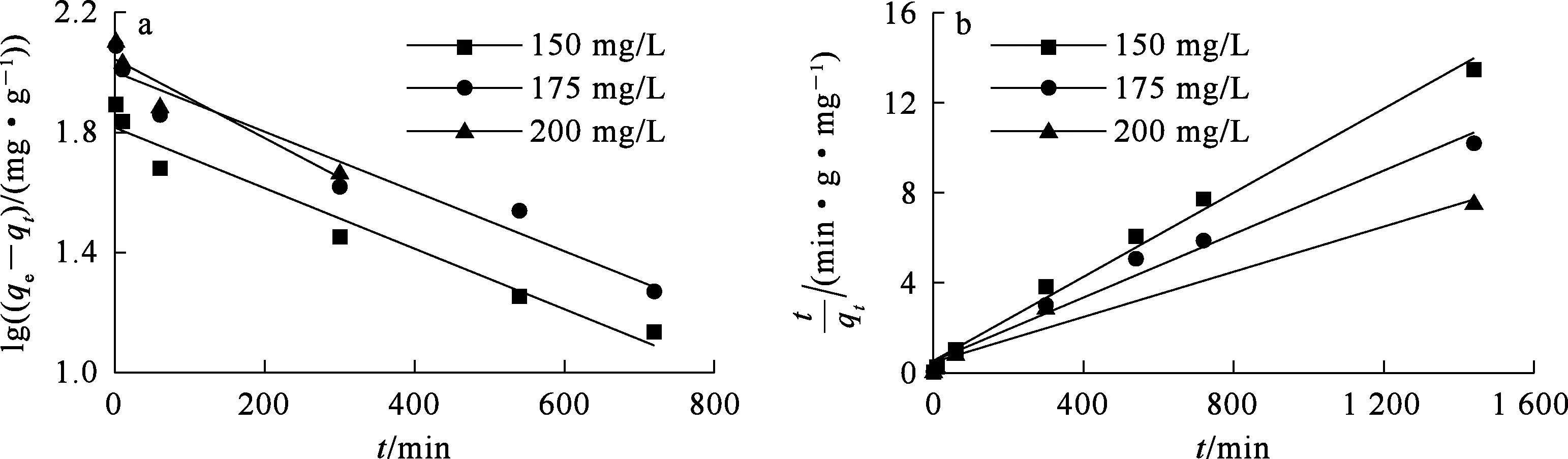
图6 EMR-PPY吸附Cr(Ⅵ)的准一级动力学(a)、准二级动力学(b)拟合曲线

表3 EMR-PPY吸附Cr(Ⅵ)的动力学拟合参数
由图6、表3看出:准二级动力学的拟合结果与实测结果更相近,说明准二级动力学能较好地描述EMR-PPY对Cr(Ⅵ)的吸附过程[17],吸附主要受表面反应控制。
2.2.2 热力学
利用不同温度下的试验数据得到热力学平衡常数,根据公式计算出ΔG、ΔH、ΔS等热力学参数,以便深入认识吸附机制。
(9)
式中:ΔHΘ—吸附过程的焓变,kJ/mol;ΔSΘ—吸附过程的熵变,J/(mol·K);T—热力学温度,K;R—理想气体常数,8.314 J/(mol·K);kc—热力学平衡常数,cm3/g。ΔHΘ和ΔSΘ由lnkc对1/T作图并线性拟合得到。
ΔGΘ=-RTlnkc。
(10)
式中,ΔGΘ—吸附自由能,J/mol。lnkc-1/T拟合曲线如图7所示,所得热力学参数见表4。
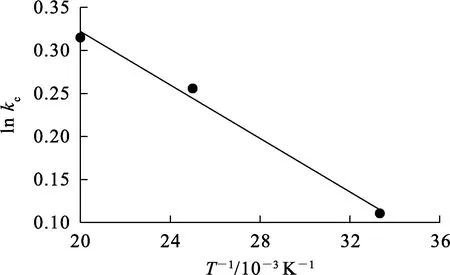
图7 ln kc-1/T拟合曲线
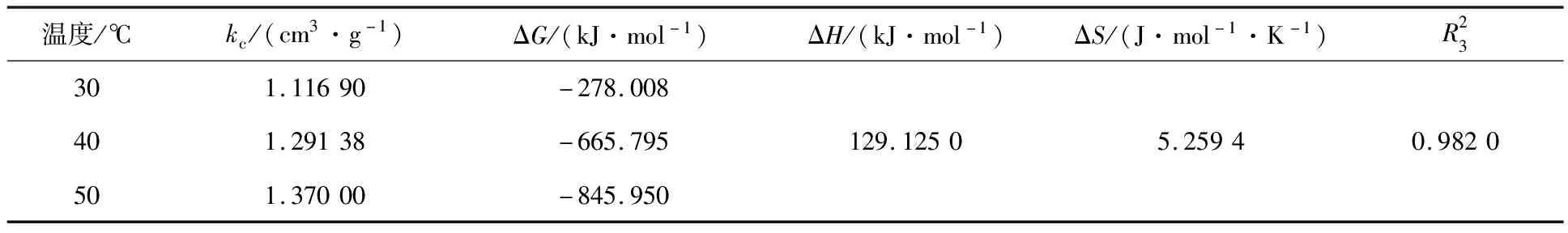
表4 热力学参数
由表4看出:ΔG随温度升高而减小,且ΔG<0,说明EMR-PPY对Cr(Ⅵ)的吸附过程可自发进行,升温有利于吸附反应进行;ΔS>0,说明吸附过程中吸热,升温有利于吸附反应进行,吸附量随温度升高而增大。
2.2.3 初始Cr(Ⅵ)质量浓度对EMR-PPY吸附Cr(Ⅵ)的影响
EMR-PPY加入量1 g/L、废水pH=2.0、室温,初始Cr(Ⅵ)质量浓度对EMR-PPY吸附Cr(Ⅵ)的影响试验结果如图8所示。
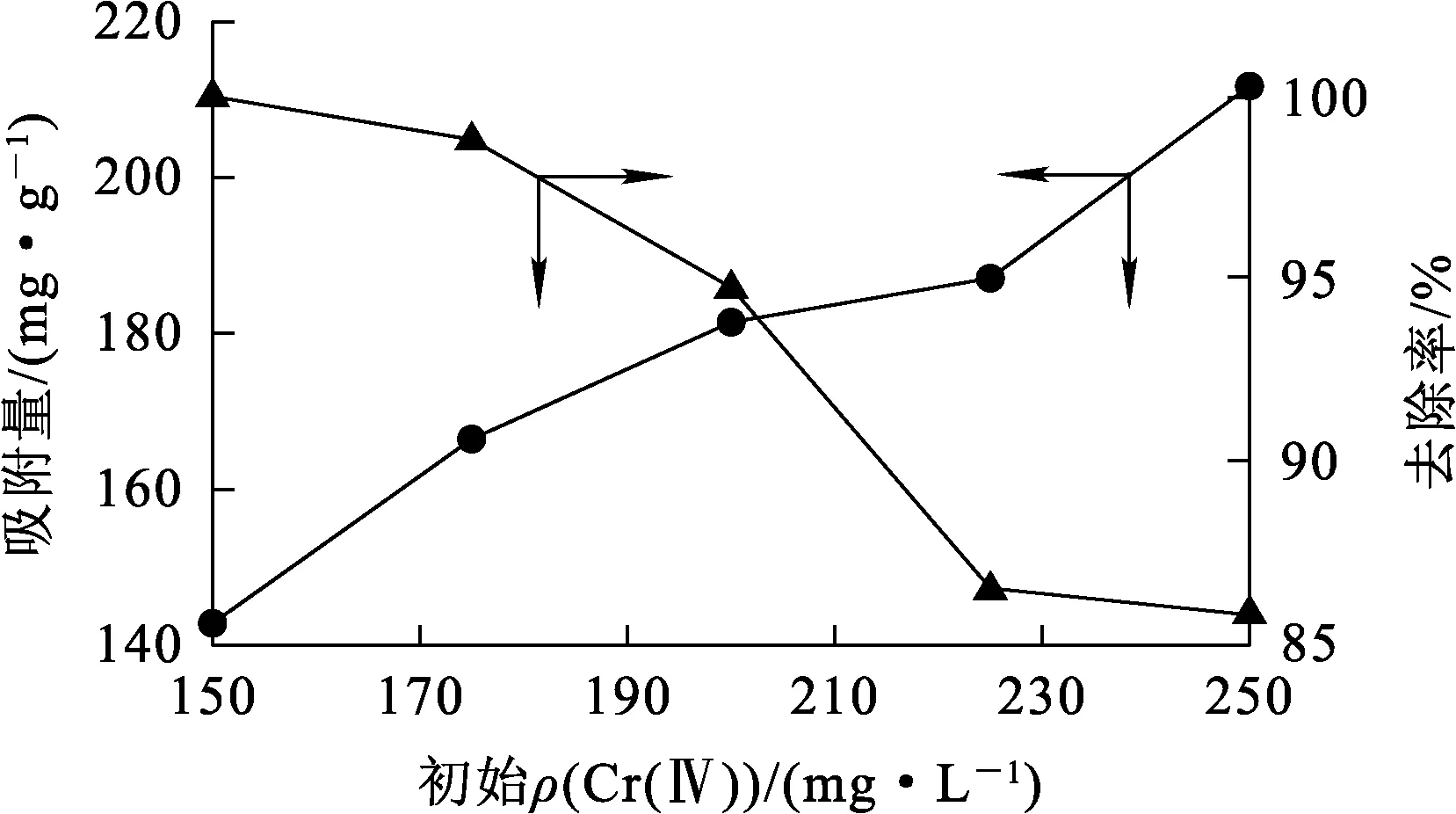
图8 初始Cr(Ⅵ)质量浓度对EMR-PPY吸附Cr(Ⅵ)的影响
由图8看出:EMR-PPY对Cr(Ⅵ)的吸附量随初始Cr(Ⅵ)质量浓度增大而升高,且逐渐达到平衡。结合动力学分析结果,EMR-PPY对Cr(Ⅵ)的吸附过程符合准二级动力学模型,提高初始Cr(Ⅵ)质量浓度,Cr(Ⅵ)与EMR-PPY表面接触概率增大,吸附量升高。
2.2.4 EMR-PPY加入量对吸附Cr(Ⅵ)的影响
废水pH=2.0,室温,初始Cr(Ⅵ)质量浓度150 mg/L,EMR-PPY加入量对Cr(Ⅵ)吸附量和去除率的影响试验结果如图9所示。
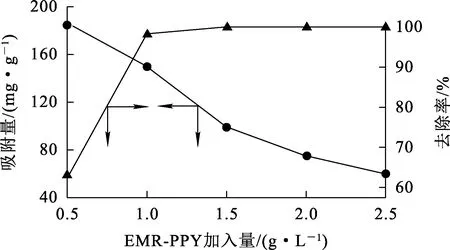
图9 EMR-PPY加入量对吸附Cr(Ⅵ)的影响
由图9看出:Cr(Ⅵ)去除率随EMR-PPY加入量增加而提高,单位吸附量则相反。EMR-PPY加入量越大,提供的活性位点越多,对Cr(Ⅵ)的吸附量越大;Cr(Ⅵ)被吸附到某个水平时,继续増大EMR-PPY加入量,导致EMR-PPY的单位吸附量反而下降。实际应用中,需综合考虑废水实际排放要求,选择合适的吸附剂加入量。
2.2.5 废水初始pH和干扰离子对EMR-PPY吸附Cr(Ⅵ)的影响
EMR-PPY加入量1 g/L,室温,初始Cr(Ⅵ)质量浓度150 mg/L,废水初始pH对EMR-PPY吸附Cr(Ⅵ)的影响试验结果及EMR-PPY的Zeta电位如图10所示。
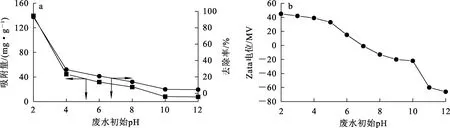
图10 废水初始pH对EMR-PPY吸附Cr(Ⅵ)的影响(a)及EMR-PPY的Zeta电位(b)
由图10看出:pH=2.0时,Cr(Ⅵ)吸附效果最好,吸附量为139 mg/g;pH在3.0~10.0的范围内,Cr(Ⅵ)去除率逐渐下降,pH>10.0后,下降更明显;pH<6.5时,EMR-PPY表面呈正电性,对阴离子Cr(Ⅵ)产生静电吸引,利于吸附[17];此外,Cr(Ⅵ)可与PPY框架中掺杂的Cl-发生离子交换;当pH>6.5时,EMR-PPY表面呈负电性,对阴离子Cr(Ⅵ)产生电荷排斥,同时高浓度OH-与Cr(Ⅵ)竞争吸附位点,减弱了EMR-PPY对阴离子的交换能力,降低了吸附效果[17]。说明静电吸引在反应过程中占主导地位。
其他干扰阴离子对EMR-PPY吸附去除Cr(Ⅵ)的影响试验结果如图11所示。
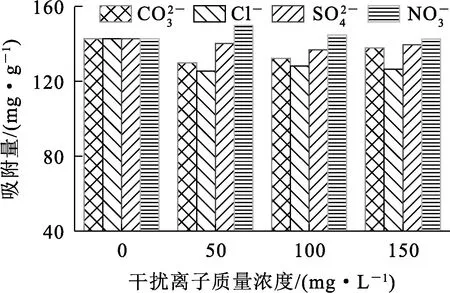
图11 干扰离子对EMR-PPY吸附Cr(Ⅵ)的影响
2.3 吸附等温线
EMR-PPY加入量1 g/L,废水pH=2.0,温度对EMR-PPY吸附Cr(Ⅵ)的影响试验结果如图12所示。
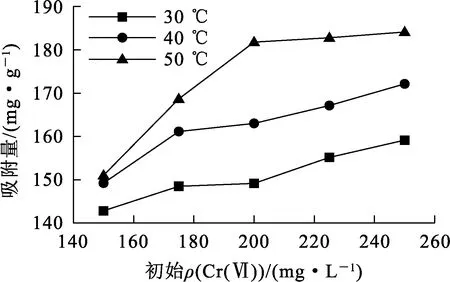
图12 温度对EMR-PPY吸附Cr(Ⅵ)的影响
由图12看出:随温度升高,相同浓度下,EMR-PPY对Cr(Ⅵ)的吸附量逐渐增大;同时,随初始Cr(Ⅵ)质量浓度升高,温度影响逐渐增大。
采用Langmuir等温吸附模型和Freundlich等温吸附模型对EMR-PPY吸附Cr(Ⅵ)的试验数据进行拟合,拟合曲线如图13所示,相关拟合参数见表5。
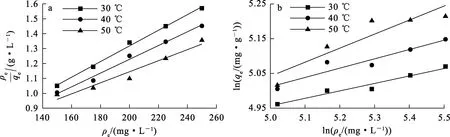
图13 EMR-PPY吸附Cr(Ⅵ)的Langmuir(a)、Freundlich(b)等温吸附拟合曲线
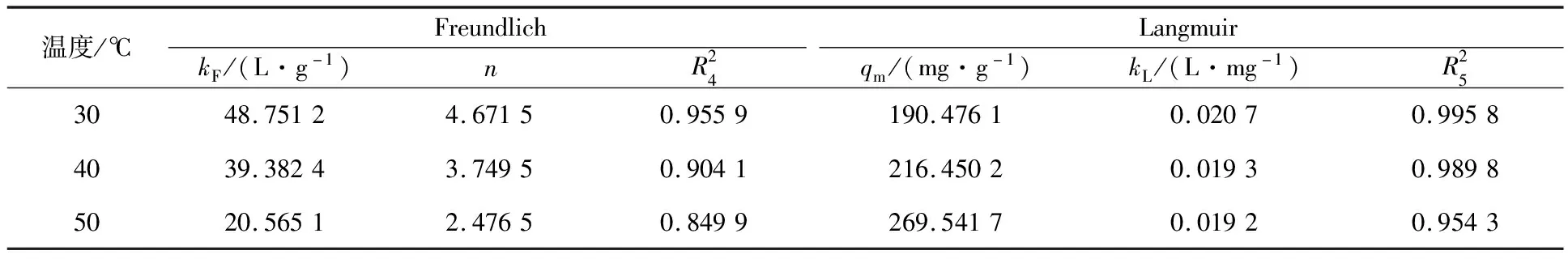
表5 EMR-PPY吸附Cr(Ⅵ)的等温吸附拟合参数
1)Langmuir等温吸附模型
Langmuir等温吸附模型是一个理想状态,主要基于以下假设:吸附点表面是均匀的,每个吸附位点只可以容纳一个吸附质分子或离子;吸附质在吸附剂表面上以单分子层形式覆盖,吸附分子或离子之间不会发生相互作用;主要用动力学方法推得。但有的多分子层吸附也符合Langmuir等温吸附方程。Langmuir吸附等温式可以用以下形式表示:
(11)
式中:qe—吸附平衡时吸附量,mg/g;qm—吸附饱和时吸附量,mg/g;kL—吸附平衡常数,L/mg。
2)Freundlich等温吸附模型
利用Freundlich等温吸附模型可以探讨非均质表面或多层吸附,不限于单层吸附。
(12)
式中:n—Freundlich等温吸附强度相关常数;kF—常数,L/g。
由图13和表5看出:EMR-PPY对Cr(Ⅵ)的吸附过程更符合Langmuir等温吸附模型,表明吸附属于单分子层吸附。
2.4 EMR-PPY的循环再生
吸附饱和的EMR-PPY从溶液中分离,烘干后继续用于吸附。吸附Cr(Ⅵ)的EMR-PPY加入到0.5 mol/L NaOH溶液中,室温下振荡1 h后过滤,并用2 mol/L HCl溶液活化0.5 h,再用去离子水洗涤至中性后,置于105 ℃下干燥。吸附试验条件与前面所述一致,EMR-PPY循环再生次数对吸附Cr(Ⅵ)的影响试验结果如图14所示。
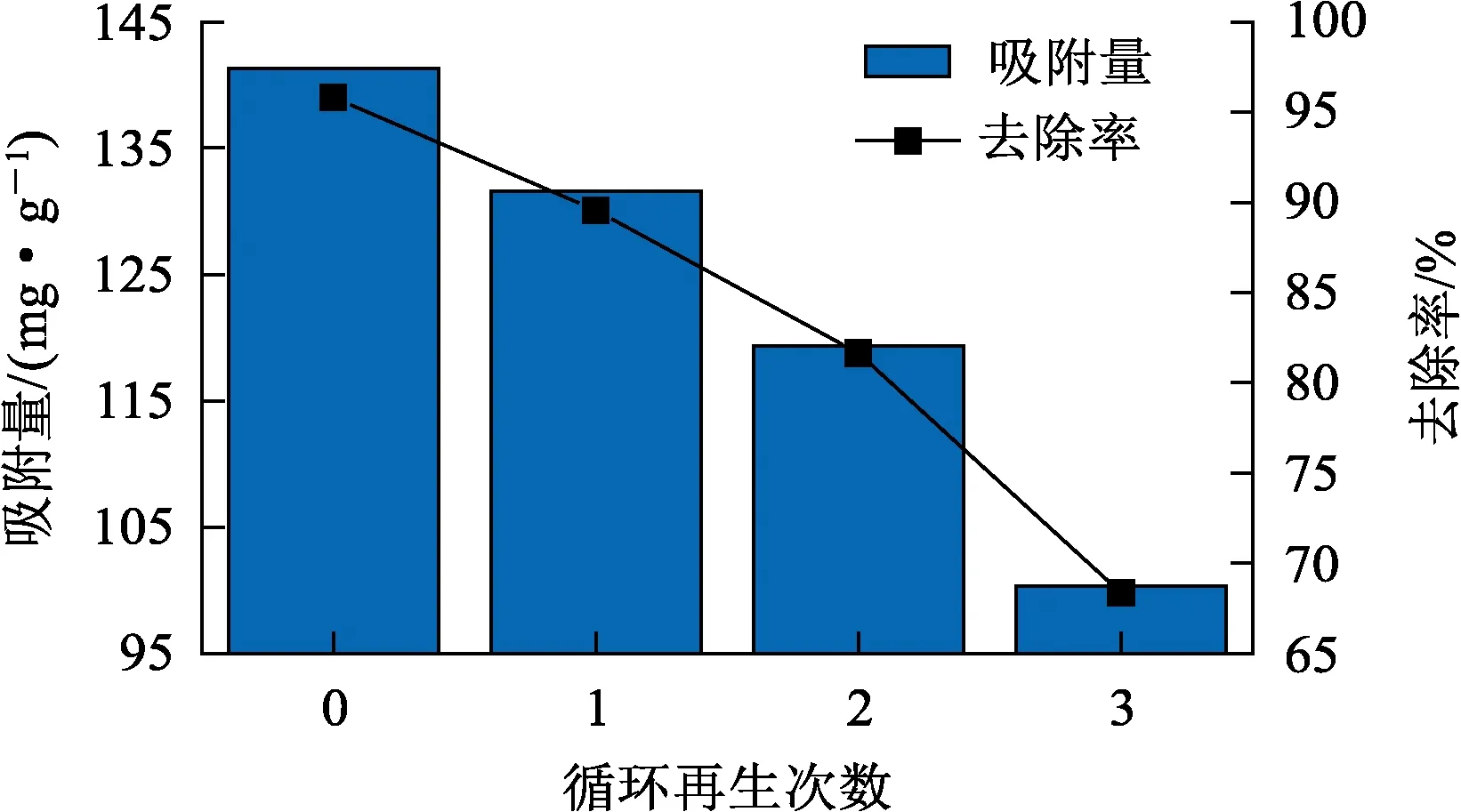
图14 EMR-PPY循环再生次数对吸附Cr(Ⅵ)的影响
由图14看出:EMR-PPY对Cr(Ⅵ)的吸附量和去除率随再生次数增加而下降。这可能是在酸性条件下,PPY上富电子的亚氨基发生还原反应,使部分Cr(Ⅵ)被还原成Cr(Ⅲ),导致吸附率下降[17];但3次循环再生后,EMR-PPY对Cr(Ⅵ)仍保持在100 mg/g以上,说明其具有较好的循环再生性。
2.5 吸附机制的探讨

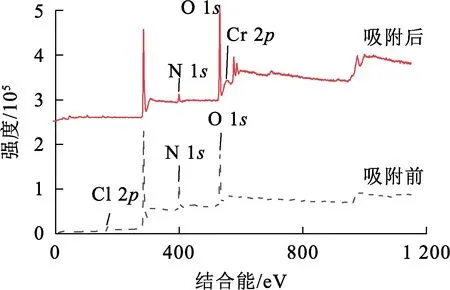
图15 EMR-PPY吸附前、后的总谱
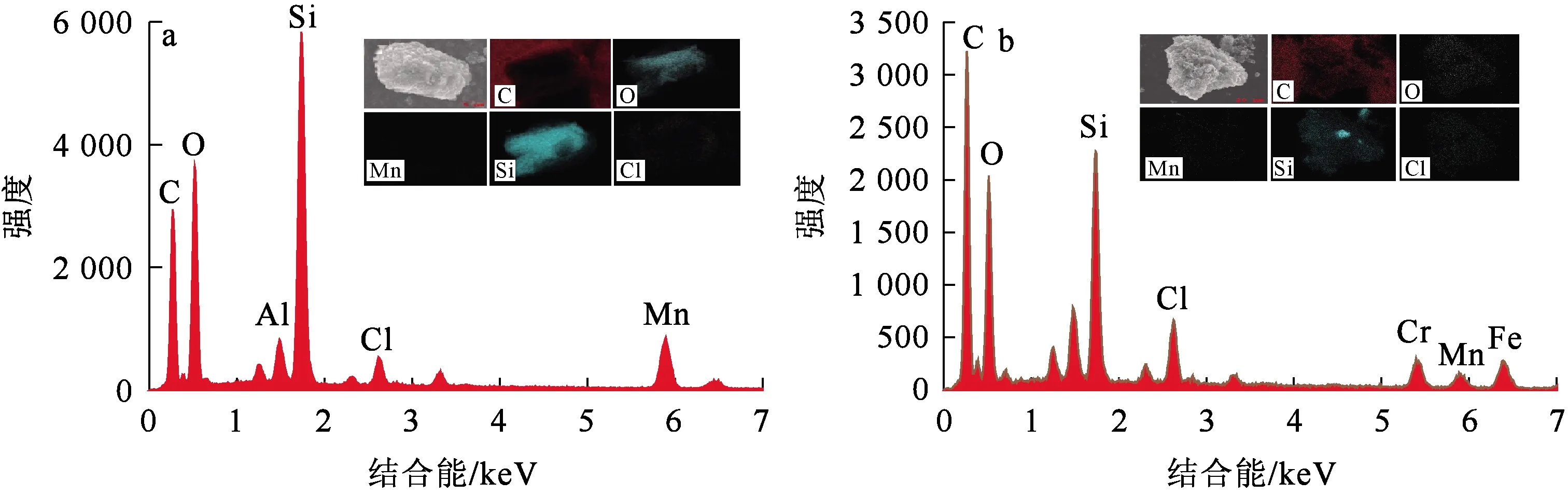
图16 EMR-PPY吸附Cr(Ⅵ)前(a)、后(b)的EDS能谱
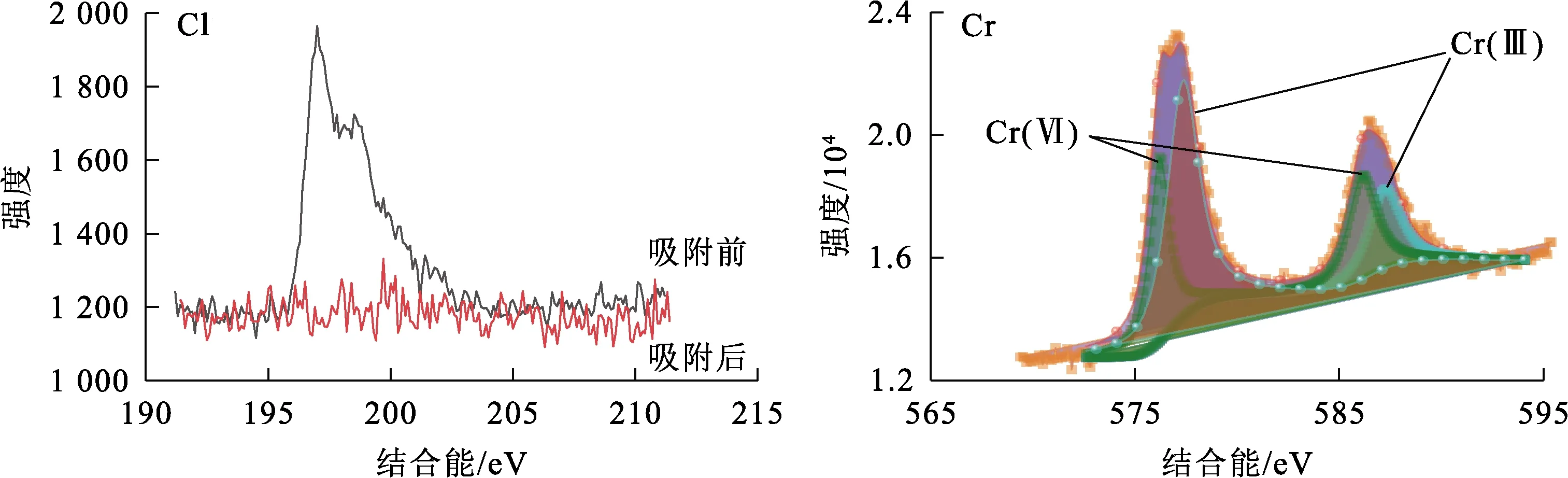
图17 吸附前、后的Cl谱和吸附后的Cr谱
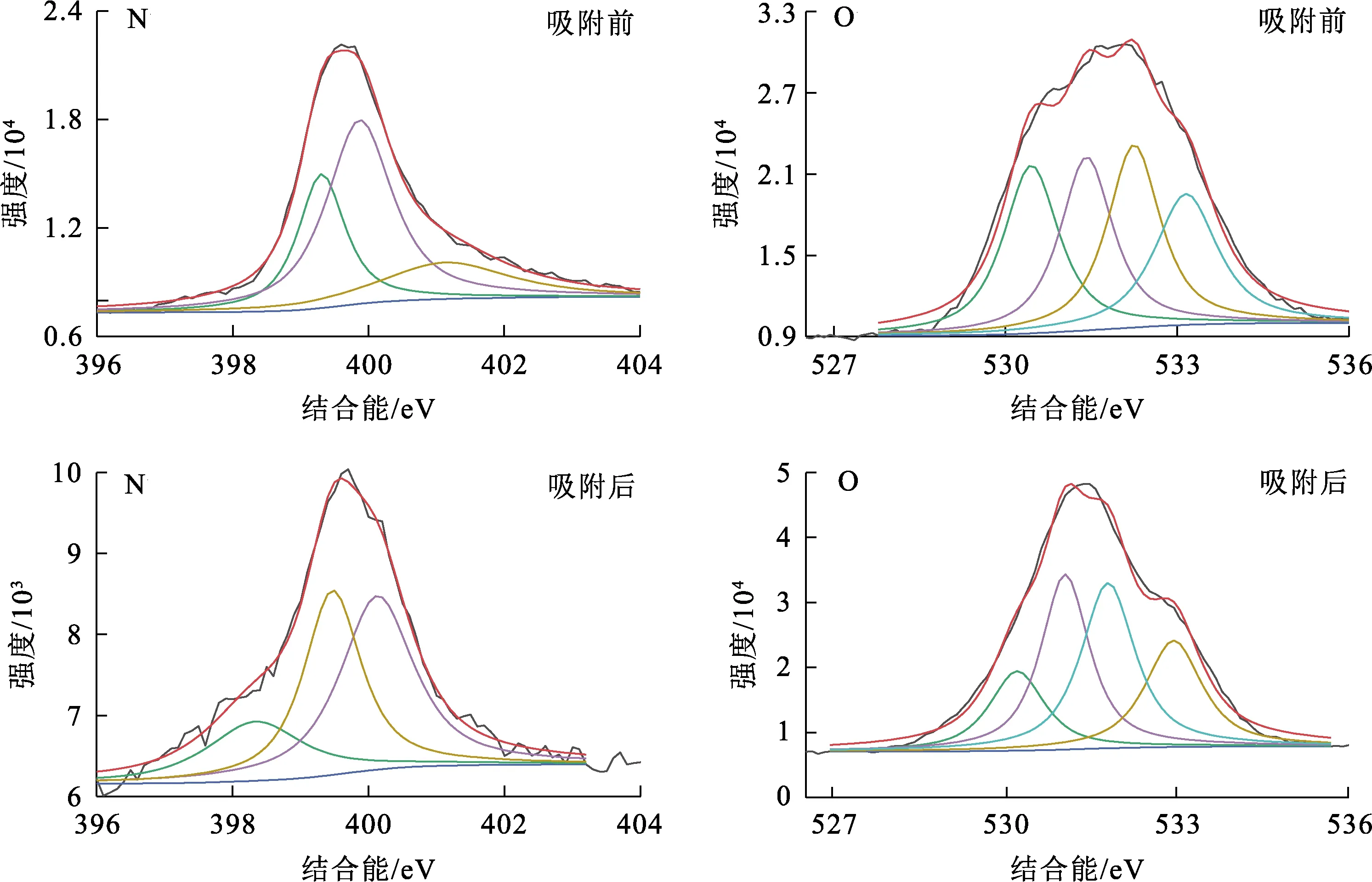
图18 吸附前、后的N谱和O谱
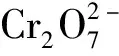
3 结论
1)采用原位聚合法在EMR颗粒表面包覆PPY制备吸附材料EMR-PPY,操作简单,所得吸附剂对废水中Cr(Ⅵ)有较好的去除效果。
2)EMR-PPY对Cr(Ⅵ)的吸附过程符合准二级动力学模型和Langmuir等温吸附模型;平衡状态下,对Cr(Ⅵ)的最大吸附量为269 mg/g。
3)EMR-PPY主要通过静电作用、离子交换过程、表面还原作用吸附去除废水中Cr(Ⅵ),其中,静电吸引和表面还原占主导地位。

