用枯草芽孢杆菌吸附去除电镀废水中的铜
谭 荣,龚 杰,龚百川,李英朋,揭方慧,王忠兵,熊甘霖,朱新伟
(1.南昌航空大学 环境与化学工程学院,江西 南昌 330063;2.江西赣昌评价检测技术咨询有限公司,江西 南昌 330000;3.江西省地质勘探研究院,江西 南昌 330000)
工业废水尤其电镀废水中存在大量重金属离子[1],需要去除或回收后外排。传统的从水溶液中去除重金属离子的方法有一定局限性,如成本较高,能耗高,效率低,易产生有毒污泥造成二次污染[2]等。与之相比,微生物吸附技术具有环境友好、成本低、效率高、操作方便、金属回收率高等优点[3]。
近年来,用微生物技术从废水中吸附去除重金属离子受到了广泛关注,相关研究较多,已筛选分离出多种功能菌株。常见的微生物有假单胞杆菌(Pseudomonassp.)[4]、蓝细菌(Spirulina[5]、Anabaena[6]和Nostoc[7])、芽孢杆菌(Bacillusthuringiensis[8]、Bacilluslicheniformis[9]和Bacillussubtilis[10])等。其中多种功能菌株对水体中重金属离子有良好吸附性能:如假单胞菌MEW079,在最佳发酵培养条件下对100 mg/L铜离子的吸附率达95.87%[11];金芽孢杆菌(Bacillus.thuringiensis016)对初始质量浓度为100 mg/L铀的吸附率接近100%,在将六价铬有效还原为三价铬的同时,对初始质量浓度为25 mg/L的铬的固定率达92%[12];从电镀厂废水中筛选得到的耐铜质量浓度高达400 mg/L的丛毛单胞菌(Comamonassp.E),在最优条件下对Cu2+的吸附量高达7.79 mg/g[13]。在目前已报道的功能菌中,Bacillus菌属能有效吸附废水中的重金属离子,但利用Bacillussubtilis吸附铜离子的相关研究报道较少,其吸附机制有待深入探讨。
试验从电镀废水中筛选出一种耐Cu2+的微生物菌种——枯草芽孢杆菌(Bacillussubtilis-TR1),研究了此菌种对Cu2+的吸附行为;借助FT-IR、XRD、SEM-EDS研究了吸附机制,以期为微生物法去除电镀废水中重金属离子提供一种新型微生物吸附剂,同时更好地实现微生物吸附法吸附处理电镀废水及工业污泥。
1 试验材料与方法
1.1 污泥来源
活性污泥:取自某污水处理厂曝气池。
1.2 培养基的制备
LB培养基[14]:称取10 g胰蛋白胨,5 g酵母提取物,10 g氯化钠,1 000 mL超纯水,用1 mol/L的NaOH和HCl溶液调pH至7.2~7.4,定容至设定体积后用高压蒸汽灭菌锅于121 ℃下灭菌20 min,冷却备用。
固体LB培养基:在上述液体LB培养基配方基础之上,再添加15 g琼脂粉,定容至指定体积后用高压蒸汽灭菌锅于121 ℃下灭菌20 min,趁热倒入无菌培养皿中,待其冷却凝固。
重金属驯化培养基:称取一定量二水氯化铜加入LB培养基中制备得到。
1.3 菌种筛选
取活性污泥于装有无菌水的锥形瓶中,摇床摇匀后依次将其稀释到10-3、10-4、10-5,备用。将LB固体培养基倒入培养皿中,冷却固化,取10-3、10-4、10-5浓度的污泥悬液100 μL,用涂布法涂铺在平板上,保持温度恒定,35 ℃培养箱中培养5~7 d;然后选择培养皿上生长的单菌落,在同一培养基上划线,重复纯化多次,纯化后的菌株放入4 ℃冰箱中备用。配制固体培养基时,在溶液中加入二水氯化铜,控制培养基中Cu2+质量浓度为10 mg/L,并将选定的菌株接种到该培养基中。培养2~3 d后,选择生长较好的菌株先接种至Cu2+质量浓度为20 mg/L的LB固体培养基中再次培养驯化,以此类推,逐级提高培养基内Cu2+质量浓度后,将所需驯化菌株依次接种至对应Cu2+质量浓度的LB固体培养基内,观察其生长情况,并挑选出一株耐铜除铜能力优良的菌种用于试验[15-16]。
1.4 菌种鉴定
1.4.1 菌种的形态特征观察
将菌液涂布于凝固后的LB固体培养基上,待菌体生长后采用扫描电镜(SU1510)放大5 000倍观察菌株的形态特征[17]。
1.4.2 16S rDNA测序
将细菌培养至对数生长期后,用Ezup柱式细菌基因组DNA抽提试剂盒提取出菌株的基因组DNA。PCR扩增反应DNA序列后对扩增产物纯化后送测序,将所测序列在NCBI官网进行Blast比对,用软件MEGA7.0构建系统发育树[18]。
1.5 单因素优化
采用单因素试验法考察反应温度、体系pH、菌体加入量、重金属离子初始质量浓度等因素对吸附Cu2+的影响[19]。
1.6 分析方法与计算
废水中Cu2+质量浓度采用电感耦合等离子体质谱仪(ICP-MS)测定。Cu2+去除率及吸附量计算公式如下:
(1)
(2)
式中:r—Cu2+去除率,%;ρ0—废水中初始Cu2+质量浓度,mg/L;ρ1—吸附后废水中Cu2+质量浓度,mg/L;V0—吸附前废水体积,L;V1—吸附后废水体积,L;q—Cu2+吸附量,mg/g;V—溶液体积,L;m—吸附剂加入量,g。
2 试验结果与讨论
2.1 菌种鉴定
通过富集驯化及分离纯化,筛选出一株对Cu2+具有较好吸附作用且能够良好生长的菌株,命名为Bacillussubtilis-TR1。Bacillussubtilis-TR1革兰氏染色呈红色,为革兰氏阳性菌。菌落形态为淡黄色,圆形,不透明,表面粗糙。扫描电镜(5 000倍)图片(图1)清晰显示其为杆状,细胞表面圆滑丰满,大小在1.5~2.0 μm之间,生长情况优良。

图1 菌株Bacillus subtilis-TR1的SEM照片
Bacillussubtilis-TR1的16Sr DNA序列比对结果显示,其与芽胞菌属细菌的同源性比较高。以MEGA 7.0软件构建系统发育树,结果如图2所示。进化树表明,该菌种与枯草芽孢杆菌BacillussubtilisNR的同源关系最近,由此判断该菌种为枯草芽孢杆菌。
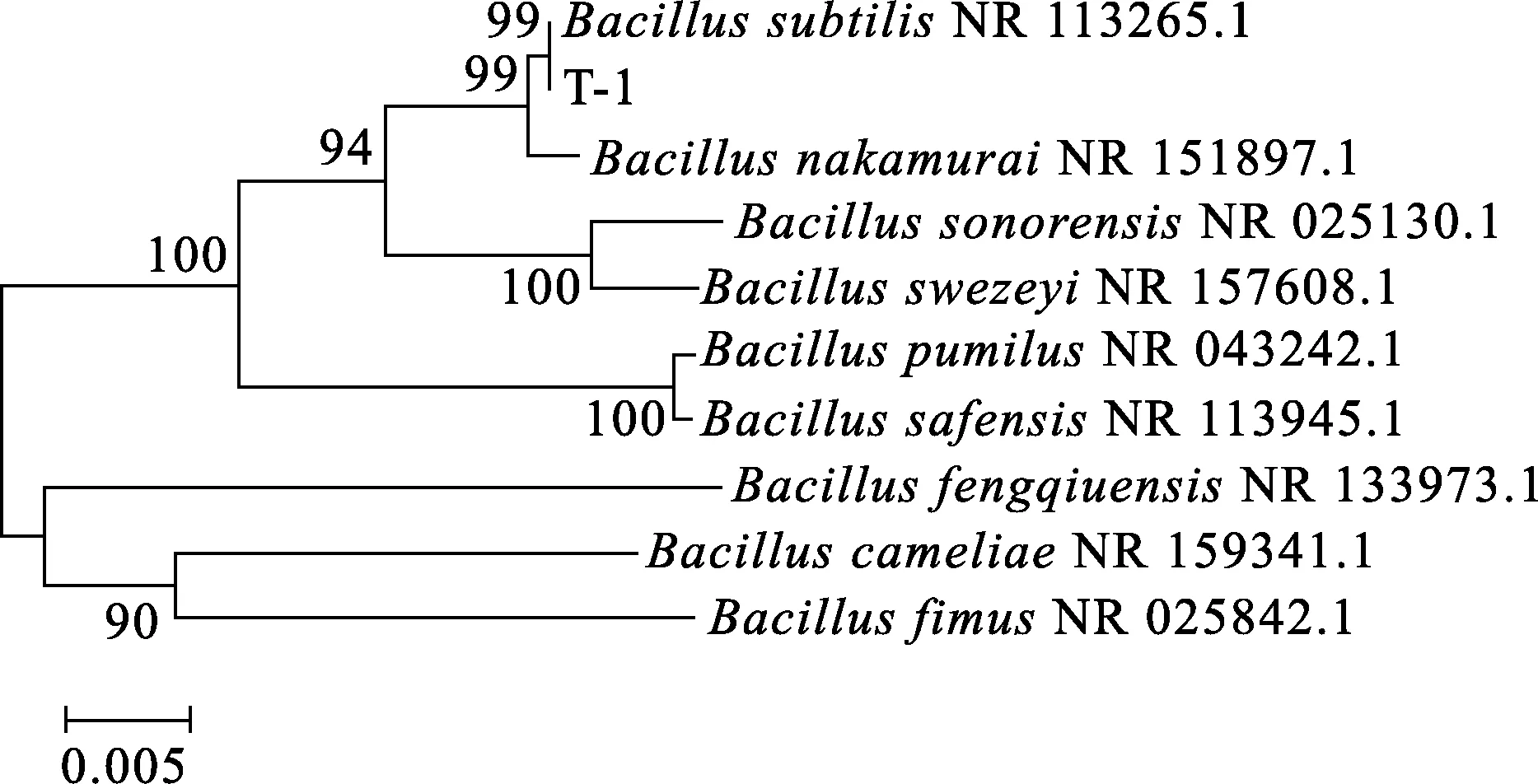
图2 基于16S rDNA序列以邻接法构建的Bacillus subtilis-TR1系统发育树
2.2 从废水中吸附Cu2+
2.2.1 体系初始pH对吸附的影响
一般认为,体系pH是影响生物吸附的最重要因素,尤其是以活细胞作吸附剂时。pH直接影响微生物菌体的活性,同时也影响溶液中离子的存在状态[20-21]。在Cu2+质量浓度50 mg/L、温度30 ℃、菌体加入量3 g/L、振荡速度150 r/min、菌体培养时间48 h条件下,调节体系初始pH在2.0~7.0之间,pH对细菌吸附Cu2+的影响试验结果如图3所示。

图3 体系初始pH对细菌吸附Cu2+的影响
由图3看出:体系初始pH为2.0~5.0时,Bacillussubtilis-TR1对Cu2+的吸附率随pH升高而升高;pH>5.0时,Bacillussubtilis-TR1对Cu2+的吸附率随pH升高而逐渐降低;pH=5.0时,吸附效率最高,达56.7%。pH过低,系统中的H+、H3O+会在细菌表面与金属离子结合位点竞争,而结合位点的缺失会导致Cu2+不能有效被细菌吸附;而如果pH过高,则溶液中开始出现大量OH-,也会阻碍细菌吸附Cu2+,它会直接与Cu2+结合从而阻碍重金属离子吸附到细菌表面[22]。因此,确定Bacillussubtilis-TR1吸附Cu2+的适宜体系pH=5.0。
2.2.2 初始Cu2+质量浓度对吸附的影响
在体系初始pH=5.0、温度30 ℃、菌体加入量3 g/L、振荡速度150 r/min、菌体培养时间48 h条件下,初始Cu2+质量浓度对细菌吸附Cu2+的影响试验结果如图4所示。
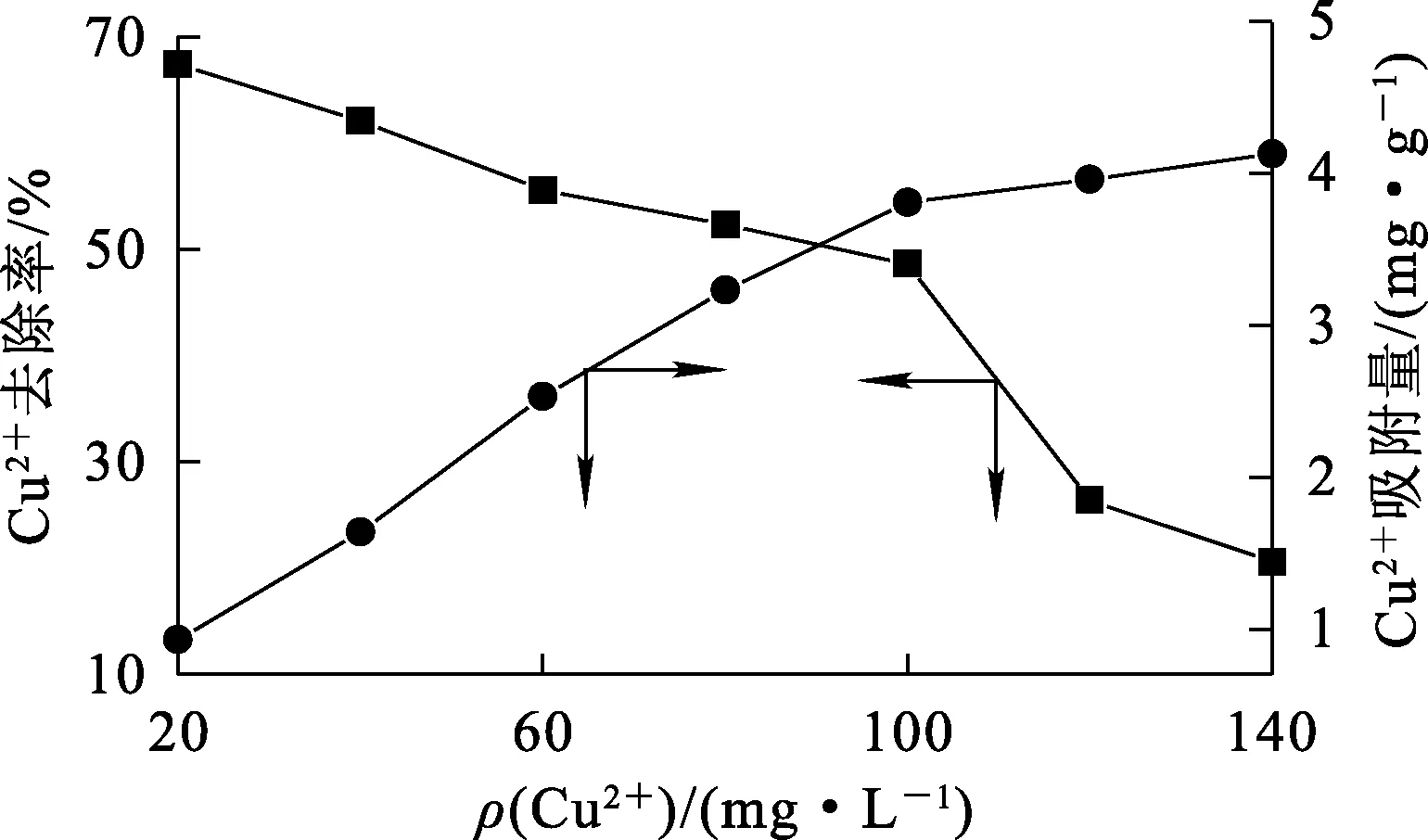
图4 初始Cu2+质量浓度对细菌吸附Cu2+的影响
由图4看出,初始Cu2+质量浓度对菌株Bacillussubtilis-TR1吸附Cu2+有明显影响:初始Cu2+质量浓度在20~140 mg/L范围内,Bacillussubtilis-TR1对Cu2+吸附率随Cu2+初始质量浓度升高呈下降趋势。可能的原因与细菌吸附位点饱和有关[23]。在Bacillussubtilis-TR1加入量一定时,其提供的结合位点数也是一定的。Cu2+质量浓度非常低时,结合位点数足够,Cu2+很易被菌体吸附,此时菌株对Cu2+的吸附率较高;而随Cu2+质量浓度升高,溶液中Cu2+总量增大,相应地,结合位点数没有变化,导致Cu2+吸附率下降。综合考虑,确定初始Cu2+质量浓度以80 mg/L为宜。
2.2.3 温度对吸附的影响
在Cu2+质量浓度80 mg/L、体系pH=5.0、菌体加入量为3 g/L、振荡速度150 r/min、菌体培养时间48 h条件下,温度对细菌吸附Cu2+的影响试验结果如图5所示。可以看出:温度在20~30 ℃范围内,随反应温度升高,菌株Bacillussubtilis-TR1对Cu2+的吸附率缓慢升高;而温度在30~40 ℃范围内,随温度升高,菌株Bacillussubtilis-TR1对Cu2+的吸附率呈缓慢下降趋势。温度对细菌的影响显而易见,因为任何一种菌体都有最适宜的生长温度范围[24]。温度过低会导致菌体生长代谢活动受到抑制,活性大幅下降;而温度过高会导致细胞壁、蛋白质等发生变异,活性消失,代谢发生障碍甚至死亡。综合考虑,确定体系温度以30 ℃最为适宜。
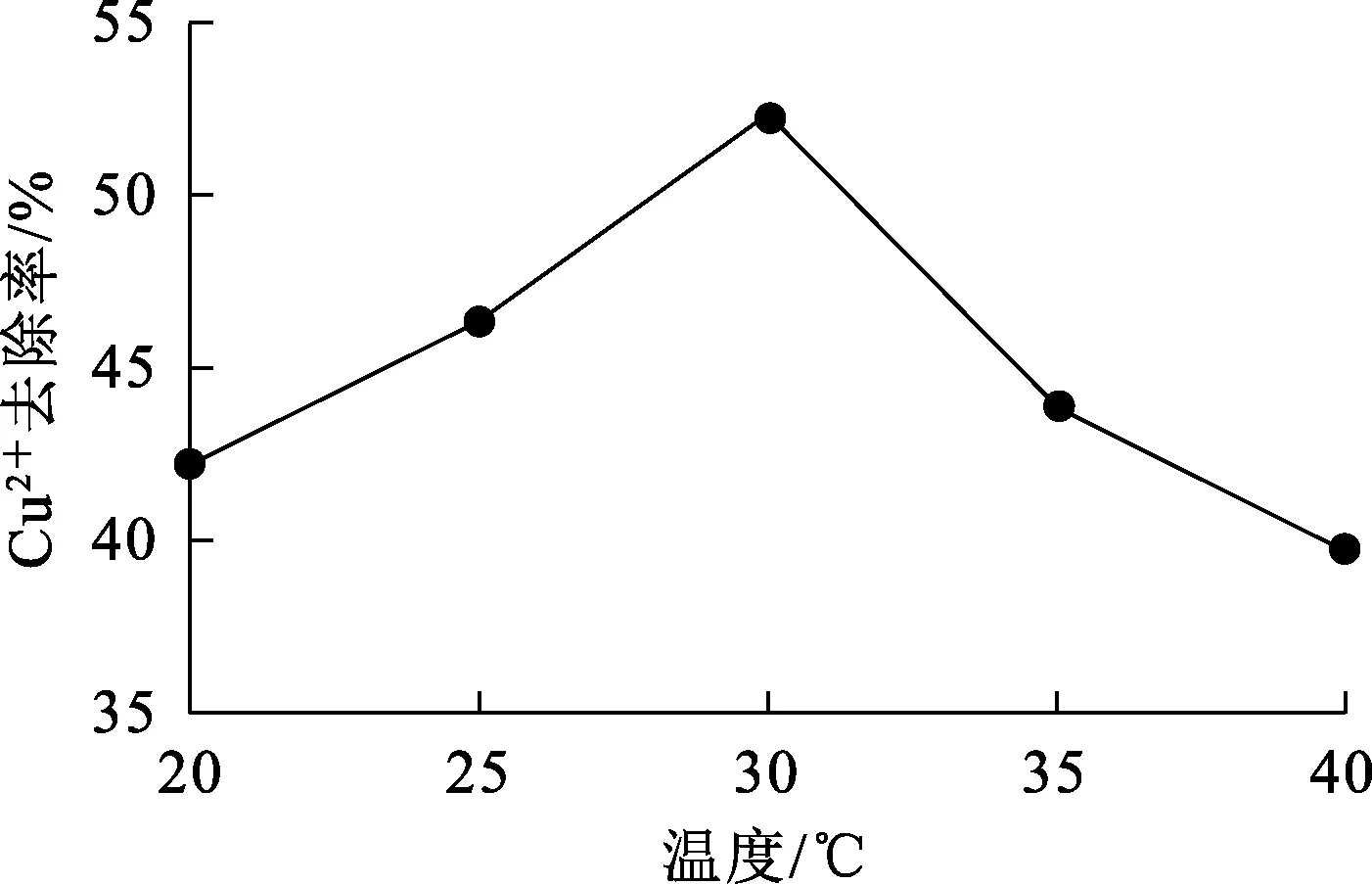
图5 温度对细菌吸附Cu2+的影响
2.2.4 菌体加入量对吸附的影响
生物体加入量在很大程度上影响对Cu2+的吸附。在Cu2+质量浓度80 mg/L、体系pH=5.0、温度30 ℃、振荡速度150 r/min、菌体培养时间48 h条件下,菌体加入量对细菌吸附Cu2+的影响试验结果如图6所示。
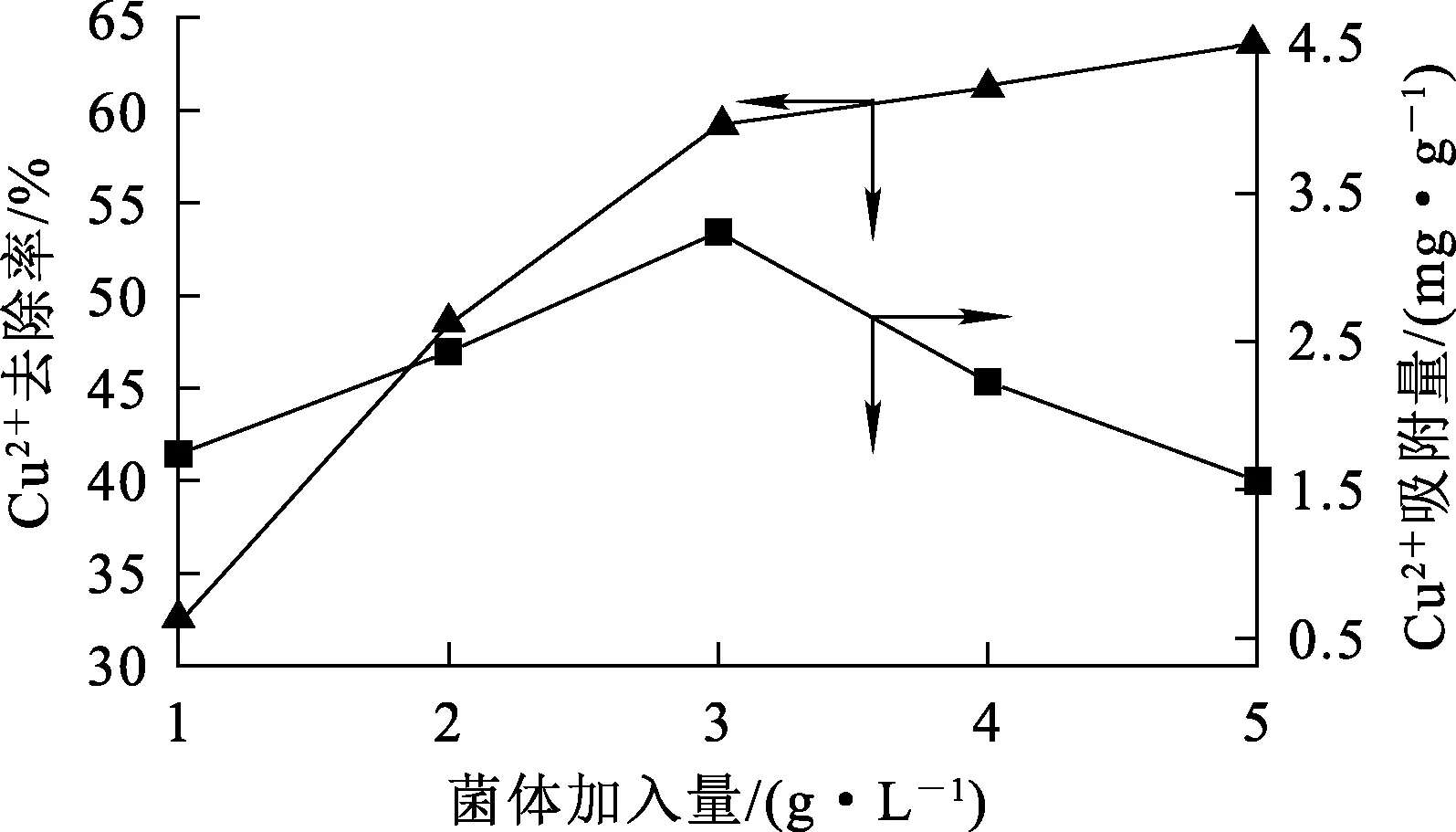
图6 菌体加入量对细菌吸附Cu2+的影响
由图6看出:随菌体加入量增大,Cu2+吸附率逐渐升高;但很明显,菌体加入量达3 g/L时,Cu2+吸附率达最大,之后缓慢下降。综合考虑,确定菌体加入量以3 g/L为宜。
生物体加入量增大,最直观的表现是吸附结合位点增多[25];但随菌体有效结合位点逐渐被金属离子及其他基团占据,并最终达到饱和,之后对金属离子的吸附量便呈下降趋势[20]。因此,菌体加入量在一定范围内效果才好。
2.2.5 菌体培养时间对吸附效果的影响
菌体培养时间不宜过长。培养基的营养有限,而菌体无限繁殖,培养时间过长会使菌体死亡代谢产物堆积,菌液杂质增多,纯度下降,对菌体的吸附效果产生直接影响[26]。在Cu2+质量浓度80 mg/L、体系pH=5.0、菌体加入量为3 g/L、温度30 ℃、振荡速度150 r/min条件下,菌体培养时间对细菌吸附Cu2+的影响试验结果如图7所示。
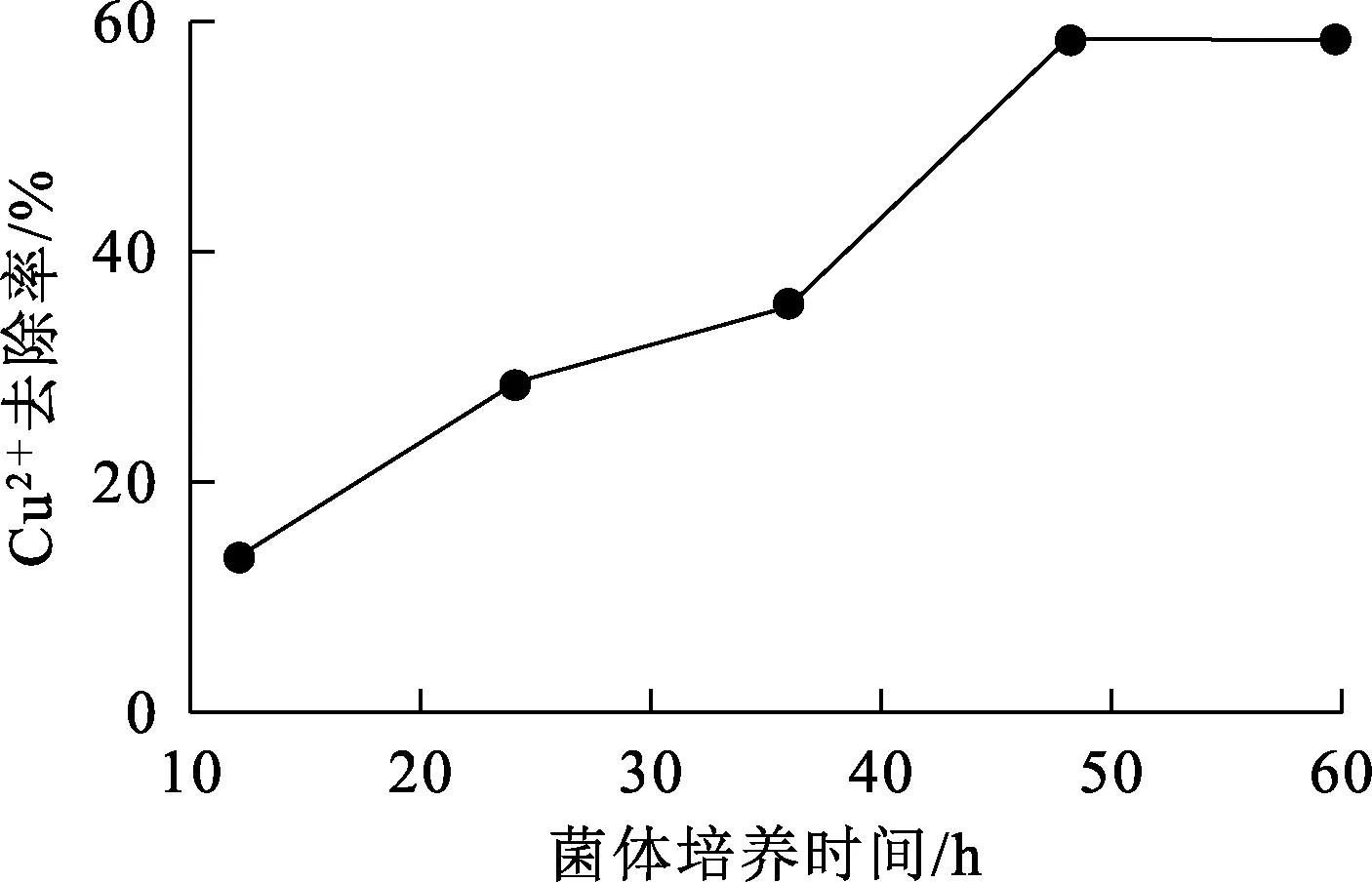
图7 菌体培养时间对细菌吸附Cu2+的影响
由图7看出:菌体培养48 h后达到对数增长期,代谢功能达到鼎盛,表面成分也比其他生长阶段多许多,对Cu2+的吸附率达最高,为58.6%;进入稳定期后,对Cu2+的吸附率逐渐平稳。综合考虑,确定菌体培养时间以48 h为宜。
2.3 吸附机制探讨

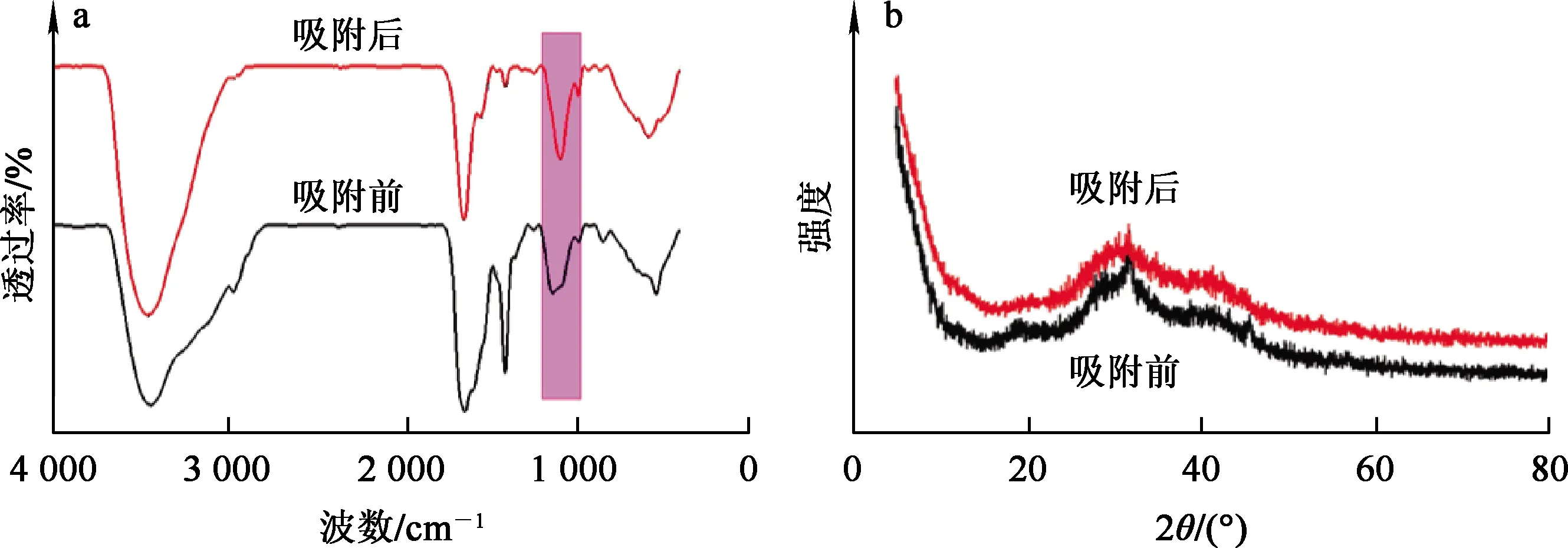
图8 菌株吸附Cu2+前、后的FT-IR谱线(a)和XRD谱线(b)
2.4 微观形貌变化
吸附前、后菌株Bacillussubtilis-TR1的SEM-EDS能谱如图9所示。可以看出,吸附后菌体中检测出Cu2+,表明菌体对Cu2+有吸附能力。

a—吸附前,SEM;b—吸附前,EDS;C—吸附后,SEM;d—吸附后,EDS。
3 结论
从电镀污泥中分离筛选得到的菌株对Cu2+有较高的吸附性能,分析其形态特征并结合16S rDNA测序和比对,确定此菌株为芽孢杆菌属中的枯草芽孢杆菌,命名为Bacillussubtilis-TR1。该菌株对Cu2+有较好的吸附效果,适宜条件(pH=5.0,初始Cu2+质量浓度80 mg/L,温度30 ℃,菌体加入3 g/L,菌种培养时间48 h)下对Cu2+的吸附量为4.02 mg/g,去除率为62.4%。
该菌株对Cu2+的吸附主要是通过其表面功能基团和静电引力,诱导废水中Cu2+发生迁移和离子交换,并与表面功能基团结合形成配合物,配合物为为典型非晶相结构。此功能菌可用于电镀污泥源头减量,并吸附去除废水中重金属离子。

