磁性多壁碳纳米管对花生油中黄曲霉毒素的脱除效果研究
吕雅芳,纪俊敏,苗红梅,3*,侯利霞,汪学德,王合宝
1.河南工业大学 粮油食品学院,河南 郑州 450001 2.河南工业大学 特色油料加工研究所,河南 郑州 450001 3.河南省农业科学院,河南 郑州 450000 4.平舆康博汇鑫油脂有限公司,河南 驻马店 463000
黄曲霉毒素(AFT)是黄曲霉和寄生曲霉的次生代谢物,是一类剧毒、致突变和致癌的化合物,会严重损害人类和动物的肝组织从而导致肝癌[1-2]。花生在种植、储存、加工过程中容易受到AFT的污染,由于AFT的亲脂性导致花生油也易受其污染,严重威胁着人们的生命健康[3]。在油脂中常见的AFT主要有黄曲霉毒素B1(AFB1)、黄曲霉毒素B2(AFB2)、黄曲霉毒素G1(AFG1)和黄曲霉毒素G2(AFG2)4种[4-5], 其中AFB1的毒性最强,被世界卫生组织以及国际癌症研究机构认定为I类致癌物。
为了保证油脂质量安全,花生油在加工过程中需要进行脱毒处理,常见的脱毒方法有物理、化学和生物3种方法[6],物理吸附以简单、方便、快捷等优点在植物油工业中得到了广泛的应用。到目前为止,活性炭、碳纳米管、蒙脱土、凹凸棒、高岭石等均可用于AFT的脱除[7-10]。然而,吸附完成后吸附剂与油不易分离,使得吸附过程更加耗时和困难。为了更高效地脱除AFT,将吸附剂与磁性Fe3O4纳米粒子相结合,获得磁性复合材料,利用Fe3O4的磁性能够有效地将复合材料从溶液中分离出来[11]。近年来,国外有不少学者将磁性材料应用于有机污染物的净化研究[12-14],但将磁性吸附剂应用于AFT脱除的报道很少[15-16]。
多壁碳纳米管(MWCNTs)以其丰富的表面基团和良好的吸附性能成为近年来的研究热点,其表面具有的丰富官能基团能提供大量的活性位点,可以对各种有毒物质进行吸附。作者采用化学沉淀法合成了磁性多壁碳纳米管(mMWCNTs),选用AFT作为目标脱除物,研究mMWCNTs磁性吸附剂对花生油中AFT的吸附性能,分析影响其脱除效果的因素,以期为AFT的高效脱除提供参考。
1 材料与方法
1.1 试验材料
花生油:市购花生,在实验室条件下自制冷榨花生油;多壁碳纳米管:苏州碳丰石墨烯科技有限公司;AFB1、AFB2、AFG1、AFG2标准品(纯度>99%):Sigma 公司;浓硫酸、浓硝酸、硫酸铁铵、硫酸亚铵、氨水:天津科密欧化学试剂有限公司;乙腈、甲醇:美国 VBS 公司;试验用水均为超纯水。
1.2 仪器与设备
Tecnai G2 F20型透射电子显微镜:美国FEI公司;NICO LET 6700型傅里叶变换红外光谱仪:德国布鲁克公司;6TZ-180型液态榨油机:郑州德源机械有限公司;ME204E型电子天平:梅特勒-托利多仪器(上海)有限公司;DF-101S型集热式恒温加热磁力搅拌器:金坛华峰仪器有限公司;SHZ-D(III) 型循环水式真空泵:巩义市予华仪器有限责任公司;LGJ-18型真空冷冻干燥机:北京松源华兴科技发展有限公司;e2695型高效液相色谱仪:美国Waters公司。
1.3 试验方法
1.3.1 AFT标准曲线的建立
AFT储备液的配制:用乙腈分别稀释AFB1、AFB2、AFG1、AFG2标准品,配制成质量浓度为200 ng/mL的AFB1、AFG1标准储备液以及质量浓度为100 ng/mL的AFB2、AFG2标准储备液,并于-40 ℃低温储藏。
AFT标准溶液的配制:用乙腈逐步稀释AFT储备液,配制质量浓度分别为 0.5、1、2.5、5、10、25、50、100 ng/mL等8个梯度浓度的AFB1和AFG1标准溶液,以及0.25、0.5、1、2.5、5、10、25、50 ng/mL等8个梯度浓度的AFB2和AFG2标准溶液,以目标物峰面积/内标物峰面积为纵坐标,目标物质量浓度/内标物质量浓度为横坐标,建立溶剂标准曲线,用于条件优化时 AFT的定量计算。
1.3.2 磁性碳纳米管的制备
1.3 观察指标 ①孕妇指标:观察两组孕妇孕期体质量增长(GWG),妊娠期糖尿病(GDM);②妊娠结局:剖宫产率,早产率,产后出血率,胎膜早破率;③新生儿指标:出生体质量,巨大儿,新生儿窒息。
参照曹慧等[17]、王彬等[18]的方法进行制备并进行一定的改进,具体如下。
酸化处理:称取2 g MWCNTs于500 mL圆底烧瓶中,加入50 mL浓硫酸和100 mL浓硝酸超声处理1 h,随后移入120 ℃磁力搅拌恒温油浴锅中冷凝回流1 h,抽滤并用蒸馏水反复水洗至中性,105 ℃烘干后研磨过200目筛网,备用。
复合:取上述处理后的 MWCNTs、硫酸亚铁铵和硫酸铁铵于500 mL三口烧瓶中,加入200 mL蒸馏水,随后置于磁力水浴搅拌器中,在氮气保护环境下逐滴加入约10 mL浓度为8 mol/L的氨水溶液,调节控制pH值为11~12,50 ℃搅拌处理30 min。反应结束后在外加磁场作用下,分离mMWCNTs复合材料,用去离子水洗涤至中性,-80 ℃条件下冷冻干燥,研磨过200目筛网,备用。
1.3.3 花生油中AFT的吸附及脱除
将含有AFT的20 g花生油加到50 mL三口瓶中,在压力≥8 kPa的条件下加热搅拌脱水,直至油面上看不到雾气。将油温加热至设定温度后加入一定量的mMWCNTs复合材料,控制油温并使油脂与mMWCNTs混合均匀,搅拌一段时间后停止加热。使油在真空条件下冷却一段时间后,关闭真空泵、冷却水。将油、mMWCNTs混合物倒入烧杯中,通过外加磁场分离出吸附剂,得到脱毒净油。
考察的吸附参数为吸附时间、温度、吸附剂量、磁负载量及AFT初始含量,以花生油中AFT的脱除率作为指标考察mMWCNTs对AFT的脱除效果。将测定结果代入1.3.1中建立的标准曲线并计算AFT含量。通过下式计算AFT的脱除率。
式中:QK为AFT的脱除率,%;C0、C分别为吸附前后油中AFT的质量浓度,ng/g。
1.3.4 仪器分析条件
试验所用的高效液相色谱仪型号为Waters-e2695分离系统,连接Waters-2475荧光检测器进行检测分析。采用柱后光化学衍生器进行衍生化处理,以增强AFT的荧光信号。色谱条件:流动相为V(甲醇/乙腈)∶V(水)=45∶ 55,其中甲醇和乙腈1∶ 1混合均匀,流速为0.8 mL/min,柱温为35 ℃,进样量为20 μL,激发波长和发射波长分别为360 nm和440 nm。在该色谱条件下,AFB1的出峰时间为27 min,AFB2的出峰时间为20 min,AFG1的出峰时间为18 min,AFG2的出峰时间为14 min,整个分析过程在40 min内完成。
1.3.5 数据处理
所有的分析测试和试验进行3次,以保证测定结果的准确性,数据为平均值±标准差。使用SPSS 24.0软件分析数据,使用Origin软件作图。
2 结果与分析
2.1 标准曲线的建立
用 1.3.1 配制的8个梯度浓度的4种AFT系列标准溶液建立溶剂标准曲线,结果如表1所示。4种AFT的标准曲线决定系数均在0.99以上,表明所有方程均具有良好的线性关系,可以用于后续AFT含量的计算。

表1 4种黄曲霉毒素系列标准溶液对应溶剂标准曲线Table 1 Solvent standard curves of four aflatoxin series standard solutions
2.2 吸附剂表征
通过TEM分析可以获得mMWCNTs材料的形貌特征。由图1 (a)可知,mMWCNTs 呈现出中空且相互交联的管状结构,管道之间的孔隙结构使mMWCNTs 具有更多的活性位点,便于对化合物的吸附。从图1 (b)可以看出,Fe3O4纳米粒子为单个球形颗粒,但由于纳米粒子之间的相互作用以及磁性粒子之间的磁吸引作用产生团聚现象。从图1(a)还可以看出,经过制备后 Fe3O4粒子成功负载在 MWCNTs表面及其孔隙间,表明mMWCNTs制备成功。
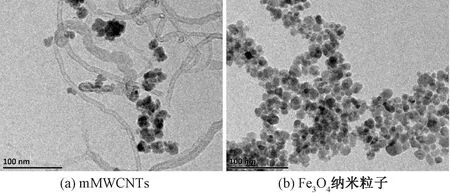
图1 mMWCNTs 和Fe3O4纳米粒子的透射电镜图Fig.1 TEM characterization of mMWCNTs and Fe3O4 nanoparticles


图2 mMWCNTs和Fe3O4纳米粒子的红外光谱图Fig.2 FT-IR spectra of mMWCNTs and Fe3O4 nanoparticles
2.3 不同吸附条件对花生油中AFT脱除率的影响
加标花生油中AFB1含量为20 ng/g,AFB2含量为5 ng/g,AFG1含量为10 ng/g,AFG2含量为5 ng/g。由于AFB1是花生油中含量最多且毒性最强的AFT,国标也只对AFB1和4种毒素总量有限量标准,故本研究主要考察mMWCNTs对花生油中AFB1及AFT(AFB1+AFB2+AFG1+ AFG2)脱除率的影响。
2.3.1 吸附时间对AFT脱除率的影响
在吸附温度60 ℃、吸附剂添加量2 mg/g的条件下,考察了吸附时间对AFT脱除率的影响,结果如图3所示。由于磁性复合吸附剂一开始有很多的表面位点可供AFT吸附,故随着时间的推移,AFB1以及AFT脱除率不断升高,在60 min时脱除率分别高达93.03%和90.57%。将反应时间从60 min延长到120 min,AFB1以及AFT的脱除率均无明显提高,说明在吸附时间为60 min时可能达到吸附剂的饱和接触点,之后脱除率基本没有变化。因此,选择60 min作为后续试验的吸附时间。
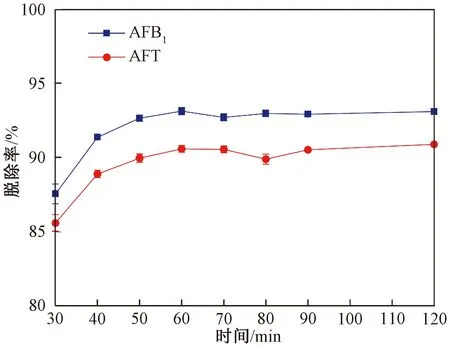
图3 吸附时间对AFT脱除率的影响Fig.3 Influence of adsorption time on AFT removal rate
2.3.2 吸附温度对AFT脱除率的影响
在吸附时间60 min、吸附剂添加量2 mg/g的条件下,考察了吸附温度对AFT脱除率的影响。由图4可知,AFB1和AFT的脱除率随着吸附温度的升高均呈先升高后降低的趋势。温度在60 ℃以下时,由于吸附短时间内达不到平衡,升高温度会加快吸附速率,从而出现脱除率升高的情况;当温度达到60 ℃时可能达到了吸附平衡,AFB1和AFT达到最大脱除率,脱除率分别为93.03%和90.80%;随着温度的进一步升高,吸附剂与AFT出现解吸,故在60~100 ℃时AFT脱除率整体略有下降。综上所述,对于花生油中AFT的脱除,吸附温度为60 ℃时脱除效果最好,因此选择60 ℃作为后续试验的吸附温度。
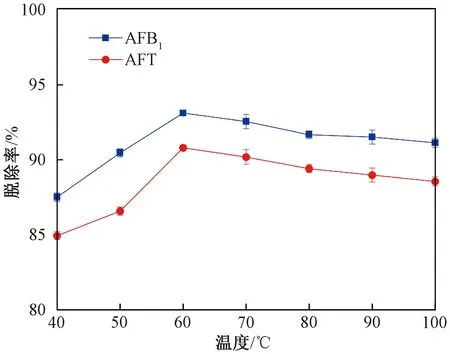
图4 吸附温度对AFT脱除率的影响Fig.4 Influence of adsorption temperature on AFT removal rate
2.3.3 吸附剂添加量对AFT脱除率的影响
在吸附温度60 ℃、吸附时间60 min的条件下,考察了吸附剂添加量对AFT脱除率的影响。从图5可以看出,随着吸附剂添加量的增加,AFB1及AFT脱除率均不断提高。在吸附剂添加量为0.5~1.5 mg/g时,随着吸附剂添加量的增加,AFB1及AFT的脱除率呈明显上升趋势,AFB1脱除率从84.86%上升到92.36%,AFT脱除率从83.02%上升到90.28%。继续增加mMWCNTs用量,会产生多余的吸附位点,由于没有多余的AFT与其作用,故脱除率不再明显上升,从而保持吸附平衡状态。从经济与安全方面考虑,选择1.5 mg/g作为后续试验的吸附剂添加量。
2.3.4 AFT初始含量对AFT脱除率的影响
在吸附温度60 ℃、吸附时间60 min、吸附剂添加量1.5 mg/g的条件下,考察了AFT初始含量对脱除率的影响。从图6可知,随着AFT初始含量的增加,AFB1和AFT脱除率不断下降,可能是由于吸附剂表面位点有限,AFT初始含量的增加导致一部分毒素没有被吸附。但在AFT初始含量为100 ng/g时脱除率仍能达到80%以上,说明mMWCNTs 对AFT有很好的脱除效果。
2.3.5 磁负载量对AFT脱除率的影响
在吸附温度60 ℃、吸附时间60 min、吸附剂添加量1.5 mg/g的条件下,考察了磁负载量对AFT脱除率的影响。从图7可以看出,随着复合吸附剂中磁负载量的增加,脱除率有所下降,说明在吸附过程中碳纳米管的表面位点起了主要的吸附作用。当Fe3O4纳米粒子与MWCNTs质量比为1∶ 4时,AFB1和AFT脱除率分别达93.76%和94.36%,Fe3O4纳米粒子与MWCNTs质量比为1∶ 1时,AFB1和AFT脱除率也仍能达85%以上,说明磁性吸附剂对花生油中AFT有较佳的脱除效果,同时磁负载量的增加能够使花生油和吸附剂快速高效地分离。
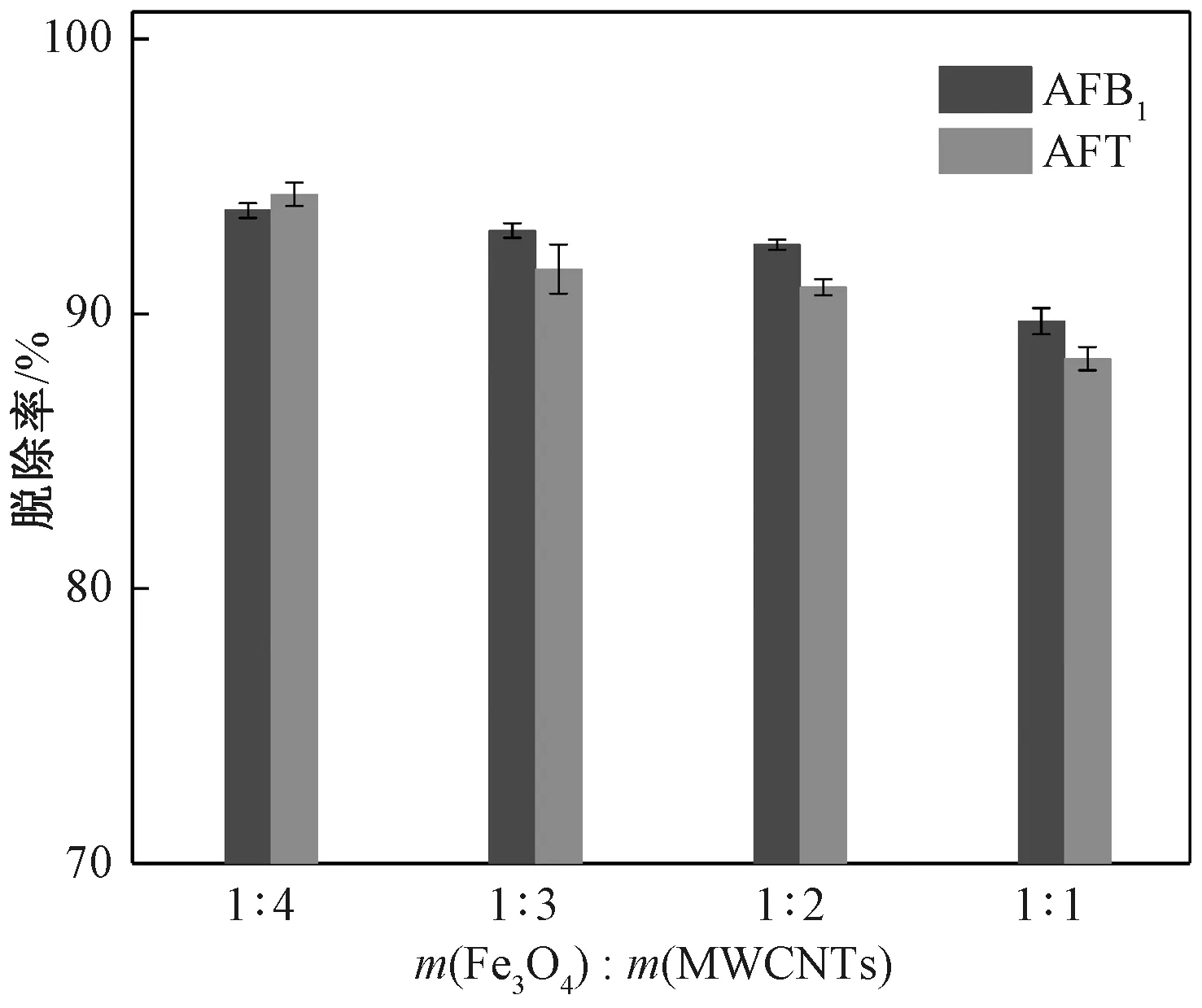
图7 磁负载量对AFT脱除率的影响Fig.7 Influence of magnetic load on AFT removal rate
3 结论
采用化学沉淀法成功制备了磁性多壁碳纳米管吸附剂,研究了mMWCNTs在不同吸附条件下对花生油中4种AFT的脱除效果。通过 TEM 和FI-IR表征,表明MWCNTs与Fe3O4粒子成功复合在一起且没有发生结构变化。在吸附时间为60 min、吸附温度为60 ℃、吸附剂添加量为1.5 mg/g时,mMWCNTs对花生油中AFT的脱除效果最好,AFB1和AFT的脱除率分别达92.36%和90.28%。在AFT初始含量为100 ng/g时脱除率仍能达到80%以上,AFT总含量从100 ng/g降到20 ng/g以下。随着吸附剂中磁负载量的增加,AFT脱除率有所降低,但始终保持在85%以上。该研究明确了mMWCNTs对花生油中AFT有较好的脱除效果且操作简单,与常规吸附剂相比大大缩短了吸附完成后油和吸附剂的分离时间。mMWCNTs在脱除AFT中展现出应用潜力,可扩展至其他磁性材料的制备。

