3,4-二氨基-5-(3,4-二氨基-1,2,4-三唑-5-基)-1,2,4-三唑及其含能离子盐的合成及性能
赵 霞,王金鑫,宋思维,亓秀娟,王康才,张庆华
(1.中国工程物理研究院化工材料研究所,四川 绵阳 621999;2.西南科技大学材料学院,四川 绵阳 621010)
1 引言
新型含能材料的设计与合成一直是含能材料基础研究的重要方向[1-3]。进入21 世纪来,围绕这一研究方向,研究人员设计合成了一系列新的含能化合物[4-6]。从结构上,主要分为以下五大类:1)共价型含能化合物[7];2)含能离子盐[8];3)含能共晶[9];4)分子钙钛矿型含能化合物[10];5)含能金属有机框架化合物[11]。其中,含能离子盐作为一类新兴的含能材料,凭借其结构的可设计性和性能的可调控性受到了广泛关注[12-14]。
近年来,国内外各科研机构围绕新型含能离子盐进行了大量研究工作,并取得了一系列重要进展。其中,Klapötke-课题组[17]设计合成的不敏感含能离子盐5,5′-双四唑-1,1′-二醇二羟铵(TKX-50)是典型的代表[15]。TKX-50 是由羟胺阳离子和羟基联四唑阴离子配对组合而成,其计算爆速高达9698 m·s-1,明显优于RDX(8838 m·s-1)[16],甚至与六硝基六氮杂异伍兹烷(CL-20,9640 m·s-1)相当[17]。TKX-50 的撞击感度达到20 J,优于TNT(15 J)[18]。此外,美国Shreeve 课题组[19]在新型含能离子盐合成方面也取得了一系列成果,并对该领域的最新进展进行了系统梳理和总结。已有研究结果表明:通过含能阴离子和高氮含量有机阳离子之间的合理搭配,能够有效地提高含能离子盐的能量和安全性。基于该策略,美国Shreeve 等[20]合成出了能量和密度均优于RDX,撞击感度优于TNT 的新型含能离子盐3,5-双(二硝基甲基)-1,2,4-三唑单胺盐,同时采用计算模拟的方法对该离子盐展现出的优异能量和安全性能进行了理论解释。该离子盐晶体结构中强的分子间π-π 相互作用和氢键网络对其优异的性能起了重要的作用。
将具有高氮含量的有机阳离子和富氧阴离子进行合理搭配,是实现目标含能离子盐性能调控的有效策略[21]。基于该策略,德国Klapötke[22]课题组采用具有稠环结构的3,6,7-三氨基-7H-[1,2,4]-三唑并[4,3-b][1,2,4]三唑鎓(TATOT)和高氯酸进行酸碱中和反应,制备了一种具有良好热稳定性的含能离子盐,其热分解温度为264 ℃。此外,范桂娟等[23]采用1H-咪唑[4,5-d]哒嗪-2,4,7-三胺阳离子和高氯酸根搭配,制备了一种高密度的含能离子盐,其密度为1.93 g·cm-3。该含能离子盐除具有高密度的特征外,还具有优异的感度特性,其撞击感度和摩擦感度分别为14 J 和168 N,优于RDX 的感度特征(撞击感度7.4 J,摩擦感度120 N)。
在前期的研究工作[24]中,采用4,7-哒嗪并氧化呋咱和高氯酸反应,制备了一种密度高达1.94 g·cm-3的含能离子盐。然而,该含能离子盐热稳定性较差,热分解温度仅为181 ℃。为了获得热稳定性更高的新型含能离子盐,本研究采用具有多氨基结构的3,4-二氨基-5(-3,4-二氨基-1,2,4-三唑-5-基)-1,2,4-三唑阳离子分别和高氯酸根(2)、硝酸根(3)进行组合,通过在目标含能离子盐晶体结构中构建氢键网络的策略,制备了两种具有高热稳定性的含能离子盐。该化合物超高的热稳定性使其在含能材料中具有较为广泛的应用前景。
2 实验部分
2.1 试剂与仪器
试剂:无水草酸、1,3-二氨基胍盐酸盐、多聚磷酸、氢氧化钠等均为分析纯,麦克林试剂公司。
仪器:德国Bruker D8 Venture X-射线单晶衍射仪;德国Bruker AVANCE 400 MHz 核磁共振波谱仪;德国Elementar Vario EL Cube 元素分析仪;德国Bruker Alpha 傅里叶变换红外光谱仪;德国耐驰公司STA449热分析仪(TG-DSC)。
测试方法:在170.0 K 条件下,对化合物2 和3 进行单晶X 射线衍射测试,采用直接法解析化合物2 和3的晶体结构,采用全矩阵最小二乘法对非氢原子坐标和各项异性热温度因子进行修正[25]。使用DMSO-d6作为氘代试剂,对化合物2 和3 进行了核磁测试。在氮气气氛下,以10 ℃·min-1的升温速率,采用差示扫描量热仪(DSC)和热重分析仪(TG)测试了化合物2和化合物3 的热稳定性。采用标准BAM 落锤法[26]和摩擦试验机对化合物2 和3 的撞击感度和摩擦感度进行了测试。采用NASACEA 软件计算了化合物2 和3的比冲和燃烧产物。具体参数设置为:燃烧室初温为298.15 K,燃烧室压强为69.98 MPa,压强比为69.4/4,收缩段面积比为1.3,扩展段面积比为5。
2.2 合成路线
采用Scheme 1 的路线,合成化合物1~3。首先,在120 ℃下,以草酸和二氨基胍盐酸盐为初始原料,多聚磷酸为溶剂,经缩合环化反应合成了高氮含能化合物3,4-二氨基-5(-3,4-二氨基-1,2,4-三唑-5-基)-1,2,4-三唑(化合物1)。然后,将化合物1分别与1M 高氯酸和1M 硝酸经中和反应合成了两种含能离子盐(化合物2 和化合物3)。
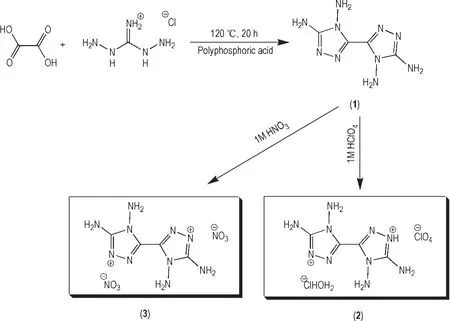
Scheme 1 Synthesis of1,2 and3
2.3 实验过程
2.3.1 3,4-二氨基-5-(3,4-二氨基-1,2,4-三唑-5-基)-1,2,4-三唑(1)的合成
取多聚磷酸7.5 g 加入至100 mL 的茄形反应瓶中,加热至120 ℃;将草酸(0.5 g,0.055 mol)和二氨基胍盐酸盐(1.8 g,0.014 mol)在研钵中研磨均匀后,少量多次加入反应瓶中,加料过程中会有大量气体产生;待原料全部加入后,保持120 ℃反应,直至反应液中无气泡产生,停止加热。待反应液降至室温后,倒入100 mL 冷水中,搅拌并用浓氢氧化钠溶液(pH=14)调节反应液的pH 值至8 左右,产生灰色沉淀。过滤留滤渣,并用冷水洗涤数次,于50 ℃烘箱中干燥12h得到纯净的化合物1(0.5g),基于草酸产率46%。
1H NMR(400 MHz,DMSO-d6,25 ℃)δ:5.91(s,2H),5.81(s,2H);13C NMR(100 MHz,DMSO-d6,25 ℃)δ:155.4,139.4;IR(KBr,ν/cm-1):3782,3400,3341,3278,3142,2348,1626,1537,1478,1421,1317,1252,1232,1085,1022,987,935,799,778,723,678,664;Anal.calcd for C4H8N10:C 24.49,H 4.08,N 71.43;found:C 24.49,H 4.11,N 71.40。
2.3.2 3,4-二氨基-5-(3,4-二氨基-1,2,4-三唑-5-基)-1,2,4-三唑高氯酸盐(2)的合成
取化合物1(0.5 g,0.0025 mol)加入10 mL 1 mol·L-1稀高氯酸中,80 ℃下加热搅拌至溶液澄清透明,停止加热,冷却后将反应液转移至小烧杯中,于常温静置3 d,过滤,干燥,得白色晶体(0.87 g,收率88%)。1H NMR(400 MHz,DMSO-d6,25 ℃)δ:6.16(s,2H),8.58(s,2H);13C NMR(100 MHz,DMSO-d6,25 ℃)δ:152.4,138.2;IR(KBr,ν/cm-1):3413,3347,3304,1696,1614,1098,1036,982,924,780,617;Anal.calcd for C4H10N10O8Cl2:C 12.10,H 2.54,N 35.27;found:C 12.36,H 2.63,N 35.24。
2.3.3 3,4-二氨基-5-(3,4-二氨基-1,2,4-三唑-5-基)-1,2,4-三唑硝酸盐(3)的合成
取化合物1(0.5 g,0.0025 mol)加入10 mL 1 mol·L-1稀硝酸中,80 ℃下加热搅拌至溶液澄清透明,停止加热,冷却后将反应液转移至小烧杯中,于常温静置3 d,过滤,干燥,得淡黄色晶体(0.67 g,收率84%)。1H NMR(400 MHz,DMSO-d6,25 ℃)δ:6.16(s,2H),8.58(s,2H);13C NMR(100 MHz,DMSO-d6,25 ℃)δ:152.4,138.2;IR(KBr,ν/cm-1):3328,3111,1691,1608,1410,1311,1050,978,943,847,681;Anal.calcd for C4H10N12O6:C 14.91,H 3.13,N 52.17;found:C 15.00,H 3.12,N 51.53。
3 结果与讨论
3.1 晶体结构
化合物2 和3 的晶体学数据如表1 所示,化合物2和化合物3 的晶体结构分别如图1 和图2 所示。
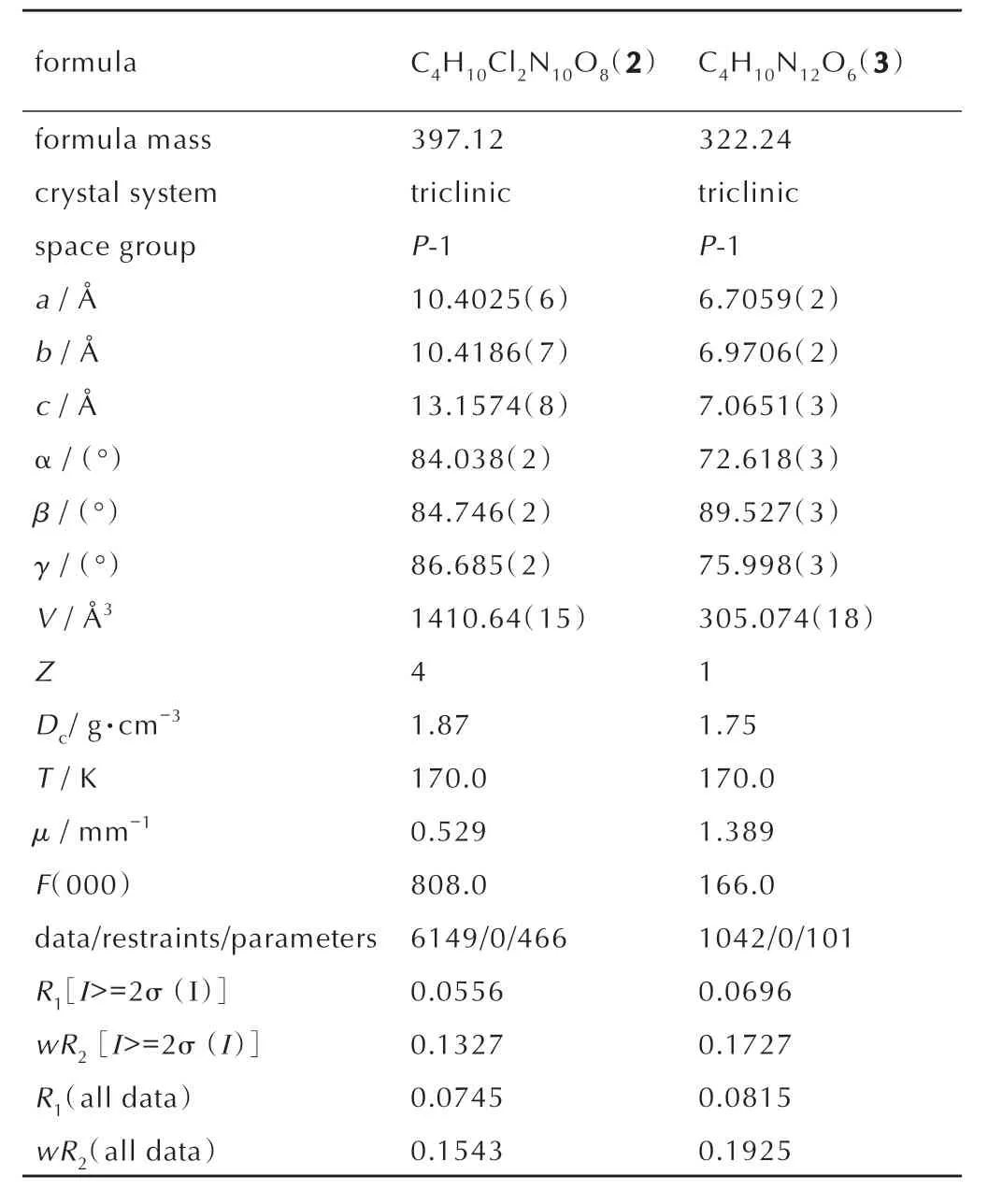
表1 化合物2 和3 的晶体学参数Table 1 Crystallographic parameters of2 and3
化合物2(CCDC:2098132)属于三斜晶系,P-1 空间群,晶胞参数为a=10.4025(6)Å,b=10.4186(7)Å,c=13.1574(8)Å,α=84.038(2)°,β=84.746(2)°,γ=86.685(2)°,V=1410.64(15)Å3,Z=4。化合物2 的不对称单元中包含两个质子化的3,4-二氨基-5(-3,4-二氨基-1,2,4-三 唑-5-基)-1,2,4-三唑阳离子(1)和四个高氯酸根离子(图1a)。阳离子中的所有非氢原子共同占有同一个平面。每个阳离子通过氢键和12 个相邻的高氯酸根相互作用(图1b),每个高氯酸根和6 个相邻的阳离子相互作用(图1c)。这些氢键键长范围为2.073(2)~2.750(2)Å。阴阳离子之间通过上述相互作用方式构筑了化合物2 的晶体结构(图1e)。化合物2 的晶体结构还可以看作是由阳离子构筑的层状结构(图1d)沿a轴堆积,高氯酸根填充在层与层之间,起到平衡电荷的作用。
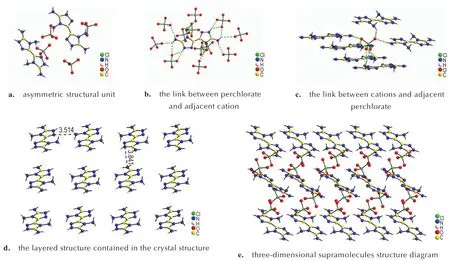
图1 化合物2 的晶体结构图Fig.1 The crystal structure of2
化合物3(CCDC:2098133)属于三斜晶系,P-1 空间群,晶胞参数为a=6.7059(2)Å,b=6.9706(2)Å,c=7.0651(3)Å,α=72.618(3)°,β=89.527(3)°,γ=75.998(3)°,V=305.07(1)Å3,Z=1。化合物3的不对称单元中包含半个阳离子和一个硝酸根离子(图2a)。阳离子分子骨架上的所有非氢原子均在同一平面上。化合物3 的晶体结构中,每个硝酸根通过氢键和5 个相邻的阳离子相互作用(图2b),每个阳离子通过氢键和10 个相邻的硝酸根相互作用(图2c)。氢键键长范围为:1.8630(1)~2.3965(1)Å。化合物3晶体中阴阳离子之间通过这些氢键相互连接,构筑了化合物3 的晶体结构(图2e)。
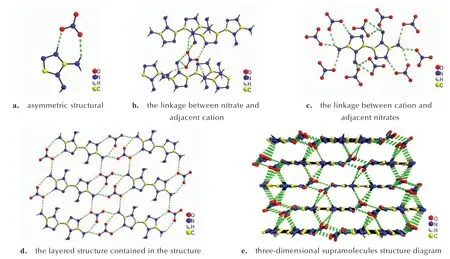
图2 化合物3 的晶体结构图Fig.2 The crystal structure of compound3
为了进一步研究化合物2 和3 晶体中各组分之间的相互作用,本研究采用Crystal Explorer 13.5[27]软件对化合物2 和3 的Hirshfeld 表面及二维指纹谱进行了拟合,具体如图3 所示。Hirshfeld 表面上红色的圆点表示分子间强相互作用力,蓝色部分示分子间弱相互作用力。从图3a 中可以看出,化合物2 中的阳离子的Hirshfeld 表面具有平整的结构,红色圆点主要分布在平面结构的四周。这些红点代表高氯酸根上氧原子和阳离子之间的氢键作用(O…H 和N…H),占Hirshfeld表面表面积的61.6%。其中,O…H 和N…H 之间的氢键占比分别为47.4%和14.2%。Hirshfeld 表面上的蓝色圆点共占其表面积的38.4%,这些蓝色部分主要代表分子间的π-π 相互作用(N…O、C…O 等)。同化合物2 相比,化合物3 的Hirshfeld 表面上的红色圆点占比相对较少,为56.9%。其中,O…H 和N…H 之间的氢键占比分别为40.6%和16.3%。化合物2 和3 具有相同阳离子,但其阳离子的二维指纹谱形状具有较大的差异。这表明二者晶体结构中,各组分之间的相互作用力不同。
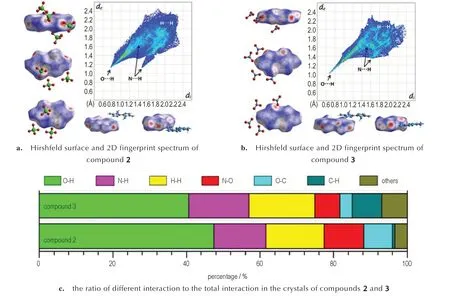
图3 化合物2 和化合物3 的Hirshfeld 表面及二维指纹谱及其晶体结构中不同相互作用力占总作用力的比例Fig 3 Hirshfeld surface and 2D fingerprint spectrum of2 and3,the ratio of different interaction to the total interaction in the crystals of2 and3
3.2 物理化学性能
密度、热分解温度、生成焓和感度是含能材料重要的物理化学性能参数,化合物2、3 以及三硝基甲苯(TNT)、黑索今(RDX)的性能对比见表2。由表2 可以看出,化合物2 和3 的晶体密度分别为1.87 g·cm-3和1.75 g·cm-3,均高于TNT 的密度[8](1.65 g·cm-3),其中化合物2 的密度甚至高于高能炸药RDX 的密度。化合物2 的高密度特征,有利于其在含能材料领域的应用。稳定性是含能材料能否进一步开发的基础保障。化合物2 和3 均具有较好的热稳定性,其热分解温度分别为338.3 ℃和289.8 ℃,均高于RDX 的热分解温度。化合物2 和3 优异的热稳定性与富氮含能化合物1 超高的热稳定性(Td=364.2 ℃)都与晶体结构中的丰富氢键网络密切相关。化合物2 和化合物3的TG-DSC 曲线如图4 所示。化合物2 的热分解温度高于大部分已知含能离子盐的热分解温度,例如:3,6,7-三氨基-7H[-1,2,4]三唑并[5,1-c][1,2,4]三唑-2-鎓硝酸盐(Td=279 ℃),3,6,7-三氨基-7H-[1,2,4]三唑并[5,1-c][1,2,4]三唑-2-鎓高氯酸盐(Td=257 ℃)[28];3,9-二氨基-6,7-二氢-5H-双([1,2,4]三唑)[4,3-e:3′,4′-g][1,2,4,5]四氮杂-2,10-二鎓硝酸盐(Td=203℃),3,9-二氨基-6,7-二氢-5H-双([1,2,4]三唑)[4,3-e:3′,4′-g][1,2,4,5]四氮杂-2,10-二鎓高氯酸盐(Td=278 ℃)[29]。
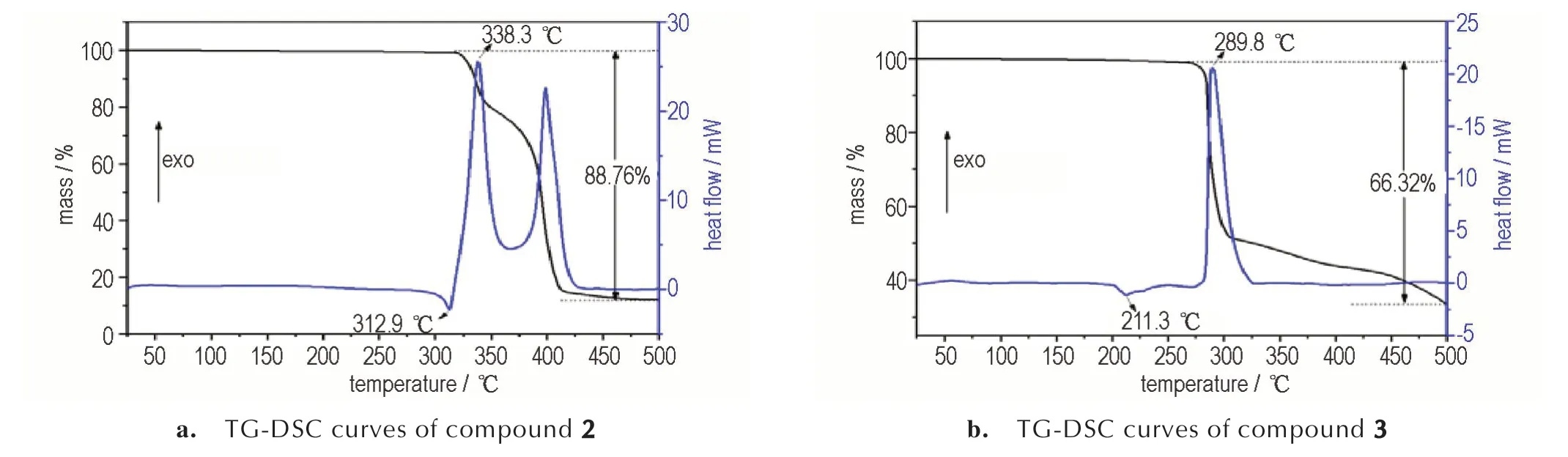
图4 化合物2 和化合物3 的TG-DSC 曲 线Fig.4 TG-DSC curves of2 and3
本研究采用Gaussian 09(D.01)软件[32]对化合物2和3的生成焓进行了理论计算,采用该方法计算的化合物2和3的生成焓分别为-0.1 kJ·mol-1和-120.7 kJ·mol-1。化合物2 的撞击感度和摩擦感度实测结果分别为4 J 和96 N;化合物3 的撞击感度和摩擦感度实测结果分别为大于20 J 和360 N。化合物2和3 之间较大的感度差异与其化学组成和晶体结构有密切的关系。含能离子盐中,高氯酸盐通常较硝酸盐具有更高的感度特征。高氯酸根具有更高的氧含量是其对应含能离子盐具有更高感度的可能原因之一。化合物2 中每个阳离子和12 个高氯酸根作用,而化合物3 中每个阳离子和10 个硝酸根作用,这可能是导致化合物2 较化合物3 具有更高感度的原因。
3.3 能量特征
含能材料的能量特征与其生成焓具有直接的关系。本研究采用EXPLO5v6.02[33]对化合物2和3的爆速和爆压进行了计算,计算结果如表2所示。由表2可以看出化合物2和3的爆速分别为8308m·s-1和8452 m·s-1,爆压分别为30.1 GPa 和27.1 GPa,均高于TNT 的爆速和爆压。除此之外,本研究还采用NASA CEA 软件[34]对化合物2 和3 的比冲和燃烧产物进行了计算模拟。化合物2 和3 的真空比冲分别为250.3 s 和214.3 s。化合物2 的真空比冲较TNT 的真空比冲(221.9 s)更高,但是低于RDX 的真空比冲(269.3 s)。通常情况下,含能材料生成焓和氢含量高,燃烧产物平均分子量小,有利于提升含能材料的比冲性能。从图5 可以看出,化合物2 和化合物3 的燃烧产物中占比最多的是氮气,分别为33.32% 和41.27%,这与化合物具有高氮含量特征相吻合。化合物2 和3 燃烧产物的平均分子量分别为26.473 和22.165。化合物3 具有更小的燃烧产物分子量的原因是其燃烧产物中含有大量的氢气(24.25%)。虽然化合物3 具有更小的燃烧产物分子量,但是其比冲依然小于化合物2 的比冲,这主要是由于化合物2 具有更高的生成焓。为了进一步解释化合物2 具有更高比冲的原因。采用NASA CEA 软件对化合物2和3的产气量进行了计算。计算结果表明:化合物2的产气量为2.4 L·g-1,化合物3 的产气量为1.8 L·g-1。化合物2 更高的产气量可能也是其具有更高比冲的主要原因之一。
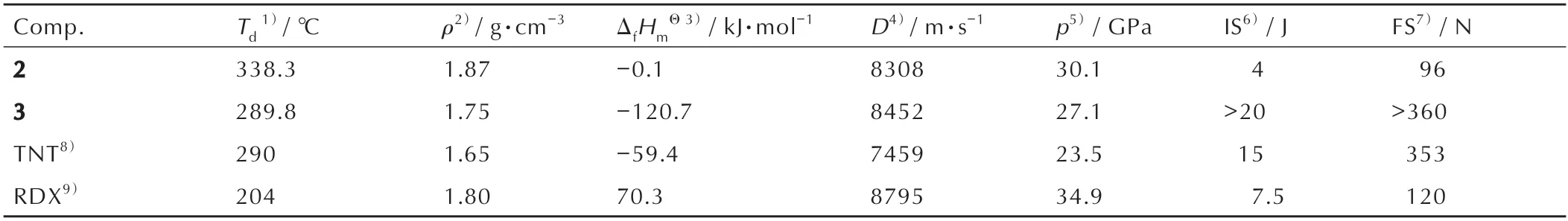
表2 化合物2、3、TNT 和RDX 和的物理化学性能Table 2 Physicochemical properties of1,2,and reference compounds
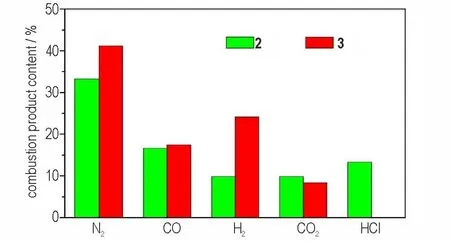
图5 化合物2 和化合物3 的理论模拟燃烧产物及其分布图Fig.5 The simulated combustion products and their contents of2 and3
4 结论
以廉价的草酸和1,3-二氨基胍盐酸盐为起始原料,在多聚磷酸中通过环化反应,制备了具有高氮含量的含能化合物3,4-二氨基-5(-3,4-二氨基-1,2,4-三唑-5-基)-1,2,4-三唑。将该化合物分别和高氯酸、硝酸作用,制备了具有高热稳定性的含能离子盐2 和3。化合物2 和3 不仅具有高密度,还具有高爆轰性能,以及优异的机械感度,具体为:
(1)化合物2 和3 的热分解温度分别为338.3 和289.8 ℃。
(2)化合物2 和3 具有高密度特征,其晶体密度分别为1.87 g·cm-3和1.75 g·cm-3,均高于TNT 的密度(1.65 g·cm-3),化合物2 的密度高于高能炸药RDX 的密度(1.80 g·cm-3)。
(3)化合物2 和3 还具有较好的爆轰性能,化合物2 的理论爆速和爆压分别为8308 m·s-1和30.1 GPa,化合物3 的理论爆速和爆压分别为8452 m·s-1和27.1 GPa。
(4)化合物3 具有比TNT 更优异的感度性能,其撞击感度和摩擦感度分别大于20 J 和360 N。
(5)化合物2 和3 优异的热稳定性,进一步验证了通过阴阳离子之间的合理搭配,可以实现对目标含能化合物性能的调控。

