含不同形貌MoO3的Al/MoO3铝热剂的热性能和燃烧性能
陈嘉琳,郭 涛,姚 淼,李 师,丁 文,宋佳星,刘 珩,肖力铭
(陆军工程大学野战工程学院,江苏 南京 210007)
1 引言
含能材料是一类含有大量化学能的化合物或混合物[1-3],其在反应过程中会释放出大量的热。其中,铝热剂以其较高的燃烧效率、能量释放率和反应放热焓而引起了许多研究者的关注,并且,铝热剂已被广泛应用于气体发生器[4-5]、焊接[6]、弹药销毁[7]、高能添加剂[8]等领域。近年来,由纳米燃料和氧化剂颗粒混合而成的纳米铝热剂,由于其较大的比表面积和较小的颗粒间距而备受关注[9]。
铝粉具有单位密度放热高、反应活性好、反应产物无毒等优点,广泛用于炸药和推进剂中以提高能量和温度[10-11],关于Al 与其他金属氧化物组成的铝热剂已有较多研究。姜艾锋等[12]制备了Al/Fe2O3铝热剂并探索了其燃烧性能;王启辉等[13]研究了Al/CuO 铝热剂,结果表明其具有良好的放热性能;宋佳星等[14]制备了Al/MnO2铝热剂作为销毁器并进行了钢靶穿透实验;Wolenski[15]对铝热剂中Al/MoO3颗粒的组成和形貌进行了改造并对燃烧行为进行调整。在化学计量比下,Al/MoO3反应的放热焓在诸多金属氧化物中(如Fe2O3、CuO、NiO、PbO2、Co3O4、Bi2O3、WO3、CuO、TiO2、Cr2O3和MoO3)是最高的[16],因此,本研究选取MoO3作为铝热剂中的氧化物的组分展开研究。MoO3的层状结构可以剥离成二维平面,以层状氧化钼为基础,通过与其它材料掺杂,可调整其性质,特别是使用氢和碱离子进行掺杂,能够大幅度提高储能效率和优化电化学系统。MoO3独特的化学和物理特性使其广泛应用于光学、电子、催化、生物和能源系统[17],此外,先前的研究表明,Al/MoO3铝热剂具有更好的点火性能[18]。
MoO3有许多不同的形态,例如,杜凯[19]制备了MoO3纳米球,其球形结构增加了其比表面积和高分散性,大大提高了MoO3的催化性能;Siciliano[20]制备了性能优异的MoO3纳米带传感器,MoO3纳米带具有宽径的结构优点,在纳米器件中占有优势;Dhage[21]合成了六方的MoO3纳米棒,其具有的亚稳态结构通常在感光变色和机械硬度方面表现出一些增强的性质[17]。对于MoO3的单一形貌已有很多研究,但对于不同形貌的MoO3对铝热剂性能的影响尚缺乏系统探索。制备球形结构MoO3所需的试剂与设备不易获得,合成工艺较为复杂,且产率较低;片状结构的MoO3大多由高能球磨法制得,所得到的MoO3片状结构不规则,且大小不一。因此,考虑到实验的可操作性和形貌可控性,本研究采用水热法制备了棒状和带状两种不同形态的MoO3,并采用超声混合法制备了Al/MoO3铝热剂。通过场发射扫描电子显微镜(FE-SEM)、X 射线衍射仪(XRD)和差示扫描量热仪(DSC)对不同形态MoO3组成的铝热剂进行了表征和分析,采用开放式和封闭管燃烧实验,探讨了其燃烧性能。最后,从反应机理方面对结果进行了初步分析,研究结果可为Al/MoO3铝热剂的性能和安全研究以及应用探索提供依据。
2 实验部分
2.1 试剂与材料
纳米铝粉A(l50~80 nm),上海耐欧纳米科技有限公司,活性约为60%;七钼酸铵(NH4)6Mo7O24·4H2O 和硝酸HNO3(68.8~69.8%),上海灵峰化学试剂有限公司;十六烷基三甲基溴化铵CTAB(96%),四川智恒工业制品有限公司;无水乙醇(纯度>99.7%)和去离子水,上海久益化学试剂有限公司。所有试剂均为分析级,不需进一步加工即可直接使用。
2.2 实验过程
使用最常用的水热合成法制备纳米MoO3,其具体流程如下。首先,将1.5 g(NH4)6Mo7O24·4H2O 和30 mL去离子水配置成钼酸铵溶液并磁力搅拌30 min。然后,将5 mL 稀释后的硝酸溶液逐滴加入到搅拌的钼酸铵溶液中,观察白色絮状物产生。随后,混合溶液在25 ℃的条件下超声10 min,将溶液转移到100 mL 聚四氟乙烯内衬中并装入到不锈钢高压反应釜中,密封,在200 ℃下加热25 h。反应完毕后,将反应釜自然恢复到室温,用去离子水清洗样品3 次并离心。随后,沉淀物在80 ℃下干燥12 h 后研磨,并置于管式煅烧炉中,在400 ℃下煅烧12 h,得到MoO3纳米棒样品。化学反应方程式如下:
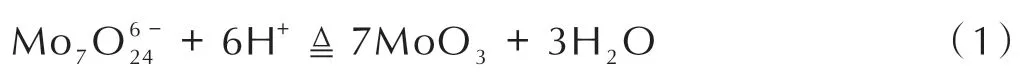
纳米带状MoO3的制备与上述工艺相同,只是在添加HNO3之前添加1 g CTAB。其他步骤保持不变。制备工艺如示意图1 所示。
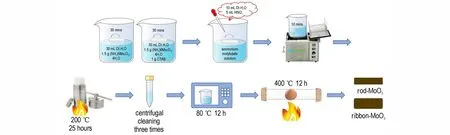
图1 纳米MoO3制备工艺示意图Fig.1 Schematic diagram of nano MoO3 preparation process
采用超声分散法制备Al/MoO3铝热剂,纳米MoO3的质量控制在120 mg。根据化学计量比制备铝热剂。根据化学方程式的计算,120 mg MoO3达到零氧平衡所需的燃料铝质量约为45 mg,然而,使用的铝粉只有约60%的活性,因此样品铝的质量为75 mg。

以Al/棒状MoO3铝热剂的制备过程为例,120 mg纳米棒状MoO3与75 mg 纳米铝粉分别溶于无水乙醇中并磁力搅拌。之后,将两溶液混合,继续搅拌20 min。随后,将混合溶液超声分散30 min 以获得均匀分散的悬浮液。最后,经过80 ℃干燥12 h 得到铝热剂样品。Al/带状MoO3铝热剂的制备流程与上述相同,只不过用的是带状MoO3。
2.3 表征与热分析
用XRD(Bruker,D8 Advance,德国)对MoO3与Al/MoO3铝热剂的相结构进行表征,30 kV 辐射源CuK(αλ=0.1542 nm)。用FE-SEM(日立高技术公司,S-4800 II,日本)观察纳米铝热剂的形貌特征,设备的加速电压为5 kV。
用DSC(耐驰STA 449F3,德国)对铝热剂样品进行热分析,测试的温度范围为30~800 ℃,升温速率分别为10、15、20、25 K·min-1,氩气流量为100 mL·min-1。为了尽可能地除去样品池中的空气,在升温之前,先启动氩气40 min 以排出空气。样品质量小于3 mg 以保证安全。
2.4 燃烧实验
通过自行设计的燃烧实验装置,分别进行了开放式和封闭管燃烧实验。开放式燃烧实验装置参见文献[22],在其基础上进行了优化与调整,其实验装置的示意图如图2 所示。
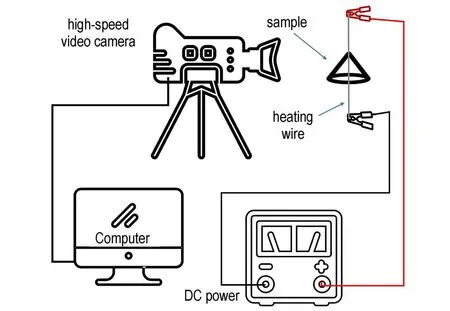
图2 开放式燃烧实验示意图Fig.2 Schematic diagram of open combustion experiment
实验过程中,称取10 mg 铝热剂样品堆放在试验台,堆放时应注意保证样品的均匀性以消除密度梯度带来的影响,之后使用一个可调节的直流发电电源来快速加热直径为0.1 mm 的镍铬丝,当电压加到一定程度后,镍铬丝会点燃铝热剂样品。整个燃烧过程使用高速摄影机(日本FASTCAM SA-Z)记录,采样率为20000 帧/s,帧大小为768×768 像素,光圈值为3.2。实验是在干燥无风的条件下进行,环境温度为24 ℃。
图3 为封闭管燃烧实验示意图。不同的是,Al/MoO3铝热剂的质量为15 mg,装在内径2 mm、长20 cm 的甲基丙烯酸甲酯管中,但装药量仅用到了甲基丙烯酸甲酯管的前段2.0 cm。实际装填密度计算为装药量(15 mg)除以装药体积(62.8 mm3),结果为0.239 g·cm-3。高速摄影机用于测量火焰反应前沿的速度,其采样率为40000 帧/s,帧大小为384×160 像素,光圈值为6.4。
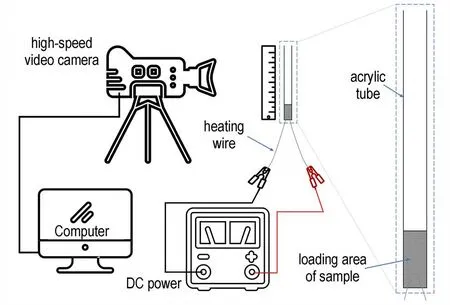
图3 封闭管燃烧实验示意图Fig.3 Schematic diagram of closed tube combustion experiment
3 结果与讨论
3.1 形貌与晶体结构分析
用FE-SEM 观察合成MoO3的微观形貌,如图4 所示。由图4 可知,未加入CTAB 试剂所合成的MoO3颗粒呈棒状(图4a),直径100~170 nm,长度10~25 μm,粒子均匀分散且表面光滑(图中黄色箭头)。加入CTAB试剂得到的MoO3呈现出带状(图4b),直径200~300 nm,长度8~20 μm,呈现出密集堆积的形状。

图4 两种MoO3的SEM 图像Fig.4 SEM images of MoO3
为确定水热法所得样品的晶体结构,对MoO3样品进行了XRD 分析,结果如图5 所示。
从图5 中可以观察到,两种样品的衍射峰大致相同,都与MoO3的标准卡(ICSD 号89-7112 MDI Jade 6.0)相匹配,12.8°、23.3°、25.7°、27.3°、39.0°、49.3°和58.8°处有7 个峰,分别对应于(200)、(101)、(400)、(210)、(600)、(020)和(810)晶面。
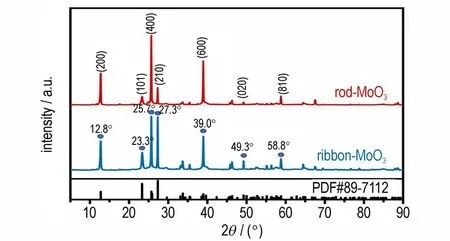
图5 棒状和带状MoO3的XRD 图谱Fig.5 XRD pattern of rod-MoO and ribbon-MoO3
Al/棒 状MoO3和Al/带状MoO3铝热剂的SEM结果如图6所示,每幅图的右侧是中间黄色框部分放大图像。由图6a 可见,Al/棒状MoO3存在纳米Al 颗粒团聚的现象,且比较多,如图中红色圈中的部分,由图6b 可见,虽然Al/带状MoO3也出现了团聚现象,但从放大的图像中能能够更清楚地看出带状的MoO3上均匀地分散着Al,这可能是因为带状结构的MoO3相比于棒状结构的MoO3能够为铝粉提供更多的附着点,因此铝粉可以在更多的附着点上分散,而棒状的MoO3由于附着点少,所以趋向于团聚。

图6 两种铝热剂的SEM 图Fig.6 SEM images of two thermites
3.2 热分析
两种铝热剂样品的DSC 曲线如图7 所示。表1 列出了铝热剂样品的主要放热峰的具体信息。
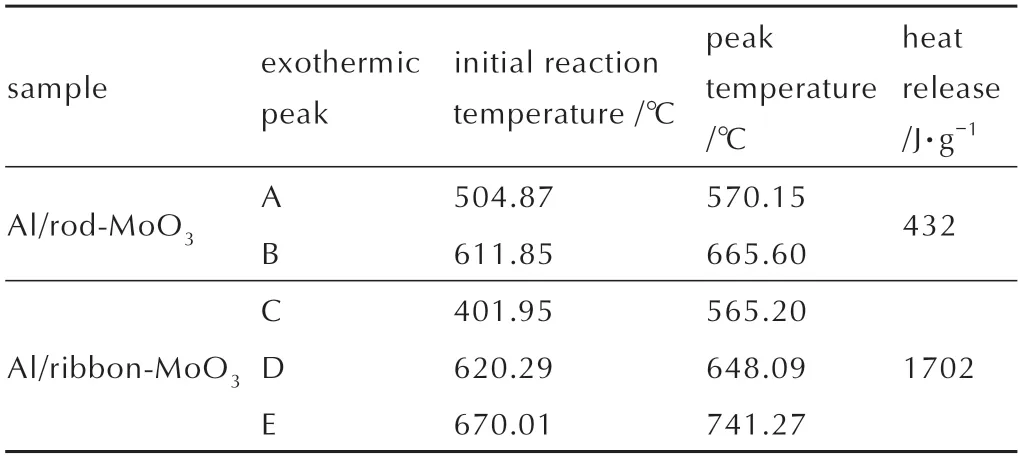
表1 两种铝热剂放热峰的初始、峰值温度及放热量信息表Table 1 The initial and peak temperature and heat release information table of the two thermites exothermic peaks
由图7 可见,Al/棒状MoO3铝热剂在237.45 ℃有一个小的吸热峰,这可能是所制备铝热剂中的表面吸附水、结构水或者溶剂或杂质的蒸发[23-25];在570.15 ℃出现了第一个放热峰A,在此温度下还未达到铝和氧化钼的熔点,所以此为固-固反应;随后在656.93℃出现了Al的熔融吸热峰[25];紧接着在665.60 ℃出现了第二个放热峰B,表明熔融的铝和剩余的棒状MoO3继续反应,这是一个固-液反应。
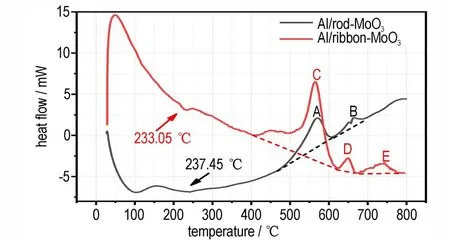
图7 两种铝热剂的DSC 曲线Fig.7 DSC curves of two thermites
Al/带状MoO3铝热剂在233.05 ℃时出现一个小的吸热峰,与Al/棒状MoO3铝热剂一样,这可能是所制备铝热剂中的表面吸附水、结构水或者溶剂或杂质的蒸发;在672.04 ℃之前,即Al 熔化之前,铝热剂出现了连续放热峰C 和D,对应于565.20 ℃和648.09 ℃,这与Al/棒状MoO3铝热剂的反应不同,出现连续放热峰的原因可能与熔融分散机理有关,即在加热过程中,铝芯会在氧化层破裂之前膨胀,导致氧化层在高压下爆裂,之后熔融的铝将以高速向外喷射[26]。第二个峰值D 就暗示着熔融的Al 碎片可能以足够的能量从加热的铝团簇中喷出,以产生二次放热反应,该反应在带状MoO3表面上会有更进一步的反应[15]。随后,在741.27 ℃时,峰E 代表液态铝和固体带状MoO3之间的铝热反应。
Al/MoO3铝热反应机理如图8 所示,一方面,团聚的Al 与棒状MoO3接触的面积小,所以铝热反应的有效作用区域小,因此,在Al/棒状MoO3铝热剂中,Al 颗粒的大量团聚(图6a)不能使其热量充分释放[27],相比之下,带状MoO3与Al 的接触面积较大,所以Al/带状MoO3有效反应区域较大。另一方面,氧化物的径向延伸能够使颗粒团聚最小化,并使热反应气体在分离的纳米Al 颗粒之间自由流动[27],这说明带状MoO3的宽直径表面积为分散Al 颗粒提供了条件,因此,Al/带状MoO3铝热剂的热分解过程更有利于Al 颗粒在热气中的流动。此外,由图8b 可见,飞溅的Al 也能够加速与带状MoO3的反应,这有效地提高了反应速率。综上,Al/带状MoO3铝热剂与Al/棒状MoO3铝热剂在热性能上会产生很大的差别,这可在DSC 实验中得到验证。由表1 的DSC 结果可知,Al/带状MoO3铝热剂的放热量为1702 J·g-1,远高于Al/棒状MoO3铝热剂的放热量432J·g-1。同时,Al/带状MoO3铝热剂的第一放热反应起始温度为401.95 ℃,比Al/棒状MoO3铝热剂的起始反应温度504.87 ℃提前。
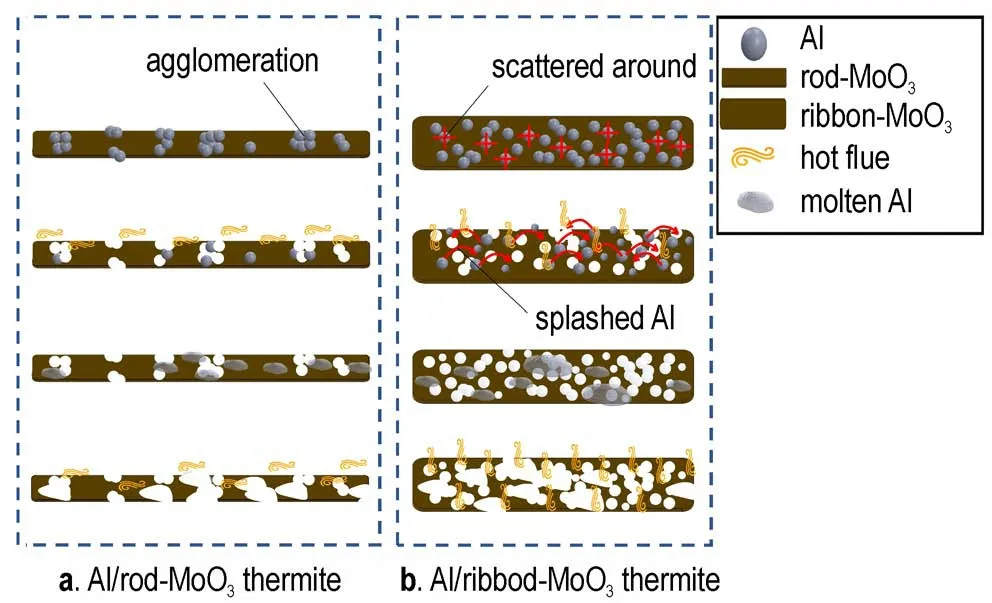
图8 两种铝热剂铝热反应机理示意图Fig.8 Schematic diagram of the reaction mechanism of two thermites
3.3 非等温热力学分析
为探索Al/MoO3铝热剂的热动力学,进行了非等温DSC 实验,得到了样品的活化能(Ea)和热爆炸临界温度(Tb)。
计算Ea的常用方法为Kissinger 与Ozawa 法,经计算,这两种方法所计算出的Ea很相似,为方便讨论,本研究采用Kissinger 方法[28](式(3))计算Ea,Tb按式(4)和式(5)计算[29]。

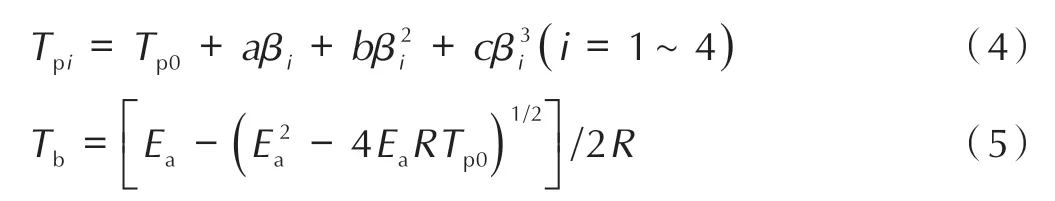
式中,A为指前因子,s-1;R为通用气体常数,8.314 J·mol-1·K-1;Tp为DSC 峰值温度,K;β为线性升温速率,K·min-1;Tp0为加热速率β接近0 时的峰值温度点,其值根据公式(4)计算而得。其中,a、b和c为拟合系数。假设样品在峰值温度下的转化率相同,则ln(β/Tp2)与1/T的 关系为直线,其直线的斜率可转换为Ea值。图9 展示了对样品DSC 实验的峰值温度点线性拟合后ln(β/Tp2)与1/T的关系。样品放热反应热力学参数的结果见表2。
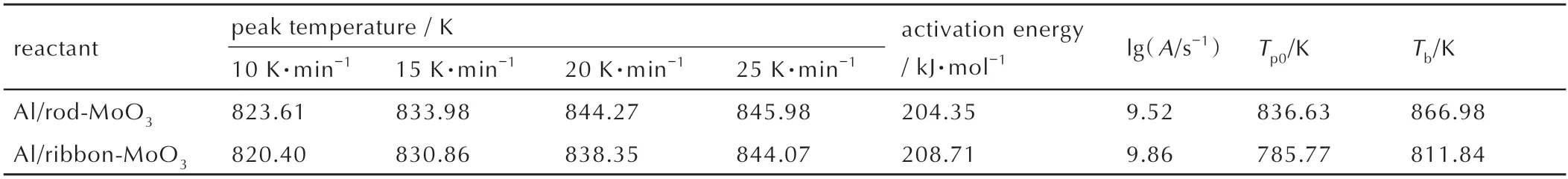
表2 两种铝热剂放热反应的热力学参数Table 2 Thermodynamic parameters of the exothermic reaction of two thermites
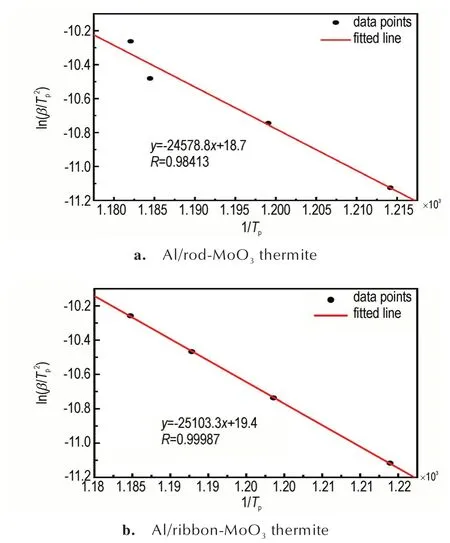
图9 两种铝热剂峰值温度点线性拟合后ln(β/Tp2)与1/Tp的关系Fig.9 The relationship between ln(β/Tp2)and 1/Tp after linear fitting of peak temperature points of two thermites
由图9a 可知,Al/棒状MoO3铝热剂的峰值温度点拟合直线为y=-24578.8x+18.7,R为0.98413,经计算,Al/棒状MoO3铝热剂的Ea为204.35 kJ·mol-1。而Al/带状MoO3铝热剂的拟合直线为y=-25103.3x+19.4,R为0.99987,拟合程度较高,得到的Ea为208.71 kJ·mol-1,与Al/棒状MoO3铝热剂的基本相同。这一结果表明,即使其中MoO3材料形态不同,但Al/棒状MoO3铝热剂与Al/带状MoO3铝热剂的Ea几乎是相同的。然而,Al/棒状MoO3铝热剂的Tb远高于Al/带状MoO3铝热剂,说明Al/棒状MoO3铝热剂的热爆炸临界温度较高,不容易从热分解或燃烧转变为爆炸,从而安全性较高。
3.4 燃烧试验
两种铝热剂开放式燃烧试验的高速摄影照片如图10 所示。其中,样品在被刚刚点燃并发出明亮白光的时刻设置为开始时间,指定为0。

图10 两种铝热剂开放式燃烧的高速摄影照片Fig.10 High-speed photography pictures of the two thermites in open combustion experiment
复合材料的可燃性与组成、粒径、装药密度等因素有关,在开放的环境中,燃烧产物可以不受限制地充分膨胀和扩散,不同制备方法制备的复合材料表现出不同的可燃性[30]。由图10 可见,两种铝热剂都被成功点燃和燃烧。火焰燃烧的持续时间为毫秒级,燃烧火焰在周围迅速膨胀和扩散,表现为整个反应和局部反应产物的散射和膨胀过程。两种铝热剂样品都在1 ms时燃烧最剧烈,火焰亮度最高,并伴有刺耳的爆炸声。在2 ms 的时候,Al/带状MoO3铝热剂产生白炽的火光,但Al/棒状MoO3铝热剂已经开始逐渐熄灭。另外,当Al/带状MoO3铝热剂即将燃烧完毕时,在其周围溅射出火花,这主要是由燃烧区高温与周围环境温差大引起的膨胀力导致的。
图11 是铝热剂在甲基丙烯酸甲酯管中的传播过程,图像按照一定的时间间隔组合,在该时间间隔内,通过编辑照片序列直观显示燃烧过程。
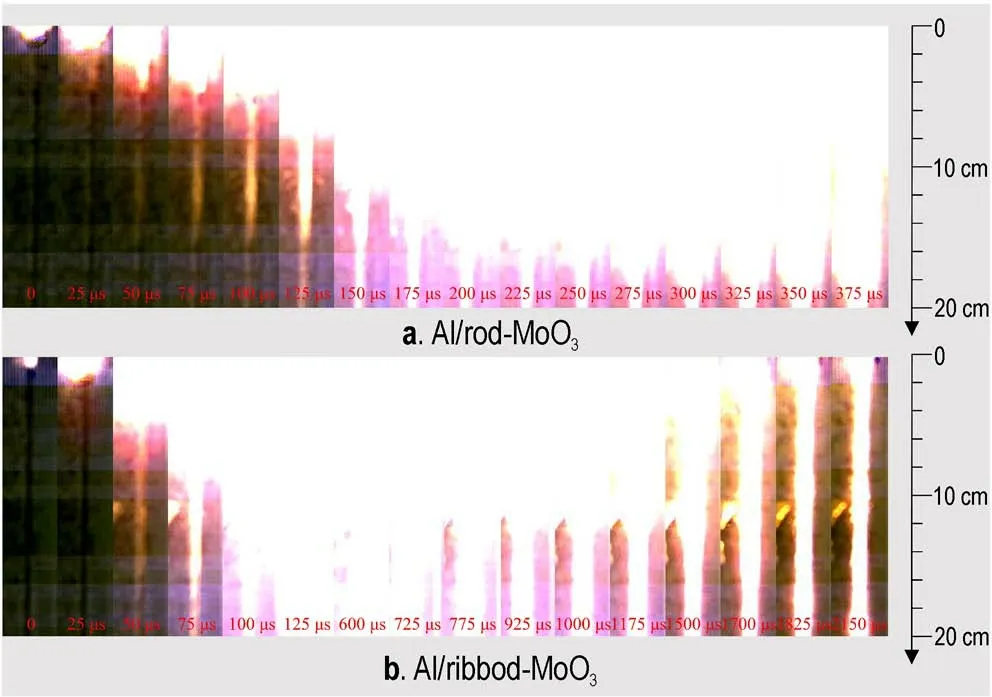
图11 两种铝热剂在封闭管中的燃烧高速照片Fig.11 High-speed photographs of the sample burning in the combustion tube
铝热剂在封闭管中燃烧,其燃烧波形成的过程中起主导作用的是对流传播,在一定装填密度范围内,之前所报告的燃烧速度通常约为每秒数百米[31]。有研究表明,对于接近化学计量比的混合物,燃烧传播模式为超音速对流传播[32]。燃烧波的波前速度被视为铝热剂火焰的燃烧速度,其中放热反应产生的对流气体以非常快的速度推动反应介质向前,图11 中所观察到的现象也验证了对流传播机制。图11 显示,两种铝热剂的燃烧波都是稳定的。
如图12a 所示,Al/棒状MoO3铝热剂的燃烧波传播速度先增大后减小,其最大传播速度达到1037 m·s-1。因为在燃烧波传播过程中达到最大速度需要一定的时间,而在中间管段,铝热剂样品的负载密度很低,这意味着对流气体可以以较小的阻力向前移动[33],所以燃烧波的速度会在中间段呈现出增加的趋势。然而,Al/带状MoO3铝热剂的燃烧波速一直呈上升趋势,受甲基丙烯酸甲酯管长度的限制,最大可测波速为2710 m·s-1,如果管的长度较长,燃烧波速将继续增大。
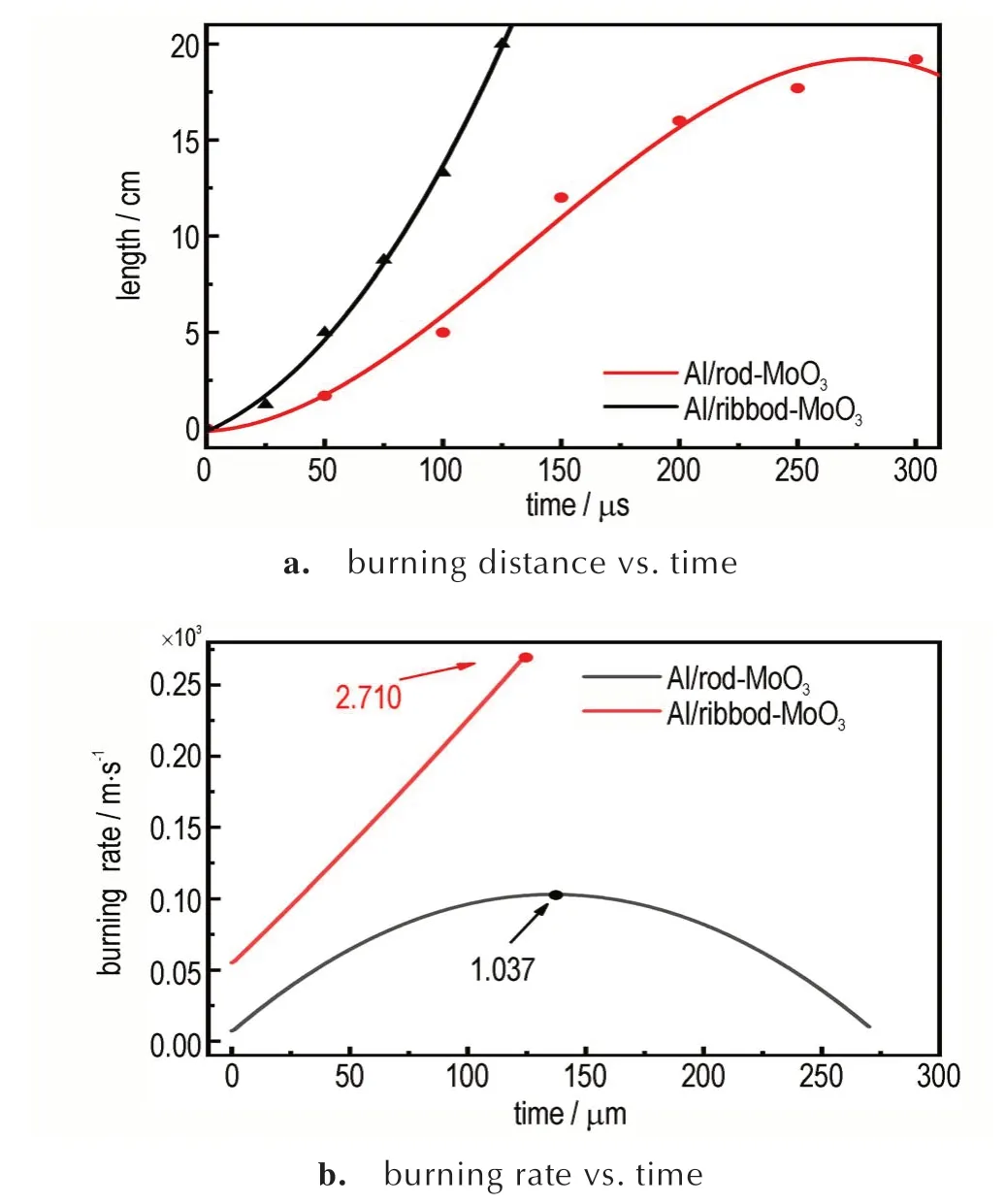
图12 两种铝热剂的燃烧传播距离和燃烧速率图Fig.12 Diagram of combustion propagation distance and burning rate of two thermites
在开放式燃烧实验中,由于样品是被堆放的,因此所表现出的燃烧行为没有实质性的不同。然而,在封闭管环境中,带状MoO3所组成的铝热剂燃烧性能更具有优势。两种铝热剂燃烧过程机理如图13 所示,由图13a 可知,棒状MoO3的大长径比和小的纳米Al 尺寸,导致纳米Al 颗粒和MoO3之间的接触面积小,而宽径带状MoO3与纳米Al 的接触面积较大,使Al 从加热的氧化铝层中释放出来,通过扩散沿着长径的方向转移,吸附在MoO3表面[15]。在这个过程中,Al 需要时间沿着MoO3表面扩散,宽直径的带状MoO3比棒状MoO3更有利于这一过程。众所周知,铝热剂的燃烧是一个自蔓延过程,如果氧化物能紧密地连接在一起,将有利于燃烧,提高燃烧速度。从形状分析来看,由于棒状MoO3的长度较大,宽度较小,所以其长径比大,当无规则排列的情况下,两根氧化钼所能够接触到的面积较小,相比之下,带状MoO3具有较大的连接面积,有利于自蔓延燃烧反应。这一现象表明,带状MoO3铝热剂的燃烧波速较快。
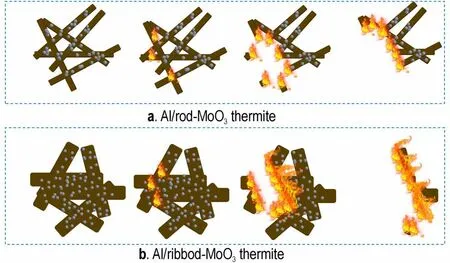
图13 两种铝热剂燃烧过程机理示意图Fig.13 Schematic diagram of the AlMoO3 thermite combustion process mechanism
4 结论
采用水热法合成了棒状和带状的MoO3,然后采用超声法制备了两种铝热剂Al/棒状MoO3铝热剂和Al/带状MoO3铝热剂。通过FE-SEM、XRD、DSC 和燃烧实验研究了它们的热性能和燃烧行为,得到了以下结论:
(1)DSC 分析表明,Al/带状MoO3铝热剂的热分解性能优于Al/棒状MoO3铝热剂,表现为Al/带状MoO3铝热剂的放热量为1702 J·g-1,其远大于Al/棒状MoO3铝热剂的432 J·g-1。Al/带状MoO3铝热剂的初始反应温度为401.95 ℃,比Al/棒状MoO3铝热剂的504.87 ℃提前了102.92 ℃。
(2)非温热力学分析结果表明,两种铝热剂的Ea没有显著差异,说明MoO3的形貌与Ea没有明显关联性,然而,Al/棒状MoO3铝热剂的Tb较高,安全性更高。
(3)在开放式燃烧实验中,两种铝热剂均被成功点燃并伴随着刺眼的亮光和刺耳的爆炸声,其火焰燃烧行为差别微小,当铝热剂燃烧即将完毕时,Al/带状MoO3铝热剂周围会溅射火花。
(4)在封闭管燃烧实验中,两种铝热剂的燃烧行为差异较大。其燃烧波的传播都是稳定的,但燃烧波的传播速度不同。Al/棒状MoO3铝热剂的速度先增大后减小,最大速度达到1037 m·s-1。然而,Al/带状MoO3铝热剂的燃烧波速呈上升趋势,最大波速为2710 m·s-1。
综上,Al/带状MoO3铝热剂的热性能和燃烧性能均优于Al/棒状MoO3铝热剂,然而Al/棒状MoO3铝热剂更安全。

