雷公藤内酯醇对Caco-2细胞紧密连接蛋白ZO-1表达的影响
朱亦邈 田君 吴晓宇
摘要:目的 研究雷公藤內酯醇(Triptolide,TL)对人结直肠腺癌细胞Caco-2紧密连接蛋白(Zonula Occludens 1,ZO-1)表达的影响。方法 在Caco-2细胞建立肠黏膜屏障体外模型的基础上,通过荧光定量PCR、Western Blot和免疫荧光分析紧密连接蛋白ZO-1的表达变化。结果 与对照组相比,TL不同浓度组Caco-2细胞内ZO-1基因和蛋白表达水平无显著变化;TNF-α组ZO-1表达显著降低;在不同浓度TL预保护后加入TNF-α,ZO-1表达水平随加入药物浓度的增加逐渐增加。对照组和TL不同浓度组内ZO-1的免疫荧光染色均表现为整齐、连续且分布规律;TNF-α组荧光强度则明显减弱,单层细胞散架且缺损,位于细胞边界的蛋白染色较模糊,蛋白定位出现弥散和不连续,表达信号减弱;在不同浓度TL预保护后加入TNF-α,ZO-1表达随药物浓度增加逐渐恢复,最高浓度下信号最强。结论 TNF-α破坏单细胞层,且抑制ZO-1表达,TL通过ZO-1促进肠黏膜屏障紧密连接恢复。提示TL可能对肠黏膜屏障有一定保护作用。
关键词:雷公藤内酯醇;Caco-2细胞;肠黏膜屏障;紧密连接蛋白
中图分类号:R285.5 文献标志码:A 文章编号:1007-2349(2022)01-0067-06
Effect of Triptolide on the Expression of Zonula Occludens Protein ZO-1 in Caco-2 Cells
ZHU Yi-miao1, TIAN Jun1, WU Xiao-yu3
(1. The Affiliated Hospital of Nanjing University of Traditional Chinese Medicine, Nanjing 210029, China; 2. Zhangjiagang Hospital Affiliated to Nanjing University of Traditional Chinese Medicine, Suzhou 215600, China; 3. The Affiliated Hospital of Nanjing University of Traditional Chinese Medicine/Jiangsu Provincial Hospitalof Traditional Chinese Medicine, Nanjing 210029, China)
【Abstract】Objective: To study the effect of triptolide (TL) on the expression of Zonula Occludens protein (ZO-1) in human colorectal adenocarcinoma cells Caco-2. Methods: Based on the establishment of an intestinal mucosal barrier in Caco-2 cells, the expression changes of Zonula Occludens protein ZO-1 were analyzed by fluorescence quantitative PCR, Western Blot and immunofluorescence. Results: Compared with that of the control group, the expression levels of ZO-1 gene and protein in Caco-2 cells of TL different concentrations did not change significantly, and the expression of ZO-1 in TNF-α group was significantly reduced, As TNF-α was added after pre-protection with TL different concentrations, the expression level of ZO-1 gradually increased with the increase of the concentration of the added drug. The immunofluorescence staining of ZO-1 in the control group and the TL different concentration groups showed neat, continuous and regular distribution. The fluorescence intensity of the TNF-α group was significantly weakened, and the monolayer cells were scattered and defective. The protein staining at the cell boundary was blurred and the protein localization was diffuse and discontinuous, and the expression signal was weakened. As TNF-α was added after pre-protection with TL different concentrations, the expression of ZO-1 gradually recovered with the increase of drug concentration, and the signal was strongest at the highest concentration. Conclusion: The TNF-α destroys the monolayer and inhibits the expression of ZO-1. The TL promotes the restoration of Zonula Occludens protein of the intestinal mucosal barrier through ZO-1. It suggests that the TL may have a protective effect on the intestinal mucosal barrier.
【Key words】Triptolide; Caco-2 Cells; Intestinal Mucosal Barrier; Zonula Occludens Protein
炎症性肠病(inflammatory bowel disease,IBD)是一组累及胃肠道的慢性炎症性疾病,且常伴有终生频繁复发的倾向[1]。IBD的病因和发病机制迄今还未明确,目前普遍认为肠黏膜屏障功能的紊乱在IBD发病机制中起重要作用[2]。
肠黏膜屏障主要包括肠上皮细胞及细胞间的连接。其中,肠上皮紧密连接是最为重要的连接方式,在维持肠粘膜结构完整性和正常功能中发挥重要作用。紧密连接[3]主要由咬合蛋白(Occludin)、闭合蛋白(Claudins)和ZO-1(Zonula Occludens 1)三种主要蛋白构成,而ZO-1专有的集中在紧密连接,且对紧密连接功能的发挥有着重要作用。
雷公藤内酯醇(Triptolide,TL)是从中草药中提取的有效活性成分,广泛应用于自身免疫病、移植排斥[4]。已有研究表明TL能够促进IBD大鼠模型的肠黏膜损伤的修复和屏障功能的恢复[5]。但是,TL对于受损肠屏障的保护机制尚未有研究报道。故而,本研究拟通过Caco-2肠上皮细胞模型,检测相关紧密连接蛋白ZO-1的表达变化,初步探索其可能的机制,为肠粘膜屏障的损伤和修复机制进一步提供理论依据,为药物的研发提供新的方向。
1 材料与方法
1.1 材料
1.1.1 实验细胞 Caco-2人结直肠腺癌细胞(human colon carcinoma cell line,Caco-2)购于中国科学院上海生科院细胞资源中心。
1.1.2 主要仪器及试剂 CO2细胞培养箱,Thermo公司生产;荧光倒置显微镜,Olympus公司生产;倒置相差显微镜,Leica公司生产;DMEM高糖培养基、谷氨酰胺、非必須氨基酸、FBS和0.25%-EDTA胰蛋白酶消化液均购自Gibco公司;Transwell 24孔System购自Corning公司;Rabbit Polyclonal to ZO-1购自Proteintech公司;Anti-Rabbit IgG,HRP-linked Antibody购自Cell Signaling公司。
1.2 方法
1.2.1 Caco-2肠黏膜屏障模型的建立与评估 本课题组在前期实验中选用Caco-2细胞建立肠黏膜屏障体外模型,具体操作参考吴茂军建立的方法及评估指标[6],并已通过形态学观察、旁路通透性检测、单层细胞完整性及细胞极性四个实验全面评价了模型的可靠性和有效性,在此过程中,我们同时观察了TL对Caco-2细胞没有细胞毒性的影响。
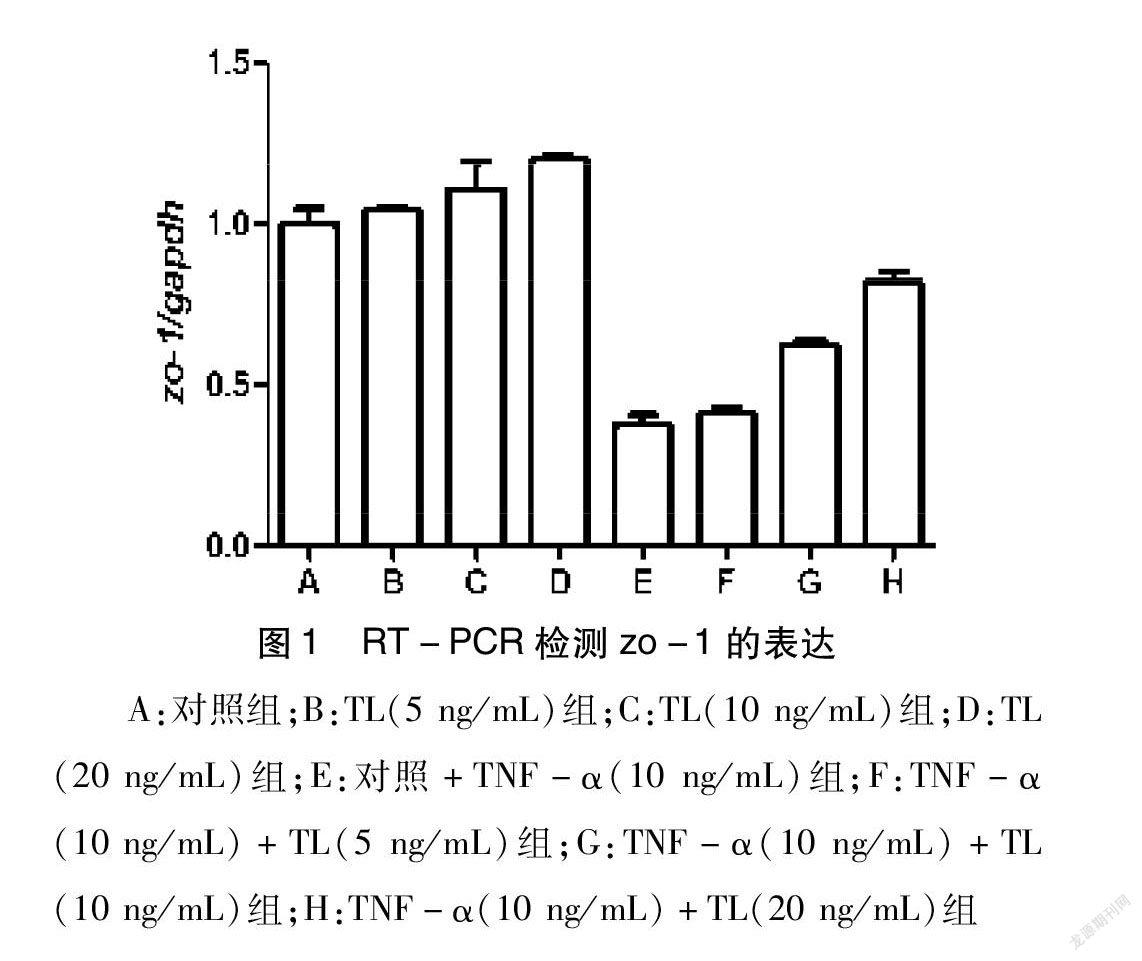
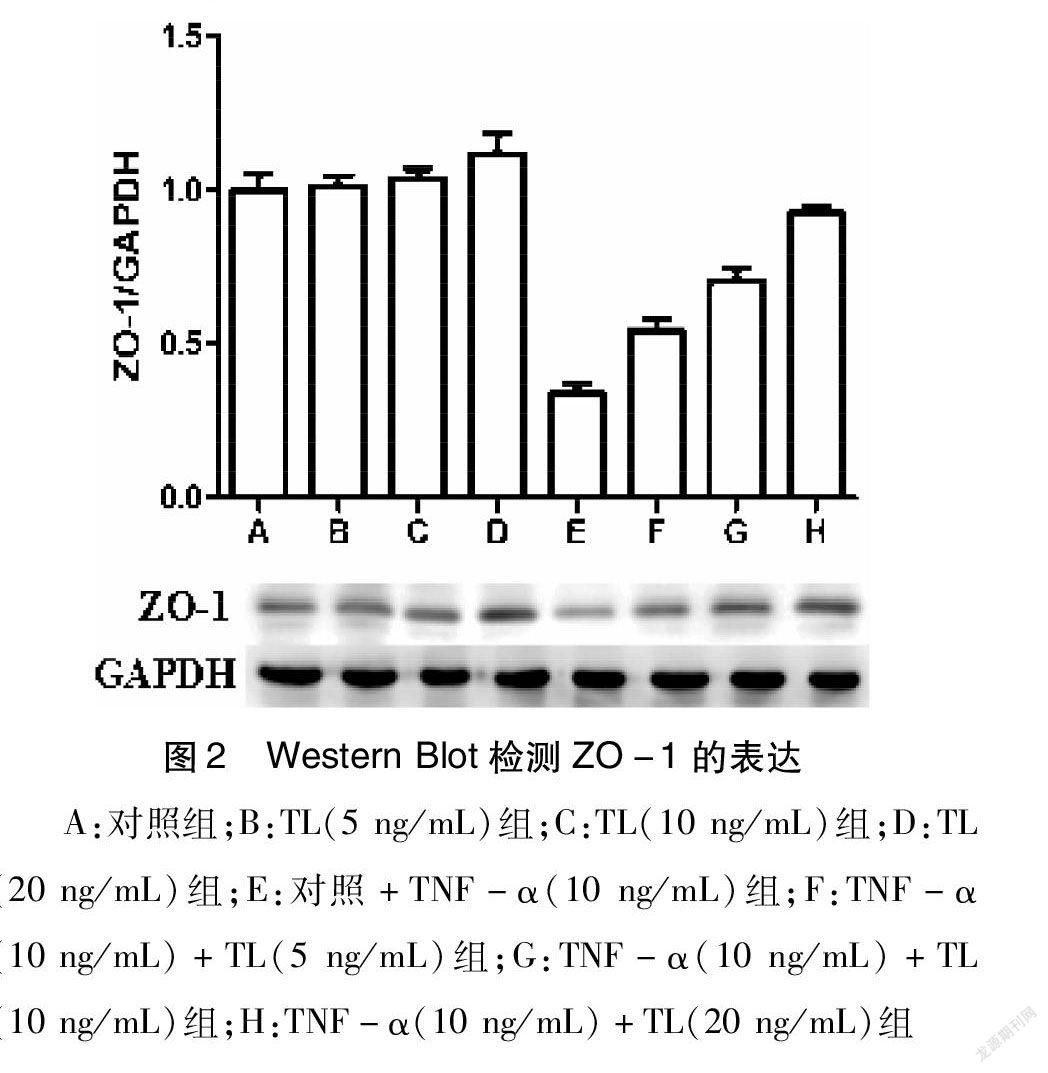
1.2.2 实验分组 实验总共分为8组:A:对照组;B:TL低剂量5ng/mL(13.87nmol/L)组;C:TL中剂量10ng/mL(27.74nmol/L)组;D:TL高剂量20ng/mL(55.49nmol/L)组;E:对照+10ng/mL TNF-α(31.96nmol/L)组;F:10ng/mL TNF-α(31.96nmol/L)+TL低剂量5ng/mL(13.87nmol/L)组;G:10ng/mL TNF-α(31.96nmol/L)+TL中剂量10ng/mL(27.74nmol/L)组;H:10ng/mL TNF-α(31.96nmol/L)+TL高剂量20ng/mL(55.49nmol/L)组。
第0d时将Caco-2细胞接种至Transwell小室,正常培养;7d时,随机分为对照组和TL组,对照组常规培养,TL组培养液中添加不同剂量(5ng/mL,10ng/mL,20ng/mL)TL培养液;21d时,E,F,G,H组加入10ng/mL的TNF-α。
1.2.3 RT-PCR检测zo-1基因的表达 收集各组细胞,采用TRIzol法提取RNA。逆转录试剂盒RevertAidTM First Strand cDNA Synthesis Kit(Thermo公司)进行逆转录反应。根据zo-1基因的mRNA序列设计RT-PCR反应引物:GAPDH:Primer-F:5-AGAAGGCTGGGGCTCATTTG-3;Primer-R:5-AGGGGCCATCCACAGTCTTC-3.ZO-1:Primer-F:5-TATCCCGAGGAAATGATGAGGC-3;Primer-R:5-TCGTATCTGTATGTGGGCTGCT-3.RT-PCR反应采用SYBR Green MiX试剂(Thermo公司),总反应体系20 μL,体系如下:SYBR Green mix 10 μL、Primer-F(10 μmol)1 μL、Primer-R(10 μmol)1 μL、cDNA 1 μL、ddH2O 7 μL。RT-PCR反应条件:94 ℃,10 min;40个循环(94 ℃,20 s;55 ℃,20 s;72 ℃,20 s),在延伸阶段收集荧光;熔解曲线分析:94 ℃,20 s;60 ℃,1 min;95 ℃,15 s。各组细胞均以内参基因gapdh校正目的基因,实验至少重复3批样本,每个样本均重复3次,使用2-ΔΔCT 法相对定量分析。
1.2.4 Western Blot检测ZO-1蛋白的表达 提取各组细胞总蛋白;BCA蛋白定量试剂盒(BIOSHARP)测定蛋白浓度;GAPDH配制12%的分离胶,ZO-1配制6%的分离胶;常规程序电泳,直至目的蛋白充分跑开;电泳结束后,以350mA,60min转膜;转膜结束后,将膜置于封闭液中室温封闭1 h;滴加一抗(1∶1000)4℃孵育过夜;用TBST洗涤3次;每次5 min,二抗(1:5000)室温孵育1 h;再用TBST洗涤6次,每次5 min,取1 mL ECL显色液显色1 min。
1.2.5 免疫荧光检测ZO-1蛋白的表达 在各组细胞的Transwell小室内加PBS洗涤三次;4%多聚甲醛固定20 min;再用0.5% TritonX-100通透20 min;5%FBS溶液室温封闭15 min;按照1∶100的比例配制ZO-1一抗溶液,4℃过夜;荧光二抗室温1 h;Hoechst 室温5 min;将小室的膜切下来,封片,观察、拍照。
1.2.6 统计学方法 应用STATA V 10.0统计分析软件对样本数据进行单因素方差分析,应用GraphPad Prism 5统计分析软件进行统计作图,数据结果用(x±s)表示,采用t检验进行比较、分析,以P<0.05为差异具有统计学意义。
2 结果
2.1 ZO-1基因水平表达变化 收集各组细胞,提取RNA,进行RT-PCR检测,实验结果显示:相比A组对照组,B、C、D组细胞内目的基因ZO-1表达水平无明显变化,其中TL最高浓度(20 ng/mL)组中目标基因ZO-1表达水平稍微有所增加(1.2±0.04 vs 1±0.04);E组TNF-α(10 ng/mL)组内目标基因ZO-1表达水平显著降低(0.38±0.02 vs 1±0.04);在不同浓度的TL(5ng/mL,10 ng/mL,20 ng/mL)预保护基础上加入TNF-α后,目标基因表达水平随着加入药物浓度的增加逐渐增加,其中最高药物剂量下,目标基因表达水平相比TNF-α组增加最为显著(0.82±0.03 vs 0.38±0.02)。见图1。
2.2 ZO-1蛋白水平表达变化 收集各组细胞,提取总蛋白,进行Western Blot检测,实验结果显示:相比A组对照组,B、C、D组细胞内目的蛋白ZO-1表达水平无明显变化,其中TL最高浓度(20 ng/mL)组中目的蛋白表达水平稍微有所增加;E组TNF-α(10 ng/mL)组内目的蛋白ZO-1表达水平显著降低(0.33±0.02 vs 1±0.05);在不同浓度的TL(5 ng/mL,10 ng/mL,20 ng/mL)预保护基础上加入 TNF-α后,目的蛋白表达水平随着加入药物浓度的增加逐渐增加,其中最高药物剂量下,目的蛋白表达水平相比TNF-α组增加最为显著(0.92±0.02 vs 0.33±0.02)。见图2。
2.3 ZO-1蛋白免疫荧光表达定位 对照组和TL 3个加药浓度组(即A,B,C,D组)细胞ZO-1免疫荧光染色呈现为整齐、连续且分布规律;TNF-α(10 ng/mL)即E组免疫荧光区域显示明显减弱,整个单层细胞散架,缺损,在细胞边界染色的蛋白变模糊,蛋白定位出现弥散和不连续,表达显著减弱;在不同浓度的TL(5 ng/mL,10 ng/mL,20 ng/mL)预保护基础上加入TNF-α后,ZO-1表达随着药物浓度增加逐渐增加,最高浓度下效果最为显著。见图3。
3 讨论
炎症性肠病(IBD)是一类由多种不明病因引发的、异常免疫介导的肠道慢性且复发性炎症。IBD已成为一种全球性疾病[7],其发病率和患病率正呈现逐年上升的趋势。虽然IBD的病因及发病机制至今尚未完全明确,但肠黏膜屏障功能的紊乱一直占据研究热点首位[2]。
肠黏膜屏障是肠腔中将细菌、抗原等与肠黏膜固有层免疫细胞隔离开的结构,其中,肠上皮屏障是肠黏膜屏障中最为重要的组成部分,是机体内外环境间的机械保护[8]。肠上皮屏障包括黏着连接、桥粒及紧密连接,紧密连接通过形成顶端闭锁结构,从而发挥封闭相邻细胞间隙、调节细胞旁通透性的作用,这对于肠黏膜屏障功能的稳定有重要作用。ZO-1蛋白则专有的集中在紧密连接,且对紧密连接功能的发挥有着重要作用。
ZO-1蛋白是第一个被证实的紧密连接蛋白[9],相对分子量约为225kDa,含有多个功能结构域,可以发挥多种功能。ZO-1在紧密连接复合体中具有重要的枢纽作用,不仅连接了跨膜蛋白还连接了细胞骨架蛋白,是紧密连接复合体的结构基础。除了结构上的功能,ZO-1还使得上皮细胞具有极性,还参与了细胞的增殖、免疫调节、信号转导等。Kim Y等[10]以葡聚糖硫酸钠(DSS)誘导的IBD小鼠模型中,肠黏膜紧密连接被破坏,ZO-1表达水平显著降低。Luo D等[11]破坏了血脑屏障紧密连接后,ZO-1表达下调。所以,ZO-1表达水平的下降亦或是活性的降低,都会破坏紧密连接的稳定性,进而影响细胞功能。
ZO-1的异常表达通常代表紧密连接的功能异常,进而可以反映出肠黏膜屏障功能的异常,故而测定ZO-1的表达情况,可以直接观察到屏障功能的变化。本研究中TNF-α组内目的蛋白ZO-1表达水平显著降低;免疫荧光区域显示ZO-1荧光强度明显减弱,单层细胞散架且缺损,位于细胞边界的蛋白染色较模糊,蛋白定位出现弥散和不连续,表达显著减弱,此时Caco-2细胞间的紧密连接被破坏。
雷公藤内酯醇(TL)是所有雷公藤二萜化合物之中免疫抑制作用最强的单体[12],具有显著的抗炎效果。在不同浓度的TL(5 ng/mL,10 ng/mL,20 ng/mL)预保护基础上加入TNF-α后,目的蛋白表达水平随着加入药物浓度的增加逐渐增加,其中最高药物剂量下,目的蛋白表达水平逐渐恢复至正常水平。在TL的保护下,Caco-2细胞间的紧密连接逐渐恢复。从本研究结果可以推测TL对细胞单层的形成起促进作用,且TL通过ZO-1促进肠黏膜屏障紧密连接的恢复。但ZO-1具体是如何影响紧密连接,以及ZO-1作为药物靶点的可能性还有待进一步研究。
参考文献:
[1]Eppinga H,Peppelenbosch MP.Worsening of Bowel Symptoms Through Diet in Patients With Inflammatory Bowel Disease[J].Inflammatory Bowel Diseases,2016,22(2):6-7.
[2]Holmberg FEO,Pedersen J,Jorgensen P,et al.Intestinal Barrier Integrity and Inflammatory Bowel Disease:Stem Cell-based Approaches to Regenerate the Barrier[J].Journal of Tissue Engineering and Regenerative Medicine,2018,12(4):923-935.
[3]Gonzalez-Castro AM,Martinez C,Salvo-Romero E,et al.Mucosal Pathobiology and Molecular Signature of Epithelial Barrier Dysfunction in the Small Intestine in Irritable Bowel Syndrome[J].Journal Of Gastroenterology And Hepatology,2017,32(1):53-63.
[4]Li SG,Shi QW,Yuan LY,et al.C-Myc-dependent Repression of Two Oncogenic miRNA Clusters Contributes to Triptolide-induced Cell Death in Hepatocellular Carcinoma Cells[J].Journal of Experimental & Clinical Cancer Research,2018,37:51.
[5]Gao SY,Wu XY,Zhang YY,et al.Tripterygium Wilfordii Polyglycosidium Ameliorates Pouchitis Induced by Dextran Sulfate Sodium in Rats[J].International Immunopharmacology,2017(43):108-115.
[6]吳茂军,侯龙龙.关于Caco-2细胞构建肠黏膜屏障模型的相关研究[J].泰山医学院学报,2016,37(4):361-364.
[7]Vegh Z,Kurti Z,Lakatos PL.Epidemiology of Inflammatory Bowel Diseases from West to East[J].Journal of Digestive Diseases,2017,18(2):92-98.
[8]Farkas AE,Nusrat A.Pharmacological Targeting of the Inflamed Intestinal Barrier[J].Current Pharmaceutical Design,2016,22(35):5400-5414.
[9]Stevenson BR,Siliciano JD,Mooseker MS,et al.Identification of ZO-1:A High Molecular Weight Polypeptide Associated with the Tight Junction(Zonula Occludens)in a Variety of Epithelia[J].Journal of Cell Biology,1986,103(3):755-766.
[10]Kim Y,West GA,Ray G,et al.Layilin is Critical for Mediating Hyaluronan 35 kDa-induced Intestinal Epithelial Tight Junction Protein ZO-1 in Vitro and In Vivo[J].Matrix Biology,2018,66:93-109.
[11]Luo D,Zhao J,Rong J.Plant-derived Triterpene Celastrol Ameliorates Oxygen Glucose Deprivation-induced Disruption of Endothelial Barrier Assembly Via Inducing Tight Junction Proteins[J].Phytomedicine,2016,23(13):1621-1628.
[12]You LT,Dong XX,Ni B,et al.Triptolide Induces Apoptosis Through Fas Death and Mitochondrial Pathways in HepaRG Cell Line[J].Frontiers In Pharmacology,2018(9):813.
(收稿日期:2021-10-18)

