结核菌素试验和血清载脂蛋白A1与抗结核药物性肝损伤的关系
瞿 荥,刘中洋
(1.锦州医科大学 研究生院,辽宁 大连 116000;2.中国人民解放军联勤保障部队第九六七医院 呼吸内科, 辽宁 大连 116000)
药物性肝损伤(drug-induced liver injury, DILI)是药物治疗过程中一种常见的不良反应,是导致治疗中断的主要原因[1]。即使在接受治疗的同时联合保肝药物,DILI的发生率仍不容小觑,其中抗结核药是我国DILI的主要诱因之一[2]。大部分抗结核药物性肝损伤(anti-tuberculosis drug-induced liver injury, ATB-DILI)患者停药或联合保肝药物治疗后肝功能可恢复正常,但仍有少数患者出现不可逆的肝损伤[3]。谷丙转氨酶(ALT)及总胆红素(TBIL)水平的升高是肝损伤的特异性标记物,且发生在肝细胞损伤之后。有研究发现,血清载脂蛋白A1(apolipoprotein A-1, ApoA-1)对ATB-DILI患者肝功能的恢复有重要的预测价值,可能与ApoA-1在机体非特异性免疫中起 “防御作用”有关[4]。目前关于结核菌素(PPD)试验及ApoA-1水平与ATB-DILI关系的研究较少,本研究主要探讨PPD试验反应强度、ApoA-1水平与ATB-DILI的相关性,评估两者可否预测ATB-DILI的发生,并指出两者的最佳临界值,为临床医师提供参考。
1 资料与方法
1.1病例选择 回顾性分析2017年1月至2021年6月于中国人民解放军联勤保障部队第九六七医院住院且确诊为肺结核的患者541例,其中发生ATB-DILI的患者56例,为病例组;未发生ATB-DILI的患者485例,为对照组。纳入标准:①所有纳入对象均符合新版肺结核诊断标准[5];②所有患者至少接受2个月的常规一线抗结核药物(HRZE)治疗;③病例组均符合药物性肝损伤诊断标准[6],并采用Roussel Uclaf因果关系评估(Roussel Uclaf causality assessment method, RUCAM)量表对抗结核药物与肝损伤的因果关系进行评分,分数≥6分为很可能或非常可能;④年龄18~60岁;⑤临床资料完整。排除标准:①入院前有肝炎、肝硬化等疾病史,或抗结核治疗前肝功能指标超出正常范围;②入院期间同时应用除抗结核药物以外的其他肝毒性药物。
1.2方法 记录患者一般临床资料,包括年龄、性别、体质量指数(BMI)、入院后PPD试验反应强度。于患者抗结核药物治疗前进行血清生化指标的检测,包括血清ApoA-1、血清载脂蛋白B(apolipoprotein B, ApoB)、ALT、谷草转氨酶(AST)、谷氨酰转移酶(GGT)等。比较抗结核治疗前两组各项指标的差异,分析PPD试验反应强度、血清ApoA-1水平与ATB-DILI的关系。

2 结 果
2.1一般临床资料及生化指标比较 两组性别、肺结核类型、入院时ApoB、ALT、AST、TBA水平比较,差异无统计学意义(均P>0.05),而年龄、抗结核治疗前PPD试验反应强度、GGT、ApoA-1水平差异有统计学意义(均P<0.05),见表1。

表1 两组一般临床资料及生化指标比较
2.2多因素Logistic回归分析 将年龄、抗结核治疗前PPD试验反应强度、GGT、ApoA-1水平作为自变量进行单因素Logistic回归分析,结果显示,抗结核药物治疗前PPD试验反应强度、ApoA-1、ApoB水平是ATB-DILI的影响因素(均P>0.05),见表2。将PPD试验反应强度、ApoA-1、ApoB水平作为自变量进行多因素Logistic回归分析,结果显示,PPD试验反应强度、ApoA-1水平是ATB-DILI的独立影响因素(均P>0.05),见表3。
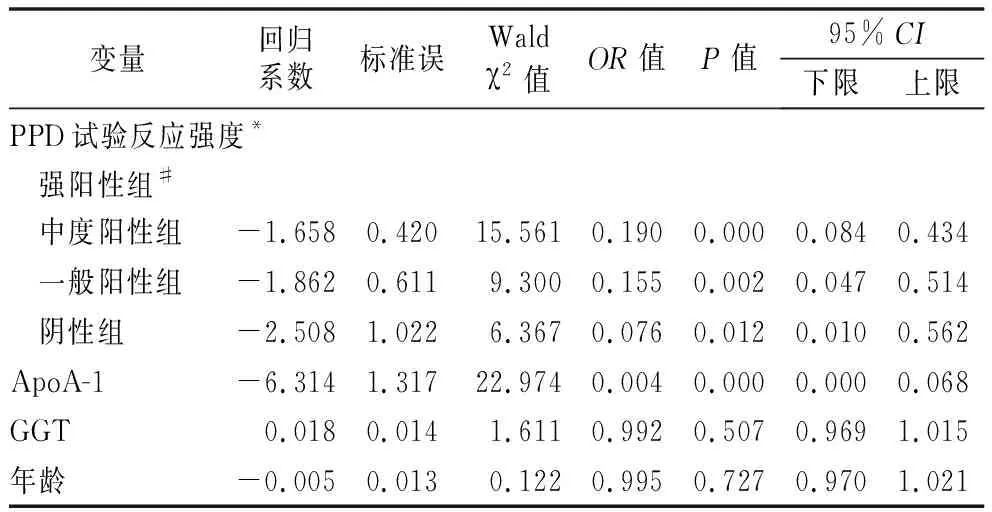
表2 ATB-DILI影响因素的单因素Logistic回归分析
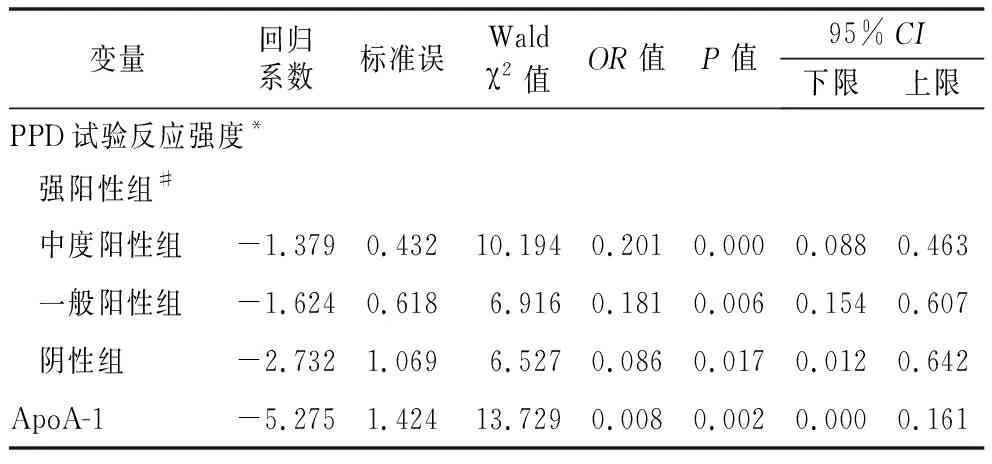
表3 ATB-DILI影响因素的多因素Logistic回归分析
2.3PPD试验反应强度、ApoA-1水平预测ATB-DILI的ROC曲线 ROC曲线显示,PPD试验反应强度(根据组别进行赋值:阴性组=1,一般阳性组=2,中度阳性组=3,强阳性组=4)、ApoA-1水平对ATB-DILI有一定的预测价值,两者联合应用预测价值更高,见表4、图1。

表4 PPD试验反应强度、ApoA-1对ATB-DILI的预测价值

图1 PPD试验反应强度、ApoA-1水平预测ATB-DILI的ROC曲线
3 讨 论
ATB-DILI与用药方案、患者身体状况等密切相关。目前临床最为常用的一线抗结核方案为异烟肼、利福平、吡嗪酰胺及乙胺丁醇。而其中吡嗪酰胺、异烟肼、利福平均与肝毒性有关,联合应用增加肝损伤的风险[7]。因此,尽早识别高危人群,预防和治疗ATB-DILI成为抗结核治疗面临的重要任务。
ATB-DILI的发病机制复杂,多种因素共同参与其中,主要包括直接毒性作用和特异质性肝毒性作用。其中,特异质性肝毒性作用是ATB-DILI发生的主要机制,是一种无剂量依赖的超敏反应[8]。在此超敏反应中,药物及其代谢产物可作为半抗原或“新抗原”激活CD4+T淋巴细胞,并促进CD8+T淋巴细胞发挥识别作用,导致变态反应,活化多种信号通路,促进肝细胞的凋亡、坏死和自噬,从而通过免疫反应破坏肝细胞,引起免疫介导的肝损伤[9-11]。近年来,研究者尝试从免疫角度出发寻找预测ATB-DILI的检验及检查方法。有研究发现,过敏原检测阳性的患者在抗结核治疗过程中ATB-DILI发病率更高[12]。此外,ApoA-1水平与ATB-DILI患者预后的相关性也与免疫机制有关[4]。Burger等[13]发现,受刺激的T细胞与单核巨噬细胞之间的直接接触是慢性炎症性疾病中触发促炎细胞因子产生的重要机制,而这种机制可以被ApoA-1阻断,这为高ApoA-1水平患者DILI预后更好作出合理解释[14]。
PPD试验作为诊断结核菌感染的一种免疫学检测方法而广泛应用于结核病的流行病学调查和监测,其原理是Ⅳ型超敏反应[15]。机体在感染结核分枝杆菌后产生致敏T淋巴细胞,当再次受抗原(PPD试剂)刺激时,产生多种细胞因子释放、局部巨噬细胞浸润等免疫反应,导致局部出现红肿、硬结,反应强烈时甚至出现双圈、水泡、坏死、淋巴管炎等,其反应的剧烈程度与机体免疫状况密切相关[16]。本研究发现PPD试验反应强度、ApoA-1水平与ATB-DILI的发生具有相关性。PPD试验呈强阳性、低ApoA-1水平的肺结核患者发生ATB-DILI的概率更高,而病例组与对照组抗结核治疗前AST、ALT、GGT等反映肝功能情况的生化指标差异无统计学意义,这表明机体免疫状态对抗结核治疗过程中的ATB-DILI具有一定预测价值。
现有研究表明,免疫机制在DILI过程中发挥着重要作用。在ATB-DILI的治疗上,寻找合适的保肝药物尤为重要[17]。甘草酸类制剂除抗炎、保护细胞膜外,还具有调节肝脏内过激免疫的作用。阮军等[18]对10篇随机对照试验研究进行meta分析,对比了异甘草酸镁与其他保肝药对ATB-DILI治疗的有效率及肝功能改善情况,结果显示,异甘草酸镁疗效更好。张志娟等[19]对7项研究进行meta分析,结果显示,在抗结核治疗的同时加用复方甘草酸苷可使ATB-DILI的发生率显著减低。在ATB-DILI的保肝治疗上,在抗结核治疗前对PPD试验强阳性、低ApoA-1水平的患者预防性应用具有免疫调节作用的保肝药物或能取得更好的预防及治疗效果。未来能否通过PPD试验反应强度指导ATB-DILI患者的个体化治疗还需更多的临床试验进一步证实。
本研究尚存在不足,如观察对象数量有限,多数病例为青壮年军人等。未来应开展多中心、大数据的临床研究,选择出评估ATB-DILI发生风险及预后更为准确的方法,为临床治疗提供帮助。

