归术益坤方对多囊卵巢综合征模型大鼠卵巢组织及SIRT1-FOXO信号通路相关蛋白表达的影响
徐道立 林青 陈颖 李晶晶 佟庆
多囊卵巢综合征(polycystic ovary syndrome,PCOS)是一种以内分泌紊乱为主、多种代谢异常导致的异质性临床综合征[1],中国育龄期妇女中PCOS发病率达到6%~10%[2],但其病因及发病机制目前仍未完全明确。SIRT1基因可通过调控多种下游蛋白表达及促进类固醇激素合成关键酶表达等多种途径影响PCOS发病[3]。归术益坤方是国医大师柴嵩岩治疗PCOS的经验方,主要以补肾健脾、养血通利为法,并以“二阳致病”理论为指导,运用补肺启肾之法,从而缓解脾肾不足、痰湿结聚的病理状态,促进卵巢功能恢复及月经来复。前期研究证实,归术益坤方能显著下调PCOS患者血清睾酮、黄体生成素(luteinizing hormone,LH)及卵泡刺激素(follicle stimulating hormone,FSH)水平,改善相关症状,提高妊娠率[4]。细胞实验证实,归术益坤方能通过调控P53/AMPK通路影响卵巢颗粒细胞自噬,改善PCOS发病[5]。本研究旨在通过建立大鼠PCOS模型,以炔雌醇环丙孕酮片作为阳性对照药,探究归术益坤方对PCOS大鼠卵巢形态学、血清学及SIRT-FOXO通路相关蛋白的影响,进一步明确归术益坤方治疗PCOS的具体作用机制。
1 材料与方法
1.1 实验动物及实验环境
SPF级健康雌性SD大鼠40只,4周龄,体质量(90±20)g,购自北京维通利华实验动物技术有限公司,动物许可证号:SCXK(京)2016-0006。饲养于北京中医医院实验动物中心,温度(22±2)℃,相对湿度(70±2)%。动物实验符合北京中医医院伦理委员会相关规定。
1.2 实验药物
归术益坤方组成:菟丝子15 g、白术12 g、当归10 g、北沙参10 g、生麦芽10 g、茜草6 g、浙贝母15 g、蛇床子3 g。饮片购于北京中医药大学东方医院草药房。购买原药50剂,所有原药加10倍量水煎煮,共煎2次,每次1小时,合并滤液后浓缩,60℃减压干燥后得浸膏986 g(得膏率27.7%),分瓶灌装密封后4℃冰箱冷藏保存备用。炔雌醇环丙孕酮片(拜耳医药保健有限公司,批号:20190630)购自北京中医药大学东方医院西药房。
1.3 主要试剂与仪器
丙酸睾酮注射液(宁波第二激素厂,批号20180624),性激素Elisa试剂盒(Solarbio公司,批号20191123),蛋白提取液(MDL公司,货号MDL91201),蛋白酶抑制剂(MDL公司,货号MD912893),BCA蛋白浓度测定试剂盒(MDL公司,货号MD913053),SDS-PAGE预制胶套装试剂盒(MDL公司,货号MD911919),蛋白上样缓冲液(MDL公司,货号MD6619),封闭液(MDL公司,货号MD912056),丽春红蛋白染液(MDL公司,货号MD6622),抗肌动蛋白抗体(Anti-Actin)(MDL公司,货号MD6553),兔抗PPAR-γ抗体(abcam公司,货号ab209350),兔抗PPARα抗体(abcam公司,货号ab245209),兔抗FOXO1抗体(Cell Singaling公司,货号2880S),兔抗FOXO3a抗体(Cell Singaling公司,货号2497S),兔抗SIRT1抗体(Cell Singaling公司,货号9475S),羊抗兔IgG-HRP(江苏凯基生物,批号20190731)。
电子天平(德国Sartorius公司,型号Cubis®MSA224S-000-DA),脱色摇床(海门其林贝尔仪器制造公司,型号TS-100),旋涡混匀器(海门麒麟医用仪器厂,型号XW-80A),电泳仪(北京百晶生物技术有限公司,型号BG-subMIDI),低温离心机(德国Sigma公司,型号3-30K),SDS-PAGE电泳系统(美国BIO-Rad公司,型号Mini-PROTEAN®Tetra Cell with Mini Trans-Blot®Module And PowerPacTMUniversal Power Supply),凝胶成像系统(美国UVP公司,型号GelDoc-It310),ChemiDoc MP化学发光成像系统(美国BIO-Rad公司,型号170-8280)。
1.4 高雄激素PCOS大鼠模型建立
4周龄雌性SD大鼠40只,随机取8只为空白组,喂食普通饲料;剩余32只给予高脂饲料。喂养的第4周起将32只高脂饲料饲养大鼠按1 mg/100 g肌注丙酸睾酮注射液(2 mL∶25 mg),连续肌注14天。每日阴道涂片并湿片观察阴道脱落细胞形态变化,每3日测量大鼠的体重并记录。
造模成功标准:(1)动情周期消失;(2)大鼠卵巢组织形态学变化:肉眼观察大鼠卵巢颜色苍白,长径增长,体积增大,卵巢表面可见数量较多透明囊泡。苏木精—伊红(hematoxylin-eosin,HE)染色光镜下观察卵巢出现数目较多的囊状扩张卵泡,卵泡内结构不完整,颗粒细胞层数为1~2层或消失,不见放射冠和卵母细胞;(3)血清睾酮超过正常值;(4)模型组大鼠体重高于空白组20%以上。
实际造模过程中无大鼠死亡,全部40只大鼠均进入分组给药环节。
1.5 分组及给药
造模期间以普通饲料喂养,未肌注丙酸睾酮的8只大鼠为空白组。将32只造模大鼠采用随机数字表法分为模型组、中药高剂量组、中药低剂量组、阳性对照组,每组8只。
中药高剂量组按人鼠1∶8比例给予归术益坤方浸膏(1.8 g/100 g),中药低剂量组按人鼠1∶4比例给予归术益坤方浸膏(0.9 g/100 g),阳性对照组按人鼠等效比例给予炔雌醇环丙孕酮片溶液(0.03 mg/kg)。各组每日给药量均用生理盐水稀释至2 mL,模型组及空白组给予每日2 mL生理盐水灌胃。每日固定15∶00灌胃,给药时间3周。
1.6 取材与指标观察
各组于末次给药后禁食12小时,水合氯醛腹腔注射麻醉后将大鼠仰卧固定,腹主动脉采血处死,血液注入生化(红)采血管中,离心后取上层血清保存于-80℃冰箱待测。下延切口,暴露子宫及双侧输卵管、卵巢,眼科剪取下双侧卵巢组织,分离清除表面输卵管及脂肪组织,称重,游标卡尺测量双侧卵巢长、宽、厚,左侧卵巢置于10%甲醛中固定,右侧卵巢冻存于液氮中备用。
1.6.1 卵巢形态学变化 (1)卵巢大体形态学比较:观察卵巢形态学变化、称重,计算椭圆形卵巢体积[体积(mm3)=0.52×长×宽×厚]。分别计算双侧卵巢体积后取平均值记录。(2)卵巢的相对质量(mg/100 g体质量):根据大鼠体质量和卵巢质量计算卵巢相对质量(脏器指数),即卵巢质量∕(体质量×10-2)。计算双侧卵巢的相对质量后取平均值记录。
1.6.2 ELISA法检测血清性激素(LH、FSH、睾酮)水平变化 参考ELISA试剂盒操作流程:以标准物浓度、OD值为横纵坐标,计算出标准曲线、回归方程,计算样品浓度,乘以稀释倍数后即可得实际样品浓度。
1.6.3 Western Blot法检测各组大鼠卵巢组织中SIRT1、PPAR-α、PPAR-γ、FOXO1、FOXO3蛋白相对表达 卵巢组织研磨匀浆后提取总蛋白,BCA蛋白定量法测定蛋白浓度,蛋白上样缓冲液将蛋白定量为5 mg/mL。制备SDS-PAGE凝胶,上样,电泳。湿转法65V转膜2小时至PVDF膜上,置封闭液中封闭1小时。加入不同的一抗孵育:兔抗SIRT1抗体(1∶1 000)、兔抗PPAR-α抗体(1∶500)、兔抗PPAR-γ抗体(1∶500)、兔抗FOXO1抗体(1∶1 000)、兔抗FOXO3抗体(1∶1 000)。TBST缓冲液室温下缓慢摇动洗涤三次,每次10分钟。羊抗兔IgG二抗用TBST稀释3 000倍,室温、避光缓慢摇动作用1小时。洗膜后用ECL发光试剂盒显色,化学发光成像系统成像。Image J软件数字化分析。目标蛋白相对表达量=目标蛋白灰度值/内参(GAPDH)灰度值。
1.7 统计学分析
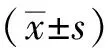
2 结果
2.1 各组PCOS大鼠卵巢体积变化
与空白组相比,模型组大鼠的卵巢体积显著增大(P<0.01),表明高雄激素PCOS大鼠模型建立成功。与模型组相比,阳性对照组、中药高、低剂量组大鼠卵巢体积均显著减小(P<0.01)。其中,中药高剂量组卵巢体积显著小于阳性对照组(P<0.05)和中药低剂量组(P<0.05),而阳性对照组卵巢体积显著低于中药低剂量组(P<0.05)。上述结果说明,中药归术益坤方和炔雌醇环丙孕酮片对PCOS大鼠模型均有治疗作用,可显著降低卵巢体积,并且高剂量归术益坤方(1.8 g/100 g)效果显著优于炔雌醇环丙孕酮片。见表1。
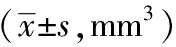
表1 各组PCOS大鼠单个卵巢体积比较
2.2 各组PCOS大鼠卵巢相对质量变化
造模后,模型组大鼠的卵巢相对质量显著增大(P<0.01)。较之模型组,阳性对照组、中药高、低剂量组大鼠卵巢相对质量均减少(P<0.01)。其中,阳性对照组和中药高剂量组的卵巢相对质量均小于中药低剂量组(P<0.05),而阳性对照组与中药高剂量组间无明显差异(P>0.05)。上述结果说明,中药归术益坤方和炔雌醇环丙孕酮片均可显著降低PCOS大鼠模型的卵巢相对质量,且归术益坤方的治疗效果与剂量有关。见表2。

表2 各组PCOS大鼠卵巢相对质量比较
2.3 各组PCOS大鼠血清LH、FSH比较
造模后,模型组大鼠血清LH/FSH比值明显上升(P<0.01),阳性对照组、中药高、低剂量组血清LH/FSH比值均有降低(P<0.05)。其中,中药高剂量组与阳性对照组比较无明显差异(P>0.05),中药高剂量组与中药低剂量组比较无明显差异(P>0.05),但阳性对照组LH/FSH比值低于中药低剂量组(P<0.05)。上述结果说明,中西药物均对改善PCOS大鼠血清LH/FSH比值有效,但差异不明显,炔雌醇环丙孕酮片的治疗效果优于低剂量中药。见表3。

表3 各组PCOS大鼠血清LH/FSH比较
2.4 各组PCOS大鼠血清睾酮比较
造模后,模型组大鼠血清睾酮水平明显上升(P<0.01),各治疗组血清睾酮水平较模型组均有改善(P<0.05)。其中,阳性对照组血清睾酮浓度显著低于中药高、低剂量组(均P<0.05),中药高剂量组与低剂量组疗效比较无明显差异(P>0.05)。这提示,炔雌醇环丙孕酮片对于改善高雄激素血症的治疗效果优于中药归术益坤方。见表4。
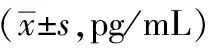
表4 各组PCOS大鼠血清睾酮比较
2.5各组PCOS大鼠卵巢组织SIRT-FOXO信号通路相关蛋白表达情况
造模后,模型组大鼠卵巢内SIRT-FOXO信号通路相关蛋白SIRT1、FOXO1、FOXO3、PPAR-α、 PPAR-γ表达均升高(P<0.01)。 与模型组比较,中药高、 低剂量组上述蛋白表达水平均显著降低(P<0.05),且中药高剂量组SIRT1、FOXO1、FOXO3、PPAR-γ蛋白的降低显著优于中药低剂量组。与模型组比较,阳性对照组FOXO1、FOXO3、PPAR-γ蛋白表达水平显著下调(P<0.05),但SIRT1、PPAR-γ蛋白表达水平升高(P<0.05)。炔雌醇环丙孕酮对SIRT1、FOXO1、FOXO3的治疗效果优于低剂量中药(P<0.05),弱于高剂量中药(P<0.05)。见表5、图1。

表5 各组PCOS大鼠卵巢组织SIRT-FOXO信号通路相关蛋白表达情况比较

图1 各组PCOS大鼠卵巢组织SIRT-FOXO信号通路相关蛋白表达
3 讨论
PCOS发生的主要病因是脏腑功能失调引起肾—天癸—冲任—胞宫轴调节紊乱,其中脾肾两虚是发病根本,肝郁是重要环节,痰湿、瘀血内阻为主要的病理机制,病性属本虚标实,多从肾、脾、肝论治[4]。柴嵩岩国医大师致力于本病研究70余年,归纳出本病“二阳致病”理论[6],并依据此理论自拟归术益坤方。全方以菟丝子、白术为君,菟丝子补肝肾,益精髓,白术味苦甘,有补气健脾、燥湿利水、止汗安胎的功效;当归为臣药,既可活血,又可补血,补中有动,行中有补;另以益母草等药为佐使。归术益坤方全方共奏补肾健脾、养血通利之功,独创从肺、脾、肾三脏共同论治之法,达到标本兼治之效。
本研究团队前期研究已证实,归术益坤方可显著上调P53基因的表达,下调AMPK基因的表达,通过调控P53/AMPK通路影响卵巢颗粒细胞自噬,从而干预PCOS发病,这为中药干预PCOS的机制研究提供了新依据[5]。
本研究目标在于SIRT1-FOXO通路。SIRT1作为一种去乙酰化酶,主要影响多种蛋白的转录,从而调节下游因子和蛋白表达水平,并可通过多种机制调控细胞凋亡,影响疾病发生[7]。SIRT1可与多种底物相互作用,通过去乙酰化形式参与调控细胞凋亡、DNA损伤的修复、脂代谢等过程[3]。
PPAR-α、PPAR-γ是SIRT1的下游基因,其表达与SIRT1正相关,升高的PPAR水平可激活脂肪动员,调节脂类重新分布[8],这提示SIRT1可通过PPAR通路影响脂肪累积,导致PCOS患者肥胖、性激素变化和胰岛素抵抗等临床症状[9]。氧化应激时,FOXO的乙酰化增强,FOXO活化通路中下游靶因子的活性,发生细胞凋亡[10]。在棕色脂肪组织中,SIRT1抑制Smad3和ATF4进而减少应激引起的细胞凋亡[11]。
前期研究的P53基因亦可与SIRT1共同发挥作用,调节FOXO家族多种蛋白活性,同时FOXO也可反向调控SIRT1的表达,发挥各自生理功能。FOXO家族在应激损伤,DNA修复和细胞凋亡中发挥重要作用[12]。FOXO属于叉头盒转录因子家族,在哺乳动物中包含FOXO1、FOXO3、FOXO4和FOXO6四个亚型,其中FOXO1最早被发现、研究[13]。而FOXO家族成员FOXO1已被证明在糖脂代谢、胰岛素抵抗及氧化应激过程中发挥着至关重要的作用[14-15]。FOXO1可通过增加血循环中葡萄糖水平来调节肝脏、胰腺、下丘脑—垂体轴和脂肪组织的循环代谢和激素分泌[16-17],FOXO1在糖异生过程中作用于葡萄糖-6-磷酸酶等关键酶升高血糖水平,并通过胰岛素影响胰岛β细胞的凋亡和糖尿病的发展[18]。另有研究发现,FOXO1的表达与PCOS患者体内C反应蛋白、白介素和肿瘤坏死因子α等慢性炎症因子呈正相关,后者通过内分泌、旁分泌和自分泌机制降低组织细胞对胰岛素的敏感性,从而引起胰岛素抵抗,导致PCOS发病[19-20]。
本研究在前期研究的基础上,进一步聚焦归术益坤方对SIRT1-FOXO通路的影响,以期进一步明确中药治疗PCOS的作用机制。结果显示,经高脂饲料喂养联合丙酸睾酮造模后,模型组大鼠卵巢体积、卵巢相对质量、血清LH/FSH比值、血清睾酮水平均有明显提升,卵巢组织SIRT1-FOXO通路各相关蛋白表达均升高。经归术益坤方干预后,卵巢体积、质量、血清学指标均有显著改善,该通路相关蛋白表达也出现下调。其中部分结果中药高剂量组优于中药低剂量组,说明药物剂量对疗效存在影响。同时,阳性对照药物炔雌醇环丙孕酮片对卵巢形态学、血清学指标均有改善,其中对血清LH/FSH比值、血清睾酮水平的疗效明显优于归术益坤方,且对FOXO1、FOXO3、PPAR-γ蛋白亦有下调作用。以上结果证明,归术益坤方可调控SIRT1-FOXO通路上相关基因表达,减轻PCOS大鼠卵巢增大、血清学改变等症状。但炔雌醇环丙孕酮并未影响PPAR-α、SIRT1蛋白表达,却能显著改善激素水平,尤其是降低血清睾酮,这提示SIRT1仍有其他下游基因,且除本通路外仍有其他可能的途径影响PCOS的发病,值得进一步探索。

