岩白菜素对硝苯地平在大鼠体内药动学的影响
隋强君,张 静,柳丽丽
(天津市第三中心医院,天津市人工细胞工程技术研究中心,天津市肝胆疾病研究所,天津 300170)
岩白菜素(bergenin)是岩白菜的主要有效活性成分,又称岩白菜内酯、矮茶素、虎耳草素[1]。岩白菜素具有选择性抑制咳嗽中枢、连续使用无耐受性、不良反应小等优势,在镇咳祛痰方面具有良好的应用前景,现已被《中国药典》收录,用于治疗慢性支气管炎。近年来研究发现,岩白菜素能够调节多种信号通路,具有免疫调节、保肝、抗氧化、抗炎、降尿酸、保护神经等作用[2-5]。但目前对于岩白菜素相关的的药物相互作用的研究较少。硝苯地平(nifedipine)作为二氢吡啶类钙通道抑制剂,在临床上应用广泛。此外,硝苯地平经CYP3A代谢为特异性产物氧化硝苯地平,可作为CYP3A酶系的探针药物,用于药物代谢和药物的相互作用等方面的研究[7-8]。本文旨在考查岩白菜素对硝苯地平药动力学的影响,为中药的开发和安全使用提供参考。
1 材料与方法
1.1 药品与试剂 岩白菜素原料药(批号101018,纯度:99.92%),山西玉森制药厂提供;硝苯地平原料药(批号091008,纯度>99%),青岛格瑞药业有限公司提供;硝苯地平对照品(批号1000338-200502)、格列齐特对照品(批号100585-200602),均购自中国药品生物制品检定所;乙腈、甲醇、乙酸乙酯,均为色谱纯,美国Dikma Technologies公司生产;甲酸,色谱纯,Sigma公司生产;羧甲基纤维素钠(CMC-Na),化学纯,国药集团化学试剂有限公司生产。
1.2 主要仪器Agilent 1200型高效液相色谱仪串联Agilent 6410三重四级杆串联质谱仪(配电喷雾离子源)、Hip-ALS SL进样器、Agilent Mass Hunter分析软件(美国Agilent公司);XW-80A型旋涡混合器(上海精科实业有限公司);PROIND离心机(德国贺利氏公司);AX-205 Delta Range电子天平(瑞士梅特勒公司)。
1.3 实验动物 健康雄性Wistar大鼠,体重为(210±10)g,购自山东大学实验动物中心,SPF级,实验动物生产许可证号:SCXK(鲁)2013 0009。大鼠饲养环境为12 h/d人工照明,温度20~25℃,相对湿度45%~60%。动物实验方案符合实验动物伦理的相关规定。
2 方法与结果
2.1 溶液的配制
2.1.1 对照品溶液的配制 精密称取硝苯地平和格列齐特对照品各0.010 g,分别置于10 ml量瓶中,用甲醇溶解并定容,配成浓度为1 mg/ml的储备液。取适量内标储备液,采用流动相稀释,得到2.0 μg/ml内标标准溶液。采用流动相梯度稀释硝苯地平储备液,配制成系列标准溶液。所有溶液置于4℃保存。
2.1.2 大鼠灌胃液的配制 称取适量岩白菜素和硝苯地平原料药,分别采用0.5%CMC-Na溶液配制成混悬液(岩白菜素3 mg/ml,硝苯地平1 mg/ml),所有灌胃给药样品均系新鲜配制。
2.2 测定方法
2.2.1 色谱条件 色谱柱为Diamonsil Plus C18-A(250 mm×4.6 mm,5 μm);柱温30℃;流动相为乙腈-0.1%甲酸(60∶40),在线脱气;流速1 ml/min;进样量5 μl。
2.2.2 质谱条件 采用电喷雾离子源(ESI),正离子模式;干燥气为高纯度氮气,流速10 L/min,温度为350℃;雾化压力40 psi,毛细管电压4 000 V;多重反应监测(MRM)模式扫描,扫描间隔为200 ms;硝苯地平和内标的定量离子对分别是m/z 347.1→254.1、324.2→127.1,碎片电压为100 V,碰撞能分别是20 eV。
2.3 血浆样品预处理 精密量取血浆样品100 μl,加入2.0 μg/ml内标溶液10 μl,涡旋混匀,加入1 ml乙酸乙酯,涡旋提取2 min。5 000 r/min离心5 min,吸取上层有机相,于40℃水浴氮气流吹干。残渣用100 μl流动相复溶,取5 μl进样分析。
2.4 专属性试验 取空白大鼠血浆100 μl,除不加内标溶液外,按照“2.3”项下的方法处理;空白血浆外加硝苯地平得到的血浆样品和大鼠给药后的血浆样品,按照“2.3”项下的方法处理。按“2.2”项下方法得色谱图,见图1。结果表明,硝苯地平和内标的保留时间分别是4.72和3.84 min,基线噪音小,各色谱峰形良好,无内源性物质干扰,方法专属性较高。

图1 空白血浆(A)空白血浆加硝苯地平和内标(B)血浆样品(C)HPLC色谱图
2.5 提取回收率与基质效应试验 取大鼠空白血浆加入硝苯地平标准溶液,配制成低、中、高(0.20、1.00和5.00 μg/ml)浓度质控样品溶液,按照“2.3”项下的方法处理,测得峰面积A1;取空白血浆,除不加内标溶液外,按照“2.3”项下的方法处理后,用100 μl浓度为0.20、1.00和5.00 μg/ml的硝苯地平对照品溶液复溶后,测定得峰面积A2。以A1/A2表示提取回收率。取100 μl相应浓度为0.20、1.00和5.00 μg/ml的硝苯地平对照品溶液,于40℃水浴氮气流吹干,用100 μl流动相复溶后,测定得峰面积A3,以A2/A3表示基质效应。内标的提取回收率和基质效应按上述同法计算。结果表明,硝苯地平的提取回收率为68.09%~71.91%,基质效应值为99.15%~102.00%,且无浓度依赖性。内标的提取回收率和基质效应数值分别为67.69%和99.66%,见表1。

表1 提取回收率与基质效应试验结果(x±s,n=5)
2.6 标准曲线的制备 取大鼠空白血浆,分别加入适量的硝苯地平标准溶液,配制成含有硝苯地平浓度为0.10、0.20、0.50、1.00、2.00、4.00和5.00 μg/ml的血浆样品溶液,按“2.3”项下的方法处理后,进样测定,每一个质量浓度进行3份样品分析。以待测物质量浓度为横坐标X,待测物与内标峰面积比值为纵坐标Y,用加权最小二乘法进行回归分析,权重系数为1/X2,线性回归方程为:Y=2.137 4X+0.100 1(r=0.996),线性范围为0.10~5.00 μg/ml。
取大鼠空白血浆加入硝苯地平标准溶液,配制成含硝苯地平浓度为0.10 μg/ml的血浆样品溶液,按“2.3”项下的方法处理后进样测定,并根据当日标准曲线计算样品浓度。结果显示,其S/N≥10,硝苯地平的最低定量限(LLOQ)为0.10 μg/ml。
2.7 准确度与精密度试验 取大鼠空白血浆加入适量的硝苯地平标准溶液,配制低、中、高(0.20、1.00和5.00 μg/ml)浓度的质控样品溶液,按“2.3”项下的方法处理后,进样分析,每一质量浓度制备5份,每天测定一次,连续测定3 d,并按当日的标准曲线计算质量浓度,与配制浓度比较,计算日内和日间的相对误差(RE)和相对标准偏差(RSD),分别考查方法的准确度与精密度,结果表明精密度与准确度符合测定要求,见表2。

表2 准确度与精密度试验结果(x±s,n=5)
2.8 稳定性试验 取大鼠空白血浆加入适量的硝苯地平标准溶液,配制低、中、高(0.20、1.00和5.00 μg/ml)浓度的质控样品溶液,按“2.3”项下的方法处理后,于进样器中放置7 h,进行样品分析,考查血浆样品提取后的室温放置稳定性。另配制低、中、高(0.20、1.00和5.00 μg/ml)浓度的质控样品,分别经冻融2次、冷冻14 d后,按“2.3”项下的方法处理后,进样测定,考查血浆样品的冻融稳定性和长期冷冻稳定性。结果,大鼠血浆样品在整个分析期间,稳定性良好。见表3。

表3 硝苯地平在不同条件下的稳定性(x±s,n=5)
2.9 药动学试验18只健康雄性Wistar大鼠适应性饲养1周后,按体重随机分为实验组(多次给药组、单次给药组)、对照组,每组各6只。多次给药组:灌服岩白菜素30 mg/kg,3次/d,连续灌服7 d;单次给药组与对照组:灌服等体积的0.5% CMC-Na溶液,3次/d,连续灌服7 d。末次灌服岩白菜素或0.5%CMC-Na溶液后,大鼠禁食不禁水12 h。之后,实验组大鼠灌服岩白菜素30 mg/kg后,立即灌服硝苯地平10 mg/kg;对照组大鼠灌服0.5%CMC-Na溶液后,立即灌服硝苯地平10 mg/kg。
于给药前和药后5 min,0.25、0.50、0.75、1.0、2.0、4.0、6.0、8.0、10、12和24.0 h抽取颈静脉血0.3 ml,立即置于肝素抗凝化的EP管中,10 000 r/min离心5 min,分离上层血浆,-80°C冷冻保存备测。在整个实验大鼠样品测定过程中,同时制备并测定质控样品。以当日的标准曲线回归方程计算硝苯地平的质量浓度。
采用药动学分析软件DAS 2.0统计矩法分析药动学特征,药动学参数包括药时曲线下面积(AUC)、平均驻留时间(MRT)、达峰时间(Tmax)、清除率(Cl)、表观分布容积(V)、药峰浓度(Cmax)、消除半衰期(t1/2);采用SPSS 20.0分析实验数据,P<0.05表示有显著性差异。
各组大鼠给药后各时间点的硝苯地平血浆浓度见表4,血药浓度-时间曲线见图2,主要药动学参数见表5。

表5 硝苯地平的主要药动学参数(x±s,n=5)
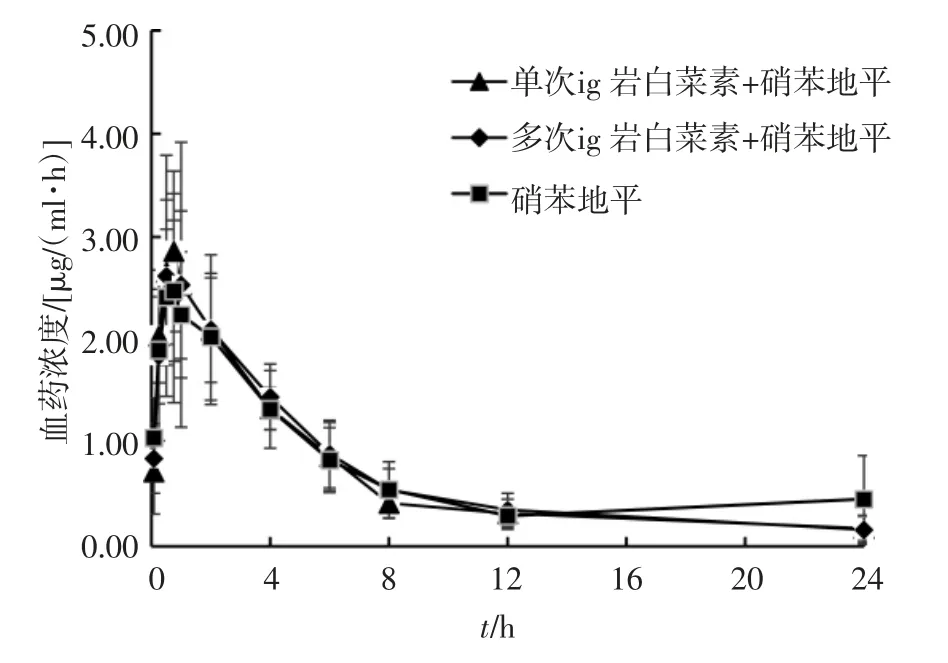
图2 大鼠硝苯地平的血药浓度均值-时间曲线(n=6)

表4 大鼠给药后各时间点的硝苯地平血药浓度均值(n=5)
3 讨论
3.1 吸收AUC和Cmax、Tmax分别作为吸收程度与吸收速度的指标。吸收程度增加会导致AUC和Cmax升高,吸收速度增快会导致Cmax升高,Tmax缩短。本研究中发现,单次灌服或连续灌胃岩白菜素1周,大鼠体内硝苯地平的AUC0-t和AUC0-∞、Tmax和Cmax均无显著性变化。
硝苯地平主要在小肠中经主动转运吸收。岩白菜素属于弱酸性物质,在酸性环境中稳定,而在中性和碱性环境易分解[1,6]。岩白菜素在小肠中主要通过被动扩散吸收,有别于硝苯地平的吸收途径,因此,对其吸收影响的可能性降低。此外,硝苯地平是CYP3A酶和外排蛋白糖蛋白(P-gp)的底物。若药物能够作用于CYP3A或P-gp,可通过竞争性抑制或直接影响CYP3A的生物转化作用、P-gp的外排作用,对硝苯地平的口服生物利用度产生一定影响[5,7,8]。本研究发现,合用岩白菜素后,大鼠体内硝苯地平的口服生物利用度无明显变化,提示岩白菜素可能对肠道细胞CYP3A酶和P-gp无影响,因此不影响肠道内硝苯地平代谢和外排。
3.2 分布与消除 表观分布容积V反映了药物在体内分布情况,MRT、t1/2、Cl是药物体内药物消除速度的评价指标。单次或多次灌服岩白菜素对大鼠体内硝苯地平的药动学参数均无显著性影响,表明岩白菜素对硝苯地平的分布和消除的影响不明显。
硝苯地平在体内分布广泛,主要经肝脏CYP3A酶系代谢代谢为氧化硝苯地平,为一相代谢。而岩白菜素进入体内后分布迅速,消除速度较快[5-6]。岩白菜素在大鼠体内主要是二相代谢,经尿苷二磷酸葡糖醛酸基转移酶(UGT)代谢为葡糖醛酸化岩白菜素,还存在硫酸化、水解合并甲基化两种代谢途径[9]。因此,岩白菜素对硝苯地平的分布和代谢途径影响小。此结果还提示,岩白菜素对硝苯地平的代谢酶的影响不显著。因此,岩白菜素与其他CYP3A底物联合应用时,可能不影响此类药物的分布和代谢,这有待于进一步研究。
本研究结果显示,岩白菜素对硝苯地平在大鼠体内的药动学过程影响不明显,对临床药物的联合应用具有一定的参考意义。但由于药物代谢酶的种属差异,人体内是否存在一致的药物相互作用,有待进一步研究论证。

