甘肃铨水掌叶大黄的HPLC 谱效研究∗
马琴国,刘效栓,罗燕燕,张中华,王引权,刘东玲
1 甘肃省中医院,甘肃 兰州 730050;2 甘肃省中药质量与标准研究重点实验室培育基地;3 甘肃中医药大学;4 西北中藏药协同创新中心
大黄为蓼科植物掌叶大黄Rheum palmatumL.、唐古特大黄Rheum tanguticumMaxim.ex Balf.或药用大黄Rheum officinaleBaill. 的干燥根及根茎。不同来源的大黄,化学成分组成比例及疗效往往不尽相同[1-4]。不同产区大黄在各类功效组分含量方面存在差异,而建立谱效图[5-6],能更准确地反映中药材和中药饮片的药效特点。现代药理研究[7-11]表明,大黄的泻下成分主要为结合蒽醌类和双蒽酮类化合物,故笔者以泻下活性成分为指标建立大黄的高效液相色谱法(high performance liquid chromatography,HPLC)图谱,对大黄质量特征进行究[12]。笔者在研究大黄泻下成分的基础上,针对铨水大黄的指纹图谱进行研究,旨在为甘肃道地药材铨水掌叶大黄的质量控制及临床合理用药提供参考。
1 仪器与试药
1.1 仪器高效液相色谱仪(Waters,1525 泵,717,2487 双通道紫外检测器Breeze),AR124CN 型电子天平(上海奥豪斯仪器有限公司),SB-3200D型超声波清洗器(宁波新芝生物科技股份有限公司)。
1.2 试药番泻苷-A(成都普瑞法科技有限公司,批号:PRF7111501,纯度≥98%)大黄酚8-o-葡萄糖苷(成都普瑞法科技有限公司,批号:BP0350,纯度≥98%),番泻苷-B(成都普瑞法科技有限公司,批号:BP1293,纯度≥98%),大黄酸8-o-β-D 葡萄糖苷(成都普瑞法科技有限公司,批号:BP1527,纯度≥98%),大黄素8-o-β-D 吡喃葡萄糖(成都普瑞法科技有限公司,批号:BP0534,纯度≥98%),色谱纯乙腈(天津市大茂化学试剂厂,批号:20160505),色谱纯磷酸(天津市大茂化学试剂厂,批号:20160307),色谱纯无水乙醇(天津市大茂化学试剂厂,批号:20160905)。大黄试样:样品12 批大黄药材,分别从甘肃礼县10 个乡采集所得,样品信息见表1。

表1 大黄药品采样表
2 方法与结果
2.1 色谱条件色谱柱:Symmetry C18柱,甲醇为流动相A,0.1%磷酸水溶液为流动相B,柱温25℃,检测波长237 nm,流速1 mL/min,梯度洗脱程序见表2。

表2 梯度洗脱程序
2.2 混合对照品溶液制备精密称取对照品番泻苷A 1.42 mg、用0.1% 的NaHCO3溶液溶解,并定容至10 mL 容量瓶中,得到0.142 mg/mL 的番泻苷A对照品。精密称取对照品番泻苷B 0.001 9 g,用70%的甲醇溶解,定容至25 mL容量瓶,得到0.076 mg/mL的番泻苷B 对照品,精密称取对照品大黄素-8-β-吡喃葡萄糖苷0.000 43 g,用甲醇溶解,定容至5 mL 容量瓶,得到0.086 mg/mL 的大黄素-8-β-吡喃葡萄糖苷对照品溶液。精密称取对照品大黄酸-8-o-D-β-葡萄糖苷0.000 43 g,用甲醇溶解,定容至5 mL容量瓶,得到0.15 mg/mL的大黄酸-8-o-D-β-葡萄糖苷对照品溶液。精密称取对照品大黄酚-8-o-葡萄糖苷0.000 38 g,用甲醇溶解,定容至5 mL 容量瓶,得到0.076 mg/mL 的大黄酚-8-o-葡萄糖苷对照品溶液。分别精密吸取上述大黄素-8-β-吡喃葡萄糖苷、大黄酸-8-o-D-β-葡萄糖苷、大黄酚-8-o- 葡萄糖苷、溶液2.0 mL,得0.017 2、0.030 0、0.015 2 mg/mL 的混合对照品。另精密番泻苷A 1.0 mL,番泻苷B 1.0 mL,至10 mL容量瓶中,用70% 的乙醇定容,得质量浓度分别为0.014 2、0.007 6 mg/mL 的混合对照品溶液,4℃冰箱避光保存。
2.3 供试品溶液制备将新鲜大黄(1~10 号)样品用熏干法干燥,粉碎,过65 目筛。取大黄粉末约200 mg,精密称定,置具塞锥形瓶中,精密加入70%乙醇25 mL,密塞,称定质量,静置12 h,60℃超声处理(功率250 W,频率40 kHz)30 min,取出,放冷,摇匀,0.45 µm微孔滤膜过滤,即得大黄粉末70% 乙醇溶液。将大黄乙醇溶液用乙醚脱脂后,定容至10 mL容量瓶,得醇提供试品。另取大黄粉末约200 mg,精密称定,置具塞锥形瓶中,精密加入0.1%NaHCO325 mL,密塞,称定重量,静置12 h,60℃超声处理(功率250 W,频率40 kHz)30 min,取出,放冷,摇匀,0.45 µm 微孔滤膜过滤,即得大黄粉末0.1%NaHCO3溶液。将大黄乙醇溶液用乙醚脱脂萃取后,定容至10 mL 容量瓶,得0.1%NaHCO3提取供试品。
2.4 系统适应性试验取混合对照品溶液,供试品溶液在“2.1”项色谱条件下进样分析,结果分离度良好,见图1。
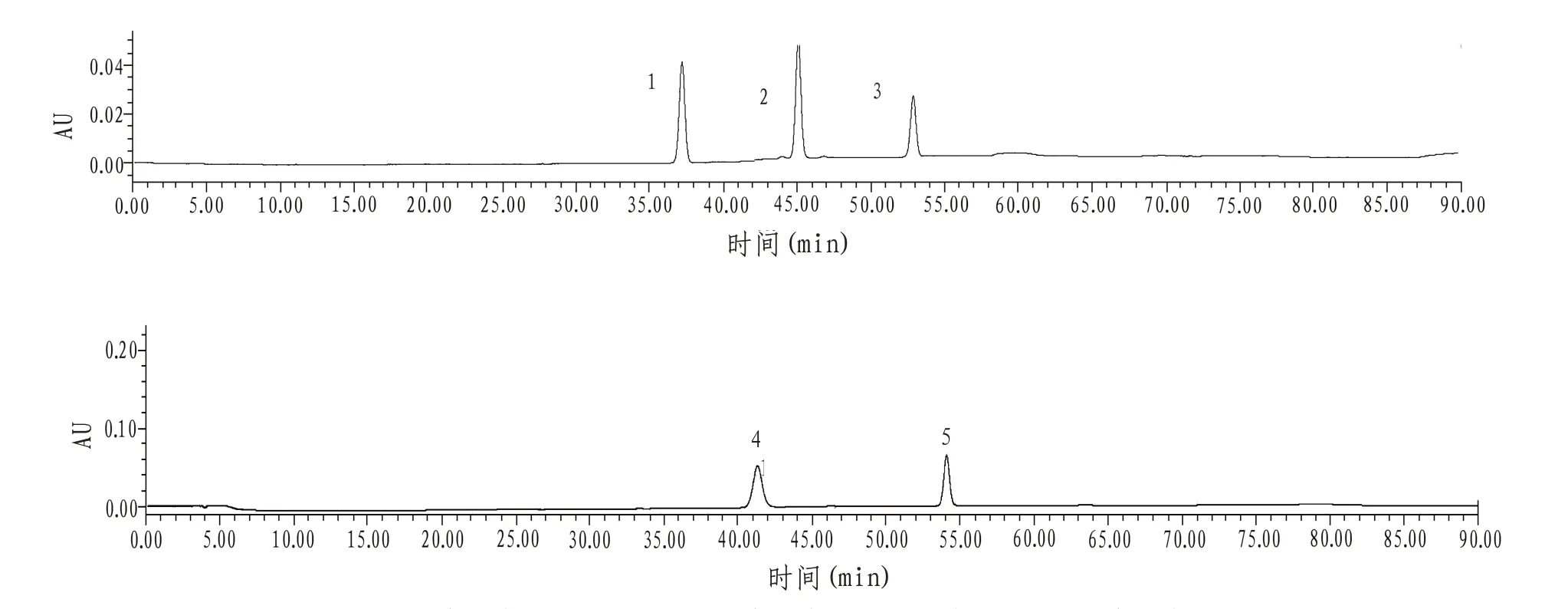
图1 混合对照品色谱图
2.5 精密度试验精密吸取“2.2”项下混合对照品溶液10 µL,连续进样5次。番泻苷A、番泻苷B、大黄素-8-β-吡喃葡萄糖苷、大黄酸-8-o-D-β-葡萄糖苷、大黄酚-8-o-葡萄糖苷的进样量分别为:0.142、0.076、0.172、0.300、0.228 µg;以(1号峰)为参照,其他共有峰相对保留时间按公式:γi,计算,共有峰相似度达到1.000。相对保留时间RSD及峰面积RSD。见表3。
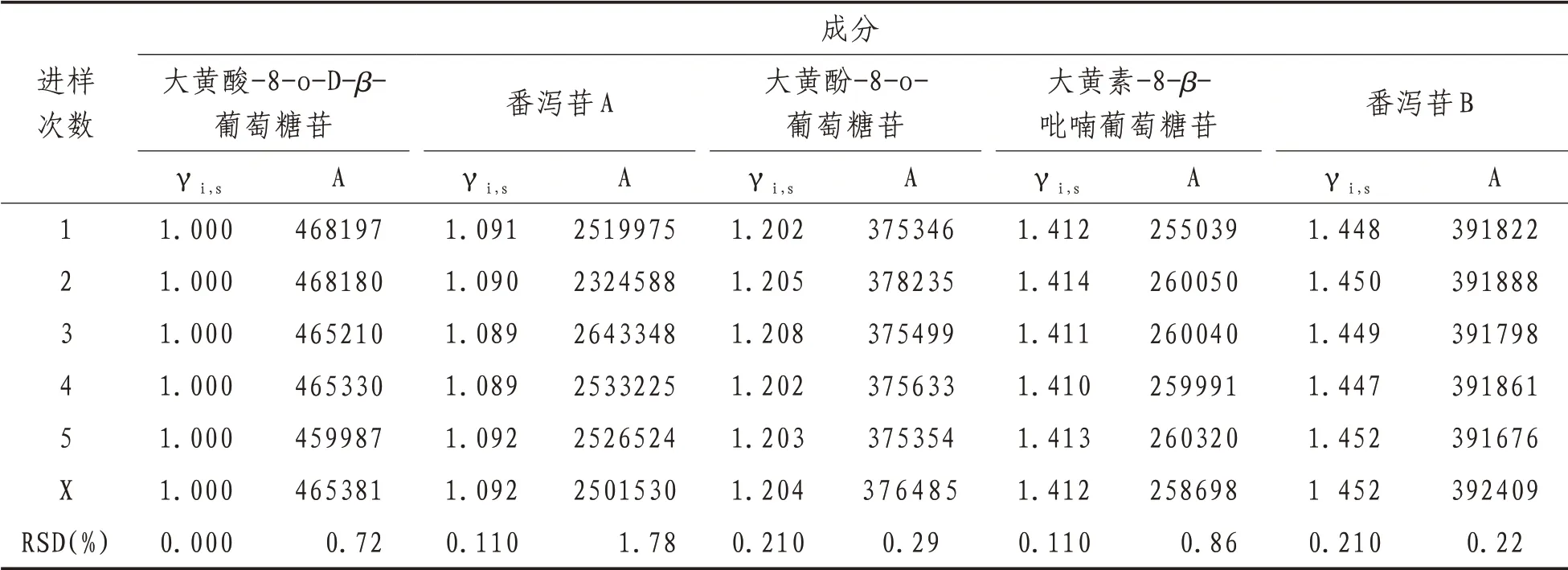
表3 精密度试验
2.6 稳定性试验取同一供试品溶液,分别在0、6、12、18、24 h 进样10 µL,检测色谱图,对其中的特征色谱峰进行分析,所得特征峰的峰面积RSD 均<3%,相对保留时间的RSD 均<2%,结果表明供试品溶液在24 h内稳定。见表4。
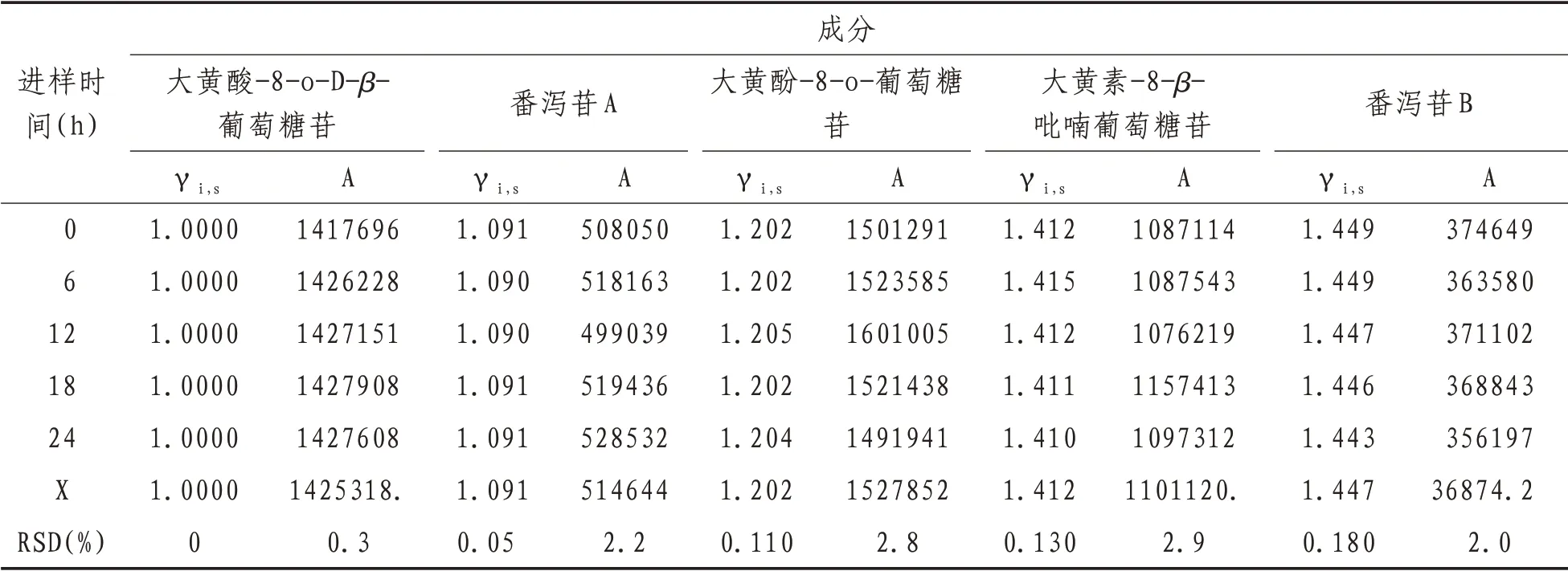
表4 稳定性试验结果
2.7 重复性试验取同一批样品(批号:20160905)6 份,约200 mg,精密称定,按“2.3”项下方法制备6 份,分别进样10 µL,检测色谱图,结果大黄素-8-β-葡萄糖苷、番泻苷A、大黄酚-8-o-葡萄糖苷、番泻苷B、大黄素-8-β-吡喃葡萄糖苷的平均含量分别为:65.40、17.94、2.97、26.05、5.92 mg/g,峰面积RSD 均<3%,相对保留时间的RSD 均<1%,相似度1.000,符合指纹图谱要求。见表5。

表5 重复性试验结果
2.8 指纹图谱的分析按照中药指纹图谱要求,检测10 批样品,其所有成分在90 min 内全部出完,见图2;采用中药色谱指纹图谱相似度评价软件(2012.130723 版本),将10 批样品HPLC 图谱数据导入软件,进行相似度分析,生成对照图谱(R),以大黄素苷(1 号峰)为参照,共有峰的保留时间、相对保留时间、峰面积百分比。见表6、图3。

图2 样品色谱图

图3 10批甘肃礼县铨水掌叶大黄HPLC指纹图谱及对照指纹图谱

表6 礼县掌叶大黄指纹图谱技术参数

续表6
2.9 相似度评价以S1 样品的指纹图谱作为参照图谱,以平均数法生成10批样品的对照指纹图谱;10 批样品与对照指纹图谱相似度分别为0.943,0.927,0.947,0.923,0.793,0.798,0.906,0.828,0.798,0.928,即:相似度在0.8~0.9 之间。非公有峰面积在20%。10 批掌叶大黄的选择了共有峰的相对保留时间的RSD 为0.801%~1.727%,相对峰面积的RSD 为28.87%~123.04%。说明10 个样品组成成分较为一致,但各成分的含量差异较大。
3 讨论
本试验首次以掌叶大黄中的泻下活性成分大黄酸-8-o-D-β-葡萄糖苷、番泻苷A、大黄酚-8-o-葡萄糖苷、番泻苷B、大黄素-8-β-吡喃葡萄糖苷为参照,应用HPLC,初步研究了甘肃道地药材掌叶大黄药效图谱,这种药效相关联的中药图谱可为中药大黄质量控制以及大黄合理应用提供参考数据。从掌叶大黄指纹图谱可以看出,番泻苷A,番泻苷B 的峰面积总和远远低于大黄酸-8-o-Dβ-葡萄糖苷、大黄酚-8-o-葡萄糖苷、大黄素-8-β-吡喃葡萄总和,番泻苷A 的峰面积分别与大黄酸-8-o-D-β-葡萄糖苷、大黄酚-8-o-葡萄糖苷、大黄素-8-β-吡喃葡萄的峰面积比值为0.12、0.21、0.37。番泻苷B 的峰面积分别与大黄酸-8-o-Dβ-葡萄糖苷、大黄酚-8-o-葡萄糖苷、大黄素-8-β-吡喃葡萄的峰面积比值为0.10、0.18、0.32。在大黄泻下作用中,二蒽醌苷类所做的贡献有可能大于双蒽酮苷类(番泻苷类),这有待于量效关系的进一步明确研究。礼县铨水掌叶大黄的泻下作用指纹图谱与唐古特大黄、药用大黄图谱的差异,有待进一步研究。
有研究表明[4],种植掌叶大黄中番泻苷的总量低于野生大黄的番泻苷总量。礼县铨水掌叶大黄中番泻苷A,番泻苷B 峰面积小,在泻下功效成分中所占比率小,可能是因产地、生态环境不同。番泻苷不耐热,在产地加工和煎煮过程中,其含量都会受影响,因此干燥温度、煎煮温度控制会影响番泻苷A、B 的含量。将来可以考察不同干燥温度对大黄番泻苷的影响。有研究报道,礼县铨水掌叶大黄的番泻苷含量低于唐古特大黄的番泻苷含量。大黄酸-8-o-D-β-葡萄糖苷、大黄酚-8-o-葡萄糖苷、大黄素-8-β-吡喃葡萄的含量差别未见报道。
本试验主要以礼县铨水掌叶大黄为研究对象,不同产地产地指纹图谱的大黄指纹图谱差异有待进一步考察。笔者利用紫外分光光度法选择最大吸收波长,最大吸收波长选择237 nm。在本试验中,番泻苷A 不容易溶于温水或乙醇,所以用0.1%的NaHCO3配置对照品溶液。根据对照品的溶解实验,在对供试品的处理中,使用0.1% 的NaHCO3溶液,温度控制在60摄氏度,尽可能对供试品中的番泻苷A、番泻苷B 提取完全,尽可能防止因温度过高而分解。

