樟树叶化学成分研究(II)
廖矛川,汪迎洲,杨芳云,李竣,任永申
(中南民族大学 药学院,武汉 430074)
樟(Cinnamomum camphora),是樟科樟属植物,别名香樟、油樟、樟木.樟树味辛、性温,其木、叶、根皮可入药,能祛风、除湿,杀虫等,主治风湿痹痛,水火烫伤,疮疡肿毒,疥癣皮肤瘙痒,毒虫咬伤[1].目前对樟树的研究主要集中在其挥发油部分[2-3],其非挥发性组分的化学成分研究较少,因此本实验主要研究樟树非挥发性化学成分,利用系统溶剂提取法、聚酰胺色谱法、正反相硅胶柱色谱法、大孔树脂,凝胶柱色谱和高效液相色谱法等现代分离技术,从樟树叶氯仿和正丁醇萃取部分进行分离纯化,获得13个化合物,根据理化性质、和波谱数据鉴定化合物结构,其中5个为苯乙醇类化合物,7个为酚类/苄基类化合物,1个为苯丙酸类化合物.13个化合物分别为熊果苷(1)、对硝基苯基-β-D-葡萄糖苷(2)、苄基-β-D-吡喃木糖基-(1-6)-β-D-吡喃葡萄糖苷(3)、淫羊藿次苷D2(4)、对羟乙基苯基-α-L-呋喃芹糖基-(1''-6')-β-D-吡喃葡萄糖苷(5)、3,5-二羟基苯乙醇-3-O-β-D-吡喃葡萄糖苷(6)、4-羟基苯乙醇-3-O-β-D-(6'-O-对羟基苯甲酰基)-β-D-吡喃葡萄糖苷(7)、3-羟基-苯乙醇-4-O-(6'-O-β-芹呋喃糖基)-β-D-葡吡喃糖苷(8)、对羟基苯甲醛(9)、香草醛(10)、对羟基苯乙酮(11)、丁香酸(12)、绿原酸正丁酯(13)(图1).其中化合2~8,13为樟属植物首次分离.
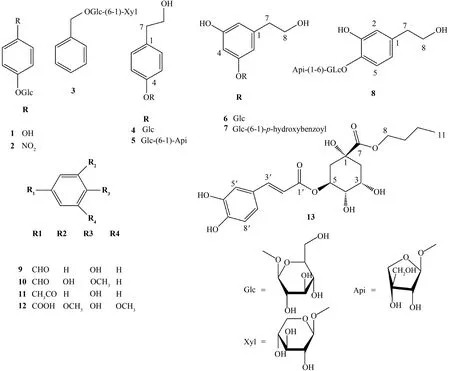
图1 化合物1~13的结构式Fig.1 Chemical structures of compounds 1-13
1 仪器与试剂
核磁共振波谱仪(AM-400/500型,德国Bruker),高效液相色谱仪(Ultimate-3000半制备型,美国Dionex),中压柱层析系统(HEP-50A型,武汉金帝仪器),色 谱 柱(YMC-Pack ODS-A,250×10 mm,5 μm),柱层析硅胶(100~200,200~300,300~400目,青岛基亿达),薄层层析硅胶(GF254高效薄层板,青岛鑫昶来),其他试剂均为分析纯(济宁佰一化工).
2 提取与分离
取干樟树叶15 kg,揉碎,用95%乙醇回流提取3次,减压回收乙醇,最后得浸膏3.94 kg.浸膏加同等质量的蒸馏水分散12 h,然后用石油醚、氯仿、乙酸乙酯和正丁醇分别萃取.取正丁醇浸膏80 g溶于水中,湿法装300 g聚酰胺柱,依次用水-乙醇梯度洗脱,收集70%醇组分后,用正相硅胶依次以氯仿-甲醇(9∶1~6∶4)梯度洗脱,TLC检测并合并相同馏分,经反复硅胶柱色谱层析、和高效液相色谱(乙腈∶水,20∶80等度洗脱)分离得到化合物1(8 mg)、2(9 mg),3(15 mg)、4(12 mg)、5(tR=6.5 min,7 mg)、6(19 mg),7(9 mg)、8(8 mg).取氯仿浸膏50 g,装大孔树脂,上样,用水,75%乙醇,甲醇洗脱,分别得到水、75%乙醇、甲醇3个组份,75%乙醇收集组份经硅胶柱色谱以环己烷-丙酮(8∶1~1∶3)洗脱,经TLC检测并合并相同馏分得到6个部分,然后用正相硅胶色谱、凝胶LH-20和HPLC(乙腈:水,35∶65等度洗脱)获得化合物9(8 mg)、10(6 mg)、11(tR=7.2 min,4 mg)、12(6 mg)和13(60 mg),未萃取粗提物经氯仿-甲醇9∶1洗脱后甲醇重结晶也可获得.
3 结构鉴定
化合物1:白色晶体(乙醇),分子式C12H16O7.1H NMR(500 MHz,CD3OD)δH:6.96(2H,d,J=7.5 Hz,H-3,5),6.69(2H,d,J=7.5 Hz,H-2,6),4.73(1H,d,J=7.5 Hz,H-1'),3.35-3.46(4H,m,H-2'-5'),3.88(1H,d,J=12.0,H-6'b),3.70(1H,dd,J=12.0,3.5 Hz,H-6'a);13C NMR(125 MHz,CD3OD)δC:151.0(C-1),118.0(C-2,6),115.2(C-3,5),152.4(C-4),102.3(C-1'),73.6(C-2'),76.7(C-3'),70.0(C-4'),76.6(C-5'),61.2(C-6').上述波谱数据与文献[4]对照基本一致,故鉴定化合物1为熊果苷.
化合物2:无色油状,分子式C12H15O8.1H NMR(500 MHz,CD3OD)δH:8.22(2H,d,J=8.0 Hz,H-9,11),7.01(2H,d,J=8.4 Hz,H-8,12),5.07(1H,d,J=6.0 Hz,H-1),3.30-4.40(m,糖氢信号);13C NMR(125 MHz,CD3OD)δC:100.2(C-1),73.3(C-2),77.0(C-3),69.8(C-4),76.4(C-5),61.0(C-6),162.5(C-7),116.3(C-8,12),125.2(C-9,11),142.5(C-10).上述波谱数据与文献[5]对照基本一致,故鉴定化合物2为对硝基苯基-β-D-葡萄糖苷.
化合物3:无色油状,分子式C18H26O10.1H NMR(400 MHz,CD3OD)δH:7.15-7.35(5H,H-1-5),4.87(1H,d,J=12.0 Hz,H-7b),4.65(1H,d,J=12.0 Hz,H-7a),4.24(2H,d,J=8.0 Hz,H-1',1'),4.78(1H,d,J=10.0 Hz,H-6'b),4.03(1H,d,J=10.0 Hz,H-6’a),3.78(1H,dd,J=12.0,5.0 Hz,H-6'b),3.67(1H,d,J=12.0 Hz,H-6'a),3.10-3.40(m,糖氢信号);13C NMR(100 MHz,CD3OD)δC:137.7(C-1),127.9(C-2,6),127.9(C-3,5),127.3(C-4),70.1(C-7),102.0(C-1'),73.7(C-2'),76.6(C-3'),70.5(C-4'),76.3(C-5'),68.4(C-6'),104.2(C-1''),73.5(C-2''),75.7(C-3''),69.8(C-4''),65.5(C-5'').上述波谱数据与文献[6]对照基本一致,故鉴定化合物3为苄基-β-D-吡喃木糖基-(1-6)-β-D-吡喃葡萄糖苷.
化合物4:淡黄色油状,分子式C14H20O7.1H NMR(400 MHz,CD3OD)δH:7.13(2H,d,J=8.4 Hz,H-2,6),7.01(2H,d,J=8.4 Hz,H-3,5),4.89(1H,d,J=7.2 Hz,H-1'),3.35-3.85(m,糖氢信号),3.68(2H,m,H-8),2.75(2H,t,J=7.2 Hz,H-7);13C NMR(100 MHz,CD3OD)δC:132.9(C-1),129.5(C-2,6),116.4(C-3,5),156.2(C-4),38.0(C-7),63.0(C-8),101.1(C-1'),73.5(C-2'),76.6(C-3'),70.0(C-4'),76.7(C-5'),61.1(C-6').上述波谱数据与文献[7]对照基本一致,故鉴定化合物4为淫羊藿次苷D2.
化合物5:无色油状,分子式C19H28O11.1H NMR(400 MHz,CD3OD)δH:7.14(2H,d,J=8.0 Hz,H-2,6),7.02(2H,d,J=8.4 Hz,H-3,5),4.96(1H,d,J=7.2 Hz,H-1'),4.81(1H,d,J=1.0 Hz,H-1''),3.15-3.90(m,糖氢信号),3.72(2H,t,J=7.0 Hz,H-8),2.75(2H,t,J=7.0 Hz,H-7);13C NMR(100 MHz,CD3OD)δC:132.9(C-1),129.5(C-2,6),116.5(C-3,5),156.2(C-4),38.0(C-7),63.0(C-8),101.2(C-1'),73.5(C-2'),76.6(C-3'),70.3(C-4'),75.6(C-5'),67.4(C-6'),109.6(C-1''),76.6(C-2''),79.1(C-3''),73.6(C-4''),64.2(C-5'').上述波谱数据与文献[8]对照基本一致,故鉴定化合物5为对羟乙基苯基-α-L-呋喃芹糖基-(1''-6')-β-D-吡喃葡萄糖苷.
化合物6:淡黄色油状,分子式C14H20O8.1H NMR(500 MHz,CD3OD)δH:6.95(1H,s,H-4),6.69(2H,s,H-2,6),4.63(1H,d,J=6.5 Hz,H-1'),3.15-3.80(m,糖氢信号),3.53(2H,t,J=7.2 Hz,H-8),2.61(2H,t,J=7.2 Hz,H-7);13C NMR(125 MHz,CD3OD)δC:130.7(C-1),123.8(C-2),145.4(C-3),115.6(C-4),145.2(C-5),118.2(C-6),38.1(C-7),62.9(C-8),102.9(C-1'),73.5(C-2'),76.3(C-3'),70.0(C-4'),76.9(C-5'),61.1(C-6').上述波谱数据与文献[9]对照基本一致,故鉴定化合物6为3,5-二羟基苯乙醇-3-O-β-D-吡喃葡萄糖苷.
化合物7:无色油状,分子式C21H24O2.1H NMR(400 MHz,CD3OD)δH:7.89(2H,d,J=8.4 Hz,H-2',6'),6.94(1H,d,J=1.7 Hz,H-2),6.82(2H,d,J=8.4 Hz,H-3',5'),6.74(1H,dd,J=8.1,1.7 Hz,H-6),6.72(1H,d,J=8.1 Hz,H-5),4.77(1H,d,J=7.8 Hz,H-1'),3.40-3.80(m,糖氢信号),4.67(1H,dd,J=12.0,2.0 Hz,H-6'b),4.39(1H,dd,J=12.0,7.0 Hz,H-6'a),3.57(2H,t,J=7.9 Hz,H-8),2.55(2H,m,H-7);13C NMR(100 MHz,CD3OD)δC:132.4(C-1),120.7(C-2),145.6(C-3),146.0(C-4),118.2(C-5),125.8(C-6),39.0(C-7),63.9(C-8),103.0(C-1'),73.5(C-2'),76.0(C-3'),170.4(C-4'),74.5(C-5'),63.6(C-6'),122.2(C-1'),132.6(C-2'),116.9(C-3'),165.1(C-4'),116.6(C-5''),133.2(C-6'),168.2(C-7').上述波谱数据与文献[10]对照基本一致,故鉴定化合物7为4-羟基苯乙醇-3-O-β-D-(6'-O-对羟基苯甲酰基)-β-D-吡喃葡萄糖苷.
化合物8:无色油状,分子式C19H28O12.1H NMR(400 MHz,CD3OD)δH:7.06(1H,d,J=8.2 Hz,H-5),6.76(1H,d,J=2.1 Hz,H-2),6.66(1H,d,J=8.2,2.1 Hz,H-6),4.98(1H,d,J=2.4 Hz,H-1''),4.70(1H,d,J=7.2 Hz,H-1'),3.40-3.90(m,糖氢信号),3.72(2H,t,J=7.1 Hz,H-8),2.05(2H,t,J=7.1 Hz,H-7);13C NMR(100 MHz,CD3OD)δC:136.6(C-1),118.3(C-2),148.2(C-3),145.2(C-4),119.6(C-5),123.1(C-6),38.3(C-7),63.1(C-8),103.1(C-1'),73.5(C-2'),76.7(C-3'),70.2(C-4'),75.8(C-5'),67.3(C-6'),109.6(C-1''),76.7(C-2''),79.1(C-3''),73.6(C-4''),64.1(C-5'').上述波谱数据与文献[11]对照基本一致,故鉴定化合物8为3-羟基-苯乙醇-4-O-(6'-O-β-芹呋喃糖基)-β-D-葡吡喃糖苷.
化合物9:黄色无定形粉末,分子式C7H6O2.1H NMR(400 MHz,Acetone)δH:9.83(1H,s,H-CHO),7.78(2H,m,H-2,6),6.99(2H,m,H-3,5).上述波谱数据与文献[12]对照基本一致,故鉴定化合物9为对羟基苯甲醛.
化合物10:白色无定形粉末,分子式C8H8O2.1H NMR(400 MHz,Acetone)δH:9.81(1H,s,H-CHO),7.46(1H,dd,J=8.0,2.0 Hz,H-6),7.43(1H,d,J=2.0 Hz,H-2),6.99(1H,d,J=8.0 Hz,H-5),3.91(3H,s,H-OCH3);13C NMR(100 MHz,Acetone)δC:129.8(C-1),110.1(C-2),148.1(C-3),152.7(C-4),115.1(C-5),126.1(C-6),190.2(C-7),55.4(C-OCH3).上述波谱数据与文献[13]对照基本一致,故鉴定化合物10为香草醛.
化合物11:白色无定形粉末,分子式C8H8O2.1H NMR(400 MHz,Acetone)δH:7.86(2H,d,J=8.4 Hz,H-2,6),6.89(2H,d,J=8.4 Hz,H-3,5),2.47(3H,s,COCH3).上述波谱数据与文献[12]对照基本一致,故鉴定化合物11为对羟基苯乙酮.
化合物12:无色晶体(丙酮),分子式C9H10O5.1H NMR(400 MHz,Acetone)δH:7.31(2H,s,H-2,6),3.87(6H,s,3,5-OCH3);13C NMR(100 MHz,Acetone)δC:120.6(C-1),107.3(C-2,6),147.4(C-3,5),140.65(C-4),166.6(C-7),55.8(3,5-OCH3).上述波谱数据与文献[14]对照基本一致,故鉴定化合物12为丁香酸.
化合物13:无色油状,分子式C20H26O9.1H NMR(400 MHz,CD3OD)δH:7.52(1H,d,J=16.0 Hz,H-3'),7.14(1H,d,J=1.4 Hz,H-5'),7.02(1H,d,J=8.4,Hz,H-9'),6.85(1H,d,J=8.2 Hz,H-8'),6.23(1H,d,J=16.0 Hz,H-2'),5.32(1H,m,H-5),4.15(1H,m,H-3),4.08(2H,t,J=8.8 Hz,H-8),3.72(1H,dd,J=5.2,3.2 Hz,H-4),2.0-2.2(4H,m,H-2,6),1.59(2H,m,H-9),1.35(2H,m,H-10),0.87(2H,m,H-11);13C NMR(100 MHz,CD3OD)δC:75.0(C-1),37.7(C-2),69.9(C-3),70.6(C-4),72.2(C-5),37.0(C-6),173.2(C-7),64.7(C-8),30.4(C-9),18.8(C-10),13.1(C-11),166.2(C-1'),114.2(C-2'),147.8(C-3'),126.8(C-4'),114.8(C-5'),145.4(C-6'),145.0(C-7'),115.5(C-8'),121.7(C-9').上述波谱数据与文献[15]对照基本一致,故鉴定化合物13为绿原酸正丁酯.
4 讨论
樟树是我国亚热带常绿阔叶林中重要的材用和特种经济树种,目前,对樟树的研究大多集中在挥发油的化学成分检测分析和粗提物生物活性方面,而对于樟树叶片中非挥发性成分的化学组成相关报道较少,本实验主要研究樟树叶非挥发性化学成分,从樟树叶提取分离得到13个化合物,13个化合物分别为熊果苷(1)、对硝基苯基-β-D-葡萄糖苷(2)、苄基-β-D-吡喃木糖基-(1-6)-β-D-吡喃葡萄糖苷(3)、淫羊藿次苷D2(4)、对羟乙基苯基-α-L-呋喃芹糖基-(1''-6')-β-D-吡喃葡萄糖苷(5)、3,5-二羟基苯乙醇-3-O-β-D-吡喃葡萄糖苷(6)、4-羟基苯乙醇-3-O-β-D-(6'-O-对羟基苯甲酰基)-β-D-吡喃葡萄糖苷(7)、3-羟基-苯乙醇-4-O-(6'-O-β-芹呋喃糖基)-β-D-葡吡喃糖苷(8)、对羟基苯甲醛(9)、香草醛(10)、对羟基苯乙酮(11)、丁香酸(12)、绿原酸正丁酯(13).化合物2~8,13为樟属植物首次分离.
分离得到成分中熊果苷有美白、祛除色素的特性以及抗氧化、抗炎等药理作用[16],香草醛具有清甜的豆香、粉香气息,可用作定香剂、协调剂及调味剂,对羟基苯甲醛能够显著对抗ADP诱导的家兔体外血小板聚集[17],对羟基苯乙酮可降低高脂血症模型大鼠血清总胆固醇和低密度脂蛋白胆固醇水平[18].以上化合物的提取分离,为樟科樟属植物的研究和开发利用提供了参考.

