超声引导下3种静脉穿刺入路静脉输液港植入术的对比研究
伏 钢,冯 军,高 远,王新润
(无锡市第二人民医院超声科,江苏无锡 214000)
植入式静脉输液港(implantable intravenous port,PORT)是目前临床最常用的肿瘤化疗患者和重症患者营养治疗的给药方式之一。可为需要长期、间断输液的患者提供安全、可靠、美观的静脉通路[1]。其通过输液导管将药物直接输送至上腔静脉下段,利用局部高速、大流量血液的稀释作用,大大降低了高渗、高毒性化疗药物引起的不良反应发生率,具有静脉并发症少和不需要换药的优势[2]。由于植入式静脉输液港属于完全植入性血管通道系统,具有操作简单、维护方便、应用期限长、感染风险低等特点,且不会对患者日常生活产生显著影响[3]。传统的静脉输液港植入术主要为腋静脉穿刺入路、经颈内静脉穿刺入路及经锁骨下静脉穿刺入路。本研究旨在探讨超声引导下3种静脉穿刺入路静脉输液港植入术在临床中的应用价值,结果报道如下。
1 资料与方法
1.1 一般资料 腋静脉入路组:选取2019年10月至2020年10月在无锡市第二人民医院介入超声科经超声引导下行腋静脉穿刺入路静脉输液港植入术患者120例[男性患者72例,女性患者48例;年龄26~87岁,平均年龄(62.13±5.59)岁]。锁骨下静脉入路组:选取2019年1月至12月在无锡市第二人民医院介入超声科经超声引导下行锁骨下静脉穿刺入路静脉输液港植入术患者100例[男性患者59例,女性患者41例;年龄33~82岁,平均年龄(61.27±6.94)岁]。颈内静脉入路组:选取2019年1月至12月在无锡市第二人民医院介入超声科经超声引导下行颈内静脉穿刺入路静脉输液港植入术患者50例[男性患者23例,女性患者27例;年龄39~89岁;平均年龄(63. 46±6.21)岁]。对3组患者的临床资料展开回顾性研究。3组患者一般资料比较,差异无统计学意义(P<0.05),有可比性。纳入标准:患者具有化疗或静脉营养指征且计划行长期化疗或静脉营养。 排除标准:①合并全身严重感染;②凝血功能异常或服用抗凝药物;③上腔静脉受压;④静脉炎及静脉血栓史 ;⑤生存预期小于半年。
1.2 麻醉方法 穿刺引导使用彩色多普勒超声诊断仪(深圳迈瑞生物医疗电子股份有限公司,型号:7Y-98000320),探头型号L11-3U,探头频率9.0MHZ。静脉输液港采用PSU型植入式静脉输液港(法国贝朗公司,型号04436946),含穿刺针、注射座、导管、导丝、导管锁、无损伤蝶翼针等。所有患者均采用标准无菌手术操作技术,病人取仰卧位,常规连接心电监护仪,空出RA导联。超声观察拟穿刺的静脉血管,确定穿刺路径。乳腺癌及肺癌患者从健侧血管入路,其余病种的患者均从右侧血管入路,港体均埋置于目标穿刺血管侧的胸部皮下。
腋静脉入路组与锁骨下静脉入路组除穿刺血管不同外,操作步骤相同,简述如下:①常规消毒铺单后,1%利多卡因局部浸润麻醉,麻醉区域包含囊袋区、手术切口及穿刺入路;②沿锁骨下约两横指处作一手术切口,长约2~2.5 cm,朝下方钝性分离至脂肪层与肌层间隙,制作囊袋并充分止血。囊袋不宜过大或过小,以轻松容下食指为宜;③超声引导下穿刺针穿刺目标血管,采用同平面斜轴穿刺法,见针头进入静脉且回抽见暗红色血液后,沿穿刺针送入J形导丝,超声下确认导丝进入上腔静脉(见图1);④退出穿刺针,沿导丝穿入扩张鞘扩张至血管内,退出扩张鞘,沿导丝穿入导管,退出导丝。以10 mL针筒抽满生理盐水连接穿刺针小心插入导管,无菌导联线连接RA导联与穿刺针,缓慢向导管内推注生理盐水的同时不断调整导管的长度,仔细观察心电监护波形,当P波高度达到QRS波高度的1/2及以上时,确定导管置入长度,剪去多余导管;⑤按照标准程序连接导管与输液港港体,确认连接牢固后将输液港港座放入囊袋中,确认港体平整,导管在皮下走行自然。用蝶翼针经皮垂直穿刺输液港座回抽见暗红色静脉血后用25 U/mL的肝素生理盐水正压封管;⑥可吸收缝线皮内缝合胸壁切口(见图2),表面以生物胶水覆盖;⑦无菌纱布覆盖切口后,至放射科拍摄胸部正侧位片明确导管尖端位置并排除有无血、气胸的发生。

图 1 导丝进入上腔静脉(三箭头所指为导丝)
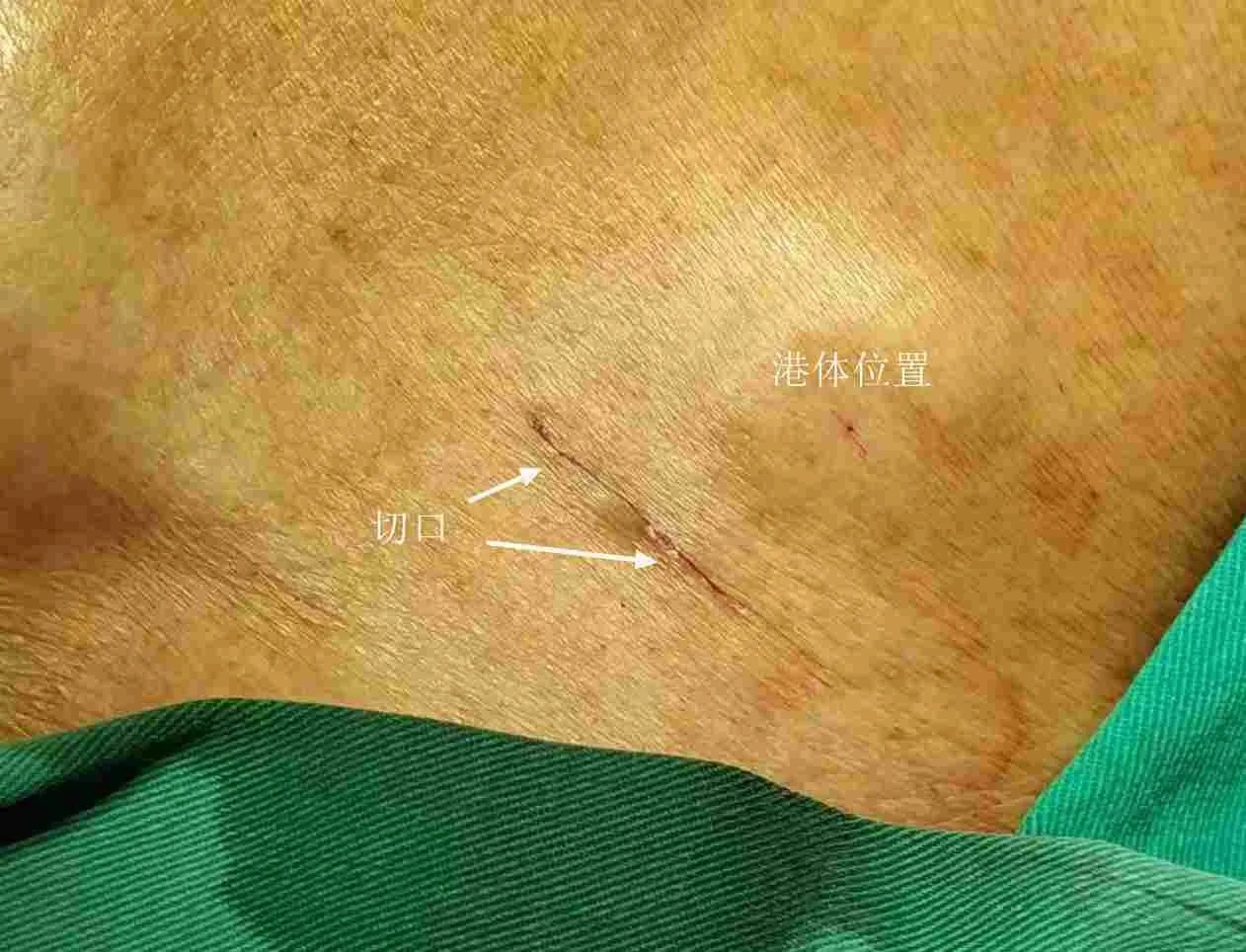
图 2 缝合后切口与港体位置
颈内静脉入路组操作方法与上述步骤相似,区别如下:步骤①需在颈内静脉穿刺点与囊袋之间沿麻醉一条皮下隧道;步骤②需要另外在颈内静脉穿刺点作一长约0.5 cm的切口;步骤⑤需通过隧道针将导管从颈内静脉穿刺点沿皮下隧道牵引至囊袋位置后,再按照标准程序连接导管与输液港港体。步骤⑥颈内穿刺点可不缝合,直接以生物胶水粘合伤口。
1.3 观察指标 ①手术指标:包括手术时间、穿刺针数。②术后疼痛情况:采用视觉模拟评分法(VAS)评分标准评估患者术后疼痛情况[4]:总分为0~10分,0分为不痛,10分为剧痛,评分越高疼痛程度越严重。③并发症发生情况:并发症包括感染、血栓、夹闭、导管打折、动脉误穿、血气胸,并发症发生率=并发症发生例数/总例数×100%。
1.4 统计学分析 采用SPSS 22.0软件进行数据分析。计量资料以(±s)表示,采用方差分析,组间比较采用LSD-t检验;计数资料以[例(%)]表示,组间比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 3组患者手术指标比较 腋静脉入路及锁骨下静脉入路组患者的手术时间相比,二者之间无统计学差异(P>0.05),但均短于颈内静脉入路组的手术时间,差异有统计学意义(P<0.05);腋静脉入路及锁骨下静脉入路组患者的平均穿刺针数相比,二者之间无统计学差异(P>0.05),但均多于颈内静脉入路组,差异有统计学意义(P<0.05),见表1。
表1 3组患者手术指标比较(±s)
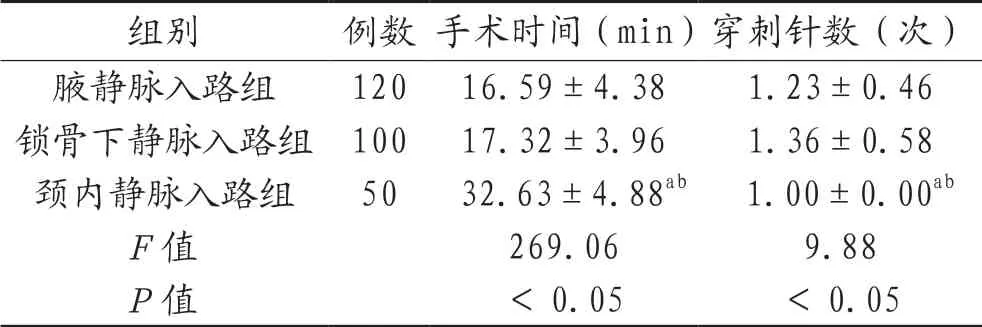
表1 3组患者手术指标比较(±s)
注:与腋静脉入路组比较,aP<0.05;与锁骨下静脉入路组比较,bP<0.05。
组别 例数 手术时间(min)穿刺针数(次)腋静脉入路组 120 16.59±4.38 1.23±0.46锁骨下静脉入路组 100 17.32±3.96 1.36±0.58颈内静脉入路组 50 32.63±4.88ab 1.00±0.00ab F值 269.06 9.88 P值 <0.05 <0.05
2.2 3组患者术后疼痛评分比较 腋静脉入路及锁骨下静脉入路组患者的术后疼痛评分比较,术后1 d及术后10 d,二者之间均无统计学差异(P>0.05),但均低于颈内静脉入路组的术后疼痛评分,差异有统计学意义(P<0.05);随着时间的延长,3种入路方式的疼痛评分均降低,术后1个月,三者之间的差异无统计学意义(P>0.05),见表2。
表2 3组患者术后疼痛评分比较(±s,分)

表2 3组患者术后疼痛评分比较(±s,分)
注:与腋静脉入路组比较,aP<0.05;与锁骨下静脉入路组比较,bP<0.05。
组别 例数 术后1 d 术后10 d 术后1个月腋静脉入路组 120 2.09±0.63 0.45±0.37 0.25±0.39锁骨下静脉入路组 100 2.16±0.75 0.48±0.41 0.24±0.42颈内静脉入路组 50 3.56±0.89ab 0.76±0.56ab 0.38±0.45 F组间,P组间 101.83,<0.05 F时间,P时间 802.84,<0.05 F交互,P交互 31.35,<0.05
2.3 3组患者术后并发症发生情况比较 腋静脉入路组术后并发症发生率低于锁骨下静脉入路组与颈内静脉入路组,差异有统计学意义(P<0.05),见表3。

表3 3组患者术后并发症发生情况比较[例(%)]
3 讨论
对于癌症病人,尤其是晚期癌症病人,静脉化疗与静脉营养支持是主要的治疗手段,但长期反复的穿刺、化疗药物刺激、药物外渗等常常会导致静脉炎,局部组织坏死的发生率也显著增加,加重了患者痛苦[5]。PORT是完全植入皮下的静脉输液装置,特别适用于需要长期反复输液的病人[6]。通过手术方式的改良,为患者提供一条长期、安全、稳定的静脉通路是本研究的主要目的。
目前,输液港港体的植入部位主要位于锁骨下窝胸壁,临床常用的穿刺入路包括颈内静脉和锁骨下静脉两种,腋静脉入路的手术方式鲜见报道。传统的两种入路术式各有其劣势:颈内静脉入路术式由于港体与穿刺点相距较远,需要打一条皮下隧道,且穿刺点需切开皮肤,增加了一个伤口;锁骨下静脉位置相对较深,穿刺难度大,其常见并发症包括气胸、血胸、误穿动脉、心律失常等[7]。腋静脉是锁骨下静脉向外的自然延续,走行于胸廓外,穿刺不易伤及胸膜及肺尖,减少了血气胸的发生率。尤其是胸小肌上缘至第一肋外侧缘的腋静脉第三段,由于表面只有胸大肌筋膜,位置相对表浅,是相对理想的穿刺入路。本研究结果显示:相对于颈内静脉入路术式,腋静脉入路术式导管植入路径更短,不需绕行,术后并发症更少。由于需要处理的手术切口只有一个,所以手术时间更短,患者术中及术后的疼痛感较低,舒适度明显提高。相对于锁骨下静脉入路术式,腋静脉入路术式由于穿刺位置更靠近外侧,所以穿刺路径更短,且穿刺时无第一肋骨和锁骨的干扰,超声图像更清晰,所以穿刺针数更少,患者术中及术后的疼痛感较轻。
综上所述,超声引导下腋静脉穿刺入路静脉输液港植入术是一种安全、便捷、损伤小、痛苦小的静脉输液港术式,为目前较为可靠的静脉输液港植入术式,值得临床推广应用。

