Ba(NO3)2 预处理对高放废液玻璃固化过程中硫酸盐分相的影响
吴 浪,徐立国,雷 杰,王 宾,滕元成
1.西南科技大学 材料科学与工程学院,四川 绵阳 621010;2.中核四川环保工程有限责任公司,四川 广元 610006
高放废液主要来自乏燃料后处理工艺中铀钚共去污循环产生的萃余液,具有化学成分复杂、放射性水平高、生物毒性大等特点,其安全处理与处置已成为影响核工业可持续发展的关键因素之一[1]。玻璃固化是目前国际上唯一工业应用的高放废液处理方法[2]。硼硅酸盐玻璃是世界各国固化高放废液的首选基材。我国现存高放废液的特点是硫和钠含量较高[3],而硫酸盐在硼硅酸盐玻璃中的溶解度较低(w(SO3)≤1%)[4],用硼硅酸盐玻璃固化含硫高放废液时通常会遇到“黄相”问题[2-9],即在玻璃熔制过程中产生分离的黄色第二相(主要成分为碱金属和碱土金属硫酸盐、钼酸盐、铬酸盐等)。黄相易溶于水,且含有一定量90Sr、137Cs等核素,玻璃固化体在深地质处置后一旦受到地下水侵蚀,将严重危害其包容和隔离核素的作用。近年来,国内外学者通过优化基础玻璃配方,或采用鼓泡、机械搅拌等措施可在一定程度上提高玻璃对硫酸盐的包容能力[2-8],但其提高能力有限,当废物包容量偏高或随着运行时间延长,在玻璃固化过程中很难避免黄相的产生。
在含硫的矿物中,以重晶石(BaSO4)矿物的化学稳定性和热稳定性为最高[10]。BaSO4的溶度积常数Ksp=1.08×10-10(25 ℃),其熔点高达1 580℃,Stern等[11]通过热力学计算,发现BaSO4在熔化时均不发生显著分解。美国汉福特处理厂从高放废液分离出的低放废液中,含量较高,在玻璃固化过程中的存在会对99Tc核素包容进入玻璃中产生不利影响[12-13]。最近,美国太平洋西北国家实验室Johnson等[14]提出采用一种Ba-Sn无机纳米复合材料对低放废液进行预处理,主要产物为BaSO4和BaCrO4,低放废液中54%~66%的可被固定在BaSO4晶体中。
本工作拟采用Ba(NO3)2溶液对模拟高硫高钠高放废液进行预处理,再利用熔融法制备硼硅酸盐玻璃固化体。着重研究预处理对玻璃固化过程中硫酸盐分相行为的影响,以期对高放废液玻璃固化过程中解决“黄相”问题提供技术支撑。我国采用焦耳加热陶瓷熔炉玻璃固化技术,熔炉的废液进料管连接有一根去离子水管,因此在工程规模运行时,可从去离子水管加入适量Ba(NO3)2溶液与高放废液进行反应。
1 实验部分
1.1 试剂和仪器
SiO2、H3BO3、Na2CO3、Li2CO3、CaCO3、Al2O3、MgO、TiO2、Na2SO4、Fe2O3、La2O3、Nd2O3、CeO2、NiO、Zr O2均为分析纯,国药集团化学试剂有限公司;NaNO3、Ba(NO3)2、MnO2、Na2MoO4·2H2O、Cr2O3、HNO3均为分析纯,成都市科龙化工试剂厂产品;Cs2CO3、Pr N3O9·6H2O,纯度≥99%,麦克林公司;H12N2O14U,纯度≥99%,湖北楚盛化工有限公司。模拟高放废液中SO3以Na2SO4形式引入,Na2O 以Na NO3形式引入。
TCF-8-16型陶瓷纤维高温炉,上海和羽良电子科技有限公司;101-1EBS型电热恒温鼓风干燥箱,北京市永光明医疗仪器厂;X'Pert PRO 型X射线衍射分析仪、Axios型X 射线荧光光谱仪,荷兰帕纳科公司;TM-4000 型背散射扫描电镜,日本日立公司。
1.2 样品制备
本实验所用硼硅酸盐基础玻璃配方和模拟高放废液组成分别列于表1和表2。该玻璃配方经过冷台架运行试验发现玻璃固化体表面存在较多的黄相[9],因此用其进行研究具有一定的代表性。根据表1玻璃氧化物组成称取原料,在研钵充分混合均匀后将样品放于刚玉坩埚中,置于马弗炉中熔制,以5 ℃/min 的升温速率从室温升至750 ℃,在750 ℃下煅烧2 h使碳酸盐分解。再以3 ℃/min 的升温速率升温至1 200 ℃,在1 200 ℃下保温2 h熔制玻璃,然后将玻璃熔体水淬,研磨获得玻璃粉。根据表2模拟高放废液组成称取原料放入烧杯中,将适量2.5 mol/L 的HNO3溶液倒入烧杯中,在磁力搅拌器上搅拌使其充分溶解。再将适量Ba(NO3)2(Ba2+和摩尔比为1∶1)溶液倒入模拟高放废液中,使其充分反应后,再置于105 ℃的烘箱中烘干,研磨混合均匀待用。按照硼硅酸盐基础玻璃w=84%和模拟高放废液氧化物w=16%的配比称量,在研钵中混合均匀后放于刚玉坩埚中,置于马弗炉中在不同温度下(850~1 150 ℃)保温约30 min后取出熔制样品观察物料熔制及分相情况,获得玻璃固化体样品。

表1 硼硅酸盐基础玻璃组成Table 1 Compositions of borosilicate base glass
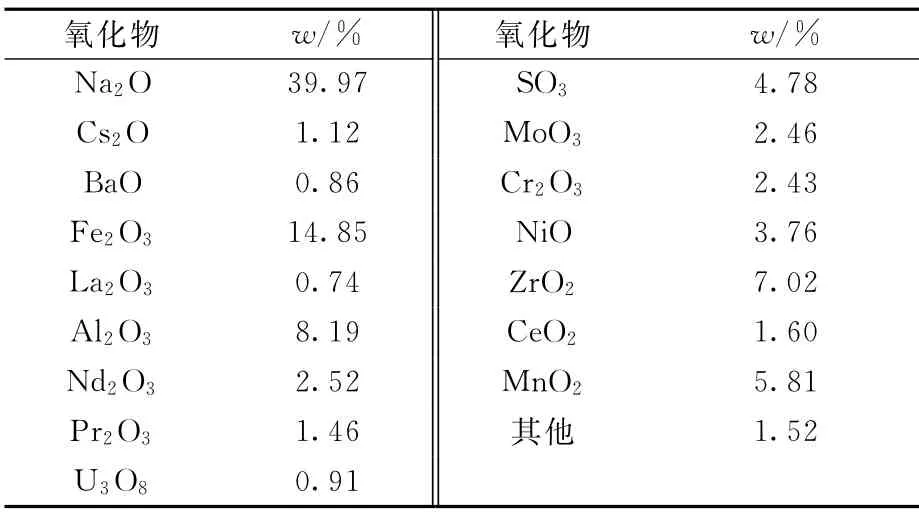
表2 模拟高硫高钠高放废液组成Table 2 Compositions of simulated HLLW with high content of sulfur and sodium
1.3 测试与表征
用X 射线衍射分析仪分析样品的物相组成,条件:λ=1.541 8Å(1Å=0.1 nm),Cu靶Kα。利用扫描电镜结合能谱分析仪观察样品的背散射图像并进行成分分析。用X 射线荧光光谱仪测试玻璃固化体样品的硫含量。
2 结果与讨论
2.1 预处理前后模拟高放废液样品的物相组成
图1为模拟高放废液预处理前后经过烘干后粉体的XRD图谱。由图1可知,预处理前后模拟高放废液样品的主要物相均为NaNO3(PDF#89-0310),还含有少量Fe2O3(PDF#87-1166)和ZrO2(PDF#65-1022)。其中模拟高放废液预处理后的样品还出现了BaSO4(PDF#89-3749)相。由于硼硅酸盐基础玻璃中不含BaO,模拟高放废液中SO2-4是以Na2SO4形式引入,因而预处理样品中的BaSO4可认为是由Ba(NO3)2与模拟高放废液中的在酸性环境(2.5 mol/L HNO3)反应生成,表明了模拟高放废液中的硫元素可被固定在BaSO4中。
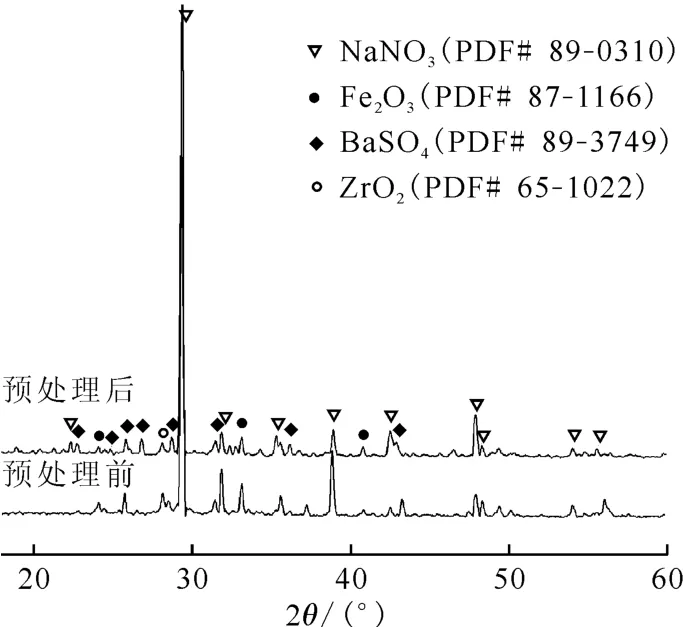
图1 预处理前后模拟高放废液烘干粉体的XRD 图Fig.1 XRD patterns of dried powders of simulated HLLW before and after pretreatment
2.2 预处理对黄相生成的影响
图2为预处理前后玻璃固化体在熔制过程中不同温度取出的样品的外观照片。由图2可知:当熔制温度为850℃时,黄相便已开始形成,因其比重较轻而漂浮在玻璃熔体表面,随着温度进一步升高,黄相的量先增多后减少,在1 150 ℃时黄相完全消失,该现象与刘丽君等[9]的研究结果一致。值得注意的是,与未经预处理的样品相比,预处理后黄相的量显著减少,表明采用Ba(NO3)2对模拟高放废液进行预处理,将废液中的硫先固定在稳定的BaSO4中,再进行玻璃固化,可有效抑制黄相的产生。这可能是由于BaSO4在硼硅酸盐玻璃熔体中比Na2SO4具有较好的热稳定性[15],硫元素以BaSO4形式引入可提高硼硅酸盐玻璃对硫酸盐的包容量。

图2 预处理前后玻璃固化体熔制过程中不同温度下取出的样品外观照片Fig.2 Appearance of samples before and after pretreatment at different temperatures during vitrification process
图3为预处理前后1 050 ℃下产生黄相样品的XRD 图谱。由图3可以看出,预处理前黄相的主要物相为Na2SO4(PDF#74-2036)和LiNaSO4(PDF#20-0638),还含有少量的CaMoO4(PDF#85-1267)、Cr2(MoO4)3(PDF#20-0309)和Na2Cr MoO4(PDF#28-1076)。预处理后主要物相为Na2SO4,LiNaSO4相的衍射峰有所减弱,Ca MoO4相的衍射峰明显增强,此外还出现了BaSO4(PDF#76-0216)、BaMoO4(PDF#29-0193)和BaCrO4(PDF#72-0747)相。这可能是由于BaSO4在高温下溶解在硼硅酸盐玻璃熔体中后,一部分Ba2+与和结合生成了BaCr O4和Ba MoO4。按照Ba2+和摩尔比为1∶1加入Ba(NO3)2,多余的与Na+结合生成Na2SO4,因而本研究中预处理后的黄相中Na2SO4含量仍然较高。上述结果表明了采用Ba(NO3)2对模拟高放废液预处理引入Ba2+可使黄相中的碱土金属硫酸盐、钼酸盐和铬酸盐含量增加。
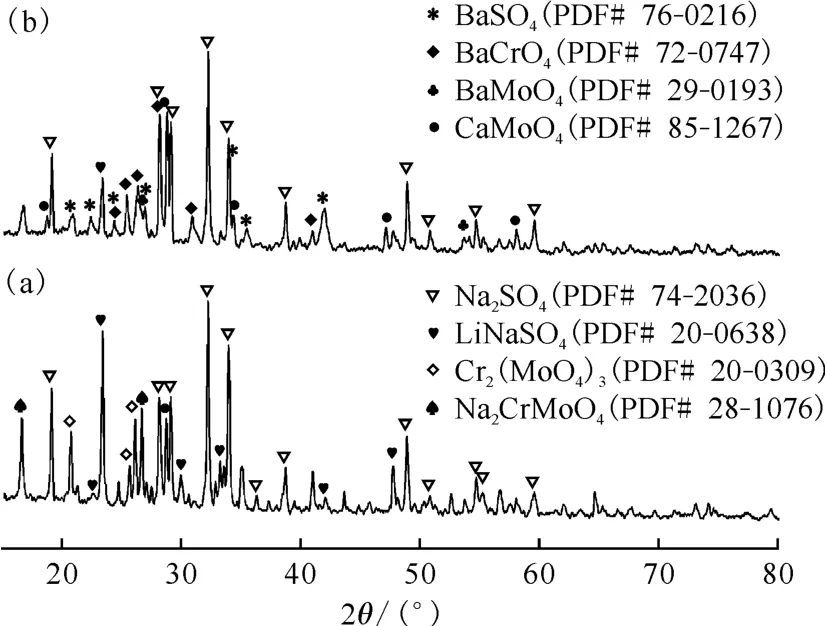
图3 预处理前(a)后(b)黄相的XRD 图谱Fig.3 XRD patterns of yellow phase before(a)and after(b)pretreatment
2.3 样品的显微结构
图4是预处理前后玻璃固化体熔制过程中所产生黄相的背散射扫描电镜(BSE)照片和X 射线能谱分析(EDX)图谱,表3列出了A、B、C点能谱分析的元素含量。从图4(a)可以看出,从模拟高放废液未经预处理在玻璃固化过程中产生的黄相中主要观察到了明暗二种晶体,结合能谱分析和XRD 分析结果可知,较暗的晶体呈方块状,对应Na2SO4晶体(A 点),较亮的晶体呈不规则块状集合体,对应Ca MoO4晶体(B 点)。模拟高放废液经过预处理后在玻璃固化过程中所产生的黄相除了观察到上述Na2SO4和Ca MoO4两种晶体之外,还观察到了一种更亮的白色晶体,经过能谱分析,可能是由BaSO4、BaCr O4和Ba MoO4的混合物组成,与黄相的XRD 分析结果保持一致。由于BaSO4在硼硅酸盐玻璃熔体中比Na2SO4具有较好的热稳定性[15],因此BaSO4的生成有利于抑制硫在高温下的挥发。印度Kaushik等[6]采用钡硼硅酸盐玻璃(Na2O-BaO-B2O3-SiO2)固化模拟含硫高放废液,产生的黄相主要物相为Na2SO4、BaSO4、Na2Cr O4和BaCr O4,而Short[16]报道硼硅酸盐玻璃固化英国高放废液所产生黄相的主要物相为LiNd Mo2O8、LixNayCszMoO4和BaxSryMoO4等。黄相成分有所差异的原因可能主要是由于基础玻璃和高放废液成分不同所致。
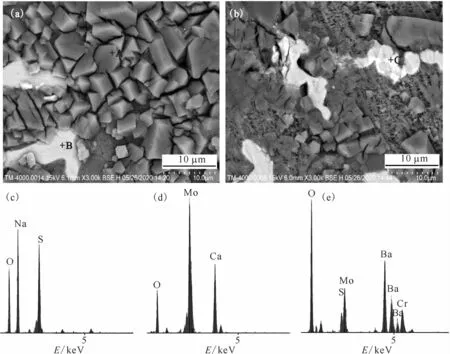
图4 玻璃固化体熔制过程中所产生黄相的BSE照片Fig.4 BSE micrographs of yellow phase samples

表3 黄相样品中几种晶体能谱分析的元素含量Table 3 Element contents of several crystals of yellow phase samples by EDX analysis
2.4 样品的硫含量
表4为预处理前后玻璃固化体在熔制过程中不同温度取出样品的硫含量。由表4可知:对于模拟高放废液未经预处理的样品,在850 ℃时样品内部硫含量(质量分数,以SO3计)约为0.80%,因部分硫从玻璃熔体中分离出来进入黄相中,此时样品内部的硫含量约占原始加入量的84%;随着温度进一步升高,从玻璃熔体中分离出来进入黄相中的硫含量逐渐增多,同时玻璃和黄相中的硫酸盐也会分解挥发,玻璃体中的硫含量逐渐降低,当温度达到1 150 ℃时,w(SO3)=0.62%;对于预处理后的样品,在850~1 050 ℃,硫含量基本保持不变(≈0.80%),随着温度进一步升高,硫含量逐渐降低。表明了将模拟高放废液中的硫元素先固定在BaSO4中,再制备硼硅酸盐玻璃固化体,在熔制温度不高于1 050 ℃时可有效提高硫酸盐的包容量。从表4还可以看出,预处理对提高玻璃固化体中硫酸盐包容量效果不明显,这可能是由于本研究中硫酸盐原始添加量不高(w(SO3)≈0.96%)。当模拟高放废液(表2)中分别添加过量2%(质量分数,以SO3计)Na2SO4和BaSO4时,在1 050 ℃熔制的样品中SO3质量分数分别为0.96%和1.33%,在1 150 ℃熔制的样品中SO3含量有所降低,分别为0.89%和1.16%。在之前的研究工作中[15],通过在硼硅酸盐玻璃中分别掺入4%(以SO3计)Na2SO4和BaSO4,在1 150 ℃熔制的样品中SO3含量分别为0.97%和1.88%。上述结果表明了当废物中硫酸盐含量较高(如w(SO3)>1%)时,预处理对提高硫酸盐的包容能力尤为显著。王孝强等[7]在基础玻璃中添加BaO 也可提高硫酸盐的包容能力,特别是废物中硫酸盐含量越高,提高越显著。
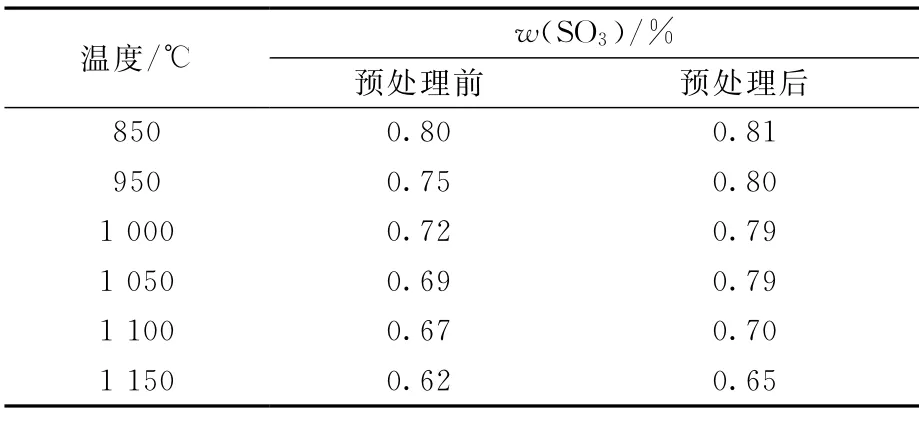
表4 预处理前后玻璃固化体熔制过程中不同温度下取出样品的硫含量Table 4 Sulfur contents of samples at different temperatures during vitrification process before and after pretreatment
3 结论
采用Ba(NO3)2对模拟高硫高钠高放废液进行预处理,对比研究了预处理前后玻璃固化体熔制过程中产生黄相的影响,并分析了黄相的物相组成、显微结构以及玻璃固化体中的硫含量。主要结论如下:
(1)采用Ba(NO3)2对模拟高硫高钠高放废液进行预处理,生成了较为稳定的BaSO4,在玻璃固化体熔制过程中黄相的量显著减少;
(2)预处理后产生的黄相中LiNaSO4相衍射峰有所减弱,Ca MoO4相衍射峰明显增强,还出现了BaSO4、Ba MoO4和BaCr O4相;
(3)预处理前玻璃固化体中的硫含量随温度升高逐渐降低,预处理后玻璃固化体中的硫含量在850~1 050 ℃温度范围内基本保持不变,随着温度进一步升高,硫含量逐渐降低;当废物中硫酸盐含量较高时,预处理对提高硫酸盐的包容能力尤为显著。

