泡沫化聚桂醇灌注治疗体表血管瘤的临床观察
吴永芳,王运成,陆美林,熊庭锋
(1.广西百色市人民医院整形美容外科,广西 百色,533000;2.九江学院附属医院整形美容科,江西 九江,332000)
以往研究表明硬化疗法用于治疗血管瘤并取得良好的效果,已被证明是血管瘤的一种治疗方法,尤其是在手术治疗不能完全切除或损伤太严重的情况下[1]。使用的硬化剂包括Polidocanol(聚乙二醇单十二醚)、油酸乙醇胺、十四烷基硫酸钠(odium tetradecyl sulfate,STDS)和乙醇等。STDS和Polidocanol是世界上应用最广泛的两种硬化剂[2],其中Polidocanol是已经被批准用于硬化治疗的药物,并在欧洲广泛使用[2],适用于静脉曲张、食管静脉曲张、血管畸形、血管瘤、内痔、囊性疾病等。直接向血管内注射液体或泡沫剂会刺激内皮细胞损伤靶血管,进而促使局部血栓形成,受损的静脉最终转化为纤维束,无法再通导致病理血管永久闭塞,最终导致瘤体的自发消退。Polidocanol的安全性已被国际医学界公认[3],但国内难以购买使用,国产聚桂醇化学成分与Polidocanol相同[4]。我院整形美容外科于2018年7月到2019年9月采用泡沫化聚桂醇灌注治疗体表血管瘤患者27例,疗效满意,现报告如下。
1 资料和方法
1.1 一般资料
我们随访6个月,共有27例体表血管瘤患者被纳入研究。收集患者年龄、性别、发病部位、治疗前后血管瘤大小、及并发症情况等,27例患者年龄从2个月到16月不等,年龄中位数为5个月,其中男性14例,女性13例。瘤体浸润皮肤呈紫红色包块,大小从0.4cm×0.6cm到5.6cm×4.7cm不等。病变部位:面部23例,四肢躯干部4例。所有患者均为单发,并都使用泡沫化聚桂醇灌注治疗,如瘤体位于体表深部,则需要B超引导穿刺灌注。
1.2 适应证
体表部位发生血管瘤患者,并排除动静脉瘘、合并感染破溃者、伴凝血功能异常者、伴严重心肺疾患等。超声引导下药物灌注治疗适用于皮下深部血管瘤。
1.3 手术方法
所有患者治疗前均进行详尽的医患沟通,并签署手术同意书。穿刺点选择:距离瘤体1cm处。先后使用碘酊、酒精消毒皮肤,常规铺巾。制备灌注液:一支20ml注射器抽吸5ml聚桂醇、另一支20ml注射器抽吸10ml空气,通过三通管反复10次混合,充分混匀发泡。表浅者:戴无菌手套后用左手捏住并提起瘤体,将其固定,右手持穿刺针(头皮针)经穿刺点刺入皮肤、皮下组织进入瘤体内,见回血后助手连接注射器与头皮针缓慢将发泡液注入瘤体内直至瘤体肿胀、皮肤发白,拔出穿刺针,纱布压迫穿刺点,包扎固定,余液丢弃。瘤体位于皮下深部者:同法消毒铺巾及制备灌注液。无菌薄膜袋包裹B超探头,超声引导下将穿刺针经穿刺点刺入皮肤、皮下组织进入瘤体内。B超直视下将发泡液缓慢注入瘤体内,当药物浸润整个瘤体内后拔出穿刺针,棉签压迫穿刺点后消毒、纱布包扎,余液丢弃。如瘤体位于肢体,则予绷带加压包扎。术后24小时更换纱布,如无出血,肢体处则需继续加压包扎24小时,而颜面部、躯干处则无须继续包扎。注意有无发热、呼吸困难、皮肤糜烂等情况,做好对症治疗。
1.4 评价标准
本研究的疗效的主要观察指标是肿瘤大小,随后我们记录症状改善情况,来对目标病灶进行疗效评价,并采用实体瘤反应性评价标准(Response evaluation criteria in solid tumors,RECIST)作为评价标准。完全缓解(complete response,CR)为所有靶病灶消失,无新病灶出现;部分缓解(partial response,PR)为靶病灶最大径之和减少≥30%;疾病稳定(stable disease,SD)为靶病灶最大径之和缩小未达 PR,或增大未达 PD;疾病进展(progression disease,PD)为靶病灶最大径之和至少增加≥20%,出现新病变也视为PD。CR及PR认为治疗有效,有效率=[(CR 例数PR 例数)/总例数]×100%[5-7]。计量资料用均数标准差反应。
2 结果
本组27例患者治疗前最大径之和为(4.33±2.53)cm,最小为1.0cm,最大值为10.3 cm,治疗后最大径之和为(0.941.55)cm,最小为0 cm,最大值为7.2 cm(表1)。
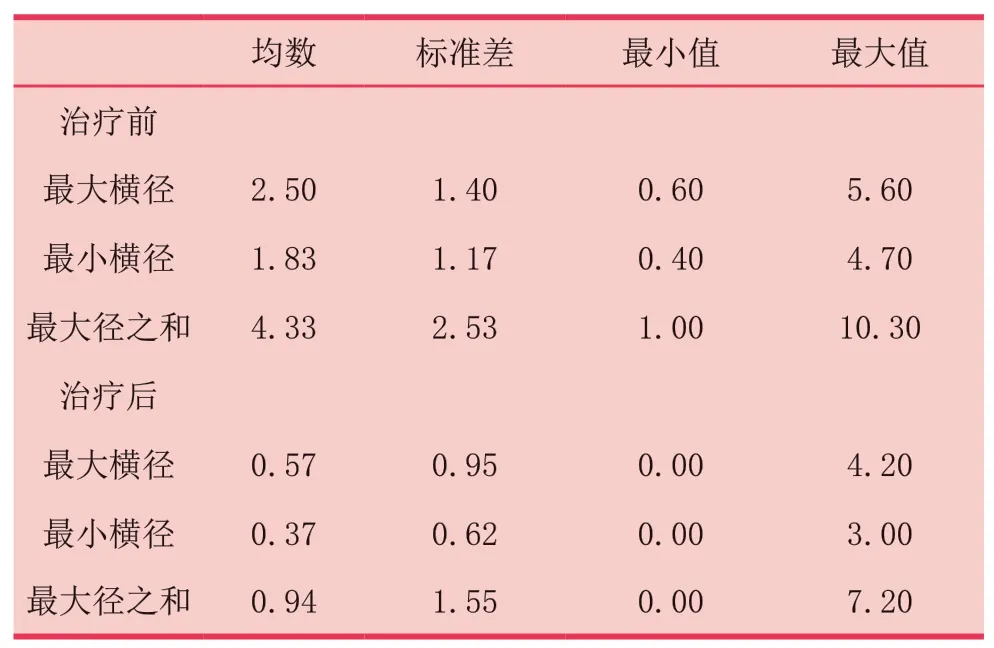
表1 治疗前后血管瘤大小(cm)
完全缓解患者15人(55.56%),部分缓解11人(40.74%),疾病稳定1人(3.70%),疾病进展0人,有效率26人(96.30%)。
所有患者均未出现严重并发症,出现轻微并发症者4人,其中一例诱发哮喘,对症治疗后恢复,1例发热(38.2℃),观察治疗后恢复正常。2例皮肤糜烂,换药后治愈。术后效果良好。典型案例见图1。
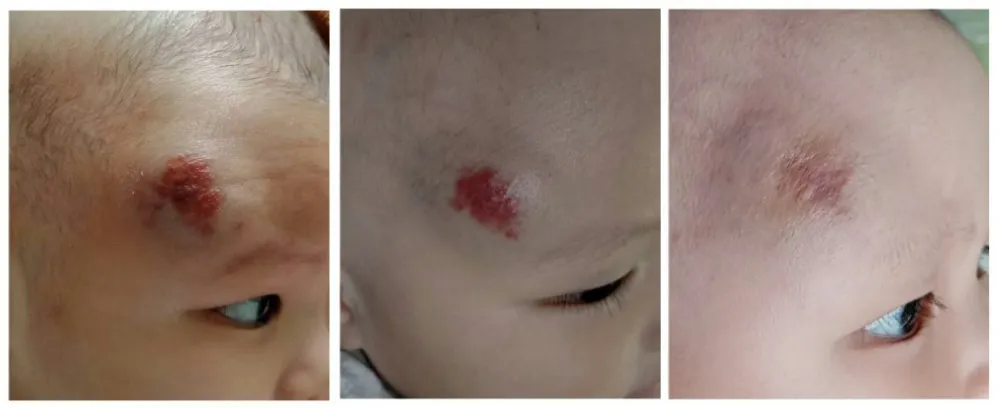
图1 泡沫化聚桂醇灌注治疗体表血管瘤术前术后对比a.术前额部瘤体明显隆起,皮肤呈紫红色;b.术后4 个月瘤体缩小、颜色变淡;c.术后6 个月额部肿物消失,皮肤有色沉,但无紫红色病变
3 讨论
传统的“血管瘤”分类可分为血管瘤和血管畸形。血管瘤以内皮细胞增生为特征的良性肿瘤,而血管畸形是血管形态出现异常的疾病[5]。当前治疗血管瘤的治疗方法主要有保守观察、激光治疗、手术治疗和药物治疗等。激光治疗血管瘤有一定效果,但对于较深部的血管瘤效果很差[6]。手术常常作为血管瘤治疗的主要方法,尤其是对小的局限性病变,但手术切除常常伴随着一些风险,例如切除不彻底、术中出血、切口瘢痕形成等,以及由于病变在邻近重要解剖结构中(眼睑、乳头、肛门等)浸润和扩张,手术治疗并不总是可行的选择。自2008年[7]以来口服普萘洛尔已经成为常见治疗药物,然而尽管其治疗效果值得肯定,但存在一定的缺陷,如需要较长时间的服药和一些并发症的产生,如睡眠障碍、腹泻、毛细支气管炎、低血糖、低血压等[8,9]。局部使用普萘洛尔也能够治疗血管瘤,但其主要适用于小的或表面的患者[10]。
硬化疗法具有低毒、低过敏反应、高效、微创、使用方便等优点,在治疗血管瘤中得到了广泛的应用[11]。我们团队把泡沫化聚桂醇灌注治疗作为婴幼儿血管瘤的首选治疗方案。选择头皮针或者长细针进行穿刺常无须麻醉,避免因局部麻醉引起组织肿胀而干扰穿刺,也避免全身麻醉增加麻醉意外风险及增加住院费用等。刺入瘤体后常有回血或者借助B超定位,可以达到精准治疗,不会因为药液外渗引起局部组织萎缩。为增加药物与瘤体接触时间,我们采用大于瘤体直径的环形塑料圈压迫瘤体周边正常皮肤、组织,压迫时间常为5分钟,但该做法是否有效及压迫时间需要进一步研究、验证。硬化治疗的预期并发症包括色素沉着、短暂的灼痛、毛细血管扩张、皮肤坏死、溃疡、血栓性静脉炎、肺栓塞等[11],但多见于治疗静脉曲张和痔疮[12]。而对于体表血管瘤治疗最常见的并发症是瘢痕的形成,在本研究中均未见明显瘢痕形成。其中Propranolol是最常用的治疗血管瘤硬化剂之一,Propranolol是一种合成的脂肪醇,由95%的羟基聚氧十二烷和5%的乙醇组成[13-14],是1931年首次被开发出来,最初用作局部麻醉剂,后发现其可用于硬化疗法治疗血管瘤,其作用机理是可能与细胞钙信号通路和一氧化氮途径激活引起的细胞损伤有关。血管内注射Propranolol可直接损伤血管内皮,进而引起血栓形成。然后产生炎性病变和组织纤维化,导致病理血管永久闭塞,从而达到硬化的目的[15]。
血管瘤的特点是在增殖周期迅速扩张,然后缓慢退化。HMs病理过程包括三个阶段:第一阶段为增殖阶段,HMs迅速增长。增殖期之后是稳定期,肿瘤生长缓慢,血管明显。最后HMs进入退化期,纤维脂肪组织最终取代肿瘤。部分血管瘤能够自行退化,30%的婴幼儿血管瘤在患者3岁时自发消退,50%在5岁时消退,70%至90%在7岁时消退,90%在9岁前完成退化[16]。血管瘤的临床表现因血管增生部位的不同而不同。并发症虽然很少见,但也可能发生如溃疡、外伤后的出血等,因此早期积极的治疗血管瘤仍具有意义。我们采用国产的Propranolol(聚桂醇)治疗血管瘤,结果显示具有较好的有效率,达96.30%,术后并发症较轻且均得到痊愈,因此我们认为泡沫化聚桂醇灌注治疗血管瘤是安全有效的。

