完全腹腔镜全胃切除食管空肠手工吻合280例报告*
周连帮 方 征 张迎峰 蒋 恒
(安徽医科大学第二附属医院胃肠外科,合肥 230601)
针对能够切除的胃癌,根治切除术仍然是治愈疾病的唯一可能途径。Kitanov等1994年报道胃癌腹腔镜辅助远端胃切除术[1],此后胃癌的外科治疗步入了腹腔镜时代,1999年Uyama等报道腹腔镜全胃切除术[2]。我国由李国新领衔的多中心随机对照试验CLASS-01研究明确了腹腔镜手术治疗进展期胃癌围手术期的安全性和可行性[3]。全腔镜胃癌手术在我国多个中心已经广泛开展,大多数消化道重建方式为Overlap、π吻合。目前采用腹腔镜下线型吻合器吻合较多,但对于胃食管结合部肿瘤,线型吻合要求更高的食管长度,部分患者可能需要经胸腔吻合。手工吻合采用食管空肠端侧吻合,对食管长度要求低且更经济,倒刺线为可吸收线更利于组织愈合。2016年11月~2020年2月,我们在280例根治性全胃切除术中采用完全腹腔镜下食管空肠手工吻合,报道如下。
1 临床资料与方法
1.1 一般资料
本组280例,男158例,女122例。年龄33~75岁,平均60岁。BMI 20~29,22.5±3.8。上腹部疼痛102例,黑便36例,呕血10例,进食哽噎感98例,无症状34例。均行胃镜检查,肿瘤位于胃体64例,贲门216例,胃镜下肿瘤长径1.5~7 cm,(2.3±4.2)cm。活检病理:腺癌268例,包括高分化腺癌2例,中分化腺癌82例,低分化腺癌104例,黏液腺癌56例,印戒细胞癌24例;神经内分泌癌12例。术前分期cT2~4 N0~1 M0期。腹部增强CT和胸部X线检查未发现腹腔、肝、肺等转移。高血压病史132例,糖尿病史56例,冠心病史5例。术前贫血162例,血红蛋白42~105 g/L(正常值:>120 g/L);低蛋白血症56例,白蛋白25~34 g/L(正常值:35~55 g/L)。ASA分级Ⅰ级50例,Ⅱ级203例,Ⅲ级27例。
纳入标准:胃镜、活检病理和消化道钡剂造影确诊为胃中上部癌,术前肿瘤分期cT2~4 N0~1 M0期。
排除标准:重要器官功能不全,有手术禁忌证;合并其他恶性肿瘤;临床和随访资料不完整。
1.2 手术方法
仰卧位,双腿分开,常规建立气腹,CO2压力15 mm Hg。观察孔为脐下缘10 mm trocar,主操作孔为右侧腹12 mm trocar,辅助操作孔分别为左、右肋缘下方和左侧腹5 mm trocar。探查腹盆腔,定位肿瘤,行全胃切除及D2淋巴结清扫。
消化道重建:常规悬吊肝左外叶,再次充分游离食管长度5 cm左右,1-0丝线结扎远端食管,超声刀离断食管下段,于脐下做2~3 cm切口取出全胃标本,检查肿瘤位置及切缘。重新建立气腹,距屈氏韧带25 cm处空肠提至食管下方,在空肠对系膜侧肠壁用超声刀切开2.5 cm,3-0倒刺线从吻合口左侧向右侧全层连续缝合后壁6~8针,放入空肠营养管及胃管通过食管空肠吻合口下方25 cm,用另一根倒刺线缝合前壁6~8针,在两根缝合线线尾交汇处打结,完成食管空肠端侧吻合(图1、2),在横膈膜与远端空肠前壁可吸收线缝合2针固定,减少吻合口张力。用腹腔镜下切割封闭器在距屈氏韧带20 cm处切断近端空肠(图3),用切割封闭器在距食管空肠吻合口40 cm处并排侧侧吻合近端空肠和远端空肠(图4),并用3-0倒刺线缝合共同开口(图5)。冲洗腹腔,放置引流管(图6)。
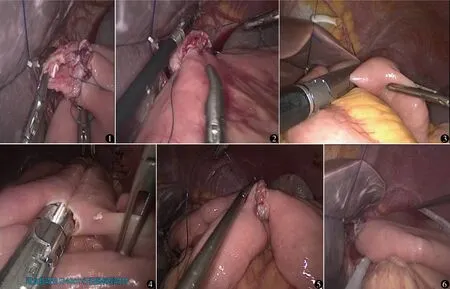
图1 3-0倒刺线食管空肠端侧吻合后壁 图2 食管空肠吻合口前壁 图3 离断距屈氏韧带20 cm处空肠 图4 距空肠吻合口40 cm处与屈氏韧带15 cm处侧侧吻合图5 3-0倒刺线缝合共同开口 图6 冲洗腹腔,放置引流管
1.3 术后处理
术后禁食水,肠外营养,空肠营养管滴入葡萄糖,2~3天排气后拔除胃管并嘱少量饮水,肠内营养支持2天,逐步过渡到流质,5天后拔除空肠营养管,7天后拔除引流管,8天后饮食良好、切口愈合佳及无腹部体征后可以出院。
术后2个月TNM分期Ⅱ期及以上者予以SOX方案(奥沙利铂+替吉奥)辅助化疗6个疗程。第1年每3个月复查一次,第2年每半年复查一次,第3年开始每年复查一次,包括血常规、肝功能、肿瘤标记物及腹盆腔CT检查。
2 结果
280例均完成手术,无中转开腹。手术时间208~292(246±36)min,其中食管空肠吻合时间10~25(18±5)min,术中出血30~65(45±12)ml。无术中并发症。
术后吻合口漏2例,十二指肠残端漏15例,肺部感染5例,腹腔感染3例,均保守治疗痊愈。无术后并发症者术后1~3 d下床活动,2~3 d排气,4~6 d进食流食,5~7 d拔除空肠营养管,7~9 d拔除引流管,术后住院时间7~10 d。
病理学检查:肿瘤直径2.5~6(4.5±1.4)cm;淋巴结16~36(26±8)枚。淋巴结和(或)血管神经浸润185例。T1期50例,T2期87例,T3期103例,T4期40例;N0期86例,N1期135例,N2期42例,N3期17例。TNM Ⅰ期91例,Ⅱ期105例,Ⅲ期84例。
280例随访4~40个月,中位时间11.6月。良性吻合口狭窄5例。肿瘤复发死亡12例,吻合口复发2例,腹腔、远处转移带瘤生存24例,无瘤生存242例。
3 讨论
完全腹腔镜消化道重建是胃癌根治手术的关键难点。虽然辅助切口根治性胃切除手术技术已经健全,但对完全腹腔镜消化道重建依然存在许多需要探讨的地方[4]。完全腹腔镜消化道重建多采用Uncut Roux-en-Y法、OrVil法以及Overlap法等[5,6]。由于对腹腔镜手术操作要求较高以及学习曲线较长,目前食管空肠手工吻合重建的报道较少,大多采用管型吻合器和直线切割闭合器完成食管空肠吻合[7~9]。
本组280例完全腹腔镜手工吻合术后出现吻合口漏2例,通过录像分析,1例因3-0倒刺线较长,缝合时线结切割吻合口的小肠及食管,导致术后针眼漏;另1例在吻合口缝合时连续缝合2针收紧缝线时较快且缝线有交叉引起组织切割,导致吻合口漏。2例吻合口漏引流通畅,肠内营养较为耐受,术后一般情况好转后,予以流质饮食,无腹部不适,21、28天拔除腹腔引流,均保守治疗痊愈。本组吻合口并发症较少,分析原因:①前后壁连续缝合,空肠及食管针边距一般为5 mm,每缝合一针并收紧,缝合组织较为坚实,未出现吻合口出血;②技术与传统外科缝合较为相似,而且高清腔镜放大下缝合更为确切,且使用可吸收缝线,与线性或圆形吻合器不可吸收钉相比,异物少,促进组织愈合,故吻合口漏发生率较低;③空肠处理不裁剪系膜,吻合口空肠血供更佳,保障吻合口血供充沛。
随访中出现吻合口狭窄5例,可能原因:①前后壁连续缝合,易导致术后吻合口瘢痕性狭窄;②术后反流且长时间进食流质饮食,未及时过度到半流质及普食,导致吻合口食物流量较小。吻合口均采用可吸收线缝合,如果出现吻合口狭窄需要扩张也相对较容易,这5例均在胃镜下多次扩张,进食困难或哽噎症状均缓解。
我们食管空肠手工吻合的经验:①游离足够长度的食管下段,至少5 cm左右,尤其对于胃食管结合部肿瘤,在保证手术切缘阴性的同时,必要时可打开膈肌角,充分清扫下纵隔淋巴结;②一般采用食管空肠端侧吻合,优势在于未离断空肠系膜,端侧吻合具有更好的血运,吻合口漏发生率低;③建议采用15 cm长3-0倒刺线,如线较长会加大对吻合口组织的损伤;④食管和空肠黏膜对黏膜手工吻合,针边距控制在5 mm左右,针间距控制在5 mm左右;⑤空肠采取后离断,可以进一步减低吻合口张力,也可以控制空肠盲襻的长度;⑥建议术中常规放置空肠营养管,一般在食管空肠吻合口下方10 cm,营养管拔除时间控制在进食流质后,避免出现吻合口漏进行肠内营养。
由于完全腹腔镜下行人工食管空肠吻合术的难度高,技术要求高,国内外报道少[10~12]。本研究单中心280例完全腹腔镜下全胃切除食管空肠手工吻合,在手术时间、术后恢复、手术切缘及并发症等方面都得到了令人满意的结果,为消化道重建提供一种备选吻合术式。

