基于生物信息学探究名老中医贾跃进治疗失眠症的用药规律和作用机制*
王瑞敏,刘毅,李菲,贾跃进
1 山西中医药大学 山西太原 030024 2 山西中医药大学附属医院 山西太原 030024
失眠症(Insomnia Disorder,ID)是临床常见病和多发病,2002年国际精神卫生和神经学基金会调查显示,我国人群中有45.5%存在睡眠问题;并有调查表明睡眠不足与抑郁症(DD)、肥胖、代谢紊乱、心脏病、精神健康问题和痴呆症有关,且有更多的研究发现在睡眠不足的情况下免疫系统会遭受多种改变,根据调查约有10%~20%的人群会受其影响。[1-2]对于ID的治疗,目前作为一线药物的苯二氮卓类受体激动剂(BzRAs)缺乏长期疗效的证据且与潜在的不良反应有关,因此并非理想手段。[3]相比之下,中医药治疗疾病有效且安全性高,具有一定优势,因此挖掘中医药对ID的治疗具有较大的意义。
贾跃进主任医师是全国名老中医工作室指导老师,从医40余年,对ID、DD等脑病治疗有独到的见解并有丰富的临床经验。本文选取贾老近5年的门诊病例,运用数据挖掘和网络药理学方法对其临床用药和处方特点进行归纳总结,并综合分析其作用机制,以图为ID的治疗及相关研究提供一定思路与 参考。
资料与方法
1 入组标准
1.1 纳入标准 根据《中国成人失眠诊断与治疗指南》[4]诊断明确并单独使用山西中医药大学附属医院中药房提供的中药颗粒剂治疗,且安全、有效的病案。
1.2 排除标准 诊断、效果或安全性不明确的病案;合并其他影响判断的精神及躯体疾病的病案;治疗手段非单独使用上述中药颗粒剂的病案。
2 数据挖掘
2.1 数据收集 收集2015年7月1日-2020年7月1日间贾跃进名老中医在山西中医药大学附属医院治未病中心门诊收治的ID病案。
2.2 数据录入与挖掘 根据纳入和排除标准筛选后,以双人双录入法将病案录入至古今医案云平台V2.2.3中,然后结合2015版中国药典[5]与第七版中药学教材[6]对中药进行名称规范,如:“炒麦芽”统一为“麦芽”、“清半夏”统一为“半夏”。将所获得的医案使用数据挖掘模块对其进行药物频次、属性统计以及关联、聚类和复杂网络分析,并得出核心药组。
3 网络药理学
3.1 核心药组药物活性成分及相关靶点获取 利用CNKI(https://www.cnki.net/)中 的 相 关 文 献 及TCMSP(http://tcmspw.com/tcmsp.php)数据库中检索核心药组各药物活性成分,将所得活性成分在SwissADME(http://www.swissadme.ch/)平台中限定胃肠道吸收(GI absorption)、血脑屏障渗透(BBB permeant)、类药性(Druglikeness)进行筛选,将筛选出的活性成分导入SwissTargetPrediction(http://www.swisstargetprediction.ch/)得出相关靶点,并匹配Uniprot(https://www.uniprot.org/)数据库中的GeneSymbol。
3.2 疾病靶点获取 在Genecards(https://www.genecards.org/)、OMIM(https://omim.org/#)数据库中分别检索“insomnia disorder”,将所得ID相关靶点合并、去重,再利用Uniprot数据库匹配GeneSymbol。
3.3 药物-疾病交集靶点获得 将3.1中所得各活性成分相关靶点与3.2中所得ID相关靶点利用微生信(http://www.bioinformatics.com.cn/)在线作图平台取交集,获得核心药组活性成分中直接与疾病相关的靶点。
3.4 疾病-组方-药物-成分-靶点及蛋白相互作用(PPI)网络构建 以疾病、核心组方、药物、药物活性成分、相关靶点为节点,其相互关系为边,在CytoscapeV3.8.0中构建网络;并将1.2.3中的药物-疾病交集靶点导入String(http://string-db.org/cgi/input.pl)数据库进行PPI分析,然后利用Cytoscape的MCODE插件将所得PPI进行聚类,从而获得核心靶点。
3.5 GO(Gene Ontology)富集分析和KEGG(Kyoto Encyclopedia of Genes and Genomes)通路富集分析
将3.3中所得交集靶点导入Cytoscape的BInGO、ClueGO插件分别进行GO生物过程、分子功能、细胞成分和KEGG通路富集分析。
4 关键活性成分与关键靶点分子对接分析
选取3.4疾病-组方-药物-成分-靶点网络中节点度较大的活性成分与PPI网络各聚类中节点度较大的关键靶点分别在Zinc(https://zinc.docking.org/)、PDB(http://www.rcsb.org/)数据库中获得其3D结构,并使用Autodock vina进行分子对接,将其中对接较好的组合进行展示。
结果
1 数据挖掘结果
1.1 药物属性及证候统计 共搜集到病案432例,根据纳入、排除标准筛选,获得验案200例。该200例验案包含方剂256首,涉及中药154味,总应用频次3447次,其中药物应用百分比大于18%的有20味,其应用频次和为2221次,约占总频次64%,见表1。将256首方剂中154味药物进行性味归经的分析,结果以雷达图表示,见图1、2,其中中药药性分布主要为:温、平、寒、微寒;药味主要为:甘、辛、苦;而药物的归经主要归:脾、肝经。中医证候多见于肝郁证、肝郁脾虚证、痰证,见图3。
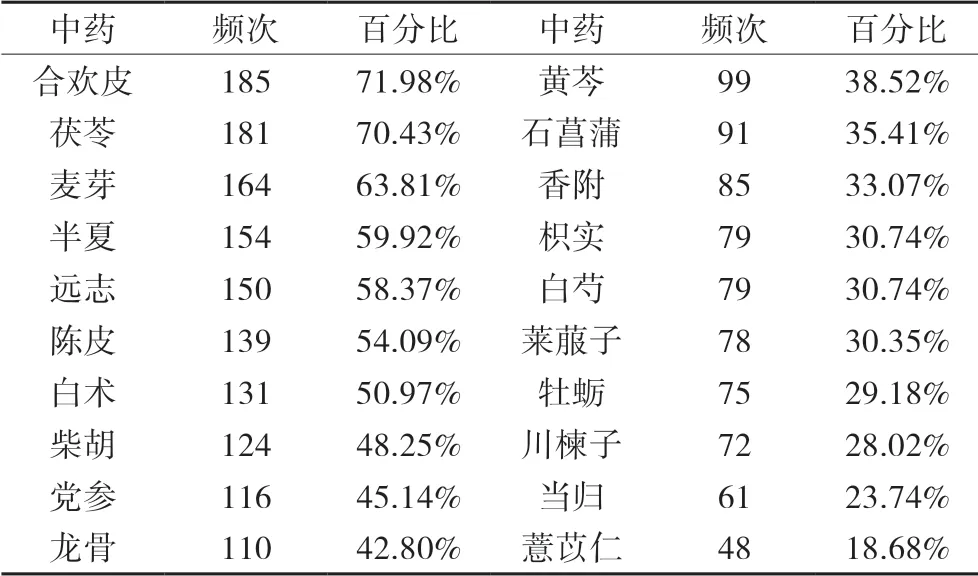
表1 药物使用频次及百分比

图1 四气五味归经频次分布雷达图 (左:四气频次分布;中:五味频次分布;右:归经频次分布)
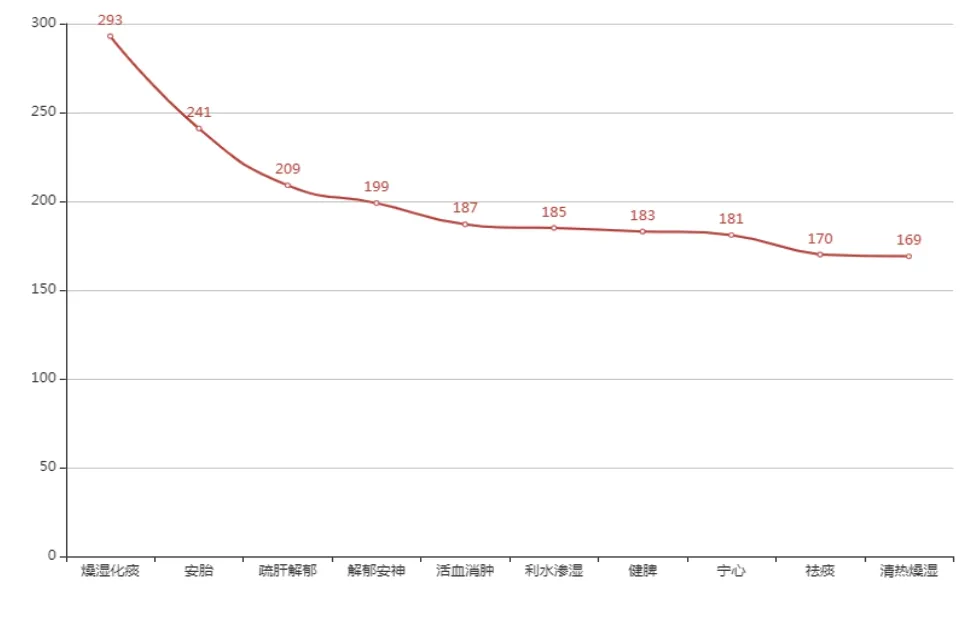
图2 药物功效统计
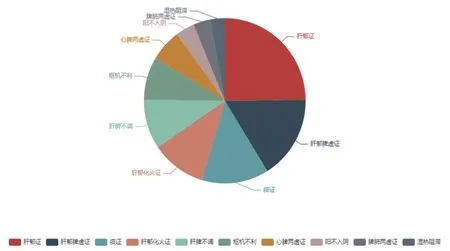
图3 中医证候分布

图4 物聚类分析
1.2 药物关联分析、聚类分析、复杂网络分析及核心组方确定 将256首处方利用云平台数据分析,首先将置信度设置≥0.7,支持度≥0.4,得到20组药物关联分析结果,并按照支持度降序排列,如表2;将2.1.1中应用频率大于18%的20味中药进行聚类分析,同时设置距离类型为欧氏距离,聚类方法为:最长距离法,可将其分为:C1:茯苓、半夏、陈皮;C2:龙骨、牡蛎、柴胡、黄芩;C3:白芍、白术、香附、川楝子、枳实、莱菔子;C4:合欢皮、麦芽、党参、远志、石菖蒲等4个聚类处方,见表4;最后设置节点度不小于95,进行中药-中药复杂网络分析,得到一个由8味中药组成的核心组合,见图5。综合以上得出最核心药物组方为:陈皮、远志、白术、合欢皮、半夏、柴胡、麦芽、茯苓。
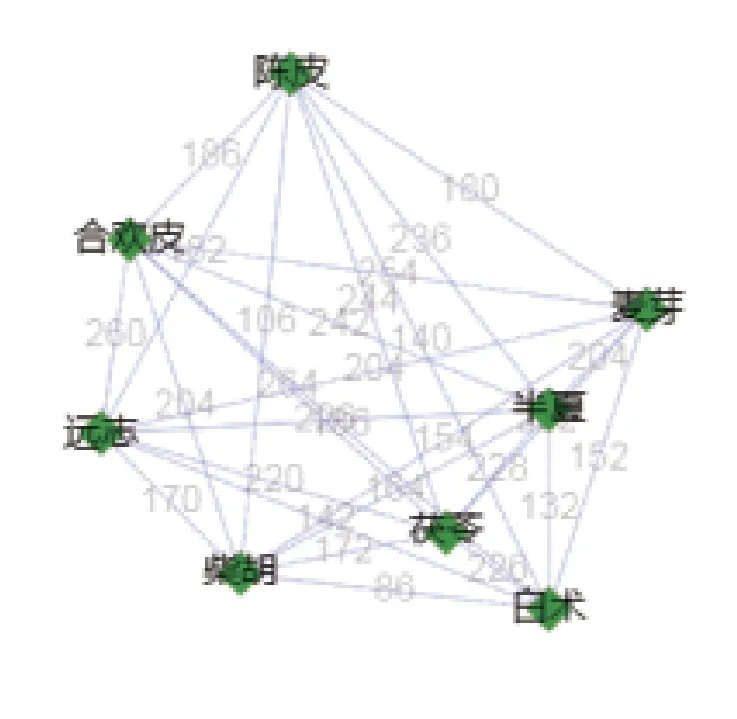
图5 药物复杂网络分析
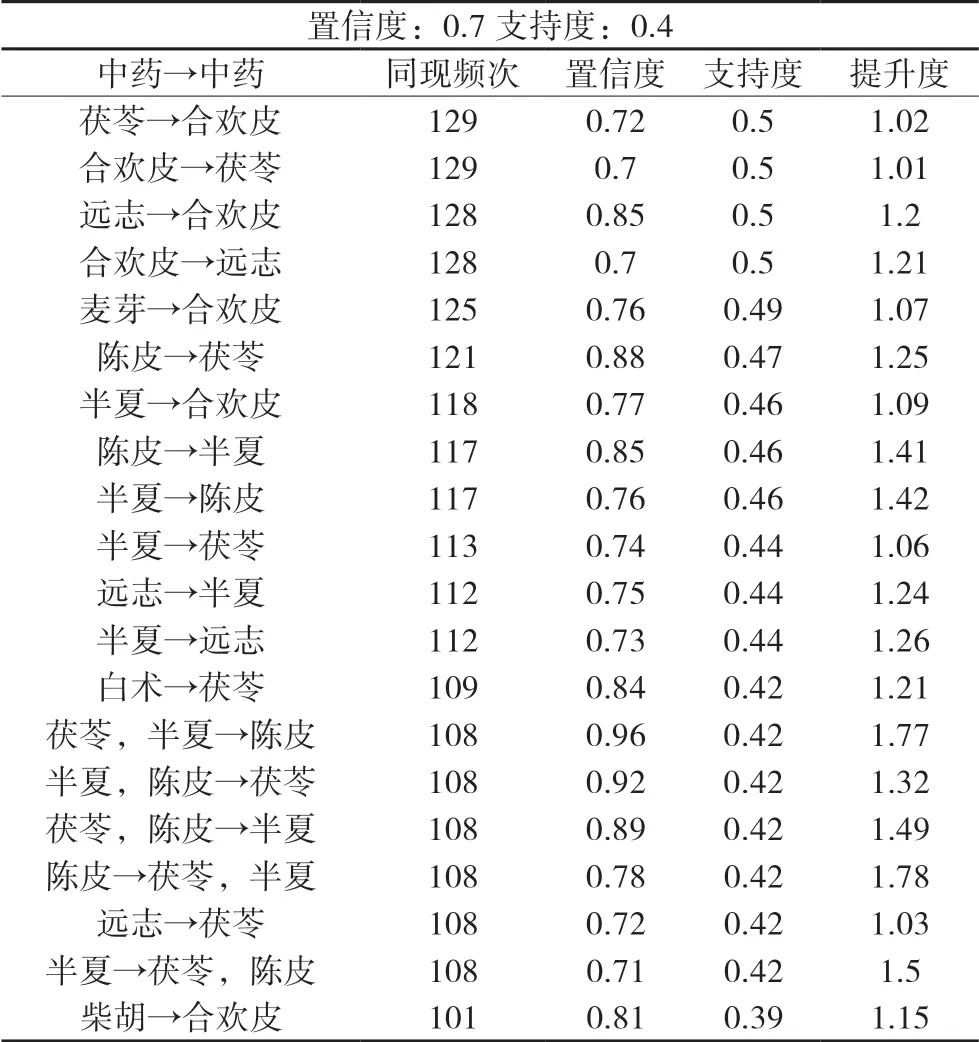
表2 药物关联分析
2 网络药理学结果
2.1 核心组方活性成分和对应靶点 通过检索CNKI与TCMSP数据库,并结合SwissADME筛选与Swisstargetprediction预测靶点,筛选出陈皮、远志、白术、合欢皮、半夏、柴胡、麦芽、茯苓有效成分各4、37、4、15、9、9、5、6种,其中重复成分6种;相关靶点分别为29、624、68、359、73、79、33、128个。经过去重、排除后,总计获得有效成分83种,相关靶点770个。见表3。
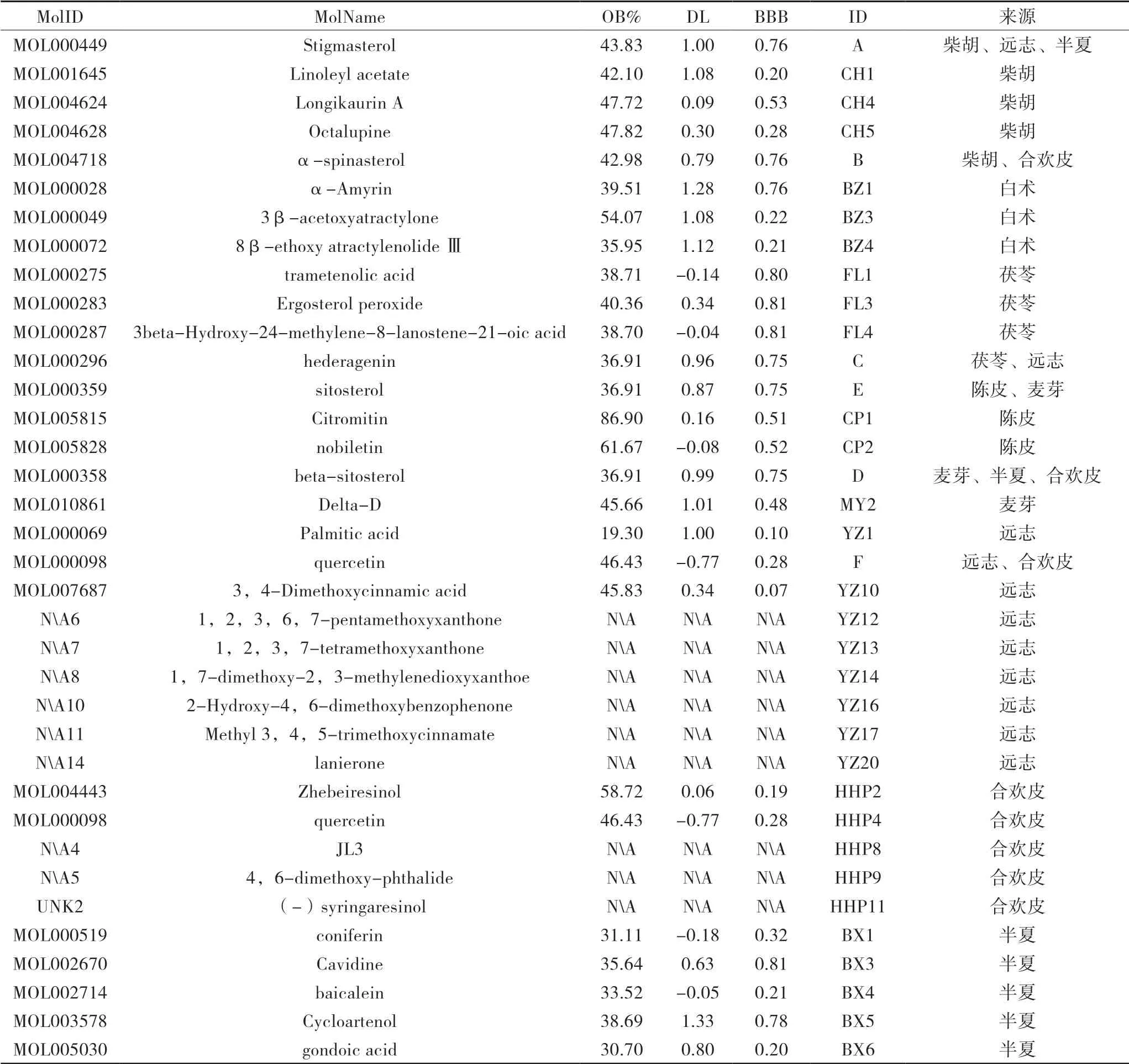
表3 核心药物组成部分成分相关信息
2.2 疾病靶点获取结果和药物-疾病靶点交集结果 将GeneCards数据库中得到的ID相关靶点按照相关度大于中位数进行筛选与OMIM数据库中所得的靶点,合并与去重,共计获得ID疾病靶点994个。利用微生信平台将2.1中求得的药物靶点与1.2中求得的疾病靶点取交集,共获得163个药物与疾病直接相关的交集靶点,见图6所示。
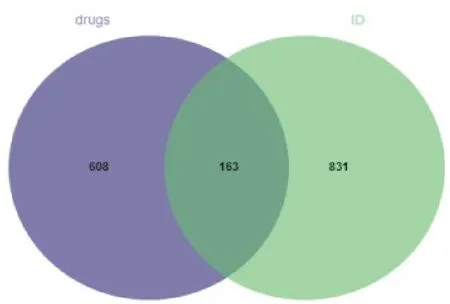
图6 药物-疾病交集基因
2.3 疾病-核心组方-药物-成分-靶点网络 将数据导入Cytoscape软件,构建ID-核心组方-中药-有效成分-对应靶点网络,见图7。图7包含861个节点,2868条边。从该网络可得节点度较大(Degree>50)的有效成分有:F、YZ16、YZ14、HHP8、YZ12、YZ13、YZ10、YZ17、FL4、FL5、A、YZ20。在String中导入163个交集靶点构建PPI网络,然后通过MCODE插件分析网络并根据聚类和节点度得出PPI核心网络,见图8所示,然后选择其中节点度值大(DC>615)的靶点作为核心靶点,有:AKT1、VEGFA、MMP9、IL6、FOS、TNF、CREB1、ESR1、DRD2、SLC6A4。
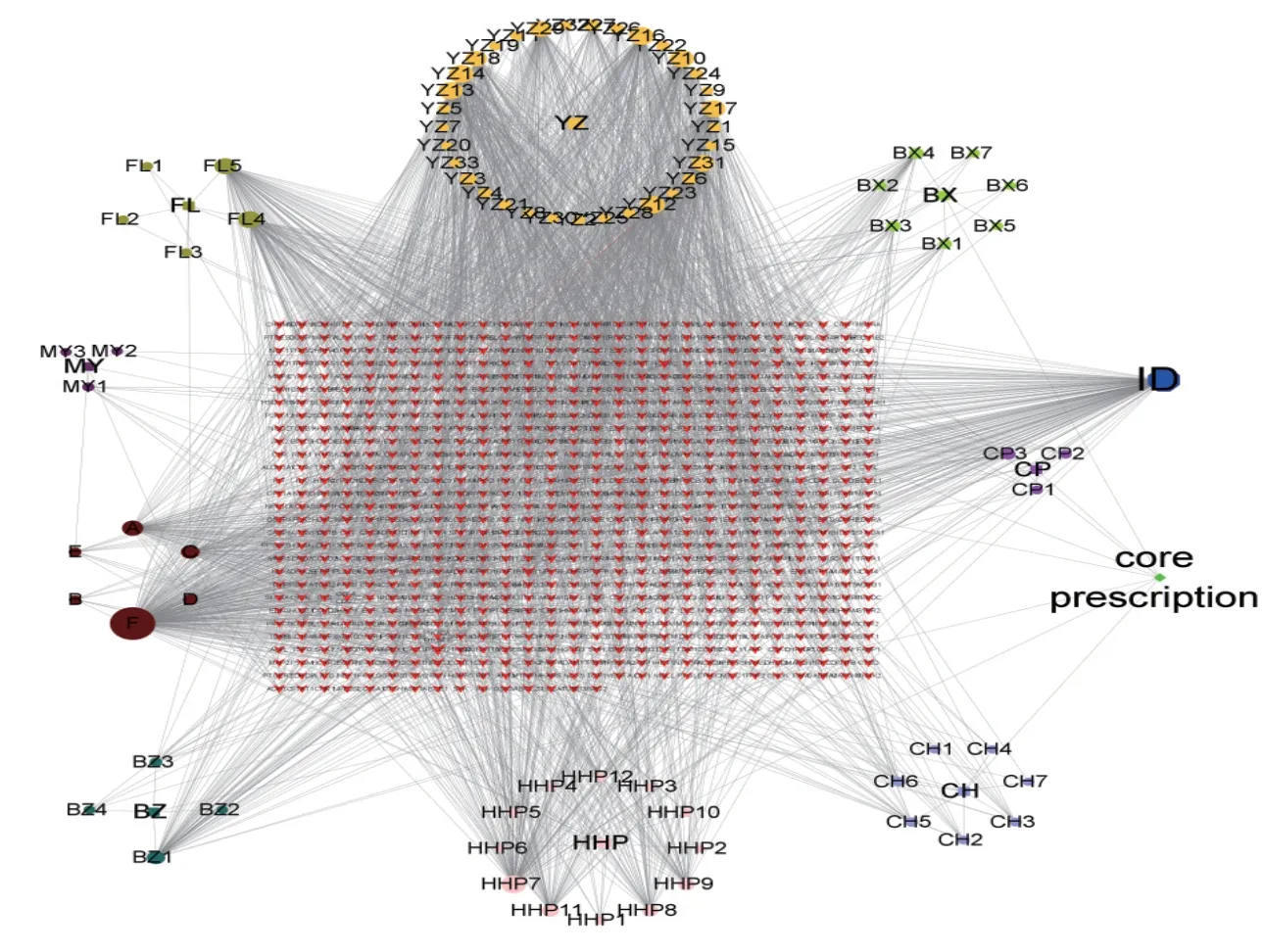
图7 疾病-核心组方-药物-成分-靶点网络
图8 蛋白互作(PPI)网络
2.4 GO富集分析和KEGG富集分析结果 将2.3中的交集靶点导入BInGO,并设置信水平为0.01,进行GO富集分析,见图9,可得GO生物过程主要包括:细胞过程、生物调节、信号过程、对刺激的反应、代谢过程等;GO分子功能则包括:结合、抗氧化活性、电子载体活性、分子传导活性、通道调节等;而GO细胞成分以:细胞器成分、突触成分、高分子结合物等为主。再将交集靶点导入ClueGO,设定p-value≤0.01,最小聚类为15,K-score为0.45进行KEGG通路富集分析,见图10,其中主要有:神经活性配体-受体相互作用、血清素能突触、HIF-1信号通路、细胞间隙连接、尼古丁成瘾、糖尿病并发症中的AGE-RAGE信号通路、前列腺癌等。然后以有效成分、靶点、通路分别为节点,其相互关系为边构建网络,以直观描述三者联系,见图11,而通过分析该网络可得节点度最大的通路为神经活性配体-受体相互作用通路,提示核心组方治疗极可能通过此通路对失眠障碍产生作用,该通路具体作用见图12。
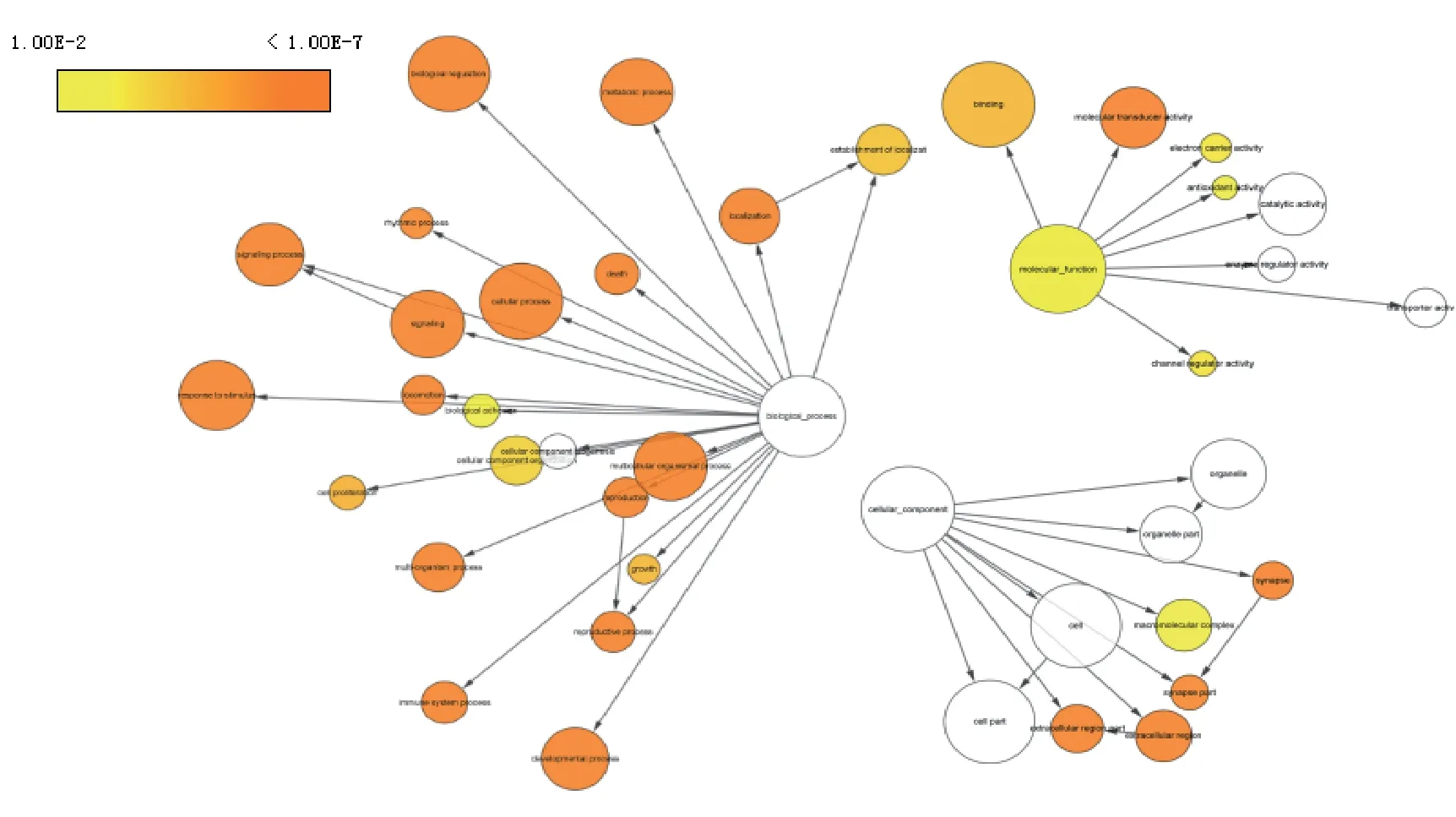
图9 GO富集分析气泡图
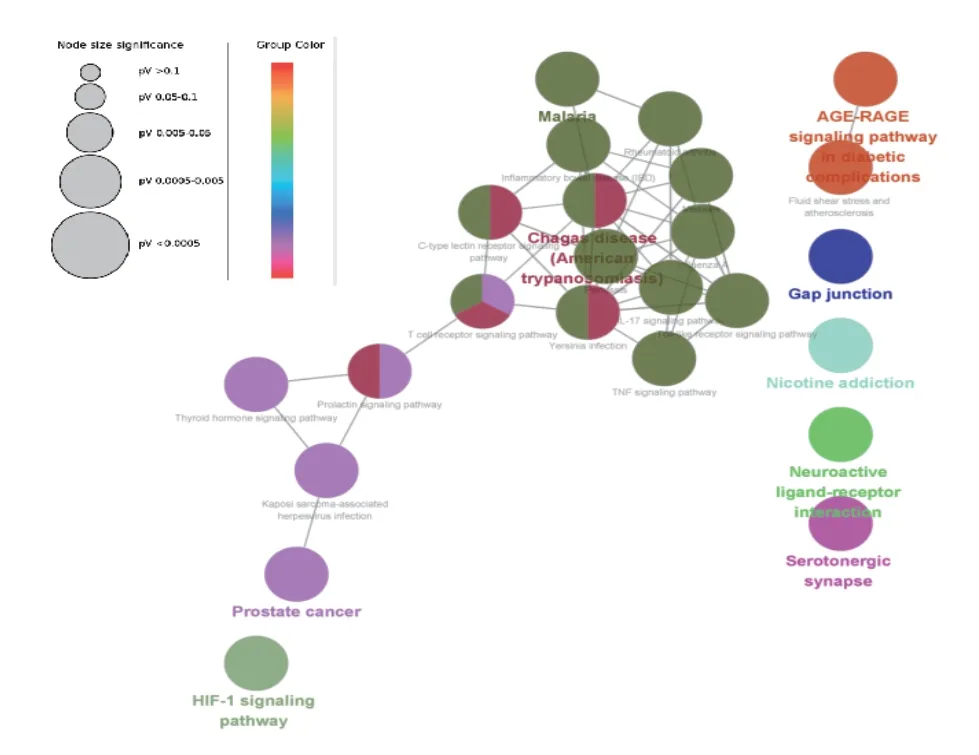
图10 KEGG通路富集分析气泡图
图11 成分-通路-靶点网络

图12 神经活性配体-受体相互作用通路
3 分子对接结果
从关键靶点和关键成分分子对接结果来看,其对接分数大多≤-5.0 kcal·mol/mol,具体见表4,提示核心药组中的关键成分和关键靶点多可稳定结合,将对接结果最好的前5个组合使用Pymol进行可视化,见图13。
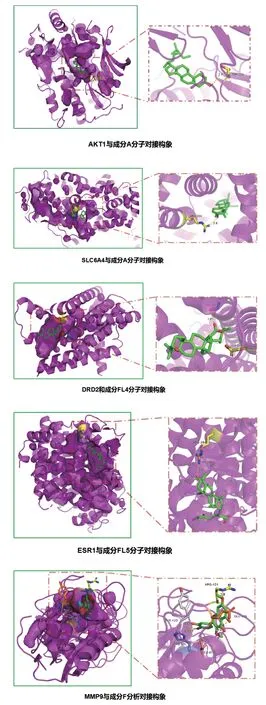
图13 分子对接构象图

表4 分子对接结果
讨论
1 贾师对“不寐”的认识
中医学称失眠为“不寐”“目不瞑”“不得眠”等;历代医家对失眠的病机阐述颇多,但总属阳盛阴衰,阴阳失交,如《灵枢·口问》曰:“阳气尽,阴气盛,则目瞑;阴气尽,而阳气盛,则寤矣”、《医效秘传·不得眠》云:“夜以阴为主,阴气盛则目闭而安卧,若阴虚为阳所胜,则终夜烦扰而不眠也”等,均记载了阴阳盛衰对失眠的影响。中医对失眠的认识不止于病因病机,还对失眠的治疗有理法方药咸备的描述,如《伤寒论》中所说:“虚劳虚烦不得眠,酸枣仁汤主之”。而现代人多食肥甘厚味,缺乏锻炼,精神紧张,导致气机不畅,气血运行失常,贾老认为失眠病机为“阳不入阴,阴阳失交”,在治疗上尤其重视“调畅气机、肝脾并治”,疗效颇佳。
2 贾师治疗的用药规律
从数据分析结果来看,使用频率最高的药物为:陈皮、远志、白术、合欢皮、半夏、柴胡、麦芽、茯苓。这些药物具有镇静催眠、调节植物神经系统、改善认知功能、神经保护等神经系统作用,另具有抗抑郁、抗炎、改善胃肠功能等作用。[7-14]从中药药性分布来看,主要为:温、平、寒、微寒,其药物的寒凉偏性不明显。药味主要为:甘、辛、苦;甘味具有补益、和中、调和药性等作用,辛具有行气、行血的作用,苦具有清泄火热、泄降气逆、燥湿、泻火存阴的作用,且辛开苦降,调畅气机,正适应失眠的治疗。药物的归经主要为归脾、肝经,中医证候多见于肝郁证、肝郁脾虚证、痰证,这反映出贾老“从肝论治”失眠的观点,另药物的归经与中医证候也体现了贾老强调的“理法方药”一致,并注重“方证相应”。药物关联分析中筛选出的20对核心关联组合均是陈皮、远志、白术、合欢皮、半夏、柴胡、麦芽、茯苓八位药物之间相互关联。其中陈皮、半夏、茯苓为二陈汤的主要组成,其功效为燥湿化痰行气;远志和合欢皮以疏肝解郁安神;白术与茯苓健脾祛湿;麦芽有行气健脾之功,既能疏解肝之郁滞,又能护卫脾之正气,为贾老常用之佐使药;整体观之,贾老治失眠,以行气疏肝健脾为主,兼以化痰祛湿。在聚类分析的处方中:C1为燥湿化痰的二陈汤;C2为和解枢机的柴胡加龙骨牡蛎汤;C3、C4为益气健脾、行气化痰的香砂六君子汤;均为贾老坚持“方证对应”中的常用方剂。复杂网络分析也是从此八位药物中所获的核心药组。以上说明,从数据挖掘中可得贾老治疗ID的核心组方为陈皮、远志、白术、合欢皮、半夏、柴胡、麦芽、茯苓,从中可看出贾老以“调畅气机、肝脾并治”论治失眠的观点。
3 核心组方的网络分析
根据药物网络构建,得出核心药组发挥作用的12个关键活性成分,其中F为广泛存在于植物中的生物类黄酮,具有多种生物活性,有动物实验表明它可显著增加非快速眼动睡眠,同时显着减少快速眼动睡眠;[15]YZ12、YZ13、YZ14、YZ20为远志中的呫吨酮类,有研究表明此类物质可通过上调Nrf2表达来赋予神经保护作用[16];YZ17的3,4,5-三甲氧基肉桂酸甲酯(MTC)是具有生物活性的天然苯基丙烷,具有抗炎和抗氧化的作用,可以改善炎性所致的失眠症状[17];HHP8为合欢皮中的木脂素类成分,该物质可能是合欢皮传统安神作用的主要有效成分之一[18];FL4、FL5是茯苓中的三萜化合物,有研究证明具有镇静兴奋性神经元和抗惊厥等作用。[19]
根据PPI网络,所得的核心靶点中TNF在睡眠中的作用涉及与全身性TNF慢性升高和睡眠中断有关的病理状况,TNF参与了广泛的紧密协调的生化网络中的睡眠调节。[20]研究表明较低的睡眠效率与较高的IL-6循环水平相关,睡眠障碍与炎症水平升高有关。[21]c-Fos是FOS中的一个因子,但c-Fos标记的睡眠活动神经元的药理学活化已显示可诱导睡眠;还有研究表明在内侧视前区中c-fos的表达与睡眠调节有因果关系,c-Fos在大脑皮层和海马体的表达可能与长时间的清醒和睡眠需求有关。[22-23]VEGFA是VEGF生长因子家族的成员,在调节情绪状态中起作用,而失眠与抑郁症呈复杂的双向关系。[24-25]在实验中发现睡眠受限后,AKT的表达水平显着降低,AKT的改变可能与慢性睡眠受限有关。[26]CREB1作为一种重要的调控蛋白质,其转录增加与睡眠阶段的记忆形成有关。[27]ESR1即雌激素受体1,雌二醇通过其对ESR1和非经典信号通路的作用来改变每日和昼夜节律。[28]多巴胺D2受体基因(DRD2)中的SNP(rs17601612)与睡眠时间显着相关,研究证明第二个DRD2信号对睡眠时间有相反的影响[29]。
目前ID的病理机制尚不明确,但比较公认的有:细胞机制障碍、生物调节异常、神经递质系统紊乱(5-羟色胺、褪黑激素、y-氨基丁酸)、信号传导障碍(下丘脑-垂体-肾上腺轴,即HPA轴)、代谢异常(葡萄糖、荷尔蒙、食欲素、瘦素等代谢异常)、遗传基因等。[30-33]由GO富集分析得到的主要生物过程对ID公认病理机制几乎都有涉及,可见核心组方参与多种机制,可从多个途径对ID发挥治疗作用。KEGG通路分析主要结果中:血清素能神经传递都与睡眠-觉醒周期的控制有关,在中枢神经系统中,5-HT(血清素能)系统在控制疼痛,情绪,唤醒,睡眠-觉醒周期,学习/记忆,焦虑和奖励行为方面起着至关重要的作用;[34-35]细胞间隙连接,如星形胶质细胞通过间隙连接介导的星形胶质网络产生并向神经元提供代谢底物的研究,证明了星形胶质网络的扰动会损害睡眠-觉醒周期;[36]研究结果表明,早期苏醒可能是尼古丁成瘾严重程度与睡眠时间短和白天过度嗜睡的不良睡眠结果之间联系的机制,尼古丁成瘾的严重性是影响睡眠质量的重要因素,而不仅仅是吸烟状态,较高的成瘾水平导致较少的睡眠和更多的白天嗜睡[37]。
分子对接结果表明,关键有效成分和关键靶点大多都结合成稳定结构,而其与各关键成分对接较好的靶点为AKT1、DRD2和ESR1,与关键靶点对接较好的成分是YZ14(1,7-二甲氧基-2,3-亚甲二氧基呫吨酮)和FL5(去氢齿孔酸),这提示核心组方可能由这两种成分作用于以上的三个靶点从而发挥治疗ID的作用。
综上所述,通过数据挖掘、网络药理学和分子对接研究,可以得到贾老中药治疗ID的核心组方:陈皮、远志、白术、合欢皮、半夏、柴胡、麦芽、茯苓,并初步揭示其多成分、多靶点、多通路作用机制,所涉及的关键成分为:1,7-二甲氧基-2,3-亚甲二氧基呫吨酮、去氢齿孔酸;核心靶点为:AKT1、DRD2和ESR1;主要通路为:神经活性配体-受体相互作用、血清素能突触、细胞间隙连接。该结论可为进一步研究和临床应用提供参考。

