番茄红素提取工艺的研究
◎ 谭敏捷
(清远市食品检验中心,广东 清远 511500)
番茄红素(C40H56)是一种非常重要的天然类胡萝卜素,与β-胡萝卜素是同分异构体。其最早从番茄中分离制得,故称番茄红素。其分子中有11个共轭双键和2个非共轭双键,因此稳定性很差,容易发生顺反异构和氧化降解。天然存在的番茄红素全为反式构型,人体组织中则大部分为顺式构型,长时间加热或者紫外线照射可使其异构化,产生部分顺式构型[1]。它在自然界中分布广泛,主要存在于番茄、胡萝卜、西瓜、葡萄、芒果、草莓等成熟的红色水果和蔬菜中。番茄红素是脂溶性色素,可溶于其他脂类和非极性溶剂中,易溶于氯仿、苯、二硫化碳,可溶于乙醚、石油醚、丙酮、乙酸乙酯等,难溶于甲醇、乙醇,不溶于水[2-3]。
番茄红素的提取及测定是目前国内外的一个研究热点,主要有有机溶剂提取法、酶反应法、色谱分离法和超临界流体萃取等方法,其中酶试剂较贵,色谱分离法和超临界流体法设备昂贵,故常用操作简单、可行性强的有机溶剂提取法,如采用氯仿、丙酮、乙醚、乙酸乙酯等为提取溶剂的提取法,其中乙酸乙酯是常用的工业溶剂,对番茄红素的提取率较高,并且成本低,常压下沸点低,易于回收,因此本试验选择乙酸乙酯作为提取溶剂,研究各种因素对提取效果的影响,从而为番茄红素的开发利用提供理论依据[4]。
1 材料与方法
1.1 试验原材料
新鲜番茄购买于百加肉菜市场
1.2 试验试剂
乙酸乙酯(分析纯),广州化学试剂厂;乙醇(分析纯),广州化学试剂厂;
氢氧化钠(分析纯),广州化学试剂厂;盐酸(分析纯),廉江市爱廉化学试剂有限公司。
1.3 主要试验仪器与设备
723N可见分光光度计(上海精密科学仪器有限公司);HH-601超级恒温水浴锅(江苏金坛市亿通电子有限公司);AUY120分析天平(SHIMADZU);pHS-3C+酸度计(成都世纪方舟科技有限公司);TH-300A梯度混合器(上海青浦泸西仪器厂);家用捣碎机(金威马);LXJ-IIB飞鸽牌离心机(上海革安亭科学仪器厂)。
1.4 试验方法
1.4.1 样品的制备
将新鲜番茄用清水冲洗干净后,用小刀切成小块,放进捣碎机打碎成浆,先离心脱水1次(4 000 r·min-1,20 min),得到红色的膏状番茄糊,用95%乙醇预处理,按番茄糊∶95%乙醇=1∶3处理,每次20 min,处理两次,然后离心去上清液后,装入棕色玻璃瓶备用。乙醇处理的目的是脱水,除去一些杂质及黄色素等。
1.4.2 番茄红素最大吸收波长的确定
用分析天平称取5.0 g已制备好的番茄泥于50.0 mL离心管,加入25.0 mL乙酸乙酯,调节pH=7,在50 ℃水浴恒温回流1.5 h后,离心取2.000 mL上清液稀释5倍于10.0 mL比色管,用乙酸乙酯定容,摇匀后迅速用可见分光光度计测定番茄红素提取液在不同波长下的吸光值。
1.4.3 番茄红素提取工艺流程
番茄红素提取工艺流程为:新鲜番茄前处理→切碎→捣碎机破碎→离心机脱水→95%乙醇预处理(两次,每次20 min)→离心→称重→乙酸乙酯水浴恒温回流→离心→取上清液定容→测吸光值。
1.4.4 番茄红素的测定及分析方法
对粗提液的测定采用吸光度法,用移液器从粗提液中取2 mL于10 mL比色管,用乙酸乙酯定容,摇匀后迅速在502 nm波长下测定溶液的吸光值(用乙酸乙酯做参比)。不同提取工艺条件下提取相同量番茄糊得到的提取液定容到相同的体积后,在502 nm波长下测定提取液的吸光值。吸光度用A表示。A=abc,其中a为吸光系数,单位L/(g·cm);b为液层厚度(通常为比色皿的厚度),单位cm;c为溶液浓度,单位g·L-1,番茄红素的含量c可通过吸光值得到,因此由吸光值可知番茄红素含量的高低,本试验番茄红素的提取率采用吸光值来表示。
1.4.5 番茄红素提取的单因素试验
对番茄红素提取过程中的提取温度、提取时间、pH、料液比、提取级数逐个进行单因素试验。
(1)pH对番茄红素提取率的影响。称取5份已预处理的番茄糊5.000 g,分别置于50.0 mL离心管,均加入25.0 mL乙酸乙酯,再用5%的NaOH调pH值分别为4、5、6、7和8,在50 ℃水浴恒温回流1.5 h,离心,取上清液2.000 mL稀释5倍于10.0 mL比色管,用乙酸乙酯定容,摇匀后迅速在502 nm处测吸光值。每组3个平行。
(2)提取温度对番茄红素提取率的影响。称取5份已预处理的番茄糊5.000 g,分别置于50.0 mL离心管,均加入25.0 mL乙酸乙酯,再用5%的NaOH调pH值为7,分别在40 ℃、50 ℃、60 ℃、70 ℃和80 ℃水浴恒温回流1.5 h,离心,取上清液2.000 mL稀释5倍于10.0 mL比色管,用乙酸乙酯定容,摇匀后迅速在502 nm处测吸光值。每组3个平行。
(3)提取时间对番茄红素提取率的影响。称取5份已预处理的番茄糊5.000 g,分别置于50.0 mL离心管,均加入25.0 mL乙酸乙酯,再用5%的NaOH均调pH值为7,在50 ℃水浴恒温分别回流0.5 h、1.0 h、1.5 h、2.0 h和2.5 h,离心,取上清液2.000 mL稀释5倍于10.0 mL比色管,用乙酸乙酯定容,摇匀后迅速在502 nm处测吸光值。每组3个平行。
(4)料液比对番茄红素提取率的影响。称取5份已预处理的番茄糊5.000 g,分别置于50.0 mL离心管,分别加入按料液比1∶4、1∶5、1∶6、1∶7和1∶8,再用5%的NaOH均调pH值为7,在50 ℃水浴恒温分别回流1.5 h,离心,取上清液2.000 mL稀释5倍于10.0 mL比色管,用乙酸乙酯定容,摇匀后迅速在502 nm处测吸光值。每组3个平行。
(5)提取级数对番茄红素提取率的影响。称取5份番茄糊5.000 g,分别置于50.0 mL离心管,均加入25.0 mL乙酸乙酯,再用5%的NaOH均调pH值为7,在50 ℃水浴恒温分别回流1.5 h离心,取上清液2 mL稀释5倍于10.0 mL比色管,用乙酸乙酯定容,摇匀后迅速在502 nm处测吸光值。再用25.0 mL乙酸乙酯对去上清后的番茄糊提取1.5 h,经上述同样的操作在502 nm下测吸光值,接着再用25.0 mL乙酸乙酯进行第3次提取,1.5 h后去上清定容,测吸光值,再接着用25.0 mL乙酸乙酯进行第4次提取,测吸光值。每组3个平行。
1.4.6 番茄红素提取的正交试验
在单因素试验的基础上,选择浸提时间、浸提温度、料液比以及提取级数为4个影响因素,每个因素3个水平进行正交试验,用极差分析法确定最佳提取工艺条件。正交试验因素水平设计见表1。

表1 正交试验因素水平表
2 结果与分析
2.1 番茄红素最大吸收波长的确定
由图1可知,番茄红素在波长440~510 nm处出现3个吸收峰,分别为444 nm、472 nm、502 nm,这与相关文献描述的基本相符。在最大吸收波长下,用可见分光光度计测定溶液的吸光度,以此来表示番茄红素的浓度,用朗伯-比尔定律计算番茄红素的含量,此法不需要昂贵的番茄红素标准品,而且操作简便,适宜番茄红素粗提取阶段的浓度测定[5-6]。由于与番茄红素共存的其他类胡萝卜素如β-胡萝卜素,在472 nm处也有1个较强的吸收峰,这会对测定造成干扰,张连富、丁霄霖等人建立了一种番茄红素的简便测定方法,即选择502 nm作为测定波长,避免了其他类胡萝卜素的影响。因此本试验的后续工作中,均在该波长下测定各次试验提取液的吸光度,比较吸光值的大小,根据朗伯-比尔定律计算番茄红素的提取率[7-10]。

图1 番茄红素的吸收光谱图
2.2 单因素试验结果
2.2.1 pH对番茄红素提取率的影响
由图2可知,在其他条件相同的情况下,不同pH下番茄红素的吸光值不同,酸性越大,番茄红素的稳定性越差,当pH=7时番茄红素提取率最高。pH>7时,番茄红素提取率有所下降。由试验可知,番茄红素的最佳提取pH为7。

图2 pH对番茄红素提取率的影响图
2.2.2 提取温度对番茄红素提取率的影响
由图3可知,在其他条件相同的情况下,番茄红素吸光度与温度关系近似线性关系,在所选范围内,当提取温度为60 ℃时,番茄红素提取率达到最佳值。这是因为随着温度的上升,分子运动速度加快,有利于番茄红素的渗出。但温度达到70 ℃以上,番茄红素氧化被破坏,提取液变浑浊,从而使番茄红素提取率下降。同时考虑到提取剂的沸点及挥发性,以减少溶剂损失。由试验可知,番茄红素的最佳提取温度约为60 ℃,这时番茄红素的质量达到最好,过滤后能得到澄清的溶液。

图3 提取温度对番茄红素得率的影响图
2.2.3 提取时间对番茄红素提取率的影响
由图4可知,在其他条件相同的条件下,不同的浸提时间吸光值不同,当浸提时间为1.5 h时,提取效果最好;提取时间小于1.5 h,提取率随提取时间的增加而增加,而当浸提时间超过1.5 h,随着浸提时间的进一步增加,番茄红素的提取率反而逐渐减小。这可能是超过一定的时间后,因为温度等其他因素的影响,番茄红素被氧化损失,提取率反而下降。因此确定最佳提取时间为1.5 h。

图4 提取时间对番茄得率的影响图
2.2.4 料液比对番茄红素提取率的影响
由图5可知,在其他条件相同的情况下,随着料液比的增大,吸光值增大,番茄红素的提取率也随之增大,但在料液比达到1∶6后,番茄红素的提取率增长缓慢,几乎趋于平缓,原因是溶剂与番茄糊已充分混合。当料液比为1∶6提取率最大,考虑到试验的成本及效率,确定最佳料液比为1∶6。

图5 料液比对番茄红素得率的影响图
2.2.5 提取级数对番茄红素提取率的影响
用提取剂提取目标产物时,提取次数越多,目标产物总提取量也越多,这是试验提取所需的结果,但同时提取剂消耗量也越多,不利于后蒸发溶剂进行浓缩的操作。由图6可知,当提取级数达到3级时,番茄红素提取液的所测吸光值已小于0.05,这时番茄红素已基本提取完全,故应选择提取级数为3。

图6 提取级数对番茄红素得率的影响图
2.3 正交试验结果
为了进一步确定番茄红素提取工艺的最优条件,在单因素试验的基础上,选择浸提时间、浸提温度、料液比和提取级数为影响因素,进行4因素3水平的L9(34)正交试验。正交试验结果,如表2所示。
由表2可知:R值由大到小依次为C>B>D>A因素,即对番茄红素提取影响最大的为料液比,然后依次为提取级数、提取温度和提取时间。根据kA2>kA3>kA1,得A2为最优水平;kB3>kB2>kB1,得B3为最优水平;kC3>kC2>kC1,得C3为最优水平;kD1>kD3>kD2,得D1为最优水平。因素主次关系为C(料液比)>B(提取级数)>D(提取温度)>A(提取时间),则正交试验得到的最优组合为A2B3C3D1,即提取时间1.5 h,提取级数为3,料液比1∶7,提取温度50 ℃。
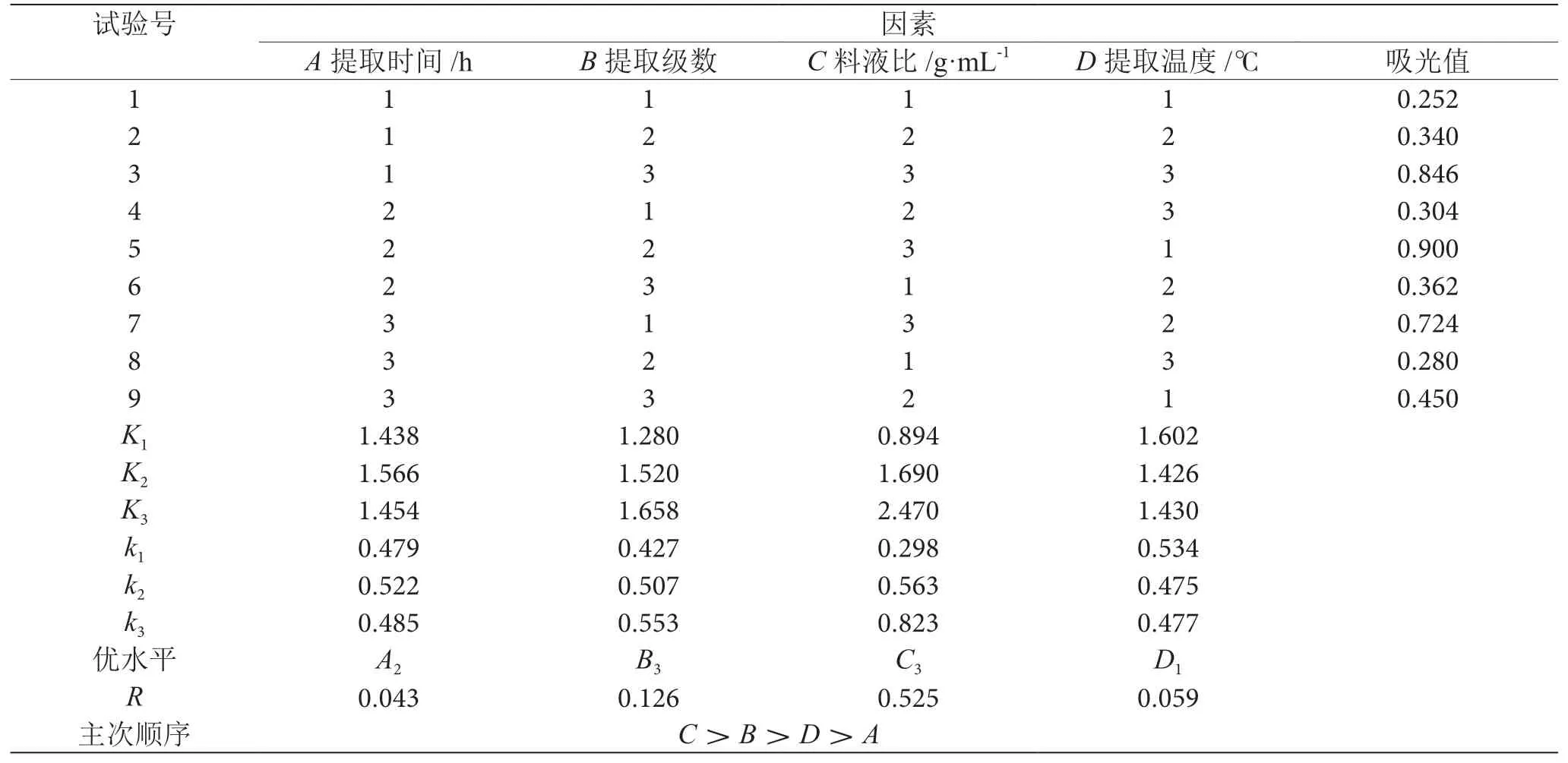
表2 番茄红素提取条件优化方案及正交试验结果表
2.4 验证试验
在最佳提取条件下,进行验证试验,得到番茄红素的吸光值为0.906,与正交试验结果相符。
3 结论
若采用新鲜番茄,打碎离心脱水后进行95%乙醇预处理两次,使一些醇溶性的黄色素和一些水溶性杂质除去,然后将番茄糊与乙酸乙酯按1∶7的料液比混合,调节pH=7,50 ℃水浴恒温回流1.5 h以提取番茄红素,提取效果最佳。50 ℃减压旋转蒸发浓缩回收乙酸乙酯,番茄红素经冷却结晶,此时的番茄红素可进行进一步纯化。乙酸乙酯低毒性,成本较低,易回收,故用此方法提取番茄红素适合工业生产,但应用于工业生产需进一步研究。

