化学共沉淀工艺对镍包覆碳化钨硬质合金粉体包覆质量的影响
赵小鹏, 王义盛, 杨 浩, 闵凡路, 张建峰
(1.中交隧道工程局有限公司, 北京 100102; 2.河海大学 岩土力学与堤坝工程教育部重点试验室, 南京 210098;3.河海大学 教育部土木与交通学院, 南京 210098; 4.河海大学 力学与材料学院, 南京 211100)
硬质合金是通过粉末冶金方法将硬质相(如WC、TiC)和黏结相(如钴、镍、铁)按照性能需要设计的形式、比例、分布组合而制成的材料[1-3]。硬质合金不仅硬度和强度高,同时还具有耐磨、耐热、耐腐蚀等性能。目前,工业制备硬质合金复合粉末的主流工艺是球磨法,该工艺是在球磨机中加入若干不同大小的磨球、碳化钨或其他硬质相粉末、黏结相金属粉末、酒精等材料,球磨机中的磨球不断对粉末进行碰撞和碾压,使球磨机内的粉末混合,最终实现合金复合粉体的制备[8]。但是,使用该工艺制备的合金复合粉体要达到均匀的混合效果,需要相当长的球磨时间,且制备的粉末粒径难以控制,易存在大量的黏结相金属团聚,这会对合金性能产生不利影响。
为寻求更佳的硬质合金制备新方法,研究人员对硬质合金复合粉末的制备方法进行了许多探索,主要方法有水热压氢还原法、喷雾转化法、化学镀法和化学共沉淀法等。候玉柏等[9]采用高压氢还原的湿法冶金工艺制备了高质量钴包覆碳化钨粉末,讨论了催化剂、试验温度、硫酸铵、氨水及氧分压等工艺参数对碳化钨粉末的钴包覆质量的影响,在大量试验的基础上得到了制备包覆完整的球形碳化钨/钴颗粒合适的工艺参数。郭圣达等[10]利用喷雾转化法制备了纳米碳化钨-钴复合粉末,并研究了喷雾转化工艺参数对复合粉末微观性能的影响,研究发现喷雾转化过程中离心转速越大,粉末松装密度越大,颗粒粒径越小,转化温度的提升可减小颗粒的粒径。LIU等[11]采用一种新的化学镀工艺,在WC粉末上镀覆一层钴金属,用激光将WC-Co复合粉末涂覆在钢表面,研究了工艺参数对WC-Co涂层的影响,并与工业WC-Co粉末涂层进行了耐磨性比较。结果表明,采用新型复合WC-Co粉末的涂层组织良好,耐磨性好。
化学共沉淀法具有制备工艺简单、成本低、制备条件易于控制、包覆均匀、合成周期短,且制备过程中不会引入杂质元素等优点。孙业熙等[12]将钴粉制备过程与粉末混合过程相结合,采用化学共沉淀-氢气还原工艺制备WC-Co包裹粉,并以包裹粉为原料成功制备了WC-8%(质量分数)Co硬质合金。王玉香等[13]以钨酸铵、硝酸钴、碳粉为原材料,采用共沉淀-喷雾干燥法成功制备出超细WC-Co复合粉,并研究了还原碳化温度对粉末平均粒径的影响;吴厚平等[14]探讨粗晶粒硬质合金的制备途径即基于有机物还原反应机理的化学包裹粉工艺,此方法可以解决传统湿磨工艺难以制备粒径不小于4.5 mm的粗晶粒硬质合金的难题,为制备粗和超粗晶粒WC-Co硬质合金提供了新途径。
目前文献中以钴包覆WC的研究工作较多,镍包覆WC的探讨不足[15]。另外,化学共沉淀法工艺条件对包覆效果的影响规律及机理研究仍有待深入开展。笔者以WC粉末为形核剂,利用化学共沉淀包覆反应,将化学共沉淀反应产生的镍盐沉积到WC粉体表面,得到WC-镍盐混合物前驱体,再通过高温氢气还原一步得到镍包覆WC粉末。分析了料液浓度、反应温度和沉淀剂加入流量等不同工艺条件对镍沉淀率及包覆形貌的影响规律,探讨了镍粒子形核及包覆机理。
1 试验材料及表征方法
1.1 试验材料
试验所用原材料主要包括:费氏粒径为4.8~5.2 μm的WC粉体(纯度≥99.96%),氢氟酸(纯度≥40.0%),硝酸(纯度≥65.0%),NiCl2·6H2O(纯度≥98.0%),(NH4)2C2O4·H2O(纯度≥99.5%)。试验步骤如下。
(1) WC原粉粗化
称量一定量的氢氟酸(HF)与硝酸(HNO3),与去离子水均匀混合后得到粗化液,将称量的碳化钨粉体加入粗化液中并充分搅拌30 min,之后将粉体用去离子水洗涤3次后烘干得到粗化后粉体。
(2) 包覆混合物前驱体(WC-NiC2O4·2H2O)
将NiCl2·6H2O和(NH4)2C2O4·H2O分别配制成相同体积不同浓度的NiCl2溶液和(NH4)2C2O4溶液,将粗化后的碳化钨粉体倒入之前配置成的NiCl2溶液中,再向NiCl2、碳化钨混合溶液中加入一定量的盐酸溶液调节混合溶液的pH值。然后将(NH4)2C2O4水溶液作为沉淀剂加入到NiCl2、碳化钨混合溶液中,由于WC的密度较大,为了防止WC的沉降影响均匀性,在包覆的过程使用电动搅拌器,这不仅能够防止WC的沉降还能使溶液混合物混合均匀。化学共沉淀反应过程如下:
NiCl2·6H2O+(NH4)2C2O4·H2O→
NiC2O4·2H2O↓+2NH4Cl+5H2O
(1)
(3) 高温氢气还原法制备出WC-Ni合金粉末
同时我们将微课资源库申报了苏州国际教育园课程共享第4批自建课程“PS大家秀”并通过评审,目前该课程已经在高校邦在线课程网站上线且形成了相应配套微课资源,苏州高等职业技术学校14、15级400多名学生已经选修,学生在使用过程中只要扫描二维码即可在线浏览微课,课后可进行复习与测试。学生在学习过程中对该课程给予了较高的评价,同时我们也根据学生学习的反馈意见不断对课程进行改进与更新。
将陈化后的混合溶液进行抽滤,然后在真空干燥箱中干燥。将混合物前驱体粉末在氢气保护气氛中以恒定高温煅烧得到WC-Ni复合粉体。高温氢气还原反应过程如下:
2NiC2O4·2H2O+5H2→2Ni(包覆在WC颗粒表面)+CO2↑+3CO↑+7H2O
(2)
1.2 试验表征方法
共沉淀反应的沉淀率体现出了化学共沉淀反应的效率、有效性和该工艺投入实际生产的可操作性。该次试验中沉淀率由下式计算得到:
v沉淀=M后/M理
(3)
式中:M后为共沉淀反应后干燥得到的粉体质量;M理为共沉淀反应后得到粉体的理论质量。
分别对碳化钨原粉、粗化后碳化钨粉体、化学共沉淀包覆反应后得到的混合前驱体粉体以及高温氢气还原后得到的复合粉体进行物相组成分析和微观形貌分析,测试仪器分别为Bruker D8 Advance型X射线粉末衍射(XRD)仪、光学显微镜和蔡思EVO18型扫描电镜(SEM)。测试过程中X射线衍射仪的各工作参数如下:X光管电压为40 kV,电流为40 mA,测试的准确度≤0.02°,测试速率为10(°)·min-1,测试角度为2°~90°。
2 试验结果及分析
2.1 工艺参数对共沉淀反应沉淀率的影响
由图1a)可看出沉淀率随料液浓度升高而增大,在料液浓度升高到0.4 mol·L-1后沉淀率升高幅度开始大幅减小,最后趋于定值。对于该试验而言当料液浓度为0.4 mol·L-1NiCl2、0.2 mol·L-1(NH4)2C2O4时,可获得最佳的包覆效果和较高的沉淀率。由图1b)可看出,沉淀率随反应温度升高先逐渐增大,当反应温度升高到65 ℃后沉淀率达到峰值,然后开始减小。对于该试验而言当反应温度为50 ℃时,可获得最佳的包覆效果和较高的沉淀率。如图1c)所示,共沉淀反应沉淀率随沉淀剂加入体积流量的加快先大幅上升,在0.17 mL·s-1加入体积流量时达到峰值,之后沉淀率开始逐渐降低最后趋于平缓。对于该试验而言当沉淀剂加入体积流量为0.17 mL·s-1时,可获得最佳的包覆效果和最高的沉淀率。

图1 不同工艺参数对共沉淀反应沉淀率的影响Fig.1 Effects of different process parameters on precipitation rate of co-precipitation reaction:a) liquid concentration; b) reaction temperature; c) precipitant addition volume flow
在共沉淀反应中,晶核的生长速率与溶液中溶质的瞬时浓度密切相关。图2给出了不同沉淀剂加入体积流量下混合物前驱体粉末的SEM形貌(NiCl2浓度为0.4 mol·L-1;(NH4)2·C2O4浓度为0.2 mol·L-1,反应温度为50 ℃,反应时间为1.5 h;pH值为6.2)。随着沉淀剂加入体积流量的减慢,溶液中颗粒的分散度和NiC2O4·2H2O颗粒在WC颗粒表面包覆的紧密程度和均匀性均得到提升,当沉淀剂加入体积流量降低到0.17 mL·s-1后,随着加入体积流量的降低NiC2O4·2H2O颗粒在WC颗粒表面包覆的紧密程度和均匀性均开始降低。

图2 不同沉淀剂加入体积流量下混合物前驱体粉末的SEM形貌Fig.2 SEM morphology of mixture precursor powder at different addition rates of precipitant
2.2 粉体的物相组成及粉体各阶段包覆效果分析
图3a)为试验所使用的WC原粉的XRD谱,可见试验所使用的WC原粉无明显杂质元素;图3b)为试验所使用的前驱体粉体的XRD谱,可见化学共沉淀反应试验得到的WC-镍盐混合物前驱体为WC-NiC2O4·2H2O,并未引入其他杂质元素,得到纯净的前驱体粉末;图3c)为混合物前驱体粉末还原后得到的合金粉末的XRD谱,可见还原后得到的WC-Ni合金粉末为纯WC相和镍相,无其他杂质相存在。通过XRD谱可证明化学共沉淀-高温氢气还原包覆粉体法的可行性和有效性。
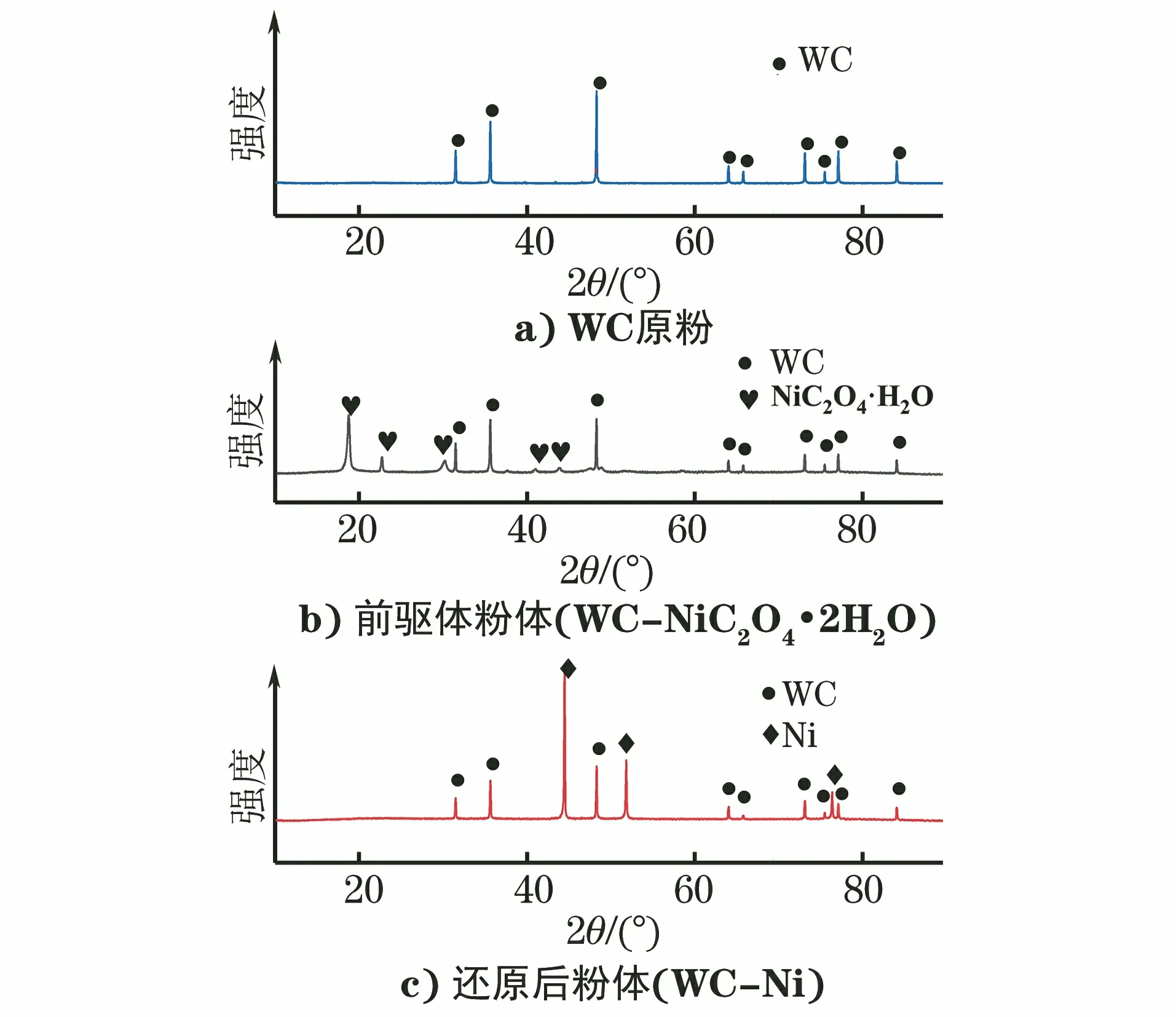
图3 化学共沉淀-高温氢气还原工艺不同阶段混合粉体的XRD谱Fig.3 XRD spectra of mixed powders in different stages of chemical co-precipitation-high temperature hydrogen reduction process:a) WC raw powder; b) precursor powder (WC-NiC2O4·2H2O);c) reduced powder (WC-Ni)
化学共沉淀-高温还原制备包覆粉体工艺各阶段粉体微观形貌如图4所示。从图4a)和b)中可看出原碳化钨粉体粒径在5 μm左右,且表面光滑,呈轮廓清晰的椭圆形。图4c)和d)是经粗化液粗化处理后的粉体,与原碳化钨粉体相比,粗化后的粉体表面由于受到强酸溶液的侵蚀后出现了较为清楚的沟壑和台阶状凹陷,这些缺陷的出现增大了碳化钨颗粒的比表面积,使化学共沉淀反应得到的NiC2O4·2H2O颗粒更容易附着到WC表面。图4e)和f)是通过化学共沉淀包覆反应得到的WC-NiC2O4·2H2O复合粉体,可见NiC2O4·2H2O颗粒在WC颗粒表面包覆得非常均匀且较为紧密。图4g)和h)是WC-NiC2O4·2H2O混合粉体在氢气氛围高温条件下反应后得到的WC-Ni复合粉体,可见WC颗粒保持了原料粉末的近球状形态,颗粒形貌较为完整,未发现明显的破碎和变形,镍相在WC颗粒表面包覆得较为均匀、致密。

图4 不同阶段粉末SEM形貌Fig.4 SEM morphology of powders at different stages:a) WC raw powders, at low magnification; b) WC raw powders, at high magnification; c) roughened WC powders, at low magnification;d) roughened WC powders, at high magnification; e) WC-NiC2O4·H2O composite powders, at low magnification;f) WC-NiC2O4·H2O composite powders, at high magnification; g) WC-Ni powders obtained after hydrogen reduction, at low magnification;h) WC-Ni powders obtained after hydrogen reduction, at high magnification
2.3 机理分析

图5 共沉淀反应的沉淀过程及机理示意图Fig.5 Schematic diagram of process and mechanism of precipitation by co-precipitation reaction
首先,晶核的生长速率和沉淀颗粒的大小与溶液中溶质的浓度密切相关,根据槐氏(Von Weiman)经验公式[16],料液浓度越高,产物颗粒之间的相互聚集越容易,沉淀生成的速率与溶液的相对过饱和度成正比。当料液浓度增大时,溶液的相对过饱和度变大,相同时间内成核的粒子数量增多,导致晶核之间相互碰撞几率增大,前驱体粒子间的团聚现象逐渐加剧[17]。另外沉淀生成速率太快还会导致表面吸附的杂质离子来不及被主沉淀的晶格离子取代,就被后来沉积上来的离子所覆盖,杂质离子就有可能陷入沉淀的内部,导致吸留现象的发生。
其次,在化学共沉淀反应中,共沉淀反应沉淀率随反应温度的升高先增大后减小[18]。这是因为当温度很低时,溶质分子的能量很低,导致NiC2O4·2H2O 晶粒的生成速率很小,所以沉淀率较低。随温度升高,一方面溶质分子的能量逐渐升高,导致晶粒的生成速率逐渐增大,但另一方面温度升高会引起过饱和度降低,从而使得沉淀成核速率减慢,有利于晶核的长大,得到的沉淀比较紧密。继续升高温度,会导致生成的NiC2O4·2H2O晶粒在溶液中的溶解度增大,同时也引起溶液中分子动能增加过快,不利于形成稳定的晶粒,因此晶粒的生成速率又趋于下降[19]。而且过高的温度一方面会导致沉淀物的溶解度增大,另一方面,由于吸附是一放热过程,因此,过高的溶液温度会降低WC颗粒表面的吸附效果,从而会降低沉淀率并影响包覆效果[20]。
最后,在化学共沉淀反应中,沉淀剂加入体积流量越大,产物颗粒之间的相互聚集也越容易,这是因为沉淀剂加入体积流量越大瞬间成核的NiC2O4·2H2O粒子数量就越多而粒径却变得越小,导致粒子之间相互碰撞几率增大且更容易相互黏结。沉淀剂若分散加入,而且加料的速率较小,同时进行搅拌,可避免溶液局部过浓而形成大量晶核,有利于制备纯度较高的晶形沉淀[21]。
3 结论
(1) 适当料液浓度下,产物颗粒之间的相互聚集越容易,相同时间内成核的粒子数量增多,导致晶核之间相互碰撞几率增大,使得包覆效果变好;料液浓度为0.4 mol·L-1NiCl2、0.2 mol·L-1(NH4)2C2O4时反应生成的前驱体颗粒表面包覆效果和分散性最佳。
(2) 随温度升高,一方面溶质分子的能量逐渐升高,导致晶粒的生成速率逐渐增大,但另一方面温度升高会引起过饱和度降低,从而使得沉淀成核速率减慢,有利于晶核的长大,得到的沉淀比较紧密;反应温度为50 ℃时化学共沉淀反应能获得较好的包覆效果、最大的颗粒粒径和较高的沉淀率。
(3) 当沉淀剂加入体积流量越大时,瞬间成核的NiC2O4·2H2O粒子数量就越多而粒径却变得越小,导致粒子之间相互碰撞几率增大更容易相互黏结。沉淀剂若分散加入,而且加料的体积流量较小,同时进行搅拌,可避免溶液局部过浓而形成大量晶核,有利于制备纯度较高的晶形沉淀。沉淀剂加入体积流量为0.17 mL·s-1时反应生成的前驱体颗粒表面包覆效果和分散性最佳,且能获得最高沉淀率。
(4) 当沉淀剂的加入体积流量过大可能使得溶液局部浓度过高,产生团聚或组成不够均匀。另外沉淀生成速率太快还会导致表面吸附的杂质离子来不及被主沉淀的晶格离子取代,就被后来沉积的离子所覆盖,则杂质离子就有可能陷入沉淀的内部,导致吸留现象的发生。

