不同热解温度制备的鸽粪生物炭对水中甲砜霉素的吸附性能
康雅欣,亢 昕,李东鹏,孙铸宇,宋新山,赵晓祥
(东华大学 环境科学与工程学院, 上海 201620)
甲砜霉素(thiamphenicol,TAP)属于第二代氯霉素类广谱抗菌药物,是一种与其他抗生素无交叉耐药性的强免疫抑制剂。与氯霉素相比,TAP具有更强的体内活性,更高且持久的血药浓度,更好的水溶性和稳定性,更容易在环境中稳定存在[1]。20世纪90年代,TAP由欧洲引入我国,开始在临床医学、兽医学中被广泛使用。近年来,TAP在各种水环境中被频繁检出,并可能会随环境水体交换而最终进入饮用水源中[2-3]。研究[4]表明TAP对人体造血系统、消化系统具有毒性作用,长期微量摄入可能导致腹泻、恶心、呕吐等胃肠道不良反应,甚至引起机体正常菌群失调,致使机体感染疾病。
据报道,纳米滤膜过滤[5]、光催化和芬顿氧化等技术[6]能有效去除水环境中的TAP,但其成本较高且会生成中间副产物。吸附法[7]是一种能耗低、效率高、绿色经济的水污染处理方法,但其去除效率很大程度上取决于吸附剂的选择。生物炭是生物质在200~900 ℃缺氧或无氧条件下,经热化学转化得到的固体物质[8],因原料廉价易得、制备工艺相对简单,常作为吸附剂和土壤改良剂应用于污染环境处理。植物废弃物[9-10]、动物凋落物[11]、污水污泥[12]等多种生物质尾料都能作为生物炭的原料。Wang等[13]用蒸汽活化法制备竹炭生物炭吸附四环素,最高去除率为95.75%;Tzeng等[14]在800 ℃热解条件下制备了牛粪生物炭,对磺胺甲嘧啶的最大吸附量达39 mmol/kg。
我国是全球范围内主要的肉鸽生产国,2017年商品肉鸽产量为6.26亿只。肉鸽常以谷物为食,粪便中含有丰富的N、P、K等营养元素,是优良的天然有机肥,但大规模集约化养殖中产生的大量粪便若直接归田堆肥,易导致土壤酸碱失调、农作物病害等问题。鸽粪经高温热解处理获得生物炭,其不仅可以消杀微生物、分解抗生素[15],还能实现废弃物资源化,增加肉鸽养殖副产品收益。以鸽粪为生物质原料,探究不同热解温度对鸽粪生物炭理化性质的影响,并通过元素分析、扫描电子显微镜(scanning electron microscope, SEM)、傅里叶变换红外光谱(Fourier transform infrared spectroscopy, FT-IR)等手段对生物炭形貌、结构进行表征。考察吸附剂投加量、污染物初始浓度、pH值、离子强度等因素对鸽粪生物炭吸附TAP的影响,对吸附过程进行动力学、热力学和等温拟合。旨在为生物炭吸附水环境中氯霉素类抗生素的应用研究提供依据,并为动物凋落物资源化利用开拓思路。
1 材料与方法
1.1 生物炭的制备
试验用鸽粪取自河南省洛阳市李村镇肉鸽养殖基地,粗选去除鸽羽后,经粉碎机粉碎过20目(孔径为0.85 mm)筛。在预试验的基础上,将上述干燥鸽粪粉末装入瓷坩埚,轻微压实,平推盖入坩埚盖以营造缺氧环境,置于马弗炉中以10 ℃/min的速率升温至600、700、800 ℃,限氧热解5 h,冷却后取出研磨过80目(孔径为0.18 mm)筛入封口袋,分别命名为P600、P700、P800,干燥器内保存待用。
1.2 生物炭的表征
鸽粪生物炭表面形貌采用场发射扫描电子显微镜(S-4800型,日本)测定;比表面积与孔径采用快速比表面积及孔径测定仪(Autosorb-iQ型,美国)测定,N2吸-脱附测试在温度为77 K条件下进行;C、H、N元素质量分数采用元素分析仪(VarioELⅢ型,德国)测定,O元素质量分数由差减法计算得出;灰分及pH值测定参考生物质固体成型燃料试验方法[16]中灰分及pH值的测定;表面基团采用傅里叶变换红外光谱仪(Tensor型,德国)定性测得;零点电荷由Zeta电位仪(NanoBrook 90型,美国)测得。
1.3 TAP的测定
TAP质量浓度测定利用Thermo U3000型高效液相色谱(high performance liquid chromatography,HPLC)工作站,DAD检测器,Waters Atlantis T3 C18反相色谱柱,流动相为乙腈∶水(体积比20∶80),流速为1 mL/min,柱温为30 ℃,进样量为20 μL,检测波长为226 nm。
1.4 TAP吸附试验
1.4.1 吸附动力学试验
准确称取0.050 g生物炭置于150 mL锥形瓶中,加入100 mL质量浓度为20 mg/L的TAP溶液,置于25 ℃、120 r/min的恒温水浴振荡器中振荡吸附,分别于0.05、0.10、0.16、0.33、0.67、1.00、1.50、2.00、2.50、3.00、4.00、6.00、8.00、10.00 h取样,过孔径为0.22 μm水系滤膜后,通过HPLC工作站定量测定TAP质量浓度。
1.4.2 吸附热力学试验
准确称取0.025 g生物炭置于100 mL锥形瓶中,加入50 mL质量浓度分别为2、5、10、15、20、25、30 mg/L的TAP溶液,分别置于25、35、45 ℃,转速为120 r/min的水浴振荡器中振荡吸附4 h取样,过孔径为0.22 μm水系滤膜后,通过HPLC工作站定量测定TAP质量浓度。
1.4.3 影响因素试验
经预试验,生物炭的最佳投加量和TAP初始质量浓度分别为0.5 g/L和20 mg/L,在此条件下探究:
(1) pH值影响,溶液pH值采用HCl和NaOH调节,pH值调节范围为2.0~11.0;
(2) 离子强度影响,对应称量使吸附体系内分别含有0、0.01、0.10、0.20、0.50 mg/L的NaCl溶液。
上述试验不特别说明均在温度为25 ℃和转速为120 r/min水浴振荡条件下进行,除pH值影响因素试验外,其他试验体系pH值均不调,每组做3次平行试验,并设有不添加生物炭的TAP空白对照组。
1.5 数据处理
生物炭产率(Y)计算如式(1)所示。
(1)
式中:m和m0分别为鸽粪生物炭和鸽粪原料的质量,g。
生物炭对TAP的吸附率(R)和吸附量(q)计算如式(2)和(3)所示。
(2)
q=(ρ0-ρe)V/m1
(3)
式中:ρ0和ρe分别为TAP的初始质量浓度和平衡质量浓度,mg/L;V为体系中TAP溶液的体积,L;m1为生物炭投加量,g。
吸附动力学数据采用准一级、准二级、Elovich[17]、粒子内扩散[18]方程进行拟合,方程分别如式(4)~(7)所示。
qt=qe(1-e-k1t)
(4)
qt=k2tqe2/(1+k2tqe)
(5)
(6)
qt=k′it1/2+ci
(7)
式中:qt和qe分别为生物炭对TAP在t时刻的吸附量和平衡吸附量,mg/g;t为吸附时间,min;k1为准一级动力学模型速率常数,h-1;k2为准二级动力学模型速率常数,g/(mg·min);α为初始吸附速率,mg/(g·h);β为与表面覆盖度有关的常数g/mg;k′i为粒子内扩散模型的速率常数;ci为方程的截距,与边界层厚度有关。
吸附等温数据采用Langmuir和Freundlich方程进行拟合,方程如式(8)和(9)所示。
qe=qmKLρe/(1+KLρe)
(8)
qe=KFρe1/n
(9)
式中:qe为生物炭对TAP的平衡吸附量,mg/g;ρe为吸附平衡时TAP的质量浓度,mg/L;qm为理论最大单分子层吸附量,mg/g;KL为Langmuir模型的吸附常数,mg/L;KF为Freundlich模型的参数,mg1-n/(g·Ln);n为Freundlich模型的常数,代表吸附强度。
热力学计算[11]如式(10)和(11)所示。
ΔG=-RTlnK
(10)
lnK=ΔS/R-ΔH/RT
(11)
式中:ΔG为吉布斯自由能变,kJ/mol;ΔS为熵变,J/(mol·K);ΔH为焓变,kJ/mol;K为热力学平衡常数,L/g;R为理想气体常数,R=8.314 J/(mol·L);T为开尔文温度,K。
2 结果与讨论
2.1 鸽粪生物炭的主要元素组成及表面特性
2.1.1 元素组成分析
鸽粪生物炭(P600、P700、P800)的产率、元素组成、灰分、pH值、比表面积和孔径结果如表1所示。由表1可知,鸽粪生物炭中C元素质量分数随热解温度的升高而降低,当热解温度由600 ℃升高到800 ℃,鸽粪生物炭中C元素质量分数由50.53%下降到33.53%,这与以往一些动物源生物炭的研究结果一致[11, 19]。H/C、O/C、(O+N)/C的比值可作为评价生物炭芳香性、亲水性和极性的活性指数[20],其中,H/C数值越小则说明生物炭的芳香性越强、炭化程度越高,O/C和(O+N)/C数值越大则说明生物炭表面亲水性和极性越强。由表1可以看出,随热解温度的升高,鸽粪生物炭表面芳香性无明显变化,而亲水性和极性由弱变强。

表1 鸽粪生物炭的物理化学性质Table 1 Physico-chemical characteristics of pigeon feces biochars
2.1.2 SEM图和BET孔径分析
通过扫描电镜图以及比表面积和孔径测试结果,可从微观上对生物炭结构和表面形态进行分析。3种鸽粪生物炭的SEM图如图1所示。由图1可以看出:P600表面粗糙,呈碎片颗粒状,分布较为无序;P700表面出现较发达的明显孔洞;P800表面的片状结构消失,呈现分布较为规整的绒状突起,可能是由于细小孔隙增多且更密集。结合表1可知,热解温度由600 ℃升高至800 ℃,P800的比表面积和微孔面积分别为P600的2倍和3倍左右。由此表明,在一定范围内提高热解温度,鸽粪生物炭表面孔隙发育更完全,比表面积更大,微孔数量更多,这与扫描电镜观察的变化结果一致。比表面积和孔隙分布在一定程度上会直接影响生物炭对污染物的吸附[21],Tzeng等[14]的研究也发现,800 ℃制备的牛粪生物炭比表面积明显大于400和600 ℃制备的生物炭,前者对磺胺甲嘧啶的吸附效果更好。因此生物炭的结构和吸附性能受热解温度影响,在适当范围内改变热解温度能够改良生物炭表面特性,提高其对污染物的吸附能力。

(a) P600
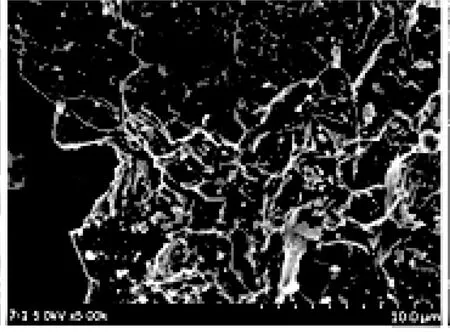
(b) P700
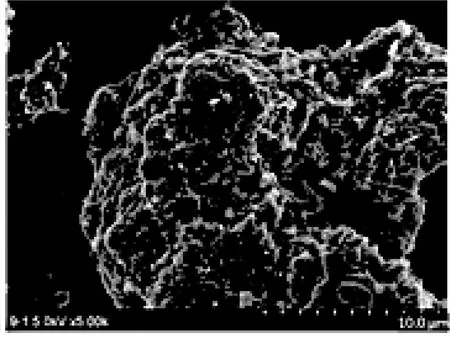
(c) P800图1 鸽粪生物炭的扫描电镜图(×5 000倍)Fig. 1 SEM images of pigeon feces biochars(×5 000 times)
2.1.3 FT-IR分析
3种鸽粪生物炭的FT-IR图谱如图2所示。由图2可知,3种鸽粪生物炭表面均含有丰富的含氧官能团,3 456 cm-1附近为羧基、酚羟基的—OH伸缩振动吸收峰[22],1 635 cm-1附近为—COOH的对称与反对称伸缩振动吸收峰,1 550 cm-1附近为羰基的CO伸缩振动吸收峰[23],1 039和1 095 cm-1附近为含氧官能团C—O和N—H的伸缩振动吸收峰[24],873 cm-1附近为芳环中C—H面内弯曲振动吸收峰,462 cm-1附近为无机盐组分Si—O—Si键伸缩振动吸收峰等。
热解温度由600 ℃升高至800 ℃时:—OH(3 456 cm-1)和C—O(1 039 cm-1)的伸缩振动吸收峰明显增强且更加窄而尖锐,这可能是由于更高的热解温度使生物炭表面形成了更多且能够在该位置产生特征吸收的含氧官能团[25];550~850 cm-1

图2 鸽粪生物炭傅里叶变换红外光谱图Fig. 2 FT-IR spectra of pigeon feces biochars
内的吸收峰则变得更为丰富,这主要是因为热解温度的提升使生物炭含有更多且更复杂的灰分,灰分中无机物质的不同官能团在该红外区域表现岀相应的特征吸收[26];938 cm-1附近出现了新的吸收峰,该位置的峰由含磷官能团PO或P—C的特征吸收产生[27],这可能是由于鸽粪中含有的P元素在高温条件下能够更好地键合到生物炭表面;873 cm-1处芳环中C—H面内弯曲振动峰[28]一直存在,且大小无差异,进一步证明生物炭芳香程度在不同热解温度条件下无明显差异,与表1中H/C比值无明显变化结论一致。
2.2 pH值对鸽粪生物炭吸附TAP的影响
溶液pH值不仅会影响生物炭的表面电荷,还会影响有机化合物在溶液中的存在形态[29],进而表现出吸附效果的差异。不同pH值条件下3种鸽粪生物炭对TAP的平衡吸附量如图3所示。由图3可知:在pH值为2.0~3.0的水环境中,鸽粪生物炭对TAP的平衡吸附量较高;在pH值为4.0~11.0的水环境中,TAP的平衡吸附量仅出现无规律的小幅度上下波动,无明显变化。

图3 pH值对TAP吸附量和鸽粪生物炭的Zeta电位的影响Fig. 3 Effects of pH value on TAP adsorption and Zeta potential of pigeon feces biochar
TAP为极性有机化合物,只有一个解离常数(pKa=11.05±0.45)。在水溶液pH值低于其pKa值的条件下,TAP主要以非电离形态存在。因此,相较于其他易电离的化合物,pH值的变化(4.0~11.0)对TAP的吸附整体影响较小,TAP分子与鸽粪生物炭之间的静电作用相对较弱。但由于TAP分子内含有—Cl、—NH—、—OH、苯环等基团,静电作用在吸附过程中仍具有一定的影响。尤其是在生物炭的零电荷点附近,溶液pH值的升高使得吸附剂表面带负电,此时由于TAP分子内的—NH—易发生质子化作用而带正电,与表面带负电的吸附剂静电作用增强,因此在鸽粪生物炭的零电荷点附近,TAP的平衡吸附量最大。随着溶液pH值继续升高,TAP分子的正电性减弱,静电作用减弱,而有机化合物的疏水性增强[30-31],使其更容易迁移到吸附剂表面,因此,TAP的平衡吸附量略有下降,随后保持基本稳定。由于P600、P700、P800的零电荷点对应的pH值略有差异,TAP的最大平衡吸附量所对应的pH值也有所不同。
2.3 离子强度对鸽粪生物炭吸附TAP的影响
溶液中盐离子(NaCl)强度对鸽粪生物炭吸附TAP的影响结果如图4所示。

图4 NaCl质量浓度对TAP吸附量的影响Fig. 4 Effect of NaCl mass concentration on TAP adsorption
由图4可知,对于P800而言,NaCl质量浓度由0增加至0.20 mg/L,TAP的吸附量由29.6 mg/g增加到35.2 mg/g,随着NaCl质量浓度继续增加到0.50 mg/L,吸附量减少至31.4 mg/g,但仍高于未加入NaCl的对照组。这可能是由于低质量浓度NaCl的加入使溶液中的TAP分子溶解度降低,疏水作用增强,即发生了“盐析作用”,有助于TAP分子在吸附剂表面的扩散[32];而当盐离子质量浓度继续增大,TAP分子与盐离子之间会产生“竞争作用”,盐离子占据了部分吸附剂表面的活性位点,使吸附剂对TAP的吸附量降低[33],但仍高于未加入盐离子的对照组。由此表明,“盐析作用”和“竞争作用”都会影响P800对TAP的吸附过程,且“盐析作用”影响程度强于“竞争作用”,因此在生物炭对TAP的吸附机制中,疏水作用可能占主导地位,静电作用相对较弱。对P700而言,盐离子加入对其影响与P800相似,也是整体表现出平衡吸附量先增大后减小的变化规律。但是,分析P600的试验结果发现,盐离子的加入会整体降低其对TAP的平衡吸附量,随盐离子质量浓度的增加,吸附量先增大后减小,且一直低于未添加盐离子的对照组,说明“竞争作用”占主导地位。这可能是由于P600比表面积小,有效活性吸附位点少,相较于另外两种生物炭,其更易形成“竞争作用”。
2.4 吸附动力学
吸附动力学可用于描述吸附速率的快慢,本研究采用准一级、准二级、Elovich、粒子内扩散方程对3种鸽粪生物炭吸附TAP的动力学过程进行模拟,曲线及拟合参数分别见图5及表2。

图5 鸽粪生物炭对TAP的吸附动力学方程拟合Fig.5 Kinetic equation fitting for TAP adsorption on pigeon feces biochars

表2 鸽粪生物炭对TAP的动力学拟合参数Table 2 Kinetic fitting parameters for TAP adsorption on pigeon feces biochars
由图5(a)可知,在25 ℃和TAP初始质量浓度为20 mg/L的条件下,P600、P700、P800对TAP的吸附量随吸附时间延长表现出一致的变化规律,即初期快速吸附,中期吸附速率逐渐降低,4 h后吸附量趋于稳定达到吸附平衡。吸附初期,吸附剂表面与溶液中污染物浓度差异最大,传质驱动力大,更有利于液体内的TAP向固体表面迁移[34],此时吸附速率最快。当吸附时间相同时,P800的吸附量高于P700和P600。这主要是因为更高热解温度制备的鸽粪生物炭具有更大的比表面积和总孔体积以及更丰富的表面官能团,在相同污染物浓度的条件下,能够提供更多的吸附位点。
对比表2中不同动力学方程的拟合参数,Elovich模型的相关系数R2均大于0.97,高于准一级和准二级动力学的R2,因此Elovich模型能够更好地描述鸽粪生物炭吸附TAP的动力学过程,说明吸附剂具有不均匀的表面。由图1也可以看出,鸽粪生物炭对TAP的吸附是发生在不均匀表面的多相化学吸附过程[35]。
为进一步确定鸽粪生物炭对TAP吸附过程的速率控制因素,采用粒子内扩散模型对动力学数据进行拟合,结果见图5(b),参数见表2。由图5(b)可以看出,鸽粪生物炭对TAP的吸附过程主要分为3个阶段:第1阶段为快速反应的液膜扩散阶段(前40 min),液体中的TAP穿透液膜到达鸽粪生物炭外表面;第2阶段为孔扩散阶段(40~180 min),主要是TAP分子通过粒子内扩散在生物炭孔隙内发生迁移;第3阶段为吸附反应阶段,一般发生在生物炭内表面[36]。拟合方程中的常参数ci代表边界层的厚度,其值为0即拟合线条过原点,粒子内扩散是吸附过程的唯一控速步骤[37],否则还存在其他的控速机制。由表2可知,3种鸽粪生物炭吸附TAP过程的ci值均不为0,且越接近吸附平衡,粒子内扩散速率常数k′i值越小(k′1>k′2>k′3),表明随吸附时间的延长则粒子内扩散作用逐渐减弱[38],且粒子内扩散并不是鸽粪生物炭对TAP吸附过程中唯一的控制步骤[30],液膜扩散和表面吸附也会影响吸附速率[18]。
2.5 等温吸附拟合
质量浓度为0.5 mg/L的鸽粪生物炭对不同初始质量浓度TAP的平衡吸附量如图6所示。

图6 鸽粪生物炭对TAP的吸附等温线拟合Fig. 6 Adsorption isotherm fitting for TAP adsorption on pigeon feces biochars
由图6可知:当TAP初始质量浓度由2 mg/L提高到15 mg/L时,P600、P700、P800对TAP的平衡吸附量快速增大;当TAP初始质量浓度大于20 mg/L时,平衡吸附量变化均趋于平缓,吸附达到饱和,P600、P700、P800饱和吸附量分别为5.37、14.97和30.30 mg/g。Fan等[38]利用比表面积更大的颗粒活性炭(944.71 m2/g)对TAP进行吸附,其最大饱和吸附量为28.06 mg/g,低于本研究所制备的P800鸽粪生物炭,表明生物炭具有成为TAP高效吸附剂的潜质。
使用Langmuir和Freundlich两种模型对25 ℃不同TAP初始质量浓度的吸附数据进行拟合,拟合参数如表3所示。由表3可知,相较Langmuir模型而言,Freundlich模型具有更大的相关系数R2,且随热解温度的升高,相关系数R2逐渐减小,表明Freundlich模型能够更好地描述鸽粪生物炭对TAP的吸附过程,热解温度越低则拟合效果越好。Freundlich模型是一种经验模型,常用于描述多分子层吸附[39],经其计算得到的参数KF的大小与结合能有关,KF值越大对吸附过程越有利[40],即吸附剂与TAP的结合能为P800>P700>P600,与动力学试验结果表现一致。综上可知,不同热解温度制备的鸽粪生物炭对TAP的吸附均为多层吸附过程,TAP分子会使吸附剂表面结构发生变化,促进吸附剂对其进行吸附[41]。

表3 鸽粪生物炭吸附TAP的等温线拟合参数Table 3 Isotherm parameters for TAP adsorption on pigeon feces biochars
2.6 吸附热力学
3种鸽粪生物炭吸附TAP的热力学拟合参数如表4所示。由表4可知,P600的吉布斯自由能变(ΔG)为正值,P700和P800的ΔG为负值,表明在所研究的温度条件下,P600对TAP的吸附为非自发过程,P700和P800对TAP的吸附为自发过程[42],进一步解释了相同温度条件下,P600对TAP的吸附量明显低于另外两种鸽粪生物炭的现象。一般来说,氢键作用、静电相互作用、范德华力所对应焓变值(ΔH)理论范围分别为2~40、20~80和4~10 kJ/mol[43]。本研究热力学拟合得到的P700、P800的ΔH为正且较小,说明P700、P800参与的吸附过程为吸热反应,温度升高有利于吸附反应的进行[44],氢键作用以及范德华力作用是吸附过程中主要的作用机制,静电相互作用可能存在但占比较小。熵变(ΔS)用于描述体系混乱度的变化,由表4可知,3种鸽粪生物炭的ΔS均大于0,表明吸附过程中吸附剂-水相界面的混乱度增大,结合动力学研究结果可知,鸽粪生物炭吸附TAP的过程同时存在化学吸附和物理吸附作用。
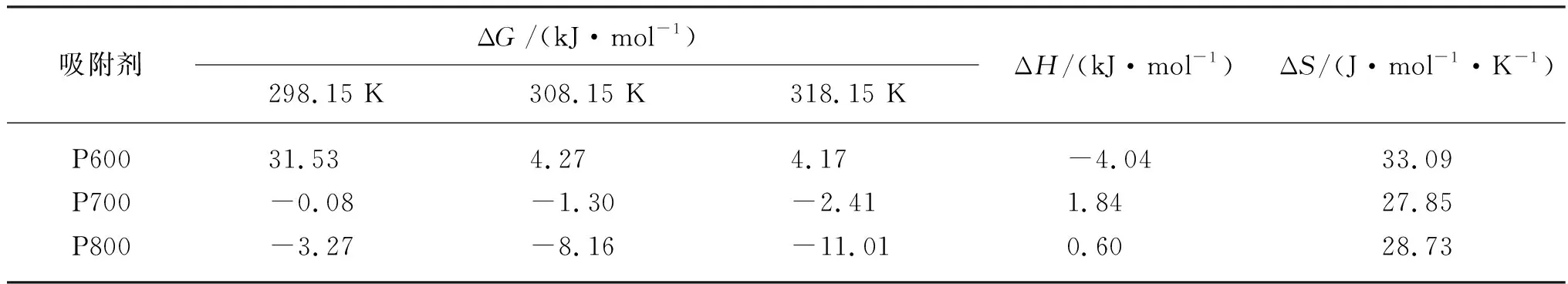
表4 鸽粪生物炭吸附TAP的热力学拟合参数Table 4 Thermodynamics parameters for TAP adsorption on pigeon feces biochars
3 结 论
(1)鸽粪生物炭的热解温度对其元素组成、表面形貌、官能团和理化性质有重要影响,随热解温度的增加,生物炭pH值升高,C元素质量分数降低,O元素质量分数升高,比表面积增大,芳香性无明显变化,亲水性、极性增强。
(2)较低的溶液pH值更有利于鸽粪生物炭对TAP的吸附,盐离子的加入能够提高P800、P700对TAP的吸附量,但对P600存在轻微抑制。
(3)鸽粪生物炭对TAP的吸附过程可分为3个阶段,平衡吸附量为P800>P700>P600,最佳吸附条件下,P800对TAP的平衡吸附量为33.63 mg/g,Elovich动力学方程和Freundlich等温方程对吸附过程的拟合度更高,3种鸽粪生物炭吸附TAP的过程是发生在不均匀表面的多相、多层化学吸附。
(4)综合分析鸽粪生物炭和TAP的结构,以及吸附动力学、热力学、影响因素等试验结果,鸽粪生物炭对TAP的吸附机制主要包括大的比表面积和丰富的孔结构提供的物理吸附,以及吸附剂与吸附质之间的疏水作用和氢键作用,同时也可能存在部分静电相互作用的化学吸附机制。

