人类遗传资源管理的现状与实践思考
胡爱珍,张雪,齐苗苗,陈亚玲,杨钟平
·调查与研究·
人类遗传资源管理的现状与实践思考
胡爱珍,张雪,齐苗苗,陈亚玲,杨钟平
400036 重庆市公共卫生医疗救治中心
人类遗传资源的研究和利用已成为当下认识生命和控制生命的关键途径[1]。然而,近年来,随着基因测序技术及信息技术的快速发展,人类遗传资源的非法采集、收集和攫取方式已由传统人体组织、细胞等实体样本转向人类基因序列等遗传信息,非法出境途径也由携带基因样本出境转变为通过互联网将基因数据发往国外[2]。国外各主要发达国家早已关注到人类遗传资源的重要性,在人类遗传资源领域已经普遍建立起了较完善的管理体系。基于我国多民族、多人口的特征,我国具有独特的人类遗传资源优势,为阻断人类遗传资源的流失,我国陆续出台了各相关法律法规以加强对人类遗传资源的保护,促进合理利用。本文将结合国内外有关人类遗传资源的法律法规和监管政策,对本中心的人类遗传资源管理情况进行分析和探讨。
1 国际人类遗传资源管理策略
目前,全球至少 60 个国家和地区已通过立法或制定指导原则对人类遗传资源活动进行规范管理。各主要发达国家已经普遍建立起了较完善的人类遗传资源管理体系,相较于发展中国家的人类遗传资源保护管理,发达国家更注重人类遗传资源的利用管理[2]。
国际人类遗传资源管理经典模式涉及的主要管理策略是制定人类遗传资源相关法律法规和指导原则,同时设立人类遗传资源管理机构,从国家战略层面加强对人类遗传资源采集、保藏、利用、信息对外提供活动的监管[2]。例如,美国通过联邦政府出台了《健康保险便利和责任法案》(HIPAA)、《反基因歧视法》和《胚胎组织移植研究公法》等法律法规,对基因专利、人类遗传资源的隐私安全和研究管理等作了相关规定,同时设立卫生与人类服务部(HHS)、美国食品药品监督管理局(FDA)和美国国立卫生研究院(NIH)分别作为人类遗传资源活动的宏观管理机构、重要监管机构和研究利用机构[3]。
其次,在立法和政策实践中以契约来规范人类遗传资源的转移,即采用材料转移协议等方式加以管理。例如,NIH 专门制定了标准生物材料转移协议,用于规范科研项目中人类遗传资源的转移行为[4]。
最后,建立国家级的人类遗传资源相关基础设施,在夯实管理的前提下,加强资源共享、开发和利用[2]。英国 2003 年建立的英国生物样本库(UK Biobank),是一个储存有海量生物样本与数据的人类遗传资源库, 旨在对中老年疾病的遗传和非遗传决定因素进行研究,是目前全球最大的生物样本库[5]。另外,加拿大、日本以及许多欧洲国家都已建有国家级的生物样本库[4]。
2 我国人类遗传资源管理现状
近年来,涉及人类遗传资源的生物技术研究活动出现了一系列新情况、新问题,这使我国的人类遗传资源管理面临更高要求。1998 年科技部、原卫生部联合制定的《人类遗传资源管理暂行办法》虽然填补了我国人类遗传资源管理的空白,但是仍存在立法位阶和效力等级不够高、法律责任不健全、处罚条款不明确等问题。为解决上述突出问题,国务院于 2019 年 5 月出台了《中华人民共和国人类遗传资源管理条例》(以下简称“《条例》”),并已于 2019 年 7 月 1 日开始施行。这一行政法规的出台及时为我国人类遗传资源管理提供了新的法制遵循[6]。继《条例》正式施行以后,2020 年 10 月 17 日颁布的《中华人民共和国生物安全法》(以下简称“《生物安全法》”)规定了保障人类遗传资源和生物资源安全方面的内容,尤其是对中国人类遗传资源的国际合作临床试验备案相关规定再次进行了明晰。《生物安全法》于 2021 年 4 月 15 日开始施行,可以预见,配套法规及监管政策将会进一步完善。《中华人民共和国数据安全法》也于 2021 年 6 月出台,自 2021 年 9 月 1 日起施行。该法的实施对涉及人类遗传资源相关活动又有了进一步的规范,使人类遗传资源信息在《条例》和《生物安全法》的基础上多了一层管束。
对于违反《条例》的处罚措施主要有责令停止违法行为,没收违法采集、保藏的人类遗传资源和违法所得以及罚款等行政处罚,情节严重的,禁止其从事采集、保藏、利用、对外提供我国人类遗传资源的活动。2020 年 12 月 26 日发布的《中华人民共和国刑法修正案》首次将人类遗传资源写入刑法,加大了对人类遗传资源的监管力度。《生物安全法》也明确了相应的行政处罚以及相关刑事责任和民事责任。在此背景下,涉及人类遗传资源管理的单位有必要重点关注相关立法与执法动态,加强有关人类遗传资源管理的合规建设。
3 实际问题应对措施
3.1 加强本中心人类遗传资源活动管理的新举措
3.1.1 建立管理制度,明确审批部门 为加强对人类遗传资源的规范管理,本中心成立了人类遗传资源管理办公室,负责审批本中心涉及人类遗传资源的临床研究。中心人类遗传资源管理办公室制订了《人类遗传资源管理制度》《人类遗传资源管理的标准操作规程》等规章制度,并加强对临床研究的监管,以确保临床研究中人类遗传资源管理的标准化、规范化和系统化。凡我中心所有涉及人类遗传资源采集、保藏、利用、对外提供等的科学研究活动,必须遵守人类遗传资源管理制度。
3.1.2 建立审查流程,保证申报资料的真实性和规范性 中心人类遗传资源管理办公室对审批流程进行了优化,申报资料须先经中心人类遗传资源管理办公室形式审查,再由办公室审查员对其真实性和规范性作进一步审查,最后经办公室主任审核通过后正式提交科技部,以确保申请资料能符合科技部的要求,从而提高申报的通过率,加快申报进程,助力临床研究开展。另外,为确保实际工作能符合人类遗传资源相关法律法规的要求,中心人类遗传资源管理办公室配备 1 名秘书,由专人担任并负责申请资料的形式审查和资料存档管理,同时配备了多名审查员,以保证申请资料审查的及时性和全面性(图 1)。
3.1.3 进一步加强国际合作项目管理 随着现代生物技术的快速发展,涉及人类遗传资源的国际科技合作日益增多[7]。严格按照《条例》及行政服务指南办理报批手续,并按照报批范围开展研究,是切实避免人类遗传资源违法违规使用的重要保障。《条例》中有指出,外方单位包括外国组织及外国组织、个人设立或者实际控制的机构。然而,我们在实际工作中发现,部分公司对外方单位的界定认识不清。为了更好实施《条例》,本中心人类遗传资源管理办公室通过以下措施加强公司外资背景管理:①公司进行自我确认,若无外资背景应提供无外资承诺书;②中心人类遗传资源管理办公室对公司提供的相关资料进行调研确认;③如有必要向中国人类遗传资源管理办公室咨询或上报。为更好地保护人类遗传资源,我们要确保申请资料的真实性,始终坚持准确获知公司是否具有外资背景后才能批准开展临床试验的原则。
3.2 本中心人类遗传资源管理现存问题及其相关改进建议
中心人类遗传资源管理办公室结合有关药物、医疗器械和体外诊断试剂临床试验的人类遗传资源审批经验,总结出几个有待进一步改善的问题,这些问题也应当在我们今后的工作中引起足够重视。
3.2.1 需提高研究者对人类遗传资源管理的认识和审查员的审查能力 随着国家对人类遗传资源的申报要求和监管力度的不断加强,我们对人类遗传资源的培训需求也逐步增加,需进一步提高研究者对人类遗传资源管理的认识和审查员的审查能力。大多数研究者对人类遗传资源管理的认知度并不高,对人类遗传资源的保护意识也较为薄弱[8]。中心人类遗传资源管理办公室需对研究者进行有针对性的人类遗传管理专项培训,强化法律意识,加强对人类遗传资源行政许可及备案的宣传和培训,使研究者逐渐意识到人类遗传资源申报在临床研究中的重要性与必要性。研究者是临床研究的实施主体,也是人类遗传资源采集、收集、使用和销毁等过程的操作者,提高研究者的人类遗传资源申报意识显得至关重要,研究者的法律意识和人类遗传资源相关知识认知的提高将可避免项目漏报情况,并提高填报资料的规范性和准确性[8]。由于大多研究者对人类遗传资源行政许可及备案的相关法律法规解读不深入、不全面,办公室审查员的审查工作在申请办理中也起着重要的作用。办公室审查员应不断学习人类遗传资源行政许可及备案的相关法律法规,并在实践中互相交流和总结经验,提升自身的审查能力,进一步确保填报资料的规范性和真实性。
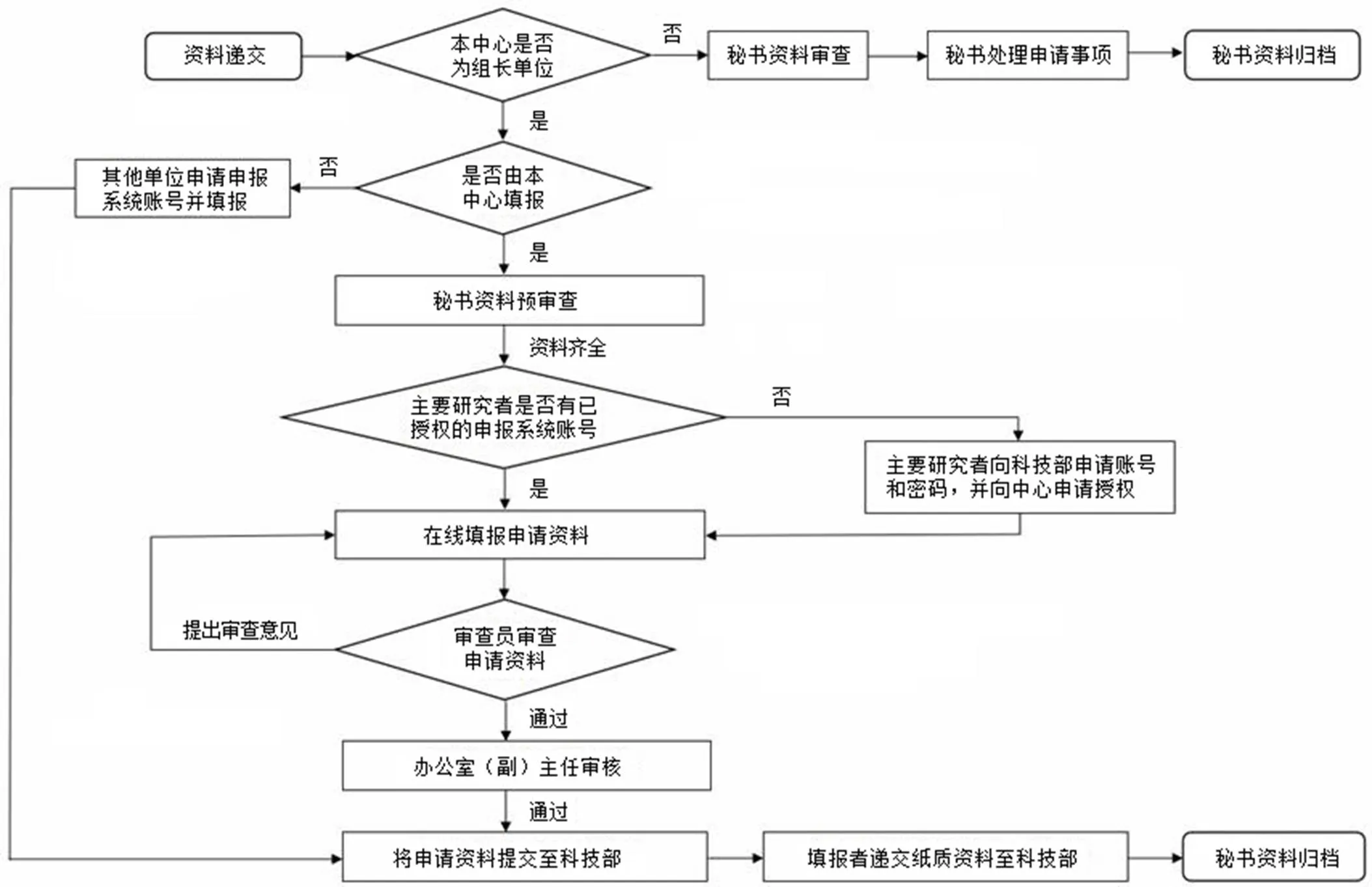
图 1 本中心人类遗传资源的审批流程
3.2.2 需加强监督第三方检测机构生物样本的使用情况 医疗机构由于无法及时而全面地获取第三方检测机构的样本使用管理情况,不能行之有效地对第三方检测机构的样本销毁及接收情况进行监督[9]。美国通过制定标准生物材料转移协议,对科研项目中人类遗传资源材料转移进行规范和管理[2]。目前本中心采用材料转移合同加以管理,即与申办者签订合同来规定各方的权利义务,合同中表明送至中心实验室的生物样本或剩余样本未经允许超范围检测,申办者应承担相关法律责任。对于生物材料转移合同内容,本中心将作进一步完善。同时,借鉴其他医院的管理经验,可要求在样本销毁后由申办者递交销毁记录。如有屡次发生样本管理缺陷的情况,则及时上报中国人类遗传资源管理办公室[9]。
3.2.3 需不断加强临床研究的人类遗传资源信息监管 《条例》明确了人类遗传资源包括人类遗传资源材料和人类遗传资源信息,并规定了中国人类遗传资源信息对外提供或开放使用应当向国务院科学技术行政部门备案并提交信息备份。《民法典》第111条规定,自然人的个人信息受法律保护。这意味着采集公民个人的人类遗传资源信息,属于《民法典》的保护范围。《中华人民共和国数据安全法》的实施又将对人类遗传资源相关活动作进一步规范。因此,为了使临床研究的开展能够遵守相关法律法规,本中心将不断加强临床研究的人类遗传资源信息监管。不仅要严格管理人类遗传资源信息对外提供或开放使用的信息备份及备案,而且要基于准确认识人类遗传资源的概念,对于仅涉及采集人类遗传资源信息的临床研究要进行严格监管,避免出现漏报情况。
4 结语
随着涉及人类遗传资源的研究活动迅速增长,我国通过制定法律法规,对人类遗传资源采集、保藏、利用和信息对外提供行为进行严格管理。为了使本中心人类遗传资源活动能符合相关法律法规的规定,中心逐步建立并不断优化人类遗传资源的管理制度和管理流程,以保证人类遗传资源的有效保护和合理利用。人类遗传资源管理作为生物安全防控的重要组成部分,其执行的力度势必会影响生物安全的全面贯彻落实,因此,加强人类遗传资源管理助推生物安全能力建设显得至关重要。
[1] Gao XD, Jiao YL. Ethical selection of informed consent models in the study and utilization of human genetic resources. Chin Med Ethics, 2021, 34(4):408-413, 432. (in Chinese)
高旭东, 焦艳玲. 人类遗传资源研究和利用中知情同意模式的伦理选择. 中国医学伦理学, 2021, 34(4):408-413, 432.
[2] Su Y, He R, Wang Y, et al. Strengthen the protection and utilization of human genetic resources in China. Chin J Clin Lab Manag (Electronic Ed), 2017, 5(1):9-11. (in Chinese)
苏月, 何蕊, 王跃, 等. 加强我国人类遗传资源保护和利用. 中华临床实验室管理电子杂志, 2017, 5(1):9-11.
[3] Yang Y, Chi H, Yin H, et al. Research on human genetic resources management of United States and the enlightenment to China. Chin Bull Life Sci, 2019, 31(7):637-643. (in Chinese)
杨渊, 池慧, 殷环, 等. 美国人类遗传资源管理研究及对我国的启示. 生命科学, 2019, 31(7):637-643.
[4] He R, Dong Y, Liu J, et al. Typical management model of human genetic resources and its enlightenment to China. Chin Med Biotechnol, 2018, 13(6):566-568. (in Chinese)
何蕊, 董妍, 刘静, 等. 典型人类遗传资源管理模式及对我国的启示. 中国医药生物技术, 2018, 13(6):566-568.
[5] Sudlow C, Gallacher J, Allen N, et al. UK biobank: an open access resource for identifying the causes of a wide range of complex diseases of middle and old age. PLoS Med, 2015, 12(3):e1001779.
[6] Zhang Y, Chen YL, Li XH. Research on the management of human genetic resource conservation activities — take Beijing Friendship Hospital as an example. China Sci Technol Resources Rev, 2020, 52(2):17-21, 40. (in Chinese)
张允, 陈奕霖, 李秀红. 人类遗传资源保藏活动管理研究——以北京友谊医院为例. 中国科技资源导刊, 2020, 52(2):17-21, 40.
[7] Hou CH, Tian LJ. Analysis of human genetic resource administration of China in international cooperative clinical trial. China Mod Med, 2018, 25(27):146-148. (in Chinese)
侯春花, 田丽娟. 国际合作临床试验中人类遗传资源管理发展历程及现状分析. 中国当代医药, 2018, 25(27):146-148.
[8] Wang LJ, Wu MF, Wang DL, et al. Strengthening the management of drug clinical trials through self-audit of administrative licenses of human genetic resources. J Shenyang Pharm Univ, 2020, 37(7):657- 661. (in Chinese)
王瓅珏, 吴明凤, 王丹蕾, 等. 通过人类遗传资源行政许可自查加强对药物临床试验管理. 沈阳药科大学学报, 2020, 37(7):657-661.
[9] Zhou Y, Ren Y, Yang HX, et al. The practice and thinking of human genetic resources management in drug clinical trial implementation. China Med Herald, 2019, 16(28):174-176, 185. (in Chinese)
周燕, 任宇, 杨宏昕, 等. 药物临床试验实施中涉及人类遗传资源管理的实践与思考. 中国医药导报, 2019, 16(28):174-176, 185.
10.3969/j.issn.1673-713X.2021.06.011
杨钟平,Email:1046580277@qq.com
2021-06-22

