可注射型富血小板纤维蛋白治疗口腔黏膜创伤性溃疡的动物研究
李维芝 郑柳红 宗娟娟
中图分类号:R781.5 文献标志码:A doi:10.3969/j.issn.1001-3733.2021.06.005
口腔黏膜疾病中有很多表现为反复发作的口腔黏膜糜烂/溃疡,如复发性口腔溃疡和糜烂型口腔扁平苔藓等。此类疾病往往病因不明,反复发作,难以根治。目前治疗此类病损的方法多是局部应用糖皮质激素[1],但长期反复使用会带来诸多不良反应,如黏膜萎缩变硬、真菌感染、停药反跳等[2]。富血小板纤维蛋白(platelet rich fibrin,PRF),因其在抗感染、促进组织愈合与再生方面的优势[3],近十多年来在临床医学各专业领域得到广泛应用[4-5]。本课题尝试将可注射型富血小板纤维蛋白(i-PRF)应用于口腔溃疡病损的治疗,并与糖皮质激素局部注射的疗效相比较,以尝试探索一种新的可行的治疗方案。
1 材料与方法
1.1 实验动物、试剂及仪器
由长沙市天勤生物技术有限公司提供新西兰兔48 只,1.5~2.0 kg,雌雄各半,动物许可证号:SCXK(湘)2014-0010。饲养温度(25±2) ℃,通风良好,预饲养1 周。盐酸奥布卡因凝胶(沈阳绿洲制药股份有限公司);曲安奈德溶液(浙江仙琚制药责任有限公司);乙酸(西陇科学股份有限公司);EOS7D相机(佳能公司,日本);普通光学显微镜(Olympus公司,日本);石蜡切片机(Leica Microsystems Nussloch Gmbh公司,德国)。
1.2 建模及分组
预饲养1 周后,目标位置碘伏消毒,涂表麻膏,将浸有15 μL 50%乙酸直径为6 mm的圆形滤纸片置于兔上前牙牙龈处1 min[6],生理盐水冲洗1 min,24 h后可见溃疡。建模成功的48 只新西兰兔按随机数法随机分为4 组:i-PRF组、曲安奈德组(TA)、生理盐水组(NS)、空白对照组(BC)。
1.3 i-PRF制备及给药
建模24 h后,自i-PRF组兔子耳缘静脉取5 mL血液,700 r/min离心3 min,i-PRF取出备用。每组兔口内消毒,表麻下分别给药,每处病损一个位点注射0.1 mL相应试剂。曲安奈德浓度为0.1 mL∶2 mg,空白对照组不做处理。
1.4 体重、进食量、进水量记录
每天记录兔子的体重及进食量、进水量。
1.5 口腔溃疡面积大小测定
建模成功后,每天拍摄口内溃疡照片,以牙周探针矫正长度,用Image J软件计算溃疡面积大小。
1.6 取材
4 组兔子于给药后的第3、6、9、12天各处死3 只兔子,取材。
1.7 HE染色
组织块水洗后,乙醇脱水,二甲苯透明,石蜡浸蜡、包埋,切片,苏木精染色。显微镜下观察、评分,评分标准参照化学灼烧法建立动物溃疡模评估药物疗效的Karavana等[7]学者的病理评分标准(表1)。

表1 评分标准Tab 1 Evaluation criterion
1.8 数据统计与分析
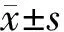
2 结 果
2.1 建模后进食量及体重变化
各组间兔子平均每天体重增量i-PRF组>TA组>BC组>NS组。且i-PRF组及TA组相较于NS组及BC组的体重增量差异有统计学意义。说明对溃疡的不同处理方式中,i-PRF组及TA组对兔子日常生活的影响更小,恢复更快,因此体重增加较另外两组快(图1)。
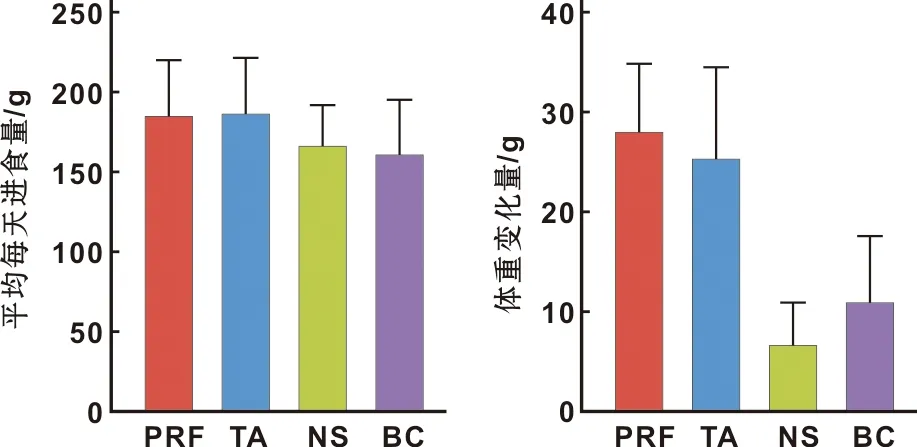
图1 各组兔子建模后平均每天进食量及体重增量
2.2 溃疡面积变化结果
建模后第1天,目标区域可见表皮组织坏死,边界清晰,周围组织红肿。给药后3 d,可见病损面减小,表皮坏死面减小。给药后第6天可见病损面积明显减小,仍可见边界红肿。给药后第9天病损区域黏膜部分愈合,无红肿(图2)。
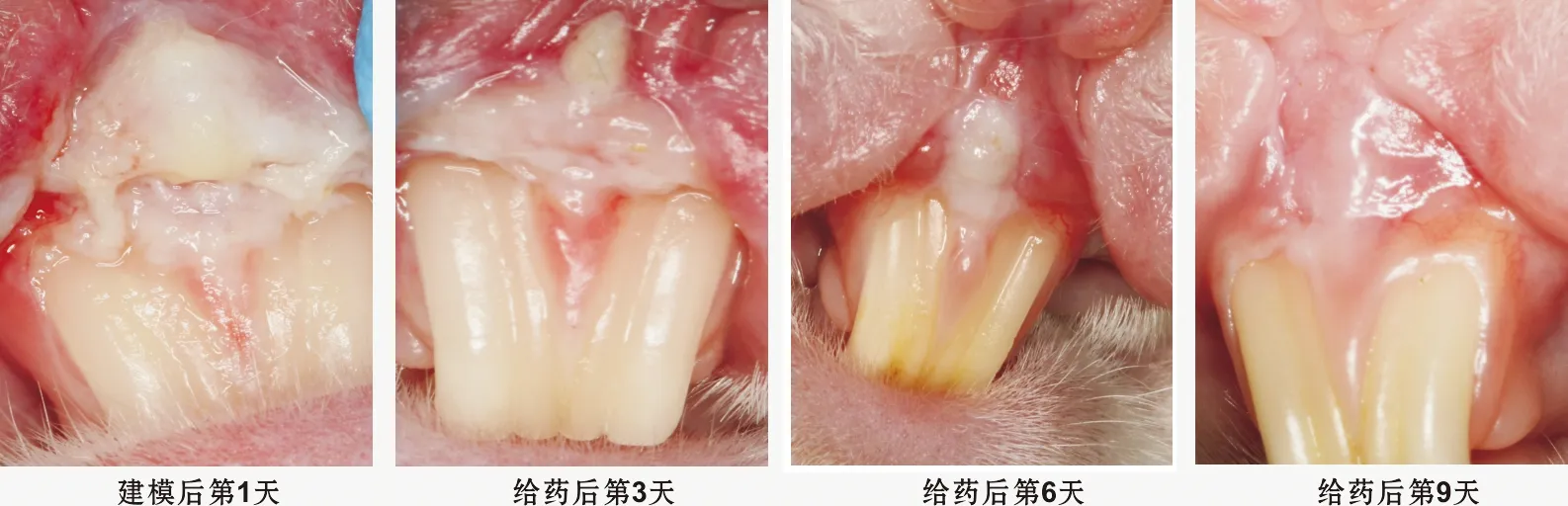
图2 溃疡变化
建模24 h后各组所形成的溃疡面积大小差异无统计学意义。由图3可知,在给药后第3、6天里均i-PRF组愈合最快,愈合效果与TA组相同。
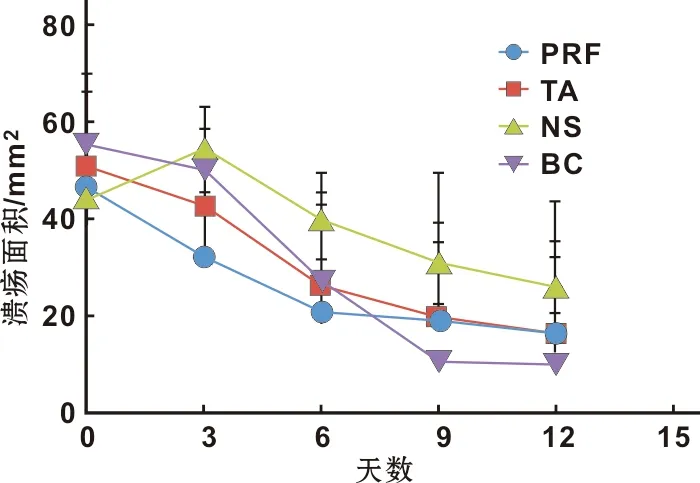
图3 各时间段各组溃疡面积对比
2.3 HE染色结果
术后第3天,4 组均可见表皮坏死,胶原纤维水肿,可见炎性细胞,无新生血管。NS组胶原纤维松散紊乱。术后第6天,i-PRF组坏死组织脱落,成纤维细胞密集,可见明显新生毛细血管,炎症细胞较3天时减少。TA组及NS水组仍可见坏死组织,胶原纤维水肿。BC组炎症细胞较其他3组密集。术后第9天,i-PRF组上皮形成,新生血管增多。TA组及NS组胶原纤维水肿,对照组无坏死组织,炎症细胞较多。术后第12天,i-PRF组及TA组部分上皮形成完成,NS组、BC组上皮未完全愈合,TA组可见纤维玻璃样变(图4)。
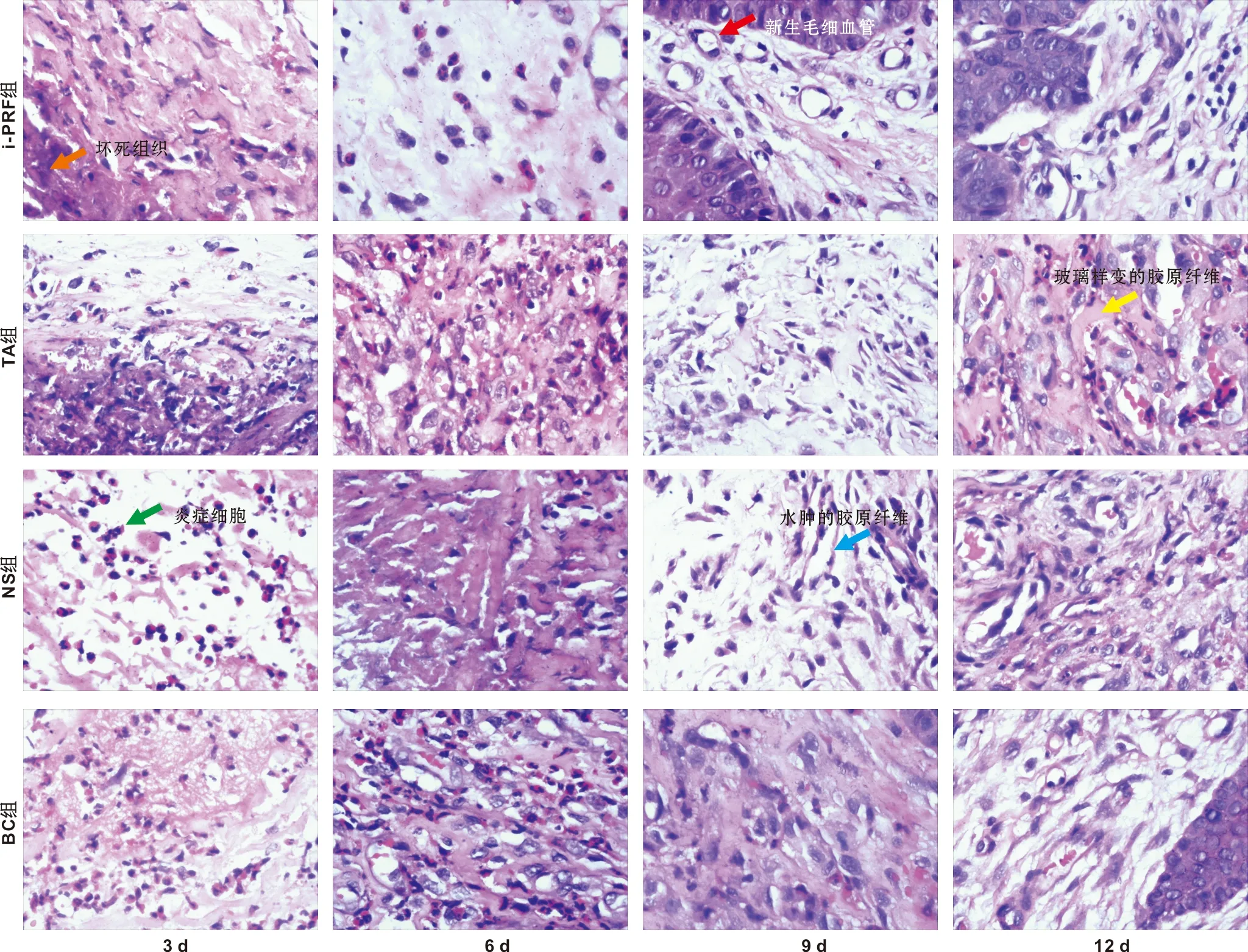
图4 各组样本HE染色(×400)
图5显示:术后各组病理评分有差异,但差异没有统计学意义(P>0.05)。其中i-PRF组随时间的推移病理评分提高最快,TA组愈合速度较理想但组织预后结果不理想。
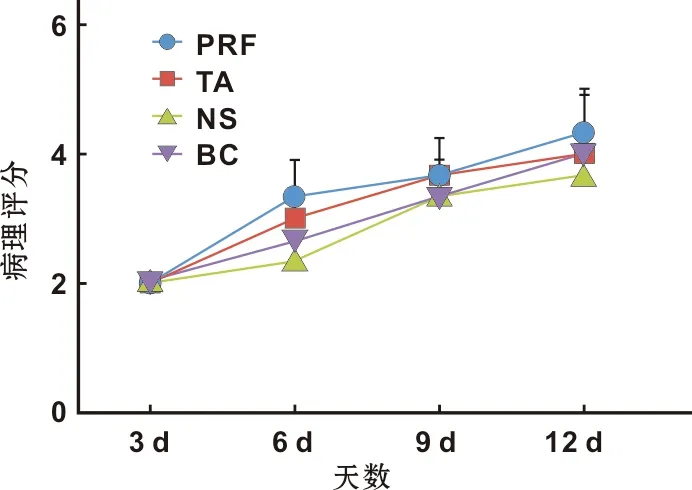
图5 各时间段各组病理评分折线图
3 讨 论
口腔黏膜病中,发病率最高的为口腔溃疡,口腔溃疡的病因与诸多因素相关,目前仍病因不明[8],因此没有根治方法。但长期不愈的溃疡严重影响患者生活,以临床治疗为出发点,设计了本实验以探索一种安全有效的治疗溃疡病损的方式。
目前建立口腔溃疡动物模型主要有物理法、生物学法及化学法。其中物理法主要包括机械创伤法及放射法建模,分别用于创伤性溃疡的研究和放射性溃疡的研究。生物学法建模中最常用的方法为:自身免疫抗原法,这是构建口腔溃疡动物模型常用方法之一,此方法需先制备抗原佐剂,每两周皮内注射抗原佐剂一次,重复5 周可建模成功。其优点是,建模原理与RAU的发病机制相似,其缺点亦显而易见:(1)建模成功率不高;(2)自身免疫抗原法建模后溃疡发生部位不定,愈合时间各异[9],不利于实验结果观察。因此本实验选用的建模方法是化学烧灼法,Cavalcante等[10]学者研究证实,该模型在病理特征和瘢痕形成机制上与人类创伤性溃疡相似,同样是研究口腔溃疡常用动物模型之一。其优点是:操作方法简单易行,建模成功率高,适用于大规模动物建模,可用于促溃疡愈合药物的临床研究。缺点是:(1)不能完全模拟口腔溃疡的发病机制;(2)化学药物腐蚀性较强,实验过程中药物易外溢,造成大面积溃疡。因此本实验建模过程中使用固定大小的滤纸片10 片浸透在150 μL的50%冰醋酸中,使药物不至于过多溢出,以固定药物的用量。
口腔糜烂/溃疡的治疗方法种类繁多,目前主要治疗目的为了加速创面愈合、缓解创面疼痛。其中最常用及疗效显著的方法为糖皮质激素的局部应用,曲安奈德注射液是最常用的糖皮质激素[11]。因此本实验将i-PRF与曲安奈德对溃疡的治疗效果做对比,以观察i-PRF是否有效。实验结果表明,i-PRF及曲安奈德对促进溃疡愈合的作用是相差无几的,甚至i-PRF促进溃疡愈合的病理评分优于曲安奈德。研究表明,反复注射曲安奈德可引起局部组织萎缩、变硬,局部抵抗力下降,易合并真菌细菌感染等并发症[11],本实验也发现曲安奈德溶液易沉积于组织中,且曲安奈德组溃疡病损处的HE染色切片可观察到组织的玻璃样变,其组织病理评分较i-PRF组低。而i-PRF有优良的促进病损愈合的作用,其原因与溃疡组织的病理变化相关,组织学上,溃疡由两个主要结构组成:一个明显的溃疡边缘区域,以及溃疡底部的肉芽组织-结缔组织成分。溃疡边缘区域表达表皮生长因子受体(EGF-R),并活跃地增殖[12],i-PRF中含有大量的EGF并且可以持续释放2周[3],EGF可通过诱导局部组织表达其受体从而促进口腔黏膜溃疡愈合[13],这与唾液中高含量的EGF以促进口腔黏膜快速更替有异曲同工之妙,且i-PRF中的EGF含量远高于唾液;溃疡底部的肉芽组织-结缔组织成分是溃疡愈合过程中的重要组成部分,因为它提供结缔组织细胞,更重要的是提供修复溃疡瘢痕内微血管所必需的微血管[14]。而i-PRF重要的特点除了含有大量的VEGF以促进毛细血管新生,更是有相对稳定的纤维蛋白基质,更有利于组织愈合。本实验结果同样显示i-PRF组相较于有同样刺激的生理盐水组组织愈合更快,这与Crisci等[15]学者的研究结果相吻合,他们应用i-PRF治疗了3 例糖尿病足伴骨髓炎患者,均取得了较好的治疗效果,且观察了术后2年,无不良反应及复发现象。
总而言之,目前治疗溃疡病损主要是通过阻止炎症介质发生反应,降低自身免疫反应以阻止病损发展;另外通过促进细胞增殖、分化以促进病损愈合。而此文所研究的i-PRF中包含大量的细胞因子,既有抗炎作用,也可以促进细胞迁移,增殖,促进毛细血管新生[16-17],因此i-PRF有促进溃疡病损愈合的基础条件。有学者将PRF以外敷的形式,用于治疗口腔溃疡[18],结果表明PRF可促进溃疡愈合。但口腔环境湿润,凝胶置于病损处难以保持,因此本实验选择了液态形式的i-PRF黏膜下注射于病损组织内,有利于其更好的在病损处发挥作用。目前局部封闭治疗仍为重型口疮重要的治疗方式。因此本实验结果或可为临床应用提供参考,但其发挥作用的机制有待进一步研究。

